Магнезоцен - Magnesocene
 | |
| Имена | |
|---|---|
| Название ИЮПАК бис(η5-циклопентадиенил) магний | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider |
|
| ECHA InfoCard | 100.110.799 |
| Номер ЕС |
|
PubChem CID |
|
| |
| |
| Характеристики | |
| C10ЧАС10Mg | |
| Молярная масса | 154.495 г · моль−1 |
| Опасности | |
| Паспорт безопасности | Внешний SDS |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H228, H250, H261, H314 | |
| P210, P231 + 232, P280, P303 + 361 + 353, P304 + 340 + 310, P305 + 351 + 338 + 310, P335 + 334, P422 | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Магнезоцен, также известный как бис (циклопентадиенил) магний (II) и иногда сокращенно MgCp2, представляет собой металлоорганическое соединение с формулой Mg (η5-C5ЧАС5)2. Это пример s-блока основная группа сэндвич-компаунд, структурно относящийся к элементу d-блока металлоцены, и состоит из центрального магний атом зажатый между двумя циклопентадиенил кольца.
Характеристики
Магнезоцен представляет собой белое твердое вещество при комнатной температуре.[1] Он имеет температуру плавления 176 ° C, хотя при атмосферном давлении он сублимируется при 100 ° C.[1] В отличие от ферроцен, магнезоцен демонстрирует небольшую диссоциацию и последующую ассоциацию ионов в полярных электронодонорных растворителях (таких как эфир и ТГФ).[2]
Хотя ферроцен стабилен в условиях окружающей среды, магнезоцен быстро разлагается под воздействием кислорода или влаги, поэтому его необходимо синтезировать и хранить в инертных условиях.[3]
Структура и склеивание
Как показал Рентгеновский кристаллографический После уточнения, твердофазный магнезоцен демонстрирует среднее расстояние связи Mg-C и C-C 2,30 Å и 1,39 Å соответственно, а кольца Cp принимают шахматную конформацию (точечная группа D5d).[4] Газовая фаза электронная дифракция показал аналогичные длины связей, хотя с кольцами Cp в затменной конформации (точечная группа D5ч).[5][6]
Природа связывания Mg-Cp горячо оспаривается относительно того, является ли взаимодействие главным образом ионный[7][8] или же ковалентный[5][6][9] в характере. Измерения дифракции электронов в газовой фазе использовались для аргументации ковалентной модели, в то время как колебательная спектроскопия измерения предоставили доказательства обоих.
Расчеты Хартри-Фока показали, что в отличие от переходный металл металлоцены, орбитали Mg 3d не играют никакой роли в связи металл-кольцо; вместо этого благоприятные связывающие взаимодействия с системой Cp π достигаются путем продвижения двух 3s-электронов к 3pх, у орбитали.[10] Дальнейшая стабилизация обеспечивается за счет отдачи от Cp-колец на орбиталь Mg 3s. Такие взаимодействия обеспечивают меньшую степень перекрытия орбиталей по сравнению с ферроценом, что приводит к сравнительно слабой связи металл-кольцо и довольно высокому эффективному локальному заряду на Mg. Таким образом, экспериментальные доказательства в пользу модели ионной связи можно объяснить очень слабыми, высокополярными взаимодействиями Mg-Cp. Слабый характер этого типа связывания ответственен за относительную нестабильность и высокую реакционную способность магнезоцена по сравнению с ферроценом.
Синтез
Высокотемпературный синтез
Первый синтез магнезоцена, как сообщает Ф. А. Коттон и Джеффри Уилкинсон в 1954 г. включал термическое разложение циклопентадиенила Реактив Гриньяра.[11] Похожая процедура была предложена W. A. Barber, в которой циклопентадиен непосредственно реагирует с твердым магнием при 500-600 ° C.[1] В условиях отсутствия воды и кислорода, свежеперегнанный мономерный циклопентадиен проходит через трубчатую печь инертным газом-носителем (таким как гелий, аргон, или же азот ) и пропитали магниевой стружкой или порошком. Магнезоценовые отложения на более холодных поверхностях за выходным концом печи. Продукт этого процесса обычно представляет собой белую пушистую массу мелких микрокристаллов, но большие бесцветные монокристаллы могут быть получены путем регулирования температуры и скорости потока. Если твердый магнезоцен не нужен, приемную колбу можно вместо этого заполнить растворителем и собрать продукт в растворе, с которым, как отметил Барбер, обращаться гораздо безопаснее, чем с чистым твердым веществом.
Эта процедура позволяет получать грамм продукта каждые две минуты в идеальных условиях, а при вертикальной установке (в которой циклопентадиен направлен вниз, а продукт собирается ниже) можно получить почти чистый продукт с выходом> 80% (циклопентадиеном). ). Было показано, что горизонтальная установка возможна, но за счет чистоты продукта из-за ограничения потока газа из-за накопления продукта.
Жидкофазные методы
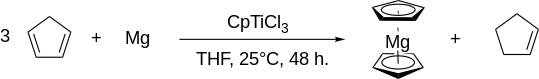
Магнезоцен можно получить из магниевой стружки в ТГФ в мягких условиях с трихлоридом циклопентадиенилтитана (CpTiCl3) действует как катализатор.[12] Масленников и др. позже показал аналогичную каталитическую активность с Cp2TiCl2, TiCl3, TiCl4, и VCl3.[13] Механизм, как показано электронный спиновой резонанс, проходит через Cp2TiH2Промежуточный MgCl.[13] Образование магнезоцена из элементарного магния не наблюдалось в ТГФ без катализатора.[13] Попытки заменить ТГФ диэтиловым эфиром, диглимом или бензолом привели только к полимеризации циклопентадиена.[13]
Синтезы магнезоцена и его производных также проводились в углеводород растворители, такие как гептан, из Cp и (пBu) (sBu) Mg.[14][15]
Металлирование циклопентадиена также может быть выполнено с помощью алкильных комплексов Mg-Al с конечным выходом магнезоцена 85%.[14]
Реакционная способность и потенциальные применения
Магнезоцен служит промежуточным звеном при получении металлоценов переходных металлов:[16]
Магнезоцен также подвергается реакциям обмена лигандов с MgX.2 (X = галогенид ) для образования полусэндвич-соединений CpMgX в THF:[17]
Результирующий полусэндвич галогениды могут служить исходными материалами для синтеза замещенных циклопентадиенов из органических галогенидов.[14]
Из-за своей высокой реакционной способности магнезоцен является привлекательной мишенью для полупроводник исследования как исходный материал для химическое осаждение из паровой фазы и допинг Приложения.[18][19]
магнезоцен также был исследован на предмет его потенциального использования в качестве электролита в ионно-магниевых батареях следующего поколения.[2]
Рекомендации
- ^ а б c Barber, W. A .; Джолли, Уильям Л. (1960), «Циклопентадиенид магния», Неорганические синтезы, John Wiley & Sons, Ltd, стр. 11–15, Дои:10.1002 / 9780470132371.ch5, ISBN 9780470132371
- ^ а б Шварц, Райнер; Пежич, Марияна; Фишер, Филипп; Маринаро, Марио; Йериссен, Людвиг; Вахтлер, Марио (21 ноября 2016 г.). «Электролиты на основе магнезоцена: новый класс электролитов для магниевых батарей». Angewandte Chemie International Edition. 55 (48): 14958–14962. Дои:10.1002 / anie.201606448. ISSN 1521-3773. PMID 27791301.
- ^ Барбер, В. А. (1957-01-01). «Новый препарат циклопентадиенида магния». Журнал неорганической и ядерной химии. 4 (5–6): 373–374. Дои:10.1016/0022-1902(57)80026-8. ISSN 0022-1902.
- ^ Bünder, W .; Вайс, Э. (1975-06-10). "Verfeinerung der kristallstruktur von dicyclopentadienylmagnesium, (η-C5H5) 2Mg [Уточнение кристаллической структуры дициклопентадиенилмагния, (η5-C5H5) 2Mg]". Журнал металлоорганической химии. 92 (1): 1–6. Дои:10.1016 / S0022-328X (00) 91094-5. ISSN 0022-328X.
- ^ а б Старовейский, Казимир Б .; Брунволл, Джон; Новак, Дэвид П .; Люштык, Януш; Хааланд, Арне (1974-01-01). «Молекулярные структуры дициклопентадиенилмагния и дициклопентадиенилхрома методом газофазной дифракции электронов». Журнал химического общества, химические коммуникации. 0 (2): 54–55. Дои:10.1039 / C39740000054. ISSN 0022-4936.
- ^ а б Haaland, A .; Lusztyk, J .; Brunvoll, J .; Старовейский, К. Б. (1975-02-11). «О молекулярной структуре дициклопентадиенилмагния». Журнал металлоорганической химии. 85 (3): 279–285. Дои:10.1016 / S0022-328X (00) 80301-0. ISSN 0022-328X.
- ^ Cotton, F. A .; Рейнольдс, Л. Т. (январь 1958 г.). «Структура и связь циклопентадиенилталлия и бис-циклопентадиенилмагния». Журнал Американского химического общества. 80 (2): 269–273. Дои:10.1021 / ja01535a004. ISSN 0002-7863.
- ^ Алексанян, В. Т .; Гарбузова, И. А .; Гавриленко, В. В .; Захаркин, Л. И. (1977-04-12). «Колебательные спектры и структура бис (циклопентадиенил) магния». Журнал металлоорганической химии. 129 (2): 139–143. Дои:10.1016 / S0022-328X (00) 92483-5. ISSN 0022-328X.
- ^ Lippincott, Ellis R .; Xavier, J .; Стил, Д. (1961-05-01). «Колебательные спектры и структура бис-циклопентадиенилмагния». Журнал Американского химического общества. 83 (10): 2262–2266. Дои:10.1021 / ja01471a011. ISSN 0002-7863.
- ^ Faegri Jr., K .; Almlöf, J .; Лют, Х. П. (1983-06-28). «Геометрия и связи магнезоцена. Исследование AB-initio MO-LCAO». Журнал металлоорганической химии. 249 (2): 303–313. Дои:10.1016 / S0022-328X (00) 99429-4. ISSN 0022-328X.
- ^ Wilkinson, G .; Коттон, Ф. А. (1954). Химия и промышленность (Лондон). 11: 307.
- ^ Сайто, Таро (1971-01-01). «Получение бисциклопентадиенилмагния с помощью титанового комплексного катализатора». Журнал химического общества D: Химические коммуникации. 0 (22): 1422. Дои:10.1039 / C29710001422. ISSN 0577-6171.
- ^ а б c d Масленников, Станислав В .; Игнатьев, Роман А .; Пискунов, Александр В .; Спирина, Ирина Валерьевна (2001-03-01). «Синтез дициклопентадиенида магния, катализируемый производными титана и ванадия». Прикладная металлоорганическая химия. 15 (3): 161–168. Дои:10.1002 / aoc.115. ISSN 1099-0739.
- ^ а б c Джемилев У. М .; Ибрагимов, А.Г .; Толстиков, Г.А. (1991-03-26). «Синтез и превращения« негриньяровских »магниевых реагентов, полученных из 1,3-диенов». Журнал металлоорганической химии. 406 (1–2): 1–47. Дои:10.1016 / 0022-328X (91) 83169-5. ISSN 0022-328X.
- ^ Eisch, J. J .; Санчес, Р. (1985-12-03). «Легкое магнирование углеродных бренстедовских кислот электрофильными, бездонорными алкилмагниевыми соединениями». Журнал металлоорганической химии. 296 (3): c27 – c31. Дои:10.1016 / 0022-328X (85) 80378-8. ISSN 0022-328X.
- ^ Hull, H. S .; Рид, Аллен Форрест; Тернбулл, Алан Г. (1967-04-01). «Теплота образования и энергия связи бис (циклопентадиенил) магния». Неорганическая химия. 6 (4): 805–807. Дои:10.1021 / ic50050a032. ISSN 0020-1669.
- ^ Форд, Уоррен Т .; Груцнер, Джон Б. (1972-08-01). «Спектры ядерного магнитного резонанса протонов и углерода-13 соединений циклопентадиенилмагния в тетрагидрофуране». Журнал органической химии. 37 (16): 2561–2564. Дои:10.1021 / jo00981a009. ISSN 0022-3263.
- ^ Лундберг, Å; Андерссон, С.Г .; Landgren, G .; Раск, М. (1988-07-01). «Резкие переходы легирования p-типа с использованием бис- (циклопентадиенил) -магния в газофазной эпитаксии металлоорганических соединений GaAs». Журнал электронных материалов. 17 (4): 311–314. Bibcode:1988JEMat..17..311R. Дои:10.1007 / BF02652111. ISSN 1543–186X.
- ^ Кондо, М .; Anayama, C .; Sekiguchi, H .; Танахаши, Т. (1 августа 1994 г.). «Переходные процессы при легировании магнием при металлоорганической газофазной эпитаксии GaAs и AlGaInP». Журнал роста кристаллов. 141 (1–2): 1–10. Bibcode:1994JCrGr.141 .... 1K. Дои:10.1016 / 0022-0248 (94) 90085-X. ISSN 0022-0248.




![{ displaystyle { ce {Mg + 2C5H6 -> [500-600 ^ oC] Mg (C5H5) 2 + H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7670c6b5fe07f9d57ffbc3dae05cf8e8f2ca2e56)