Синтез Фридлендера - Friedländer synthesis
| Синтез Фридлендера | |
|---|---|
| Названный в честь | Пауль Фридлендер |
| Тип реакции | Реакция образования кольца |
| Идентификаторы | |
| Портал органической химии | Фридлендер-синтез |
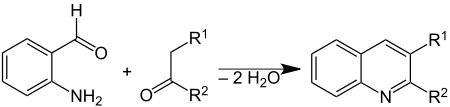
В Синтез Фридлендера это химическая реакция из 2-аминобензальдегиды[1] с кетоны формировать хинолин производные.[2][3] Назван в честь немецкого химика. Пауль Фридлендер (1857–1923).
Эта реакция была катализатором трифторуксусная кислота,[4] толуолсульфоновая кислота,[5] йод,[6] и Кислоты Льюиса.[7]
Опубликовано несколько обзоров.[8][9][10]
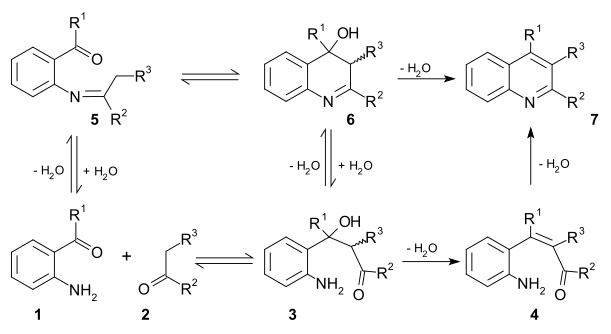
Механизм
Два жизнеспособных механизмы реакции существуют для этой реакции. По первому механизму 2-амино замещенное карбонильное соединение 1 и карбонильное соединение 2 реагировать в ограничивающий шаг к альдол аддукт 3. Этот промежуточный продукт теряет воду в реакция элиминации к ненасыщенное карбонильное соединение 4 а затем снова теряет воду в я добываю образование хинолина 7. Во втором механизме первый шаг База Шиффа формирование для 5 с последующей альдольной реакцией на 6 и устранение 7.[11]
В Реакция Пфитцингера и Ниментовский синтез хинолина являются вариациями реакции Фридлендера.
Смотрите также
Рекомендации
- ^ Органический синтез, Сб. Vol. 3, стр. 56 (1955); Vol. 28, стр. 11 (1948 г.). (Статья )
- ^ Фридлендер, П. (1882). «Уэбер о-Амидобензальдегид». Chemische Berichte. 15 (2): 2572–2575. Дои:10.1002 / cber.188201502219.
- ^ Friedländer, P .; Геринг, К. Ф. (1883). "Ueber eine Darstellungsmethode im Pyridinkern заместитель хинолинпроизводное". Бер. 16 (2): 1833–1839. Дои:10.1002 / cber.18830160265.
- ^ Shaabani, A .; Soleimani, E .; Бадри, З. (2007). «Трифторуксусная кислота как эффективный катализатор синтеза хинолина». Синтетические коммуникации. 37 (4): 629–635. Дои:10.1080/00397910601055230. S2CID 98625429.
- ^ Jia, C.-S .; Zhang, Z .; Tu, S.-J .; Ван, Г.-В. (2006). «Быстрый и эффективный синтез полизамещенных хинолинов с помощью п-толуолсульфоновой кислоты в условиях отсутствия растворителя: сравнительное исследование микроволнового излучения по сравнению с обычным нагревом». Орг. Biomol. Chem. 4 (1): 104–110. Дои:10.1039 / b513721g. PMID 16358003.
- ^ Wu, J .; Xia, H.-G .; Гао, К. (2006). «Молекулярный йод: высокоэффективный катализатор в синтезе хинолинов посредством аннулирования Фридлендера». Орг. Biomol. Chem. 4 (1): 126–129. Дои:10.1039 / b514635f. PMID 16358006.
- ^ Varala, R .; Enugala, R .; Адапа, С. Р. (2006). «Эффективный и быстрый синтез Фридлендера функционализированных хинолинов, катализируемых гексагидратом нитрата неодима (III)». Синтез. 2006 (22): 3825–3830. Дои:10.1055 / с-2006-950296.
- ^ Манске, Р. Х. (1942). «Химия хинолинов». Chem. Ред. 30: 113–144. Дои:10.1021 / cr60095a006.
- ^ Бергстром, Ф. В. (1944). «Гетероциклические соединения азота. Часть IIA. Гексациклические соединения: пиридин, хинолин и изохинолин». Chem. Ред. 35 (2): 77–277. Дои:10.1021 / cr60111a001.
- ^ Cheng, C.-C .; Ян, С.-Дж. (2004). «Синтез Фридлендера хинолинов». Органические реакции. Дои:10.1002 / 0471264180.or028.02. ISBN 0471264180.
- ^ Хосе Марко-Контеллес; Елена Перес-Майораль; Абделуахид Самади; Мария ду Карму Каррейрас; Елена Сориано (2009). «Последние достижения в реакции Фридлендера». Химические обзоры. 109 (6): 2652–71. Дои:10.1021 / cr800482c. PMID 19361199.