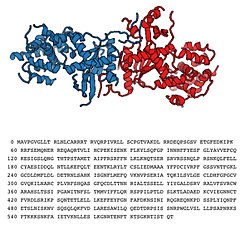
GLD-2 - GLD-2
Эта статья включает Список ссылок, связанное чтение или внешняя ссылка, но его источники остаются неясными, потому что в нем отсутствует встроенные цитаты. (Март 2016 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
GLD-2 (что означает Развитие зародышевой линии 2) представляет собой цитоплазматическую поли (А) полимеразу (cytoPAP), которая добавляет последовательные AMP мономеры на 3 ’конце определенных РНК, образуя поли (A) хвост, что является процессом, известным как полиаденилирование.
Для специфичности РНК GLD-2 ассоциируется с РНК-связывающим белком, обычно с GLD-3, с образованием гетеродимер который действует как цитоплазматический PAP. Этот белок выполняет ферментативную функцию и принадлежит к семейству (семейство ДНК-полимераз типа B), которое включает несколько подобных ферментов, таких как GLD-1, GLD-3 и GLD-4.
Это семейство цитоплазматических PAP было описано у нескольких различных видов, включая Homo sapiens, Caenorhabditis elegans, Xenopus, Mus musculus и Дрозофила. Более того, поскольку это цитоплазматический PAP, он отличается от ядерных PAP в некоторых аспектах. В то время как ядерные PAP содержат каталитический домен и РНК-связывающий домен, члены семейства GLD-2 имеют только каталитический домен.
Локализация
GLD-2 - распространенный и широко распространенный, но пока еще довольно неизвестный белок, который уже был обнаружен в каждом из пять королевств. В животном мире это было специально обнаружено у Homo sapiens, Дрозофила, Xenopus и Mus musculus. Однако также было замечено присутствие GLD-2 в Arabidopsis thaliana который принадлежит царству растений; Кишечная палочка в Монере и грибковые микроорганизмы албиканс в грибах.
У людей он в основном выражается в головном мозге и внутри него, в мозжечке, гиппокампе и продолговатом мозге. Мы также можем найти их в некоторых других исходных тканях, таких как фибробласты, клетки HeLa, клетки MCF-7, клеточная линия меланомы и вилочковая железа. Внутри этих клеток он может находиться в ядре и митохондрия поскольку его основная функция связана с полиаденилированием ДНК, и эти клеточные органеллы - единственные, в которых ДНК может быть обнаружена. Однако в цитозоле также присутствуют растворимые GLD-2, хотя причина их появления до сих пор не ясна.
В Кишечная палочка, этот ферментный белок можно найти в клеточной мембране и в цитозоль, тогда как в Drosophila melanogaster, он преобладает в ядре и цитоплазме мозга, яйцеклетках, яичниках и семенниках. Наконец, в Arabidopsis thaliana, он находится в ядре цветка, клетках корня, ствола и листа.
Связанные функции
GLD-2 в первую очередь стабилизирует мРНК, которые подавляются трансляцией, а также сильно способствует массовому полиаденилированию. Удивительно, но эти функции, по-видимому, мало влияют на динамизацию эффективной трансляции мРНК-мишени, поскольку это эффективная поли (A) полимераза, которая помогает развивать активность полиаденилирования. Эта активность стимулируется его взаимодействием с предполагаемым РНК-связывающим белком: GLD-3. Некоторые исследования предполагают, что GLD-3 стимулирует GLD-2, рекрутируя его в РНК. Если это так, то приведение GLD-2 к РНК другими способами также должно стимулировать ее активность.
Молекулярная функция
Связывание АТФ
GLD-2, как поли (A) полимераза (PAP), действует, включая АТФ на 3'-конце мРНК независимым от матрицы образом.
Ферментативная активность: активность полинуклеотида аденилилтрансферазы.
Было обнаружено, что этот белок обладает каталитической активностью, другими словами, он обладает способностью увеличивать скорость химических реакций, которые не могли бы происходить так быстро. Это известно катализ следующая реакция (для которой требуется следующий кофактор: Mg (2+)):
АТФ + РНК (n) ⇄ дифосфат + РНК (n + 1)
В зависимости от окружающей среды оптимальный pH варьируется от 8 в цитоплазме до 8,3 в ядре.
Биологический процесс
Дифференцировка гемопоэтических клеток-предшественников
Белок GLD-2 вместе с еще 136 белками участвует в молекулярном процессе кроветворный дифференцировка клеток-предшественников в протеоме человека. Это процесс, при котором тип клеток-предшественников приобретает особые черты гематопоэтических клеток-предшественников, разновидностей клеток, включая миелоидные клетки-предшественники и лимфоидные клетки-предшественники.
Обработка мРНК полиаденилированием РНК
Активность GLD-2 по полиаденилированию, как мы уже упоминали, стимулируется физическим взаимодействием с РНК-связывающим белком, GLD-3. Чтобы проверить, может ли GLD-3 стимулировать GLD-2 путем привлечения его к РНК, в некоторых исследованиях GLD-2 C. elegans был привязан к мРНК в Xenopus ооциты с использованием белка оболочки MS2. Привязанный GLD-2 добавляет поли (А) и стимулирует трансляцию мРНК, демонстрируя, что рекрутирование достаточно для стимуляции активности полиаденилирования. Гетеродимер PAP, в котором GLD-2 содержит активный сайт, а GLD-3 обеспечивает специфичность связывания РНК. Белок оболочки MS2 был присоединен к GLD-2, чтобы привлечь его к РНК.
Кроме того, активность GLD-2 также важна для поддержания или повышения уровня множества мРНК, поскольку цитоплазматическое полиаденилирование играет важную роль в активации материнской трансляция мРНК во время раннего развития. В позвоночные, для реакции требуется CPEB, РНК-связывающий белок и поли (A) полимераза GLD-2.
В Xenopus Фермент, который существует в двух близкородственных формах, полиаденилирует РНК, с которыми он связан, и усиливает их трансляцию. Аналогичным образом он взаимодействует с факторами цитоплазматического полиаденилирования, включая Фактор специфичности расщепления и полиаденилирования и CPEB, и с целевыми мРНК. Эти данные подтверждают и расширяют недавнее сообщение о том, что фермент GLD-2 является давно искомым PAP, ответственным за цитоплазматическое полиаденилирование в ооцитах.
Кроме того, считается, что формирование долговременной памяти не контролирует трансляцию локализованных мРНК. У млекопитающих дендрит мРНК сохраняются в подавленном состоянии и активируются при повторяющейся стимуляции. Считается, что несколько регуляторных белков, необходимых для контроля трансляции на раннем этапе развития, необходимы для формирования памяти, что предполагает сходные молекулярные механизмы. В эксперименте с использованием Дрозофилабыл обнаружен фермент, ответственный за удлинение поли (A) в головном мозге, и также было продемонстрировано, что его активность необходима именно для долговременной памяти. Эти находки предоставляют убедительные доказательства того, что цитоплазматическое полиаденилирование критически важно для формирования памяти и что GLD2 является ответственным ферментом.
Медицинские последствия
Также было обнаружено, что GLD2 имеет медицинское применение.
Например, такой фермент сверхэкспрессируется у пациентов, страдающих рак; поэтому его можно использовать как прогностический фактор для раннего появления у больных раком груди. Более того, активность PAP используется для измерения эффекта противоопухолевых препаратов. этопозид и кордицепин в двоем карцинома Сотовые линии: HeLa, который является эпителиоидной карциномой шейки матки человека, и MCF-7 (рак груди человека). Однако, несмотря на его полезность, он также может быть вовлечен в проявление нескольких распространенных заболеваний, таких как: лейкемия, цирроз печени, травмы головного мозга, гепатит и в некоторых случаях бесплодие у пациентов мужского пола.
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000164329 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000042167 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
дальнейшее чтение
- "UniProtKB - Q6PIY7 (GLD2_HUMAN)". UniProt.
- Ноуш М., Ерослализ А., Хаберманн Б., Экманн С.Р. (октябрь 2014 г.). «Цитоплазматические поли (А) полимеразы GLD-2 и GLD-4 способствуют общей экспрессии генов посредством различных механизмов». Исследования нуклеиновых кислот. Оксфордские журналы. 42 (18): 11622–33. Дои:10.1093 / нар / gku838. ЧВК 4191412. PMID 25217583.
- "ГЛД-2". InteractiveFly: GeneBrief.
- Kwak JE, Wang L, Ballantyne S, Kimble J, Wickens M (март 2004 г.). «Гомологами GLD-2 млекопитающих являются поли (А) полимеразы». Труды Национальной академии наук Соединенных Штатов Америки. 101 (13): 4407–12. Bibcode:2004ПНАС..101.4407К. Дои:10.1073 / pnas.0400779101. ЧВК 384760. PMID 15070731.
- Квак Дж. Э., Викенс М (июнь 2007 г.). «Семейство поли (U) полимераз». РНК. 13 (6): 860–7. Дои:10.1261 / rna.514007. ЧВК 1869031. PMID 17449726.
- Мартин Г., Мёглих А., Келлер В., Дубле С. (август 2004 г.). «Биохимические и структурные сведения о связывании субстрата и каталитическом механизме поли (А) полимеразы млекопитающих». Журнал молекулярной биологии. 341 (4): 911–25. Дои:10.1016 / j.jmb.2004.06.047. PMID 15328606.
- «PAPD4» Поли (А) РНК-полимераза GLD2 [EC 2.7.7.19] ». Nexprot BETA.
- «GO: 0002244» Дифференцировка гемопоэтических клеток-предшественников ». NextProt BETA.
- Ноуш М., Ерослализ А., Хаберманн Б., Экманн С.Р. (октябрь 2014 г.). «Цитоплазматические поли (А) полимеразы GLD-2 и GLD-4 способствуют общей экспрессии генов посредством различных механизмов». Исследования нуклеиновых кислот. 42 (18): 11622–33. Дои:10.1093 / нар / gku838. ЧВК 4191412. PMID 25217583.
- Накель К., Бонно Ф., Экманн С.Р., Конти Е. (июль 2015 г.). «Структурная основа активации неканонической цитоплазматической поли (А) -полимеразы GLD-2 C. elegans с помощью GLD-3». Труды Национальной академии наук Соединенных Штатов Америки. 112 (28): 8614–9. Bibcode:2015ПНАС..112.8614Н. Дои:10.1073 / pnas.1504648112. ЧВК 4507228. PMID 26124149.
- «Информация о EC 2.7.7.19 - полинуклеотид аденилилтрансфераза». База данных BRENDA.