Полиаденилирование - Polyadenylation

Полиаденилирование это добавление поли (А) хвост к транскрипту РНК, обычно информационная РНК (мРНК). Поли (А) хвост состоит из нескольких аденозинмонофосфаты; другими словами, это участок РНК, который имеет только аденин базы. В эукариоты, полиаденилирование является частью процесса образования зрелой мРНК для перевод. Во многих бактерии поли (А) хвост способствует деградации мРНК. Следовательно, это часть более широкого процесса экспрессия гена.
Процесс полиаденилирования начинается с транскрипция из ген прекращается. В 3'-самый сегмент новообразованной пре-мРНК сначала отщепляется набор белков; эти белки затем синтезируют поли (А) хвост на 3'-конце РНК. В некоторых генах эти белки добавляют поли (А) хвост в одном из нескольких возможных сайтов. Следовательно, полиаденилирование может производить более одного транскрипта из одного гена (альтернативное полиаденилирование), похожий на альтернативное сращивание.[1]
Поли (A) хвост важен для ядерного экспорта, трансляции и стабильности мРНК. Хвост со временем укорачивается, и, когда он достаточно короткий, мРНК подвергается ферментативной деградации.[2] Однако в некоторых типах клеток мРНК с короткими поли (A) хвостами сохраняются для последующей активации путем повторного полиаденилирования в цитозоле.[3] Напротив, когда полиаденилирование происходит у бактерий, оно способствует деградации РНК.[4] Иногда то же самое и с эукариотическими некодирующие РНК.[5][6]
Молекулы мРНК как у прокариот, так и у эукариот имеют полиаденилированные 3'-концы, причем поли (А) хвосты прокариот обычно короче, а молекулы мРНК полиаденилированы.[7]
Справочная информация о РНК
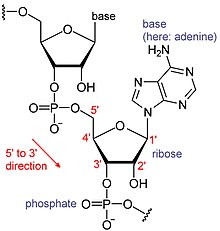
- Для получения дополнительной информации см. РНК и Посланник РНК
РНК - это тип больших биологических молекул, отдельные строительные блоки которых называются нуклеотидами. Название поли (А) хвост (для хвоста полиадениловой кислоты)[8] отражает способ сокращения нуклеотидов РНК, с буквой для основания, которое содержит нуклеотид (A для аденин, C для цитозин, G для гуанин и U для урацил ). РНК продуцируются (записано ) из ДНК шаблон. По соглашению, последовательности РНК записываются в направлении от 5 'до 3'. 5'-конец - это часть молекулы РНК, которая транскрибируется первой, а 3'-конец транскрибируется последней. На 3'-конце также находится поли (А) хвост на полиаденилированных РНК.[1][9]
Информационная РНК (мРНК) - это РНК, которая имеет кодирующую область, которая действует как матрица для синтеза белка (перевод ). Остальная мРНК, непереведенные регионы, настройте, насколько активна мРНК.[10] Есть также много не транслируемых РНК, называемых некодирующими РНК. Подобно нетранслируемым областям, многие из этих некодирующих РНК выполняют регуляторные роли.[11]
Ядерное полиаденилирование
Функция
При ядерном полиаденилировании поли (А) хвост добавляется к РНК в конце транскрипции. На мРНК поли (А) хвост защищает молекулу мРНК от ферментативной деградации в цитоплазма и помогает в терминации транскрипции, экспорте мРНК из ядра и трансляции.[2] Почти все мРНК эукариот полиаденилированы,[12] за исключением репликационно-зависимых гистон мРНК.[13] Это единственные мРНК у эукариот, у которых отсутствует поли (А) хвост, вместо этого заканчивающийся стебель-петля структура, за которой следует богатая пуринами последовательность, называемая нижележащим элементом гистона, который указывает место разрезания РНК, так что образуется 3'-конец мРНК гистона.[14]
Многие эукариотические некодирующие РНК всегда полиаденилируются в конце транскрипции. Существуют небольшие РНК, в которых поли (A) -хвост виден только в промежуточных формах, но не в зрелой РНК, поскольку концы удаляются во время процессинга, причем наиболее заметными из них являются микроРНК.[15][16] Но для многих длинные некодирующие РНК - на вид большая группа регулирующий РНК, которые, например, включают РНК Xist, который является посредником Инактивация Х-хромосомы - поли (А) хвост является частью зрелой РНК.[17]
Механизм
| Участвующие белки:[12][18] CPSF: фактор специфичности расщепления / полиаденилирования |
В процессивный комплекс полиаденилирования в ядре эукариот работает на продуктах РНК-полимераза II, такие как предшественник мРНК. Здесь мультибелковый комплекс (см. компоненты справа)[18] расщепляет 3'-большую часть вновь образованной РНК и полиаденилирует конец, образованный в результате этого расщепления. Расщепление катализируется ферментом CPSF[13][18] и находится на 10–30 нуклеотидов ниже своего сайта связывания.[19] Этот сайт часто имеет сигнальную последовательность полиаденилирования AAUAAA на РНК, но ее варианты, которые более слабо связываются с CPSF существует.[18][20] Два других белка добавляют специфичность связыванию с РНК: CstF и CFI. CstF связывается с GU-богатой областью ниже по ходу от сайта CPSF.[21] CFI распознает третий сайт на РНК (набор последовательностей UGUAA у млекопитающих[22][23][24]) и может набирать CPSF, даже если последовательность AAUAAA отсутствует.[25][26] Сигнал полиаденилирования - мотив последовательности, распознаваемый комплексом расщепления РНК, - варьируется между группами эукариот. Большинство сайтов полиаденилирования человека содержат последовательность AAUAAA,[21] но эта последовательность менее распространена у растений и грибов.[27]
РНК обычно расщепляется до терминации транскрипции, поскольку CstF также связывается с РНК-полимеразой II.[28] Благодаря плохо изученному механизму (по состоянию на 2002 г.) он дает сигнал РНК-полимеразе II, чтобы ускользнуть из транскрипта.[29] В расщеплении также участвует белок CFII, но неизвестно, каким образом.[30] Сайт расщепления, связанный с сигналом полиаденилирования, может варьироваться примерно до 50 нуклеотидов.[31]
Когда РНК расщепляется, начинается полиаденилирование, катализируемое полиаденилатполимеразой. Полиаденилат-полимераза строит поли (A) хвост, добавляя аденозинмонофосфат единиц от аденозинтрифосфат к РНК, отщепляя пирофосфат.[32] Другой белок, PAB2, связывается с новым коротким поли (A) хвостом и увеличивает сродство полиаденилатполимеразы к РНК. Когда поли (А) хвост составляет примерно 250 нуклеотиды долго фермент больше не может связываться с CPSF, и полиаденилирование прекращается, что определяет длину поли (A) хвоста.[33][34] CPSF находится в контакте с РНК-полимеразой II, что позволяет ей сигнализировать полимеразе о прекращении транскрипции.[35][36] Когда РНК-полимераза II достигает «терминирующей последовательности» ('TTTATT³ на матрице ДНК и ⁵'AAUAAA³ на первичном транскрипте), сигнализируется окончание транскрипции.[37] Аппарат полиаденилирования также физически связан с сплайсосома, комплекс, удаляющий интроны из РНК.[26]
Последующие эффекты
Поли (A) хвост действует как сайт связывания для поли (A) -связывающий белок. Поли (A) -связывающий белок способствует экспорту из ядра и трансляции, а также ингибирует деградацию.[38] Этот белок связывается с поли (А) хвостом до экспорта мРНК из ядра, а в дрожжах также рекрутирует поли (А) нуклеазу, фермент, который укорачивает поли (А) хвост и позволяет экспортировать мРНК. Поли (A) -связывающий белок экспортируется в цитоплазму вместе с РНК. мРНК, которые не экспортируются, разрушаются экзосома.[39][40] Поли (A) -связывающий белок также может связываться и, таким образом, рекрутировать несколько белков, влияющих на трансляцию,[39] один из них фактор инициирования -4G, который, в свою очередь, набирает 40S рибосомная субъединица.[41] Однако поли (А) хвост не требуется для трансляции всех мРНК.[42] Кроме того, поли (A) хвостовая часть (олигоаденилирование) может определять судьбу молекул РНК, которые обычно не являются поли (A) -концевыми (такими как (небольшие) некодирующие (sn) РНК и т. Д.), И тем самым индуцировать их РНК. распад.[43]
Деаденилирование
В эукариотических соматические клетки поли (А) хвосты большинства мРНК в цитоплазме постепенно становятся короче, а мРНК с более коротким поли (А) хвостом транслируются меньше и быстрее разрушаются.[44] Однако может пройти много часов, прежде чем мРНК распадется.[45] Этот процесс деаденилирования и деградации может быть ускорен микроРНК, комплементарными 3 'нетранслируемая область мРНК.[46] В незрелые яйцеклетки, мРНК с укороченными поли (A) хвостами не деградируют, а вместо этого хранятся и трансляционно неактивны. Эти короткохвостые мРНК активируются цитоплазматическим полиаденилированием после оплодотворения, во время активация яйца.[47]
У животных поли (А) рибонуклеаза (ПАРН ) может быть привязан к Крышка 5 футов и удалить нуклеотиды из поли (А) хвоста. Уровень доступа к 5'-кэпу и поли (А) хвосту важен для контроля того, как скоро мРНК деградирует. PARN деаденилирует меньше, если РНК связывается факторами инициации 4E (на 5'-кэпе) и 4G (на поли (A) хвосте), поэтому трансляция снижает деаденилирование. Скорость деаденилирования также может регулироваться РНК-связывающими белками. После удаления поли (A) -хвоста комплекс декапирования удаляет 5'-кэп, что приводит к деградации РНК. Несколько других белков участвуют в деаденилировании в бутоньерки и человеческие клетки, в первую очередь CCR4-Нет сложный.[48]
Цитоплазматическое полиаденилирование
В цитозоле некоторых типов животных клеток, а именно в цитозоле, происходит полиаденилирование. линия зародыша, в начале эмбриогенез и в пост-синаптический сайты нервные клетки. Это удлиняет поли (А) хвост мРНК с укороченным поли (А) хвостом, так что мРНК будет переведено.[44][49] Эти укороченные поли (A) хвосты часто состоят из менее 20 нуклеотидов и удлинены примерно до 80–150 нуклеотидов.[3]
В раннем эмбрионе мыши цитоплазматическое полиаденилирование материнских РНК из яйцеклетки позволяет клетке выживать и расти, даже если транскрипция не начинается до середины 2-клеточной стадии (4-клеточная стадия у человека).[50][51] В мозге цитоплазматический полиаденилирование активно во время обучения и может играть роль в долгосрочное потенцирование, который является усилением передачи сигнала от нервной клетки к другой в ответ на нервные импульсы и важен для обучения и формирования памяти.[3][52]
Для цитоплазматического полиаденилирования необходимы РНК-связывающие белки. CPSF и CPEB, и может включать другие РНК-связывающие белки, такие как Пумилио.[53] В зависимости от типа клетки, полимераза может быть полиаденилат-полимеразой (PAP) того же типа, что и в ядерном процессе, или цитоплазматической полимеразой. GLD-2.[54]
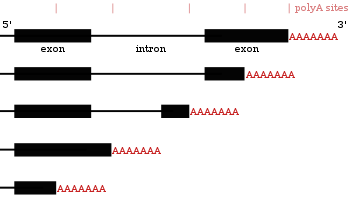
Альтернативное полиаденилирование
Многие гены, кодирующие белок, имеют более одного сайта полиаденилирования, поэтому ген может кодировать несколько мРНК, которые различаются по своему 3 ′ конец.[27][55][56] 3’-область транскрипта содержит множество сигналов полиаденилирования (PAS). Когда используются более проксимальные (ближе к 5’-концу) сайты PAS, это укорачивает длину 3 ’нетранслируемой области (3’ UTR) транскрипта.[57] Исследования как на людях, так и на мухах показали тканеспецифический APA. Нейронные ткани предпочитают использование дистальных PAS, что приводит к более длинным 3 ’UTR, а ткани семенников предпочитают проксимальные PAS, что приводит к более коротким 3’ UTR.[58][59] Исследования показали, что существует корреляция между уровнем консервативности гена и его тенденцией к альтернативному полиаденилированию, при этом высококонсервативные гены демонстрируют больше APA. Точно так же высоко экспрессируемые гены следуют той же схеме.[60] Рибо-секвенирование данные (секвенирование только мРНК внутри рибосом) показали, что изоформы мРНК с более короткими 3 ’UTR транслируются с большей вероятностью.[57]
Поскольку альтернативное полиаденилирование изменяет длину 3 'UTR,[61] он также может изменить, какие сайты привязки доступны для микроРНК в 3 ′ UTR.[19][62] МикроРНК имеют тенденцию подавлять трансляцию и способствовать деградации мРНК, с которыми они связываются, хотя есть примеры микроРНК, которые стабилизируют транскрипты.[63][64] Альтернативное полиаденилирование также может укорачивать кодирующую область, тем самым создавая код мРНК для другого белка,[65][66] но это гораздо менее распространено, чем просто укорачивание нетранслируемой 3'-области.[27]
Выбор сайта поли (А) может зависеть от внеклеточных стимулов и зависит от экспрессии белков, которые принимают участие в полиаденилировании.[67][68] Например, выражение CstF-64, подразделение фактор стимуляции расщепления (CstF), увеличивается макрофаги в ответ на липополисахариды (группа бактериальных соединений, вызывающих иммунный ответ). Это приводит к отбору слабых поли (A) сайтов и, следовательно, более коротких транскриптов. Это удаляет регуляторные элементы в 3'-нетранслируемых областях мРНК для продуктов, связанных с защитой, таких как лизоцим и TNF-α. Эти мРНК имеют более длительный период полураспада и продуцируют больше этих белков.[67] РНК-связывающие белки, отличные от тех, которые входят в аппарат полиаденилирования, также могут влиять на использование сайта полиаденилирования,[69][70][71][72] сканирование Метилирование ДНК рядом с сигналом полиаденилирования.[73]
Метка деградации у эукариот
Для многих некодирующие РНК, в том числе тРНК, рРНК, мяРНК, и snoRNA, полиаденилирование - это способ маркировки РНК для деградации, по крайней мере, в дрожжи.[74] Это полиаденилирование осуществляется в ядре ТРАМПОВЫЙ комплекс, который поддерживает хвост длиной около 4 нуклеотидов до 3'-конца.[75][76] Затем РНК разрушается экзосома.[77] Поли (А) хвосты также были обнаружены на фрагментах рРНК человека, как в форме гомополимерных (только А), так и гетерполимерных (в основном А) хвостов.[78]
В прокариотах и органеллах

У многих бактерий полиаденилированы могут как мРНК, так и некодирующие РНК. Этот поли (A) хвост способствует деградации за счет деградосома, который содержит два фермента, разрушающих РНК: полинуклеотидфосфорилаза и РНКаза E. Полинуклеотидфосфорилаза связывается с 3'-концом РНК, а 3'-удлинение, обеспечиваемое поли (A) хвостом, позволяет ей связываться с РНК, чьи вторичная структура иначе заблокировал бы 3 'конец. Последовательные раунды полиаденилирования и деградации 3'-конца полинуклеотидфосфорилазой позволяют деградосома чтобы преодолеть эти вторичные структуры. Поли (A) хвост может также привлекать РНКазы, которые разрезают РНК надвое.[79] Эти бактериальные поли (A) хвосты имеют длину около 30 нуклеотидов.[80]
В таких разных группах, как животные и трипаносомы, то митохондрии содержат как стабилизирующие, так и дестабилизирующие поли (А) хвосты. Дестабилизирующее полиаденилирование нацелено как на мРНК, так и на некодирующие РНК. Поли (А) хвосты в среднем имеют длину 43 нуклеотида. Стабилизирующие из них начинаются со стоп-кодона, и без них стоп-кодон (UAA) не является полным, поскольку геном кодирует только часть U или UA. Митохондрии растений обладают только дестабилизирующим полиаденилированием. Митохондриальное полиаденилирование никогда не наблюдалось ни у почкующихся, ни у делящихся дрожжей. [81][82]
Хотя многие бактерии и митохондрии имеют полиаденилат-полимеразы, у них также есть другой тип полиаденилирования, осуществляемый полинуклеотидфосфорилаза сам. Этот фермент содержится в бактериях,[83] митохондрии,[84] пластиды[85] и как составная часть экзосомы архей (в тех археи которые имеют экзосома ).[86] Он может синтезировать 3'-расширение, где подавляющее большинство оснований являются аденинами. Как и у бактерий, полиаденилирование полинуклеотидфосфорилазой способствует деградации РНК в пластидах.[87] а также, вероятно, архей.[81]
Эволюция
Хотя полиаденилирование наблюдается почти у всех организмов, оно не универсально.[7][88] Однако широкое распространение этой модификации и тот факт, что она присутствует в организмах всех трех домены жизни подразумевает, что последний универсальный общий предок Предполагается, что все живые организмы имеют ту или иную форму системы полиаденилирования.[80] Некоторые организмы не полиаденилируют мРНК, что означает, что они утратили свои механизмы полиаденилирования в процессе эволюции. Хотя не известны примеры эукариот, в которых отсутствует полиаденилирование, мРНК бактерии Mycoplasma gallisepticum и солеустойчивый архей Haloferax volcanii отсутствует эта модификация.[89][90]
Самый древний фермент полиаденилирования - это полинуклеотидфосфорилаза. Этот фермент входит в состав как бактериального деградосома и архей экзосома,[91] два тесно связанных комплекса, которые рециклируют РНК в нуклеотиды. Этот фермент разрушает РНК, атакуя связь между 3'-крайними нуклеотидами с фосфатом, разрывая дифосфатный нуклеотид. Эта реакция обратима, поэтому фермент может также расширить РНК с помощью большего количества нуклеотидов. Гетерополимерный хвост, добавленный полинуклеотидфосфорилазой, очень богат аденином. Выбор аденина, скорее всего, является результатом более высокого ADP концентрации, чем другие нуклеотиды в результате использования АТФ в качестве энергетической валюты, что увеличивает вероятность ее включения в этот хвост на ранних этапах жизни. Было высказано предположение, что участие богатых аденином хвостов в деградации РНК вызвало более позднюю эволюцию полиаденилатных полимераз (ферментов, которые продуцируют поли (A) хвосты без других нуклеотидов в них).[92]
Полимеразы полиаденилата не такие древние. Они отдельно развились как у бактерий, так и у эукариот из CCA-добавляющий фермент, который является ферментом, завершающим 3'-концы тРНК. Его каталитический домен гомологичен другим полимеразы.[77] Предполагается, что горизонтальный перенос бактериального фермента, добавляющего CCA, к эукариотам, позволил архейподобному ферменту, добавляющему CCA, переключить функцию на поли (A) полимеразу.[80] Некоторые родословные, например археи и цианобактерии, никогда не выделяли полиаденилат-полимеразу.[92]
Хвосты полиаденилата наблюдаются у нескольких РНК-вирусы, в том числе Грипп А,[93] Коронавирус[94], Вирус мозаики люцерны,[95] и Утиный гепатит А.[96] Некоторые вирусы, например ВИЧ-1 и Полиовирус, ингибируют поли-А связывающий белок клетки (PABPC1 ), чтобы подчеркнуть экспрессию их собственных генов над экспрессией клетки-хозяина.[97]
История
Поли (A) полимераза была впервые идентифицирована в 1960 году как ферментативная активность в экстрактах, сделанных из ядер клеток, которые могут полимеризовать АТФ, но не АДФ, в полиаденин.[98][99] Хотя эта активность идентифицирована во многих типах клеток, эта активность не имела известной функции до 1971 года, когда последовательности поли (A) были обнаружены в мРНК.[100][101] Первоначально считалось, что единственной функцией этих последовательностей является защита 3'-конца РНК от нуклеаз, но позже были идентифицированы специфические роли полиаденилирования в ядерном экспорте и трансляции. Полимеразы, ответственные за полиаденилирование, были впервые очищены и охарактеризованы в 1960-х и 1970-х годах, но большое количество дополнительных белков, контролирующих этот процесс, было обнаружено только в начале 1990-х годов.[100]
Смотрите также
использованная литература
- ^ а б Праудфут, штат Нью-Джерси, Фургер А., Дай М.Дж. (февраль 2002 г.). «Интеграция обработки мРНК с транскрипцией». Ячейка. 108 (4): 501–12. Дои:10.1016 / S0092-8674 (02) 00617-7. PMID 11909521. S2CID 478260.
- ^ а б Гуханийоги Дж., Брюэр Дж. (Март 2001 г.). «Регулирование стабильности мРНК в клетках млекопитающих». Ген. 265 (1–2): 11–23. Дои:10.1016 / S0378-1119 (01) 00350-X. ЧВК 3340483. PMID 11255003.
- ^ а б c Рихтер Дж. Д. (июнь 1999 г.). «Цитоплазматическое полиаденилирование в развитии и за его пределами». Обзоры микробиологии и молекулярной биологии. 63 (2): 446–56. Дои:10.1128 / MMBR.63.2.446-456.1999. ЧВК 98972. PMID 10357857.
- ^ Стидж Д.А. (август 2000 г.). «Новые особенности распада мРНК у бактерий». РНК. 6 (8): 1079–90. Дои:10.1017 / S1355838200001023. ЧВК 1369983. PMID 10943888.
- ^ Чжуан И, Чжан Х, Лин С. (июнь 2013 г.). «Полиаденилирование 18S рРНК в водорослях (1)». Журнал психологии. 49 (3): 570–9. Дои:10.1111 / иен.12068. PMID 27007045. S2CID 19863143.
- ^ Андерсон Дж. Т. (август 2005 г.). «Оборот РНК: неожиданные последствия хвоста». Текущая биология. 15 (16): R635-8. Дои:10.1016 / j.cub.2005.08.002. PMID 16111937. S2CID 19003617.
- ^ а б Саркар Н. (июнь 1997 г.). «Полиаденилирование мРНК у прокариот». Ежегодный обзор биохимии. 66 (1): 173–97. Дои:10.1146 / annurev.biochem.66.1.173. PMID 9242905.
- ^ Стивенс А. (1963). «Рибонуклеиновые кислоты - биосинтез и деградация». Ежегодный обзор биохимии. 32: 15–42. Дои:10.1146 / annurev.bi.32.070163.000311. PMID 14140701.
- ^ Ленингер А.Л., Нельсон Д.Л., Кокс М.М., ред. (1993). Принципы биохимии (2-е изд.). Нью-Йорк: стоит. ISBN 978-0-87901-500-8.[страница нужна ]
- ^ Абаза I, Гебауэр Ф (март 2008 г.). «Торговый перевод с помощью РНК-связывающих белков». РНК. 14 (3): 404–9. Дои:10.1261 / rna.848208. ЧВК 2248257. PMID 18212021.
- ^ Маттик Дж. С., Макунин И. В. (апрель 2006 г.). «Некодирующая РНК». Молекулярная генетика человека. 15 ТУ № 1 (90001): Р17-29. Дои:10.1093 / hmg / ddl046. PMID 16651366.
- ^ а б Хант А.Г., Сюй Р., Аддепалли Б., Рао С., Форбс К.П., Микс Л.Р., Син Д., Мо М., Чжао Х., Бандйопадхьяй А., Дампанабойна Л., Марион А., Фон Ланкен С., Ли QQ (май 2008 г.). «Аппарат полиаденилирования мРНК Arabidopsis: всесторонний анализ белок-белковых взаимодействий и профилирование экспрессии генов». BMC Genomics. 9: 220. Дои:10.1186/1471-2164-9-220. ЧВК 2391170. PMID 18479511.
- ^ а б Давила Лопес М., Самуэльссон Т. (январь 2008 г.). «Ранняя эволюция процессинга 3'-конца гистоновой мРНК». РНК. 14 (1): 1–10. Дои:10.1261 / rna.782308. ЧВК 2151031. PMID 17998288.
- ^ Марзлафф В.Ф., Гонджиди П., Вудс К.Р., Джин Дж., Мальтийский Л.Дж. (ноябрь 2002 г.). «Репликационно-зависимые гены гистонов человека и мыши». Геномика. 80 (5): 487–98. Дои:10.1016 / S0888-7543 (02) 96850-3. PMID 12408966.
- ^ Сайни Х. К., Гриффитс-Джонс С., Энрайт А. Дж. (Ноябрь 2007 г.). «Геномный анализ транскриптов микроРНК человека». Труды Национальной академии наук Соединенных Штатов Америки. 104 (45): 17719–24. Bibcode:2007ПНАС..10417719С. Дои:10.1073 / pnas.0703890104. ЧВК 2077053. PMID 17965236.
- ^ Йошикава М., Перагин А., Парк М.Я., Поэтиг Р.С. (сентябрь 2005 г.). «Путь биогенеза транс-действующих миРНК у Arabidopsis». Гены и развитие. 19 (18): 2164–75. Дои:10.1101 / gad.1352605. ЧВК 1221887. PMID 16131612.
- ^ Амарал П.П., Мэттик Дж. С. (август 2008 г.). «Некодирующая РНК в разработке». Геном млекопитающих. 19 (7–8): 454–92. Дои:10.1007 / s00335-008-9136-7. PMID 18839252. S2CID 206956408.
- ^ а б c d Bienroth S, Keller W, Wahle E (февраль 1993 г.). «Сборка комплексного процесса полиаденилирования матричной РНК». Журнал EMBO. 12 (2): 585–94. Дои:10.1002 / j.1460-2075.1993.tb05690.x. ЧВК 413241. PMID 8440247.
- ^ а б Лю Д., Брокман Дж. М., Дасс Б., Хатчинс Л. Н., Сингх П., Маккарри Дж. Р., Макдональд С. К., Грабер Дж. Х. (2006). «Систематические вариации сигналов 3'-процессинга мРНК во время сперматогенеза мышей». Исследования нуклеиновых кислот. 35 (1): 234–46. Дои:10.1093 / нар / gkl919. ЧВК 1802579. PMID 17158511.
- ^ Lutz CS (октябрь 2008 г.). «Альтернативное полиаденилирование: поворот в формировании 3'-конца мРНК». ACS Химическая биология. 3 (10): 609–17. Дои:10.1021 / cb800138w. PMID 18817380.
- ^ а б Beaudoing E, Freier S, Wyatt JR, Claverie JM, Gautheret D (июль 2000 г.). «Паттерны использования варианта сигнала полиаденилирования в генах человека». Геномные исследования. 10 (7): 1001–10. Дои:10.1101 / гр.10.7.1001. ЧВК 310884. PMID 10899149.
- ^ Браун К.М., Гилмартин Г.М. (декабрь 2003 г.). «Механизм регуляции 3'-процессинга пре-мРНК человеческим фактором расщепления Im». Молекулярная клетка. 12 (6): 1467–76. Дои:10.1016 / S1097-2765 (03) 00453-2. PMID 14690600.
- ^ Ян Кью, Гилмартин GM, Doublié S (июнь 2010 г.). «Структурная основа распознавания UGUA белком Nudix CFI (m) 25 и значение регуляторной роли в процессинге 3 'мРНК». Труды Национальной академии наук Соединенных Штатов Америки. 107 (22): 10062–7. Bibcode:2010PNAS..10710062Y. Дои:10.1073 / pnas.1000848107. ЧВК 2890493. PMID 20479262.
- ^ Ян К., Козено М., Гилмартин Г. М., Дубле С. (март 2011 г.). «Кристаллическая структура человеческого комплекса фактора расщепления CFI (m) 25 / CFI (m) 68 / РНК дает представление о распознавании сайта поли (A) и образовании петель РНК». Структура. 19 (3): 368–77. Дои:10.1016 / j.str.2010.12.021. ЧВК 3056899. PMID 21295486.
- ^ Венкатараман К., Браун К.М., Гилмартин Г.М. (июнь 2005 г.). «Анализ неканонического поли (А) сайта показывает трехчастный механизм распознавания поли (А) сайта позвоночных». Гены и развитие. 19 (11): 1315–27. Дои:10.1101 / gad.1298605. ЧВК 1142555. PMID 15937220.
- ^ а б Миллевой С., Лулерг С., Деттвайлер С., Караа С.З., Келлер В., Антониу М., Вагнер С. (октябрь 2006 г.). «Взаимодействие между U2AF 65 и CF I (m) связывает оборудование для сварки и обработки 3 'концов». Журнал EMBO. 25 (20): 4854–64. Дои:10.1038 / sj.emboj.7601331. ЧВК 1618107. PMID 17024186.
- ^ а б c Шен Й, Джи Джи, Хаас Би Джей, Ву Х, Чжэн Дж, Риз Джи Джи, Ли Кью (май 2008 г.). «Анализ на уровне генома сигналов процессинга 3'-конца мРНК риса и альтернативного полиаденилирования». Исследования нуклеиновых кислот. 36 (9): 3150–61. Дои:10.1093 / nar / gkn158. ЧВК 2396415. PMID 18411206.
- ^ Гловер-Каттер К., Ким С., Эспиноза Дж., Бентли Д.Л. (январь 2008 г.). «РНК-полимераза II приостанавливается и связывается с факторами процессинга пре-мРНК на обоих концах генов». Структурная и молекулярная биология природы. 15 (1): 71–8. Дои:10.1038 / nsmb1352. ЧВК 2836588. PMID 18157150.
- ^ Молекулярная биология клетки, глава 6, «От ДНК к РНК». 4-е издание. Альбертс Б., Джонсон А., Льюис Дж. И др. Нью-Йорк: наука о гирляндах; 2002 г.
- ^ Штумпф Г, Домди Х (ноябрь 1996 г.). «Зависимость процессинга 3'-конца дрожжевой пре-мРНК от CFT1: последовательность гомолога фактора связывания AAUAAA млекопитающих». Наука. 274 (5292): 1517–20. Bibcode:1996Научный ... 274.1517S. Дои:10.1126 / science.274.5292.1517. PMID 8929410. S2CID 34840144.
- ^ Исели К., Стивенсон Б.Дж., де Соуза С.Дж., Самайя Х.Б., Камарго А.А., Буетоу К.Х., Штраусберг Р.Л., Симпсон А.Дж., Бухер П., Джонженел CV (июль 2002 г.) «Дальняя гетерогенность на 3'-концах мРНК человека». Геномные исследования. 12 (7): 1068–74. Дои:10.1101 / гр.62002. ЧВК 186619. PMID 12097343.
- ^ Бальбо ПБ, Бом А (сентябрь 2007 г.). «Механизм поли (А) полимеразы: структура тройного комплекса фермент-MgATP-РНК и кинетический анализ». Структура. 15 (9): 1117–31. Дои:10.1016 / j.str.2007.07.010. ЧВК 2032019. PMID 17850751.
- ^ Viphakone N, Voisinet-Hakil F, Minvielle-Sebastia L (апрель 2008 г.). «Молекулярное рассечение мРНК поли (A) длины хвоста у дрожжей». Исследования нуклеиновых кислот. 36 (7): 2418–33. Дои:10.1093 / nar / gkn080. ЧВК 2367721. PMID 18304944.
- ^ Wahle E (февраль 1995 г.). «Регулирование длины хвоста поли (А) вызвано прекращением процесса синтеза». Журнал биологической химии. 270 (6): 2800–8. Дои:10.1074 / jbc.270.6.2800. PMID 7852352.
- ^ Дихтль Б., Бланк Д., Садовски М., Хюбнер В., Вайзер С., Келлер В. (август 2002 г.). «Yhh1p / Cft1p напрямую связывает распознавание поли (A) сайта и терминацию транскрипции РНК-полимеразы II». Журнал EMBO. 21 (15): 4125–35. Дои:10.1093 / emboj / cdf390. ЧВК 126137. PMID 12145212.
- ^ Наг А., Нарсин К., Мартинсон Х.Г. (июль 2007 г.). «Поли (A) -зависимая транскрипционная пауза опосредуется CPSF, действующим на тело полимеразы». Структурная и молекулярная биология природы. 14 (7): 662–9. Дои:10.1038 / nsmb1253. PMID 17572685. S2CID 5777074.
- ^ Tefferi A, Wieben ED, Dewald GW, Whiteman DA, Bernard ME, Spelsberg TC (август 2002 г.). «Учебник по медицинской геномике, часть II: Основные принципы и методы молекулярной генетики». Труды клиники Мэйо. 77 (8): 785–808. Дои:10.4065/77.8.785. PMID 12173714. S2CID 2237085.
- ^ Коллер Дж. М., Грей Н. К., Викенс депутат (октябрь 1998 г.). «Стабилизация мРНК поли (А) связывающим белком не зависит от поли (А) и требует трансляции». Гены и развитие. 12 (20): 3226–35. Дои:10.1101 / gad.12.20.3226. ЧВК 317214. PMID 9784497.
- ^ а б Сиддики Н., Мангус Д.А., Чанг Т.С., Палермино Дж.М., Шю А.Б., Геринг К. (август 2007 г.). «Поли (А) нуклеаза взаимодействует с С-концевым доменом полиаденилат-связывающего белка, домена поли (А) -связывающего белка». Журнал биологической химии. 282 (34): 25067–75. Дои:10.1074 / jbc.M701256200. PMID 17595167.
- ^ Винчигерра П., Штуц Ф (июнь 2004 г.). «Экспорт мРНК: конвейер от генов до ядерных пор». Текущее мнение в области клеточной биологии. 16 (3): 285–92. Дои:10.1016 / j.ceb.2004.03.013. PMID 15145353.
- ^ Грей Н.К., Коллер Дж. М., Диксон К. С., Викенс М. (сентябрь 2000 г.). «Множественные части поли (А) -связывающего белка стимулируют трансляцию in vivo». Журнал EMBO. 19 (17): 4723–33. Дои:10.1093 / emboj / 19.17.4723. ЧВК 302064. PMID 10970864.
- ^ Мо С., Ван Хоф А. (июль 2006 г.). «Дрожжевые транскрипты, расщепленные внутренним рибозимом, дают новое понимание роли кэпа и поли (А) хвоста в трансляции и распаде мРНК». РНК. 12 (7): 1323–37. Дои:10.1261 / rna.46306. ЧВК 1484436. PMID 16714281.
- ^ Каргаполова Ю., Левин М., Лакнер К., Данквардт С. (июнь 2017 г.). «sCLIP - интегрированная платформа для изучения РНК-белковых взаимодействий в биомедицинских исследованиях: идентификация CSTF2tau в альтернативном процессинге малых ядерных РНК». Исследования нуклеиновых кислот. 45 (10): 6074–6086. Дои:10.1093 / нар / gkx152. ЧВК 5449641. PMID 28334977.
- ^ а б Meijer HA, Bushell M, Hill K, Gant TW, Willis AE, Jones P, de Moor CH (2007). «Новый метод поли (А) фракционирования позволяет выявить большую популяцию мРНК с коротким поли (А) хвостом в клетках млекопитающих». Исследования нуклеиновых кислот. 35 (19): e132. Дои:10.1093 / нар / гкм830. ЧВК 2095794. PMID 17933768.
- ^ Ленер Б., Сандерсон К.М. (июль 2004 г.). «Каркас взаимодействия белков для деградации мРНК человека». Геномные исследования. 14 (7): 1315–23. Дои:10.1101 / gr.2122004. ЧВК 442147. PMID 15231747.
- ^ Ву Л., Фан Дж., Беласко Дж. Г. (март 2006 г.). «МикроРНК направляют быстрое деаденилирование мРНК». Труды Национальной академии наук Соединенных Штатов Америки. 103 (11): 4034–9. Bibcode:2006PNAS..103.4034W. Дои:10.1073 / pnas.0510928103. ЧВК 1449641. PMID 16495412.
- ^ Цуй Дж., Сактон К.Л., Хорнер В.Л., Кумар К.Э., Вольфнер М.Ф. (апрель 2008 г.). «Wispy, гомолог GLD-2 у дрозофилы, необходим во время оогенеза и активации яиц». Генетика. 178 (4): 2017–29. Дои:10.1534 / genetics.107.084558. ЧВК 2323793. PMID 18430932.
- ^ Вилуш CJ, Wormington M, Peltz SW (апрель 2001 г.). «Руководство от шапки к хвосту по обороту мРНК». Обзоры природы Молекулярная клеточная биология. 2 (4): 237–46. Дои:10.1038/35067025. PMID 11283721. S2CID 9734550.
- ^ Юнг М.Ю., Лоренц Л., Рихтер Д.Д. (июнь 2006 г.). «Контроль трансляции нейрогидином, эукариотическим фактором инициации 4E и связывающим белком CPEB». Молекулярная и клеточная биология. 26 (11): 4277–87. Дои:10.1128 / MCB.02470-05. ЧВК 1489097. PMID 16705177.
- ^ Сакураи Т., Сато М., Кимура М. (ноябрь 2005 г.). «Разнообразные модели удлинения поли (A) хвоста и укорочения материнских мРНК мышей от полностью выросшего ооцита до стадии 2-клеточного эмбриона». Сообщения о биохимических и биофизических исследованиях. 336 (4): 1181–9. Дои:10.1016 / j.bbrc.2005.08.250. PMID 16169522.
- ^ Taft RA (январь 2008 г.). «Достоинства и ограничения преимплантационного эмбриона мыши как модельной системы». Териогенология. 69 (1): 10–6. Дои:10.1016 / j.theriogenology.2007.09.032. ЧВК 2239213. PMID 18023855.
- ^ Рихтер Дж. Д. (июнь 2007 г.). «КПЭБ: жизнь в переводе». Тенденции в биохимических науках. 32 (6): 279–85. Дои:10.1016 / j.tibs.2007.04.004. PMID 17481902.
- ^ Пике М., Лопес Дж. М., Фуассак С., Гиго Р., Мендес Р. (февраль 2008 г.). «Комбинаторный код для управления трансляцией через CPE». Ячейка. 132 (3): 434–48. Дои:10.1016 / j.cell.2007.12.038. PMID 18267074. S2CID 16092673.
- ^ Бенуа П., Папин С., Квак Дж. Э., Викенс М., Симонелиг М. (июнь 2008 г.). «Поли (А) полимеразы типа PAP и GLD-2 необходимы для последовательного цитоплазматического полиаденилирования и оогенеза у Drosophila». Развитие. 135 (11): 1969–79. Дои:10.1242 / dev.021444. PMID 18434412.
- ^ Тиан Б., Ху Дж., Чжан Х., Лутц С.С. (2005). «Масштабный анализ полиаденилирования мРНК генов человека и мыши». Исследования нуклеиновых кислот. 33 (1): 201–12. Дои:10.1093 / нар / gki158. ЧВК 546146. PMID 15647503.
- ^ Danckwardt S, Hentze MW, Kulozik AE (февраль 2008 г.). «Обработка 3'-конца мРНК: молекулярные механизмы и последствия для здоровья и болезней». Журнал EMBO. 27 (3): 482–98. Дои:10.1038 / sj.emboj.7601932. ЧВК 2241648. PMID 18256699.
- ^ а б Тиан, Бин; Мэнли, Джеймс Л. (2017). «Альтернативное полиаденилирование предшественников мРНК». Обзоры природы. Молекулярная клеточная биология. 18 (1): 18–30. Дои:10.1038 / nrm.2016.116. ISSN 1471-0080. ЧВК 5483950. PMID 27677860.
- ^ Чжан, Хайбо; Ли, Джу Юн; Тиан, Бин (2005). «Предвзятое альтернативное полиаденилирование в тканях человека». Геномная биология. 6 (12): R100. Дои:10.1186 / gb-2005-6-12-r100. ISSN 1474-760X. ЧВК 1414089. PMID 16356263.
- ^ Смиберт, Питер; Миура, Педро; Westholm, Jakub O .; Шенкер, Сол; Мэй, Джемма; Дафф, Майкл O .; Чжан, Даю; Идс, Брайан Д .; Карлсон, Джо; Браун, Джеймс Б .; Эйсман, Роберт С. (2012). «Глобальные паттерны тканеспецифичного альтернативного полиаденилирования у дрозофилы». Отчеты по ячейкам. 1 (3): 277–289. Дои:10.1016 / j.celrep.2012.01.001. ISSN 2211-1247. ЧВК 3368434. PMID 22685694.
- ^ Ли, Джу Юн; Цзи, Чжэ; Тиан, Бин (2008). «Филогенетический анализ сайтов полиаденилирования мРНК выявил роль мобильных элементов в эволюции 3'-конца генов». Исследования нуклеиновых кислот. 36 (17): 5581–5590. Дои:10.1093 / nar / gkn540. ISSN 1362-4962. ЧВК 2553571. PMID 18757892.
- ^ Огородников А., Каргаполова Ю., Данквардт С. (июнь 2016). «Процессинг и расширение транскриптома на 3'-конце мРНК при здоровье и болезни: поиск правильного конца». Pflügers Archiv. 468 (6): 993–1012. Дои:10.1007 / s00424-016-1828-3. ЧВК 4893057. PMID 27220521.
- ^ Сандберг Р., Нейлсон-младший, Сарма А., Шарп П.А., Бердж CB (июнь 2008 г.). «Пролиферирующие клетки экспрессируют мРНК с укороченными 3'-нетранслируемыми областями и меньшим количеством сайтов-мишеней для микроРНК». Наука. 320 (5883): 1643–7. Bibcode:2008Sci ... 320.1643S. Дои:10.1126 / science.1155390. ЧВК 2587246. PMID 18566288.
- ^ Тили Э., Мишей Дж. Дж., Калин Г. А. (апрель 2008 г.). «Экспрессия и функция микро-РНК в иммунных клетках в нормальном или болезненном состоянии». Международный журнал медицинских наук. 5 (2): 73–9. Дои:10.7150 / ijms.5.73. ЧВК 2288788. PMID 18392144.
- ^ Гош Т., Сони К., Скария В., Халимани М., Бхаттачарджи С., Пиллаи Б. (ноябрь 2008 г.). «Опосредованная микроРНК повышающая регуляция альтернативно полиаденилированного варианта гена цитоплазматического {бета} -актина мыши». Исследования нуклеиновых кислот. 36 (19): 6318–32. Дои:10.1093 / нар / gkn624. ЧВК 2577349. PMID 18835850.
- ^ Alt FW, Bothwell AL, Knapp M, Siden E, Mather E, Koshland M, Baltimore D (июнь 1980 г.). «Синтез секретируемых и связанных с мембраной тяжелых цепей иммуноглобулина mu управляется мРНК, которые различаются по своим 3'-концам». Ячейка. 20 (2): 293–301. Дои:10.1016/0092-8674(80)90615-7. PMID 6771018. S2CID 7448467.
- ^ Тиан Б., Пан З., Ли Дж.Й. (февраль 2007 г.). «Широко распространенные события полиаденилирования мРНК в интронах указывают на динамическое взаимодействие между полиаденилированием и сплайсингом». Геномные исследования. 17 (2): 156–65. Дои:10.1101 / гр.5532707. ЧВК 1781347. PMID 17210931.
- ^ а б Shell SA, Hesse C, Morris SM, Milcarek C (декабрь 2005 г.). «Повышенные уровни фактора стимуляции расщепления 64 кДа (CstF-64) в макрофагах, стимулированных липополисахаридами, влияют на экспрессию генов и вызывают выбор альтернативного поли (A) сайта». Журнал биологической химии. 280 (48): 39950–61. Дои:10.1074 / jbc.M508848200. PMID 16207706.
- ^ Огородников А., Левин М., Таттикота С., Токалов С., Хок М., Шерзингер Д., Марини Ф., Поэтч А., Биндер Х, Махер-Геппингер С., Пробст Х.С., Тиан Б., Шефер М., Лакнер К. Дж., Вестерманн Ф, Данквардт С. ( Декабрь 2018 г.). «Организация 3'-конца транскриптома с помощью PCF11 связывает альтернативное полиаденилирование с образованием и нейрональной дифференцировкой нейробластомы». Nature Communications. 9 (1): 5331. Bibcode:2018НатКо ... 9.5331O. Дои:10.1038 / s41467-018-07580-5. ЧВК 6294251. PMID 30552333.
- ^ Licatalosi DD, Mele A, Fak JJ, Ule J, Kayikci M, Chi SW, Clark TA, Schweitzer AC, Blume JE, Wang X, Darnell JC, Darnell RB (ноябрь 2008 г.). «HITS-CLIP позволяет глубже понять процессинг альтернативной РНК мозга». Природа. 456 (7221): 464–9. Bibcode:2008Натура.456..464L. Дои:10.1038 / природа07488. ЧВК 2597294. PMID 18978773.
- ^ Холл-Погар Т., Лян С., Гаага, Л.К., Лутц, CS (июль 2007 г.). «Специфические транс-действующие белки взаимодействуют с элементами полиаденилирования вспомогательной РНК в 3'-UTR COX-2». РНК. 13 (7): 1103–15. Дои:10.1261 / rna.577707. ЧВК 1894925. PMID 17507659.
- ^ Danckwardt S, Kaufmann I., Gentzel M, Foerstner KU, Gantzert AS, Gehring NH, Neu-Yilik G, Bork P, Keller W., Wilm M, Hentze MW, Kulozik AE (июнь 2007 г.). «Факторы сплайсинга стимулируют полиаденилирование посредством USE по сигналам образования неканонических 3'-концов». Журнал EMBO. 26 (11): 2658–69. Дои:10.1038 / sj.emboj.7601699. ЧВК 1888663. PMID 17464285.
- ^ Danckwardt S, Gantzert AS, Macher-Goeppinger S, Probst HC, Gentzel M, Wilm M, Gröne HJ, Schirmacher P, Hentze MW, Kulozik AE (февраль 2011 г.). «p38 MAPK контролирует экспрессию протромбина с помощью регулируемого процессинга 3'-конца РНК». Молекулярная клетка. 41 (3): 298–310. Дои:10.1016 / j.molcel.2010.12.032. PMID 21292162.
- ^ Вуд А.Дж., Шульц Р., Вудфайн К., Колтовска К., Бичи К.В., Петерс Дж., Буркхис Д., Оки Р.Дж. (май 2008 г.). «Регулирование альтернативного полиаденилирования с помощью геномного импринтинга». Гены и развитие. 22 (9): 1141–6. Дои:10.1101 / gad.473408. ЧВК 2335310. PMID 18451104.
- ^ Райниш К.М., Волин С.Л. (апрель 2007 г.). «Новые темы в контроле качества некодирующих РНК». Текущее мнение в структурной биологии. 17 (2): 209–14. Дои:10.1016 / j.sbi.2007.03.012. PMID 17395456.
- ^ Цзя Х, Ван Х, Лю Ф, Гюнтер УП, Сринивасан С., Андерсон Дж. Т., Янковски Э. (июнь 2011 г.). «РНК-геликаза Mtr4p модулирует полиаденилирование в комплексе TRAMP». Ячейка. 145 (6): 890–901. Дои:10.1016 / j.cell.2011.05.010. ЧВК 3115544. PMID 21663793.
- ^ ЛаКава Дж., Хаусли Дж., Савяну К., Петфальски Е., Томпсон Е., Жакье А., Толлервей Д. (июнь 2005 г.). «Расщепление РНК экзосомой стимулируется ядерным комплексом полиаденилирования». Ячейка. 121 (5): 713–24. Дои:10.1016 / j.cell.2005.04.029. PMID 15935758. S2CID 14898055.
- ^ а б Мартин Дж., Келлер В. (ноябрь 2007 г.). «РНК-специфические рибонуклеотидилтрансферазы». РНК. 13 (11): 1834–49. Дои:10.1261 / rna.652807. ЧВК 2040100. PMID 17872511.
- ^ Сломович С., Лауфер Д., Гейгер Д., Шустер Г. (2006). «Полиаденилирование рибосомальной РНК в клетках человека». Исследования нуклеиновых кислот. 34 (10): 2966–75. Дои:10.1093 / нар / gkl357. ЧВК 1474067. PMID 16738135.
- ^ Ренье П., Аррайано CM (март 2000 г.). «Деградация мРНК в бактериях: появление повсеместных признаков». BioEssays. 22 (3): 235–44. Дои:10.1002 / (SICI) 1521-1878 (200003) 22: 3 <235 :: AID-BIES5> 3.0.CO; 2-2. PMID 10684583.
- ^ а б c Анантараман В., Кунин Е.В., Аравинд Л. (апрель 2002 г.). «Сравнительная геномика и эволюция белков, участвующих в метаболизме РНК». Исследования нуклеиновых кислот. 30 (7): 1427–64. Дои:10.1093 / nar / 30.7.1427. ЧВК 101826. PMID 11917006.
- ^ а б Сломович С., Портной В., Ливяну В., Шустер Г. (2006). «Полиаденилирование РНК в прокариотах и органеллах; разные хвосты рассказывают разные истории». Критические обзоры в науках о растениях. 25: 65–77. Дои:10.1080/07352680500391337. S2CID 86607431.
- ^ Чанг, Чон Хо; Тонг, Лян (2012). «Митохондриальная поли (А) полимераза и полиаденилирование». Biochimica et Biophysica Acta (BBA) - механизмы регуляции генов. 1819 (9–10): 992–997. Дои:10.1016 / j.bbagrm.2011.10.012. ISSN 0006-3002. ЧВК 3307840. PMID 22172994.
- ^ Чанг С.А., Козад М., Маки Г.А., Джонс Г.Х. (январь 2008 г.). «Кинетика полинуклеотидфосфорилазы: сравнение ферментов Streptomyces и Escherichia coli и эффекты нуклеозиддифосфатов». Журнал бактериологии. 190 (1): 98–106. Дои:10.1128 / JB.00327-07. ЧВК 2223728. PMID 17965156.
- ^ Нагайке Т., Сузуки Т., Уэда Т. (апрель 2008 г.). «Полиаденилирование в митохондриях млекопитающих: выводы из недавних исследований». Biochimica et Biophysica Acta (BBA) - механизмы регуляции генов. 1779 (4): 266–9. Дои:10.1016 / j.bbagrm.2008.02.001. PMID 18312863.
- ^ Уолтер М., Килиан Дж., Кудла Дж. (Декабрь 2002 г.). «Активность PNPase определяет эффективность процессинга 3'-конца мРНК, деградацию тРНК и степень полиаденилирования в хлоропластах». Журнал EMBO. 21 (24): 6905–14. Дои:10.1093 / emboj / cdf686. ЧВК 139106. PMID 12486011.
- ^ Портной В., Шустер Г. (2006). «Полиаденилирование и деградация РНК в различных архее; роль экзосомы и РНКазы R». Исследования нуклеиновых кислот. 34 (20): 5923–31. Дои:10.1093 / нар / gkl763. ЧВК 1635327. PMID 17065466.
- ^ Иегудай-Решефф С., Портной В., Йогев С., Адир Н., Шустер Г. (сентябрь 2003 г.). «Доменный анализ полинуклеотидфосфорилазы хлоропластов выявляет дискретные функции в деградации РНК, полиаденилировании и гомологии последовательностей с белками экзосом». Растительная клетка. 15 (9): 2003–19. Дои:10.1105 / tpc.013326. ЧВК 181327. PMID 12953107.
- ^ Сломович С., Портной В., Шустер Г. (2008). Обмен РНК в прокариотах, архее и органеллах: Глава 24 Обнаружение и характеристика полиаденилированной РНК у эукарий, бактерий, архей и органелл. Методы в энзимологии. 447. С. 501–20. Дои:10.1016 / S0076-6879 (08) 02224-6. ISBN 978-0-12-374377-0. PMID 19161858.
- ^ Портной В., Евгеньева-Хакенберг Е., Кляйн Ф., Вальтер П., Лоренцен Э., Клуг Г., Шустер Г. (декабрь 2005 г.). «Полиаденилирование РНК у архей: не наблюдается в Haloferax, в то время как полинуклеотидилат экзосомы РНК у Sulfolobus». Отчеты EMBO. 6 (12): 1188–93. Дои:10.1038 / sj.embor.7400571. ЧВК 1369208. PMID 16282984.
- ^ Портной В., Шустер Г. (июнь 2008 г.). «Mycoplasma gallisepticum как первая проанализированная бактерия, у которой РНК не полиаденилирована». Письма о микробиологии FEMS. 283 (1): 97–103. Дои:10.1111 / j.1574-6968.2008.01157.x. PMID 18399989.
- ^ Евгеньева-Хакенберг Э., Роппельт В., Финстерсайфер П., Клуг Г. (декабрь 2008 г.). «Rrp4 и Csl4 необходимы для эффективной деградации, но не для полиаденилирования синтетической и естественной РНК экзосомой архей». Биохимия. 47 (50): 13158–68. Дои:10.1021 / bi8012214. PMID 19053279.
- ^ а б Сломович С., Портной В., Иегудай-Решефф С., Бронштейн Е., Шустер Г. (апрель 2008 г.). «Полинуклеотидфосфорилаза и экзосома архей как поли (А) -полимеразы». Biochimica et Biophysica Acta (BBA) - механизмы регуляции генов. 1779 (4): 247–55. Дои:10.1016 / j.bbagrm.2007.12.004. PMID 18177749.
- ^ Пун, Лео Л. М .; Притлов, Дэвид С.; Фодор, Эрвин; Браунли, Джордж Г. (1 апреля 1999 г.). «Прямые доказательства того, что поли (A) хвост мРНК вируса гриппа A синтезируется путем повторного копирования трека U в матрице РНК вириона». Журнал вирусологии. 73 (4): 3473–3476. Дои:10.1128 / JVI.73.4.3473-3476.1999.
- ^ Ву, Хун-И; Кэ, Тинг-Юнг; Ляо, Вэй-Ю; Чанг, Най-Юн (2013). «Регулирование длины хвоста поли (А) коронавируса во время инфекции». PLOS ONE. 8 (7): e70548. Bibcode:2013PLoSO ... 870548W. Дои:10.1371 / journal.pone.0070548. ЧВК 3726627. PMID 23923003.
- ^ Нилман, Лида; Olsthoorn, René C.L .; Linthorst, Huub J.M .; Бол, Джон Ф. (4 декабря 2001 г.). «Трансляция неполиаденилированной вирусной РНК усиливается за счет связывания вирусного белка оболочки или полиаденилирования РНК». Труды Национальной академии наук. 98 (25): 14286–14291. Bibcode:2001ПНАС ... 9814286Н. Дои:10.1073 / pnas.251542798. ЧВК 64674. PMID 11717411.
- ^ Чен, Цзюнь-Хао; Чжан, Руй-Хуа; Линь, Шао-Ли; Ли, Пэн-Фэй; Лань, Цзин-Цзин; Песня, Ша-Ша; Гао, Цзи-Мин; Ван, Ю; Се, Чжи-Цзин; Ли, Фу-Чанг; Цзян, Ши-Цзинь (2018). «Функциональная роль 3'-нетранслируемой области и поли (A) хвоста вируса гепатита А типа 1 у уток в репликации вирусов и регуляции IRES-опосредованной трансляции». Границы микробиологии. 9: 2250. Дои:10.3389 / fmicb.2018.02250. ЧВК 6167517. PMID 30319572.
- ^ https://viralzone.expasy.org/909?outline=all_by_species
- ^ Эдмондс М., Абрамс Р. (апрель 1960 г.). «Биосинтез полинуклеотидов: образование последовательности аденилатных единиц из аденозинтрифосфата ферментом из ядер тимуса». Журнал биологической химии. 235 (4): 1142–9. PMID 13819354.
- ^ Колган Д.Ф., Мэнли Д.Л. (ноябрь 1997 г.). «Механизм и регуляция полиаденилирования мРНК». Гены и развитие. 11 (21): 2755–66. Дои:10.1101 / gad.11.21.2755. PMID 9353246.
- ^ а б Эдмондс, М. (2002). История последовательностей поли А: от образования к факторам, чтобы функционировать. Прогресс в исследованиях нуклеиновых кислот и молекулярной биологии. 71. С. 285–389. Дои:10.1016 / S0079-6603 (02) 71046-5. ISBN 978-0-12-540071-8. PMID 12102557.
- ^ Эдмондс М., Воан М.Х., Наказато Х. (июнь 1971 г.). «Последовательности полиадениловой кислоты в гетерогенной ядерной РНК и быстро меченой полирибосомной РНК клеток HeLa: возможное свидетельство предшественника связи». Труды Национальной академии наук Соединенных Штатов Америки. 68 (6): 1336–40. Bibcode:1971ПНАС ... 68.1336Е. Дои:10.1073 / пнас.68.6.1336. ЧВК 389184. PMID 5288383.
дальнейшее чтение
- Danckwardt S, Hentze MW, Kulozik AE (февраль 2008 г.). «Обработка 3'-конца мРНК: молекулярные механизмы и последствия для здоровья и болезней». Журнал EMBO. 27 (3): 482–98. Дои:10.1038 / sj.emboj.7601932. ЧВК 2241648. PMID 18256699.
внешние ссылки
 СМИ, связанные с Полиаденилирование в Wikimedia Commons
СМИ, связанные с Полиаденилирование в Wikimedia Commons
