Транскрипция (биология) - Transcription (biology)

Транскрипция это первый из нескольких шагов ДНК на основании экспрессия гена в котором конкретный сегмент ДНК копируется в РНК (особенно мРНК ) посредством фермент РНК-полимераза.
И ДНК, и РНК являются нуклеиновых кислот, которые используют пар оснований из нуклеотиды как дополнительный язык. Во время транскрипции последовательность ДНК считывается РНК-полимеразой, которая производит комплементарный антипараллельный Нить РНК называется первичная стенограмма.
Транскрипция происходит в следующих общих шагах:
- РНК-полимераза вместе с одним или несколькими общие факторы транскрипции, привязан к промоторная ДНК.
- РНК-полимераза генерирует пузырь транскрипции, который разделяет две нити спирали ДНК. Это делается путем нарушения водородные связи между комплементарными нуклеотидами ДНК.
- РНК-полимераза добавляет РНК нуклеотиды (которые комплементарны нуклеотидам одной цепи ДНК).
- Сахарно-фосфатный остов РНК формируется с помощью РНК-полимеразы с образованием цепи РНК.
- Водородные связи спирали РНК – ДНК разрываются, освобождая вновь синтезированную цепь РНК.
- Если в ячейке есть ядро, РНК может быть подвергнута дальнейшей обработке. Это может включать полиаденилирование, укупорка, и сращивание.
- РНК может оставаться в ядре или выходить в цитоплазма сквозь ядерная пора сложный.
Участок ДНК, транскрибируемый в молекулу РНК, называется блок транскрипции и кодирует хотя бы один ген. Если ген кодирует белок, транскрипция производит информационная РНК (мРНК); мРНК, в свою очередь, служит шаблоном для синтеза белка посредством перевод. Альтернативно, транскрибируемый ген может кодировать некодирующая РНК такие как микроРНК, рибосомальная РНК (рРНК), переносить РНК (тРНК) или ферментативные молекулы РНК, называемые рибозимы.[1] В целом РНК помогает синтезировать, регулировать и обрабатывать белки; поэтому он играет фундаментальную роль в выполнении функций в ячейка.
В вирусология, этот термин также может использоваться в отношении синтеза мРНК из молекулы РНК (то есть репликации РНК). Например, геном отрицательногосмысл Одноцепочечная РНК (оцРНК -) вируса может быть матрицей для положительно-смысловой одноцепочечной РНК (оцРНК +)[требуется разъяснение ]. Это связано с тем, что положительно-смысловая цепь содержит информацию, необходимую для трансляции вирусных белков для вирусная репликация потом. Этот процесс катализируется вирусным РНК-репликаза.[2][требуется разъяснение ]
Задний план
Единица транскрипции ДНК, кодирующая белок, может содержать как кодирующая последовательность, который будет переведен в белок, и регуляторные последовательности, которые направляют и регулируют синтез этого белка. Регуляторная последовательность перед ("вверх по течению "из) кодирующая последовательность называется пять основных непереведенных регионов (5'UTR); последовательность после ("вниз по течению "из) кодирующая последовательность называется три основных непереведенных региона (3'UTR).[1]
В отличие от Репликация ДНК, транскрипция приводит к РНК-комплементу, который включает нуклеотид урацил (U) во всех случаях, когда тимин (T) произошел бы в дополнении ДНК.
Только одна из двух цепей ДНК служит шаблоном для транскрипции. В антисмысловой цепь ДНК читается РНК-полимеразой от 3 'конца до 5' конца во время транскрипции (3 '→ 5'). Комплементарная РНК создается в противоположном направлении, в направлении 5 '→ 3', что соответствует последовательности смысловой цепи, за исключением замены урацила на тимин. Эта направленность обусловлена тем, что РНК-полимераза может добавлять нуклеотиды только к 3'-концу растущей цепи мРНК. Такое использование только цепи ДНК 3 '→ 5' устраняет необходимость в Фрагменты Окадзаки которые видны в репликации ДНК.[1] Это также устраняет необходимость в Праймер РНК для инициирования синтеза РНК, как в случае репликации ДНК.
В не-шаблонная (смысловая) цепь ДНК называется кодирующая нить, потому что его последовательность такая же, как и вновь созданный транскрипт РНК (за исключением замены тимина на урацил). Это нить, которая используется по соглашению при представлении последовательности ДНК.[3]
Транскрипция имеет некоторые механизмы проверки, но они менее эффективны и менее эффективны, чем средства контроля для копирования ДНК. В результате транскрипция имеет более низкую точность копирования, чем репликация ДНК.[4]
Основные шаги
Транскрипция делится на инициация, побег промоутера, удлинение и прекращение.[5]
Инициация
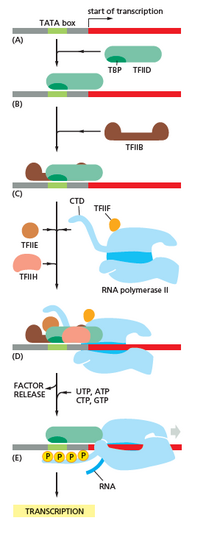
Транскрипция начинается со связывания РНК-полимеразы вместе с одним или несколькими общие факторы транскрипции, к конкретной последовательности ДНК, называемой "промоутер "с образованием" замкнутого комплекса "РНК-полимераза-промотор. В" замкнутом комплексе "промоторная ДНК все еще является полностью двухцепочечной.[5]
Затем РНК-полимераза с помощью одного или нескольких общих факторов транскрипции раскручивает приблизительно 14 пар оснований ДНК с образованием «открытого комплекса» РНК-полимераза-промотор. В «открытом комплексе» промоторная ДНК частично разматывается и является одноцепочечной. Открытая одноцепочечная ДНК называется «пузырем транскрипции».[5]
РНК-полимераза с помощью одного или нескольких общих факторов транскрипции затем выбирает сайт начала транскрипции в пузыре транскрипции связывается с инициирующим NTP и расширение NTP (или короткая РНК грунтовка и удлиняющий NTP), комплементарный последовательности сайта начала транскрипции, и катализирует образование связи с получением исходного продукта РНК.[5]
В бактерии, РНК-полимераза холоэнзим состоит из пяти субъединиц: 2 субъединиц α, 1 субъединицы β, 1 субъединицы β 'и 1 субъединицы ω. У бактерий есть один общий фактор транскрипции РНК, известный как фактор сигма. Фермент ядра РНК-полимеразы связывается с бактериальным фактором общей транскрипции (сигма) с образованием холофермента РНК-полимеразы, а затем связывается с промотором.[5](РНК-полимераза называется холоферментом, когда сигма-субъединица присоединена к ферменту ядра, который состоит из 2 субъединиц α, 1 субъединицы β, только 1 субъединицы β ').
В археи и эукариоты, РНК-полимераза содержит субъединицы гомологичный к каждой из пяти субъединиц РНК-полимеразы в бактериях, а также содержит дополнительные субъединицы. У архей и эукариот функции общего бактериального фактора транскрипции сигма выполняются множеством общих факторов транскрипции, которые работают вместе.[5] У архей есть три основных фактора транскрипции: TBP, TFB, и TFE. У эукариот, у РНК-полимераза II -зависимая транскрипция, существует шесть общих факторов транскрипции: TFIIA, TFIIB (ан ортолог архейного ТФБ), TFIID (фактор мультисубъединицы, в котором ключевая субъединица, TBP, является ортолог архей TBP), TFIIE (ан ортолог архейного ТТИ), ТФИИФ, и TFIIH. TFIID - это первый компонент, связывающийся с ДНК из-за связывания TBP, тогда как TFIIH - последний компонент, который будет задействован. У архей и эукариот закрытый комплекс РНК-полимераза-промотор обычно называют "преинициативный комплекс."[6]
Инициирование транскрипции регулируется дополнительными белками, известными как активаторы и репрессоры, и, в некоторых случаях, связанные коактиваторы или корепрессоры, которые модулируют образование и функцию комплекса инициации транскрипции.[5]
Побег промоутера
После того, как первая связь синтезирована, РНК-полимераза должна покинуть промотор. В течение этого времени наблюдается тенденция к высвобождению транскрипта РНК и образованию усеченных транскриптов. Это называется неудачное начало, и является общим как для эукариот, так и для прокариот.[7] Прерванная инициация продолжается до тех пор, пока не будет синтезирован продукт РНК с пороговой длиной приблизительно 10 нуклеотидов, после чего происходит ускользание промотора и образование комплекса элонгации транскрипции.
Механически выход промотора происходит через Скручивание ДНК, обеспечивая энергию, необходимую для разрыва взаимодействия между холоферментом РНК-полимеразы и промотором.[8]
У бактерий исторически считалось, что фактор сигма определенно высвобождается после очистки промотора. Эта теория была известна как модель обязательного выпуска. Однако более поздние данные показали, что после и после удаления промотора сигма-фактор высвобождается в соответствии с стохастическая модель известный как стохастическая модель выпуска.[9]
У эукариот на промоторе, зависимом от РНК-полимеразы II, после клиренса промотора TFIIH фосфорилирует серин 5 на карбоксиконцевом домене РНК-полимеразы II, что приводит к рекрутированию кэпирующего фермента (CE).[10][11] Точный механизм того, как CE вызывает клиренс промотора у эукариот, пока не известен.
Удлинение

Одна нить ДНК, шаблон прядь (или некодирующая цепь), используется в качестве матрицы для синтеза РНК. По мере того как транскрипция продолжается, РНК-полимераза пересекает цепочку матрицы и использует комплементарность спаривания оснований с шаблоном ДНК для создания копии РНК (которая удлиняется во время обхода). Хотя РНК-полимераза пересекает матричную цепь от 3 '→ 5', кодирующая (не матричная) цепь и вновь образованная РНК также могут использоваться в качестве контрольных точек, поэтому транскрипцию можно описать как происходящую 5 '→ 3'. Это дает молекулу РНК из 5 '→ 3', точную копию кодирующей цепи (за исключением того, что тимин заменены на урацилы, а нуклеотиды состоят из рибозного (5-углеродного) сахара, где ДНК содержит дезоксирибозу (на один атом кислорода меньше) в сахарно-фосфатном скелете).[нужна цитата ]
Транскрипция мРНК может включать несколько РНК-полимераз на одной матрице ДНК и несколько раундов транскрипции (амплификация определенной мРНК), поэтому из одной копии гена можно быстро получить множество молекул мРНК.[нужна цитата ] Характерные скорости удлинения у прокариот и эукариот составляют около 10-100 нт / сек.[12] Однако у эукариот нуклеосомы действуют как основные препятствия для транскрипции полимераз во время удлинения транскрипции.[13][14] У этих организмов пауза, индуцированная нуклеосомами, может регулироваться факторами удлинения транскрипции, такими как TFIIS.[14]
Удлинение также включает в себя механизм корректуры, который может заменить неправильно встроенные основы. У эукариот это может соответствовать коротким паузам во время транскрипции, которые позволяют соответствующим факторам редактирования РНК связываться. Эти паузы могут быть характерны для РНК-полимеразы или из-за структуры хроматина.[нужна цитата ]
Прекращение
Бактерии используют две разные стратегии терминации транскрипции - Rho-независимое завершение и Rho-зависимое завершение. В Rho-независимое прекращение транскрипции, Транскрипция РНК останавливается, когда вновь синтезированная молекула РНК образует G-C-богатый петля для шпильки за которым следует бег Нас. Когда образуется шпилька, механическое напряжение разрывает слабые связи rU-dA, заполняя гибрид ДНК-РНК. Это вытягивает транскрипт поли-U из активного сайта РНК-полимеразы, завершая транскрипцию. В "Rho-зависимом" типе терминации белковый фактор, называемый "Ро «дестабилизирует взаимодействие между матрицей и мРНК, высвобождая вновь синтезированную мРНК из комплекса элонгации.[15]
Терминация транскрипции у эукариот менее изучена, чем у бактерий, но включает расщепление нового транскрипта с последующим независимым от матрицы добавлением аденинов на его новом 3'-конце в процессе, называемом полиаденилирование.[16]
Роль РНК-полимеразы в посттранскрипционных изменениях РНК
РНК-полимераза играет очень важную роль на всех этапах, включая посттранскрипционные изменения в РНК.
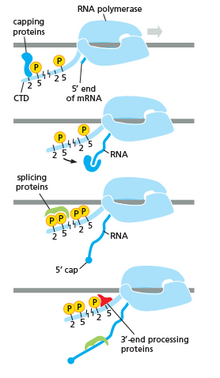
Как показано на изображении справа, вы можете видеть, что CTD (C Terminal Domain) - это хвост, который меняет свою форму, и затем этот хвост будет использоваться в качестве носителя для сращивания, закрытия и полиаденилирование. что мы видим на изображении слева.[17]
Ингибиторы
Ингибиторы транскрипции можно использовать в качестве антибиотики против, например, патогенные бактерии (антибактериальные препараты ) и грибы (противогрибковые ). Примером такого антибактериального средства является рифампицин, что подавляет бактериальная транскрипция ДНК в мРНК путем ингибирования ДНК-зависимых РНК-полимераза путем связывания своей бета-субъединицы, а 8-гидроксихинолин является противогрибковым ингибитором транскрипции.[18] Эффекты метилирование гистонов также может подавлять действие транскрипции. Сильные, биоактивные природные продукты, такие как триптолид, которые ингибируют транскрипцию млекопитающих посредством ингибирования субъединицы XPB общего фактора транскрипции TFIIH, недавно были описаны в качестве конъюгата глюкозы для нацеливания на гипоксические раковые клетки с повышенной экспрессией переносчика глюкозы.[19]
Эндогенные ингибиторы
У позвоночных большинство генов промоутеры содержать Остров CpG с многочисленными CpG сайты.[20] Когда многие из промоторных сайтов CpG гена метилированный ген становится подавленным (заглушенным).[21] Колоректальный рак обычно бывает от 3 до 6. Водитель мутации и от 33 до 66 автостопщик или пассажирские мутации.[22] Однако подавление транскрипции (молчание) может иметь большее значение, чем мутации, в развитии рака. Например, при колоректальном раке от 600 до 800 генов транскрипционно ингибируются метилированием CpG-островков (см. регуляция транскрипции при раке ). Репрессия транскрипции при раке также может происходить другими эпигенетический механизмы, такие как измененное выражение микроРНК.[23] При раке груди подавление транскрипции BRCA1 может происходить чаще из-за сверхэкспрессии микроРНК-182, чем из-за гиперметилирования промотора BRCA1 (см. Низкая экспрессия BRCA1 при раке груди и яичников ).
Фабрики транскрипции
Активные единицы транскрипции сгруппированы в ядре в дискретных сайтах, называемых фабрики транскрипции или эухроматин. Такие сайты можно визуализировать, позволив задействованным полимеразам расширить свои транскрипты в помеченных предшественниках (Br-UTP или Br-U) и пометив иммуно-меченую растущую РНК. Фабрики транскрипции также могут быть локализованы с помощью флуоресцентной гибридизации in situ или помечены антителами, направленными против полимераз. В нуклеоплазме человека насчитывается ~ 10 000 фабрик. HeLa клетка, среди которых ~ 8000 фабрик полимеразы II и ~ 2000 фабрик полимеразы III. Каждая фабрика полимеразы II содержит ~ 8 полимераз. Поскольку наиболее активные единицы транскрипции связаны только с одной полимеразой, каждая фабрика обычно содержит ~ 8 различных единиц транскрипции. Эти единицы могут быть связаны через промоторы и / или энхансеры, при этом петли образуют «облако» вокруг фактора.[24]
История
Молекула, позволяющая реализовать генетический материал в виде белка, была впервые выдвинута гипотезой Франсуа Жакоб и Жак Моно. Северо-Очоа Выиграл Нобелевская премия по физиологии и медицине в 1959 г. за разработку процесса синтеза РНК in vitro с полинуклеотидфосфорилаза, что было полезно для взлома генетический код. Синтез РНК РНК-полимераза было установлено in vitro несколькими лабораториями к 1965 г .; однако РНК, синтезируемая этими ферментами, обладала свойствами, которые предполагали существование дополнительного фактора, необходимого для правильного завершения транскрипции.[нужна цитата ]
В 1972 г. Уолтер Фирс стал первым человеком, который на самом деле доказал существование терминирующего фермента.
Роджер Д. Корнберг выиграл 2006 Нобелевская премия по химии "за исследования молекулярных основ эукариотическая транскрипция ".[25]
Измерение и обнаружение
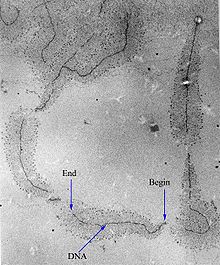
Транскрипцию можно измерить и обнаружить разными способами:[нужна цитата ]
- Кассета G-Less анализ транскрипции: измеряет силу промотора
- Транскрипция второго тура анализ: определяет сайты начала транскрипции (TSS)
- Ядерная отработка анализ: измеряет относительное количество вновь образованных транскриптов
- KAS-seq: измеряет одноцепочечную ДНК, генерируемую РНК-полимеразами; может работать с 1000 ячеек.[26]
- Анализ защиты от РНКазы и ЧИП-Чип из RNAP: обнаружение активных сайтов транскрипции
- ОТ-ПЦР: измеряет абсолютное содержание общей или ядерной РНК, которое, однако, может отличаться от скорости транскрипции.
- ДНК-микрочипы: измеряет относительное содержание глобальных уровней общей или ядерной РНК; однако они могут отличаться от показателей транскрипции
- Гибридизация in situ: определяет наличие стенограммы
- Теги MS2: путем включения РНК стержневые петли, такие как MS2, в ген, они включаются во вновь синтезированную РНК. Затем петли ствола могут быть обнаружены с помощью слияния GFP и белка оболочки MS2, который имеет высокое сродство, специфичное для последовательности взаимодействие с петлями ствола MS2. Рекрутирование GFP в сайт транскрипции визуализируется как единое флуоресцентное пятно. Этот новый подход показал, что транскрипция происходит прерывистыми пакетами или импульсами (см. Транскрипционный разрыв ). За заметным исключением методов in situ, большинство других методов обеспечивают средние значения клеточной популяции и не способны обнаружить это фундаментальное свойство генов.[27]
- Нозерн-блот: традиционный метод, и до появления РНК-Seq, самый количественный
- РНК-Seq: применяет методы секвенирования следующего поколения для секвенирования всего транскриптомы, что позволяет измерять относительное количество РНК, а также обнаруживать дополнительные вариации, такие как гены слияния, посттранскрипционные правки и новые сайты сплайсинга.
- Одноклеточная РНК-Seq: амплифицирует и считывает частичные транскриптомы из изолированных клеток, что позволяет проводить подробный анализ РНК в тканях, эмбрионах и раковых опухолях
Обратная транскрипция
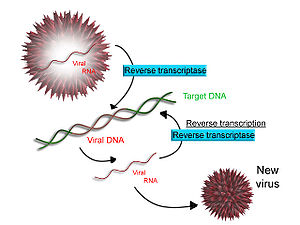
Немного вирусы (такие как ВИЧ, причина СПИД ), обладают способностью транскрибировать РНК в ДНК. У ВИЧ есть геном РНК, который обратная расшифровка в ДНК. Полученная ДНК может быть объединена с геномом ДНК клетки-хозяина. Главный фермент, отвечающий за синтез ДНК из матрицы РНК, называется обратная транскриптаза.
В случае ВИЧ обратная транскриптаза отвечает за синтез комплементарная ДНК цепь (кДНК) в геном вирусной РНК. Фермент рибонуклеаза H затем переваривает цепь РНК, и обратная транскриптаза синтезирует комплементарную цепь ДНК с образованием двойной спиральной структуры ДНК («кДНК»). КДНК интегрируется в геном клетки-хозяина ферментом интегрировать, который заставляет клетку-хозяин генерировать вирусные белки, которые собираются в новые вирусные частицы. В случае ВИЧ после этого клетка-хозяин подвергается запрограммированной гибели клетки, или апоптоз из Т-клетки.[28] Однако у других ретровирусов клетка-хозяин остается неповрежденной, когда вирус выходит из клетки.
Некоторые эукариотические клетки содержат фермент с активностью обратной транскрипции, называемый теломераза. Теломераза - это обратная транскриптаза, удлиняющая концы линейных хромосом. Теломераза несет матрицу РНК, из которой она синтезирует повторяющуюся последовательность ДНК, или «мусорную» ДНК. Эта повторяющаяся последовательность ДНК называется теломер и его можно рассматривать как «шапку» для хромосомы. Это важно, потому что каждый раз, когда удваивается линейная хромосома, она укорачивается. С помощью этой «мусорной» ДНК или «крышки» на концах хромосом сокращение устраняет некоторую несущественную повторяющуюся последовательность, а не последовательность ДНК, кодирующую белок, которая находится дальше от конца хромосомы.
Теломераза часто активируется в раковых клетках, чтобы раковые клетки могли бесконечно дублировать свои геномы без потери важной последовательности ДНК, кодирующей белок. Активация теломеразы может быть частью процесса, который позволяет раковым клеткам становиться бессмертный. Фактор бессмертия рака за счет удлинения теломер за счет теломеразы, как было доказано, встречается в 90% всех канцерогенных опухолей. in vivo оставшиеся 10% используют альтернативный способ поддержания теломер, называемый ALT или альтернативное удлинение теломер.[29]
Смотрите также
- Жизнь
- Клетка (биология)
- Деление клеток
- ген
- генная регуляция
- экспрессия гена
- Эпигенетика
- Геном
- Центральная догма Крика, в котором продукт транскрипции, мРНК, является переведено формировать полипептиды, и где утверждается, что обратные процессы никогда не происходят
- Генная регуляция
- Длинная некодирующая РНК
- Миссенс мРНК
- Сращивание - процесс удаления интроны из предшественника матричной РНК (пре-мРНК ), чтобы сделать РНК-мессенджер (мРНК )
- Транскриптомика
- Перевод (биология)
использованная литература
- ^ а б c Эльдра П. Соломон, Линда Р. Берг, Дайана В. Мартин. Биология, 8-е издание, международное студенческое издание. Томсон Брукс / Коул. ISBN 978-0495317142
- ^ Кунин Е.В., Горбаленя А.Е., Чумаков К.М. (июль 1989 г.). «Предварительная идентификация РНК-зависимых РНК-полимераз вирусов дцРНК и их отношения к вирусным полимеразам с положительной цепью РНК». Письма FEBS. 252 (1–2): 42–6. Дои:10.1016/0014-5793(89)80886-5. PMID 2759231. S2CID 36482110.
- ^ «Нити ДНК». www.sci.sdsu.edu. В архиве из оригинала 27 октября 2017 г.. Получено 1 мая 2018.
- ^ Берг Дж., Тимочко Дж. Л., Страйер Л. (2006). Биохимия (6-е изд.). Сан-Франциско: В. Х. Фриман. ISBN 0-7167-8724-5.
- ^ а б c d е ж г Уотсон Дж. Д., Бейкер Т. А., Белл С. П., Ганн А. А., Левин М., Лосик Р. М. (2013). Молекулярная биология гена (7-е изд.). Пирсон.
- ^ Рёдер, Роберт Г. (1991). «Сложности инициации эукариотической транскрипции: регуляция сборки преинициационного комплекса». Тенденции в биохимических науках. 16 (11): 402–408. Дои:10.1016 / 0968-0004 (91) 90164-Q. ISSN 0968-0004. PMID 1776168.
- ^ Гольдман С.Р., Ebright RH, Nickels BE (май 2009 г.). «Прямое обнаружение абортивных транскриптов РНК in vivo». Наука. 324 (5929): 927–8. Bibcode:2009Sci ... 324..927G. Дои:10.1126 / science.1169237. ЧВК 2718712. PMID 19443781.
- ^ Ревякин А., Лю С., Эбрайт Р.Х., Стрик Т.Р. (ноябрь 2006 г.). «Прерывистая инициация и продуктивная инициация с помощью РНК-полимеразы включают сжатие ДНК». Наука. 314 (5802): 1139–43. Bibcode:2006Научный ... 314.1139R. Дои:10.1126 / science.1131398. ЧВК 2754787. PMID 17110577.
- ^ Raffaelle M, Kanin EI, Vogt J, Burgess RR, Ansari AZ (ноябрь 2005 г.). «Переключение голоферментов и стохастическое высвобождение сигма-факторов из РНК-полимеразы in vivo». Молекулярная клетка. 20 (3): 357–66. Дои:10.1016 / j.molcel.2005.10.011. PMID 16285918.
- ^ Мандал СС, Чу С., Вада Т., Ханда Х., Шаткин А.Дж., Рейнберг Д. (май 2004 г.). «Функциональные взаимодействия РНК-кэпирующего фермента с факторами, которые положительно и отрицательно регулируют ускользание промотора с помощью РНК-полимеразы II». Труды Национальной академии наук Соединенных Штатов Америки. 101 (20): 7572–7. Bibcode:2004ПНАС..101.7572М. Дои:10.1073 / pnas.0401493101. ЧВК 419647. PMID 15136722.
- ^ Гудрич Дж. А., Тьян Р. (апрель 1994 г.). «Факторы транскрипции IIE и IIH и прямой клиренс промотора гидролиза АТФ с помощью РНК-полимеразы II». Ячейка. 77 (1): 145–56. Дои:10.1016/0092-8674(94)90242-9. PMID 8156590. S2CID 24602504.
- ^ Майло, Рон; Филипс, Роб. «Клеточная биология в цифрах: что быстрее, транскрипция или перевод?». book.bionumbers.org. В архиве с оригинала 20 апреля 2017 г.. Получено 8 марта 2017.
- ^ Ходжес С., Бинту Л., Любковска Л., Кашлев М., Бустаманте С. (июль 2009 г.). «Нуклеосомные колебания определяют динамику транскрипции РНК-полимеразы II». Наука. 325 (5940): 626–8. Bibcode:2009Sci ... 325..626H. Дои:10.1126 / science.1172926. ЧВК 2775800. PMID 19644123.
- ^ а б Фитц В., Шин Дж., Эрлих С., Фарнунг Л., Крамер П., Забурдаев В., Гриль С.В. (2016). «Расположение нуклеосом влияет на динамику транскрипции одиночных молекул». Труды Национальной академии наук. 113 (45): 12733–12738. Дои:10.1073 / pnas.1602764113. ЧВК 5111697. PMID 27791062.
- ^ Ричардсон JP (сентябрь 2002 г.). «Rho-зависимая терминация и АТФазы в терминации транскрипта». Biochimica et Biophysica Acta (BBA) - Структура и экспрессия гена. 1577 (2): 251–260. Дои:10.1016 / S0167-4781 (02) 00456-6. PMID 12213656.
- ^ Lykke-Andersen S, Jensen TH (октябрь 2007 г.). «Перекрывающиеся пути диктуют прекращение транскрипции РНК-полимеразы II». Биохимия. 89 (10): 1177–82. Дои:10.1016 / j.biochi.2007.05.007. PMID 17629387.
- ^ Cramer, P .; Armache, K.-J .; Баумли, С .; Benkert, S .; Brueckner, F .; Buchen, C .; Damsma, G.E .; Dengl, S .; Гейгер, С.Р .; Jasiak, A.J .; Джавари, А. (июнь 2008 г.). «Структура эукариотических РНК-полимераз». Ежегодный обзор биофизики. 37 (1): 337–352. Дои:10.1146 / annurev.biophys.37.032807.130008. ISSN 1936-122X.
- ^ Информация о 8-гидроксихинолине от СИГМА-ОЛЬДРИХ. Дата обращения: февраль 2012 г.
- ^ Датан Э, Минн И, Пэн Х, Хе КЛ, Ан Х, Ю Б., Помпер М.Г., Лю Джо (2020). «Конъюгат глюкоза-триптолид селективно поражает раковые клетки в условиях гипоксии». iScience. 23 (9). Дои:10.1016 / j.isci.2020.101536. PMID 33083765.
- ^ Саксонов С., Берг П., Брутлаг Д.Л. (январь 2006 г.). «Полногеномный анализ динуклеотидов CpG в геноме человека позволяет выделить два различных класса промоторов». Труды Национальной академии наук Соединенных Штатов Америки. 103 (5): 1412–7. Bibcode:2006ПНАС..103.1412С. Дои:10.1073 / pnas.0510310103. ЧВК 1345710. PMID 16432200.
- ^ Птица А (январь 2002 г.). «Паттерны метилирования ДНК и эпигенетическая память». Гены и развитие. 16 (1): 6–21. Дои:10.1101 / gad.947102. PMID 11782440.
- ^ Фогельштейн Б., Пападопулос Н., Велкулеску В.Э., Чжоу С., Диас Л.А., Кинзлер К.В. (март 2013 г.). «Пейзажи генома рака». Наука. 339 (6127): 1546–58. Bibcode:2013Научный ... 339.1546V. Дои:10.1126 / наука.1235122. ЧВК 3749880. PMID 23539594.
- ^ Tessitore A, Cicciarelli G, Del Vecchio F, Gaggiano A, Verzella D, Fischietti M, Vecchiotti D, Capece D, Zazzeroni F, Alesse E (2014). «МикроРНК в сети повреждения / восстановления ДНК и рака». Международный журнал геномики. 2014: 820248. Дои:10.1155/2014/820248. ЧВК 3926391. PMID 24616890.
- ^ Папантонис А., Кохро Т., Бабу С., Ларкин Дж. Д., Дэн Б., Шорт П, Цуцуми С., Тейлор С., Канки Й, Кобаяши М., Ли Дж., По Х. М., Руан Х, Абуратани Х, Руан Й, Кодама Т., Вада Й , Cook PR (ноябрь 2012 г.). «TNFα передает сигналы через специализированные фабрики, где транскрибируются ответные кодирующие гены и гены miRNA». Журнал EMBO. 31 (23): 4404–14. CiteSeerX 10.1.1.919.1919. Дои:10.1038 / emboj.2012.288. ЧВК 3512387. PMID 23103767.
- ^ «Химия 2006». Нобелевский фонд. В архиве с оригинала 15 марта 2007 г.. Получено 29 марта, 2007.
- ^ Ву, Т. (апрель 2020 г.). «Секвенирование одноцепочечной ДНК с помощью кетоксала фиксирует глобальную динамику транскрипции и активность энхансера in situ». Природные методы. 17 (5): 515–523. Дои:10.1038 / s41592-020-0797-9. S2CID 214810294.
- ^ Радж А., ван Ауденаарден А. (октябрь 2008 г.). «Природа, воспитание или случай: стохастическая экспрессия генов и ее последствия». Ячейка. 135 (2): 216–26. Дои:10.1016 / j.cell.2008.09.050. ЧВК 3118044. PMID 18957198.
- ^ Колесникова И.Н. (2000). «Некоторые закономерности механизма апоптоза при ВИЧ-инфекции». Диссертация (по-русски). В архиве из оригинала 10 июля 2011 г.. Получено 20 февраля, 2011.
- ^ Чезаре А.Дж., Реддел Р.Р. (май 2010 г.). «Альтернативное удлинение теломер: модели, механизмы и последствия». Природа Обзоры Генетика. 11 (5): 319–30. Дои:10.1038 / nrg2763. PMID 20351727. S2CID 19224032.
внешние ссылки
- Интерактивное Java-моделирование инициации транскрипции. От Центр моделей жизни в Институте Нильса Бора.
- Интерактивное Java-моделирование интерференции транскрипции - игра доминирования промотора в бактериальном вирусе. От Центр моделей жизни в Институте Нильса Бора.
- Коллекция анимации виртуальной клетки, введение в транскрипцию
