Ядерная пора - Nuclear pore
| Ядерная пора | |
|---|---|
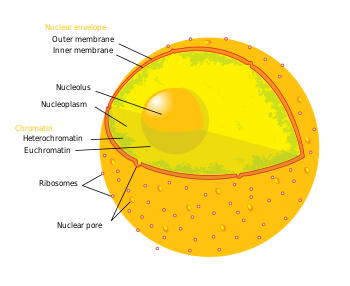 Схема ядра клетки человека. Ядерная пора обозначена внизу слева | |
 Ядерная пора. Вид сбоку. 1. Ядерная оболочка. 2. Наружное кольцо. 3. Спицы. 4. Корзина. 5. Нити. (Рисунок основан на изображениях, полученных с помощью электронной микроскопии) | |
| Подробности | |
| Идентификаторы | |
| латинский | Порус ядерный |
| MeSH | D022022 |
| TH | H1.00.01.2.01005 |
| FMA | 63148 |
| Анатомическая терминология | |
А ядерная пора является частью большого комплекс белков, известный как ядерный поровый комплекс что охватывает ядерная оболочка, что является двойным мембрана окружающий эукариотический ядро клетки. В ядерной оболочке клетки позвоночного имеется около 1000 комплексов ядерных пор (NPC), но это зависит от типа клетки и стадии жизненного цикла.[1] Комплекс ядерных пор человека (hNPC) представляет собой 110 мегадальтон (MDa) структура. Белки, составляющие комплекс ядерных пор, известны как нуклеопорины; каждый NPC содержит по крайней мере 456 отдельных белковых молекул и состоит из 34 различных белков нуклеопоринов.[2]Около половины нуклеопоринов обычно содержат соленоидные белковые домены - либо альфа соленоид или бета-винт сложить, или в некоторых случаях оба как отдельные структурные области. Другая половина демонстрирует структурные характеристики, типичные для «естественно развернутых» или внутренне неупорядоченные белки, то есть это очень гибкие белки, не имеющие упорядоченной третичной структуры.[3] Эти неупорядоченные белки являются FG нуклеопорины, названные так потому, что их аминокислотная последовательность содержит много фенилаланин —глицин повторяется.[4]
Комплексы ядерных пор позволяют переносить молекулы через ядерную оболочку. Этот транспорт включает РНК и рибосомальный белки, перемещающиеся из ядра в цитоплазму и белки (Такие как ДНК-полимераза и ламины ), углеводы, сигнальные молекулы и липиды движется в ядро. Примечательно, что ядерный поровый комплекс (NPC) могут активно проводить 1000 транслокаций за комплекс в секунду. Хотя молекулы меньшего размера просто размытый через поры более крупные молекулы могут распознаваться специфическими сигнальными последовательностями и затем диффундировать с помощью нуклеопорины в ядро или из него. Недавно было показано, что эти нуклеопорины имеют специфические эволюционно консервативные особенности, закодированные в их последовательностях, которые дают представление о том, как они регулируют транспорт молекул через ядерную пору.[5][6] Опосредованный нуклеопорином транспорт не требует непосредственной энергии, но зависит от градиентов концентрации, связанных с Цикл RAN. Каждая из восьми белковых субъединиц, окружающих настоящую пору (внешнее кольцо), проецирует белок в форме спиц над каналом поры. Центр поры часто имеет структуру, похожую на пробку. Пока неизвестно, соответствует ли это реальной пробке или это просто груз, пойманный в пути.
Размер и сложность
Весь комплекс ядерных пор у позвоночных имеет диаметр около 120 нанометров.[7] Диаметр канала у человека составляет от 5,2 нанометра.[8] до 10,7 нм у лягушки Xenopus laevis, глубиной примерно 45 нм.[9] мРНК, которая является одноцепочечной, имеет толщину примерно от 0,5 до 1 нм.[10] В молекулярная масса NPC млекопитающих составляет около 124 мегадальтон (МДа)[11] и он содержит примерно 30 различных белковых компонентов, каждый в нескольких копиях.[12] В отличие от дрожжей Saccharomyces cerevisiae меньше, с массой всего 66 МДа.[13]
Транспорт через ядерный поровый комплекс

Мелкие частицы (до 30–60 кДа ) способны проходить через комплекс ядерных пор путем пассивной диффузии.[14][15] Более крупные частицы также способны пассивно диффундировать через поры большого диаметра со скоростью, которая постепенно уменьшается с увеличением молекулярной массы. Для эффективного прохождения комплекса требуется несколько белковых факторов,[16] и, в частности, рецепторы ядерного транспорта которые связываются с молекулами груза и опосредуют их перемещение через NPC либо в ядро (importins ) или вне (Exportins ). Самым большим семейством ядерных транспортных рецепторов являются кариоферины, который включает в себя десятки импортинов и экспортинов; это семейство далее подразделяется на подсемейства кариоферин-α и кариоферин-β. Другие рецепторы ядерного транспорта включают NTF2 и некоторые NTF2-подобные белки.
Для объяснения механизма транслокации были предложены три модели:
- Градиенты сходства вдоль центральной пробки
- Броуновское сродство
- Избирательная фаза
Импорт белков
Любой груз с сигнал ядерной локализации (NLS) будут предназначены для быстрой и эффективной транспортировки через поры. Известно несколько последовательностей NLS, обычно содержащих консервативную последовательность с основными остатками, такими как ПКККРКВ. Любой материал с NLS будет приниматься импортинами в ядро.
Классическая схема импорта NLS-белка начинается с первого связывания импортина-α с последовательностью NLS, которая затем действует как мост для прикрепления импортина-β. Комплекс импортинβ-импортинα-груз затем направляется к ядерной поре и диффундирует через нее. Как только комплекс оказывается в ядре, RanGTP связывается с Importin-β и вытесняет его из комплекса. Тогда белок предрасположенности к апоптозу (CAS), экспортин, который в ядре связан с RanGTP, вытесняет Importin-α из груза. Таким образом, белок NLS свободен в нуклеоплазме. Комплекс Importinβ-RanGTP и Importinα-CAS-RanGTP диффундирует обратно в цитоплазму, где GTP гидролизуются до GDP, что приводит к высвобождению Importinβ и Importinα, которые становятся доступными для нового раунда импорта NLS-белка.
Хотя груз проходит через поры с помощью белков-шаперонов, перемещение через поры не зависит от энергии. Однако весь цикл импорта требует гидролиза 2 ГТФ и, таким образом, зависит от энергии и должен рассматриваться как активный транспорт. Цикл импорта приводится в действие нуклео-цитоплазматическим градиентом RanGTP. Этот градиент возникает из-за исключительной ядерной локализации RanGEFs, белков, которые обменивают GDP на GTP на молекулах Ran. Таким образом, в ядре наблюдается повышенная концентрация RanGTP по сравнению с цитоплазмой.
Экспорт белков
Некоторые молекулы или макромолекулярные комплексы необходимо экспортировать из ядра в цитоплазму, как и рибосома подразделения и информационные РНК. Таким образом, существует механизм экспорта, аналогичный механизму импорта.
В классической схеме экспорта белки с последовательность ядерного экспорта (NES) может связываться в ядре с образованием гетеротримерного комплекса с экспортином и RanGTP (например, экспортином CRM1). Затем комплекс может диффундировать в цитоплазму, где гидролизуется GTP и высвобождается NES-белок. CRM1-RanGDP распространяется обратно в ядро, где GDP обменивается на GTP с помощью RanGEF. Этот процесс также зависит от энергии, поскольку он потребляет один GTP. Экспорт с помощью exportin CRM1 может быть запрещен Лептомицин Б.
Экспорт РНК
Существуют разные пути экспорта через NPC для каждого РНК класс, который существует. Экспорт РНК также опосредуется сигналом (NES); NES находится в РНК-связывающих белках (за исключением тРНК, у которой нет адаптера). Примечательно, что все вирусные РНК и клеточные РНК (тРНК, рРНК, U мяРНК, микроРНК ) за исключением того, что мРНК зависят от RanGTP. Консервированные факторы экспорта мРНК необходимы для ядерного экспорта мРНК. Факторами экспорта являются Mex67 / Tap (большая субъединица) и Mtr2 / p15 (малая субъединица). Считается, что у высших эукариот экспорт мРНК зависит от сплайсинга, который, в свою очередь, привлекает белковый комплекс TREX к сплайсированным сообщениям. TREX действует как адаптер для TAP, который является очень слабым связывающим РНК белком. Однако существуют альтернативные пути экспорта мРНК, которые не зависят от сплайсинга для передачи специализированных сообщений, таких как гистоны. Недавние работы также подтверждают взаимодействие между зависимым от сплайсинга экспортом и одним из этих альтернативных путей экспорта мРНК для секреторных и митохондриальных транскриптов.[17]
Сборка NPC
Поскольку NPC контролирует доступ к геному, важно, чтобы он существовал в больших количествах на стадиях клеточного цикла, где необходима большая транскрипция. Например, циклические колебания клеток млекопитающих и дрожжей удваивают количество NPC в ядре между фазами G1 и G2 клеточный цикл, а ооциты накапливают большое количество NPC, чтобы подготовиться к быстрому митозу, который существует на ранних стадиях развития. Межфазный клетки также должны поддерживать уровень генерации NPC, чтобы поддерживать постоянный уровень NPC в ячейке, поскольку некоторые из них могут быть повреждены. Некоторые клетки могут даже увеличивать количество NPC из-за повышенной потребности в транскрипции.[18]
Теории сборки
Есть несколько теорий относительно того, как собираются NPC. Поскольку иммунное истощение определенных белковых комплексов, таких как комплекс Nup 107–160, приводит к образованию ядер без пор, кажется вероятным, что комплексы Nup участвуют в слиянии внешней мембраны ядерной оболочки с внутренней, а не то, что сплавление мембраны начинает образование поры. Это может привести к формированию полноценного NPC несколькими способами.
- Одна из возможностей состоит в том, что как белковый комплекс он связывается с хроматин. Затем он вставляется в двойную мембрану рядом с хроматином. Это, в свою очередь, приводит к сплавлению этой мембраны. Вокруг этого белкового комплекса в конечном итоге связываются другие, образуя NPC. Этот метод возможен во время каждой фазы митоза, поскольку двойная мембрана присутствует вокруг хроматина до того, как комплекс белков слияния мембран может быть вставлен. Постмитотические клетки могут сначала образовывать мембрану, в которую после образования вставляются поры.
- Другая модель образования NPC - это создание препоры в качестве начала, а не единого белкового комплекса. Эта препора должна образовываться, когда несколько комплексов Nup объединяются и связываются с хроматином. Это будет иметь двойную мембранную форму вокруг себя во время митотической сборки. Возможные структуры препоры наблюдались на хроматин перед ядерная оболочка (NE) формирование с помощью электронной микроскопии.[19] Во время интерфазы клеточного цикла формирование препоры происходит внутри ядра, причем каждый компонент транспортируется через существующие NPC. Эти Nups будут связываться с импортином, будучи однажды сформированным, предотвращая сборку препоры в цитоплазме. После транспортировки в ядро Ran GTP будет связываться с импортином и заставлять его высвобождать груз. Этот Nup мог бы свободно формировать препору. Связывание importins по крайней мере, было показано, что нуклеопорины Nup 107 и Nup 153 попадают в ядро.[18] Сборка NPC - это очень быстрый процесс, но при этом возникают определенные промежуточные состояния, которые наводят на мысль, что сборка происходит поэтапно.[20]
Разборка
Во время митоза NPC, кажется, разбирается поэтапно. Периферийный нуклеопорины такие как Nup 153 Nup 98 и Nup 214 отделяются от NPC. Остальные, которые можно рассматривать как каркасные белки, остаются стабильными в виде комплексов с цилиндрическими кольцами внутри ядерной оболочки. Эта разборка периферических групп NPC в значительной степени считается управляемой фосфатом, поскольку некоторые из этих нуклеопоринов фосфорилируются на стадиях митоза. Однако фермент, участвующий в фосфорилировании, in vivo неизвестен. У многоклеточных животных (которые претерпевают открытый митоз) NE быстро деградирует после потери периферических Nups. Причина этого может быть связана с изменением архитектуры NPC. Это изменение может сделать NPC более проницаемым для ферментов, участвующих в деградации NE, таких как цитоплазматический тубулин, а также сделать возможным проникновение ключевых белков-регуляторов митоза. У организмов, которые подвергаются полуоткрытому митозу, например нитчатых грибов Aspergillus nidulans, 14 из 30 нуклеопоринов отделяются от основной структуры каркаса за счет активации киназ NIMA и Cdk1, которые фосфорилируют нуклеопорины и открывают ядерные поры.[21][22] тем самым расширяя ядерные поры и позволяя входить митотическим регуляторам.[23]
Сохранение целостности
Было показано, что у грибов, подвергающихся закрытый митоз (где ядро не разбирается), что изменение барьера проницаемости NE было связано с изменениями внутри NPC и это то, что позволяет входить митотическим регуляторам. В Aspergillus nidulans на состав NPC, по-видимому, влияет митотическая киназа NIMA, возможно, за счет фосфорилирования нуклеопоринов Nup98 и Gle2 / Rae1. Это ремоделирование, по-видимому, позволяет белковому комплексу cdc2 / cyclinB проникать в ядро, а также многим другим белкам, таким как растворимый тубулин. Каркас NPC остается неповрежденным на протяжении всего закрытого митоза. Похоже, что это сохраняет целостность NE.
Рекомендации
- ^ Maul, Gerd G; Дивен, Ларри (1977). «Количественное определение комплексов ядерных пор в циклических клетках с различным содержанием ДНК». Журнал клеточной биологии. 73 (3): 748–760. Дои:10.1083 / jcb.73.3.748. ЧВК 2111421. PMID 406262.
- ^ Лин, Д. Х., Стуве, Т., Шильбах, С., Рандлет, Э. Дж., Перриче, Т., Моббс, Г.,… Хельц, А. (2016). Архитектура сложного симметричного ядра ядерной поры. Наука, 352 (6283), aaf1015. http://doi.org/10.1126/science.aaf1015
- ^ Деннинг Д., Патель С., Уверский В., Финк А., Рексач М. (2003). «Нарушение в комплексе ядерной поры: области повторов FG нуклеопоринов изначально развернуты». Proc Natl Acad Sci USA. 100 (5): 2450–5. Дои:10.1073 / pnas.0437902100. ЧВК 151361. PMID 12604785.
- ^ Петерс Р. (2006). Введение в ядерно-цитоплазматический транспорт: молекулы и механизмы. Методы Мол Биол. Методы молекулярной биологии ™. 322. С. 235–58. Дои:10.1007/978-1-59745-000-3_17. ISBN 978-1-58829-362-6. PMID 16739728. Архивировано из оригинал на 2007-09-28. Получено 2007-04-04.
- ^ Пейро, М .; Soheilypour, M .; Lee, B.L .; Мофрад, М.Р.К. (2015-11-06). «Эволюционно сохраненные особенности последовательности регулируют формирование сети FG в центре ядерного порового комплекса». Научные отчеты. 5: 15795. Дои:10.1038 / srep15795. ЧВК 4635341. PMID 26541386.
- ^ Андо, Дэвид; Колвин, Майкл; Рексач, Майкл; Гопинатан, Аджай (16 сентября 2013 г.). «Кластеризация физических мотивов внутри изначально неупорядоченных последовательностей нуклеопоринов выявляет универсальные функциональные особенности». PLOS ONE. 8 (9): e73831. Дои:10.1371 / journal.pone.0073831. ЧВК 3774778. PMID 24066078.
- ^ Вини, Марк; Ярар, Дефне; Гиддингс-младший, Томас Х; Мастронарде, Дэвид Н. (1 ноября 1997 г.). «Количество и распределение ядерных поровых комплексов в клеточном цикле Saccharomyces cerevisiae путем трехмерной реконструкции из электронных микрофотографий ядерных оболочек». Молекулярная биология клетки. 8 (11): 2119–2132. Дои:10.1091 / mbc.8.11.2119. ЧВК 25696. PMID 9362057.
- ^ Мор, Дагмар; Фрей, Штеффен; Фишер, Торстен; Гюттлер, Томас; Герлих, Дирк (13 августа 2009 г.). «Характеристика барьера пассивной проницаемости ядерных поровых комплексов». Журнал EMBO. 28 (17): 2541–2553. Дои:10.1038 / emboj.2009.200. ЧВК 2728435. PMID 19680228.
- ^ Кеминер, Оливер; Питерс, Райнер (июль 1999 г.). «Проницаемость одиночных ядерных пор». Биофизический журнал. 77 (1): 217–228. Дои:10.1016 / S0006-3495 (99) 76883-9. ЧВК 1300323. PMID 10388751.
- ^ Кузнецов, Юрий Г .; Дайджого, Сара; Чжоу, Цзяшу; Semler, Bert L .; Макферсон, А. (март 2005 г.). "Анализ РНК вируса икосаэдра с помощью атомно-силовой микроскопии" (PDF). Журнал молекулярной биологии. 347 (1): 41–52. Дои:10.1016 / j.jmb.2005.01.006. PMID 15733916.
- ^ Reichelt, R; Holzenburg, A; Buhle Jr., E L; Ярник, М; Энгель, А; Эби, Ю (1 апреля 1990 г.). «Корреляция между структурой и массовым распределением ядерного порового комплекса и отдельных компонентов порового комплекса». Журнал клеточной биологии. 110 (4): 883–894. CiteSeerX 10.1.1.277.5930. Дои:10.1083 / jcb.110.4.883. ЧВК 2116066. PMID 2324201.
- ^ Альбер, Франк; Докудовская, Светлана; Veenhoff, Liesbeth M .; Чжан, Вэньчжу; Киппер, Джулия; Девос, Дэмиен; Супрапто, Адисетиантари; Карни-Шмидт, Орит; Уильямс, Розмари; Chait, Брайан Т .; Раут, Майкл П .; Сали, Андрей (29 ноября 2007 г.). «Определение архитектур макромолекулярных сборок». Природа. 450 (7170): 683–694. Дои:10.1038 / природа06404. PMID 18046405.
- ^ Rout MP, Blobel G (ноябрь 1993 г.). «Выделение дрожжевого комплекса ядерных пор». J. Cell Biol. 123 (4): 771–83. Дои:10.1083 / jcb.123.4.771. ЧВК 2200146. PMID 8227139.
- ^ Родригес М., Даргемонт С., Штутц Ф. (3 августа 2004 г.). «Ядерный экспорт РНК». Биология клетки. 96 (8): 639–55. Дои:10.1016 / j.biolcel.2004.04.014. PMID 15519698.
- ^ Марфори М., Минотт А., Эллис Дж. Дж. И др. (Октябрь 2010 г.). «Молекулярная основа специфичности ядерного импорта и предсказания ядерной локализации». Biochimica et Biophysica Acta. 1813 (9): 1562–77. Дои:10.1016 / j.bbamcr.2010.10.013. PMID 20977914.
- ^ Reed R, Hurt E (февраль 2002 г.). «Консервативный механизм экспорта мРНК, связанный со сплайсингом пре-мРНК». Клетка. 108 (4): 523–31. Дои:10.1016 / S0092-8674 (02) 00627-X. PMID 11909523.
- ^ Cenik, C; и другие. (2011). «Геномный анализ показывает взаимодействие между интронами 5 'UTR и экспортом ядерной мРНК для секреторных и митохондриальных генов». PLOS Genetics. 7 (4): e1001366. Дои:10.1371 / journal.pgen.1001366. ЧВК 3077370. PMID 21533221.
- ^ а б Рабут Г., Ленарт П., Элленберг Дж. (Июнь 2004 г.). «Динамика организации комплекса ядерных пор в клеточном цикле». Текущее мнение в области клеточной биологии. 16 (3): 314–21. Дои:10.1016 / j.ceb.2004.04.001. PMID 15145357.
- ^ Шихан М.А., Миллс А.Д., Слиман А.М., Ласки Р.А., Блоу Дж.Дж. (январь 1988 г.). «Этапы сборки репликационно-компетентных ядер в бесклеточной системе из яиц Xenopus». Журнал клеточной биологии. 106 (1): 1–12. Дои:10.1083 / jcb.106.1.1. ЧВК 2114961. PMID 3339085.
- ^ Киселева Е., Резерфорд С., Коттер Л.М., Аллен Т.Д., Голдберг М.В. (октябрь 2001 г.). «Этапы разборки и повторной сборки комплекса ядерных пор во время митоза у ранних эмбрионов дрозофилы». Журнал клеточной науки. 114 (Pt 20): 3607–18. PMID 11707513.
- ^ Маркосян, Сарин; Суреш, Суббулакшми; Османи, Айша Х .; Османи, Стивен А. (2015-02-15). «Nup2 требует сильно дивергентного партнера, NupA, для выполнения функций в комплексах ядерных пор и митотической области хроматина». Молекулярная биология клетки. 26 (4): 605–621. Дои:10.1091 / mbc.E14-09-1359. ISSN 1059-1524. ЧВК 4325833. PMID 25540430.
- ^ Де Соуза, Колин П.К .; Османи, Айша Х .; Hashmi, Shahr B .; Османи, Стивен А. (2004). «Частичная разборка комплекса ядерных пор во время закрытого митоза у Aspergillus nidulans». Текущая биология. 14 (22): 1973–1984. Дои:10.1016 / j.cub.2004.10.050. ISSN 0960-9822. PMID 15556859.
- ^ Соуза, Колин П. К. Де; Османи, Стивен А. (2007-09-01). «Митоз, не только открытый или закрытый». Эукариотическая клетка. 6 (9): 1521–1527. Дои:10.1128 / EC.00178-07. ISSN 1535-9778. ЧВК 2043359. PMID 17660363.
внешняя ссылка
- Гистологическое изображение: 20104loa - Система обучения гистологии в Бостонском университете
- Ядерный + поры в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Анимация комплекса ядерных пор
- Ядерный поровый комплекс иллюстрации
- 3D-электронная микроскопия структур NPC и составляющих белков из EM Data Bank (EMDB)
- NCDIR - Национальный центр динамического взаимодействия[постоянная мертвая ссылка ]

