MECP2 - MECP2
MECP2 (метил CpG-связывающий белок 2) это ген[5] который кодирует белок MECP2.[6] MECP2, по-видимому, необходим для нормального функционирования нервные клетки. Этот белок особенно важен для зрелых нервных клеток, где он присутствует в больших количествах. Белок MECP2, вероятно, участвует в выключении («репрессии» или «заглушить ") несколько других генов. Это не позволяет генам производить белки, когда они не нужны. Недавние исследования показали, что MECP2 может также активировать другие гены.[7] Ген MECP2 расположен на длинном (q) плече Х хромосома в полосе 28 ("Xq28"), от базовая пара 152 808 110 к базовой паре 152 878 611.
MECP2 является важным считывающим устройством метилирования ДНК. Его метил-CpG-связывающий домен (MBD) распознает и связывает 5-мкл регионы. MECP2 является X-сцепленным и подлежит X инактивация. Мутации гена MECP2 являются причиной большинства случаев Синдром Ретта, прогрессирующее неврологическое нарушение развития и одна из наиболее частых причин когнитивной инвалидности у женщин.[8]
Функция
Белок MECP2 присутствует во всех клетки в теле, в том числе мозг, действуя как репрессор и активатор транскрипции, в зависимости от контекста. Тем не менее, идея, что функции MECP2 как активатор является относительно новым и остается спорным.[9] В головном мозге он обнаруживается в высоких концентрациях в нейроны и связано с созреванием Центральная нервная система (ЦНС) и в формировании синаптические контакты.[10]
Механизм действия
Белок MeCP2 связывается с формами ДНК это было метилированный. Затем белок MeCP2 взаимодействует с другими белками, образуя комплекс, который выключает ген. MeCP2 предпочитает связываться с участками генома с химическими изменениями, внесенными в цитозин (C) когда это происходит в определенной последовательности ДНК, "CpG ". Это форма Метилирование ДНК. Многие гены имеют Острова CpG, которые часто встречаются в начале гена. MECP2 в большинстве случаев не связывается с этими островками, поскольку они не метилированы. В выражение нескольких генов могут регулироваться посредством метилирования их CpG-островка, и MECP2 может играть роль в их подмножестве. Исследователи еще не определили, какие гены нацелены на белок MeCP2, но такие гены, вероятно, важны для нормального функционирования центральной нервной системы. Однако первое крупномасштабное картирование сайтов связывания MECP2 в нейронах показало, что только 6% сайтов связывания находятся на островках CpG, и что 63% промоторов, связанных с MECP2, активно экспрессируются и только 6% сильно метилированы, что указывает на то, что Основная функция MECP2 - это нечто иное, чем подавление метилированных промоторов.[11]
После связывания MeCP2 будет конденсировать хроматин конструкции, образуют комплекс с гистоновые деацетилазы (HDAC) или блокировать факторы транскрипции напрямую. Более поздние исследования продемонстрировали, что MeCP2 может также функционировать как активатор транскрипции за счет привлечения фактора транскрипции. CREB1. Это было неожиданным открытием, которое предполагает, что MeCP2 является ключевым регулятором транскрипции с потенциально двойной ролью в экспрессии генов. Фактически, большинство генов, которые регулируются MeCP2, по-видимому, активируются, а не подавляются.[12] Однако остается спорным, регулирует ли MeCP2 эти гены напрямую или эти изменения являются вторичными по своей природе.[9] Дальнейшие исследования показали, что в некоторых случаях MeCP2 может напрямую связываться с неметилированной ДНК.[13] MeCP2 участвует в регуляции импринтированных генов и локусов, которые включают UBE3A и DLX5.[14]
Пониженная экспрессия MECP2 в Mecp2 +/- нервные стволовые клетки вызывает увеличение старение, нарушение пролиферативной способности и накопление неизлечимых Повреждения ДНК.[15] После обработки клеток Mecp2 +/- любым из трех различных агентов, повреждающих ДНК, клетки накапливали больше повреждений ДНК и были более склонны к гибели клеток, чем контрольные клетки.[15] Был сделан вывод, что снижение экспрессии MECP2 вызывает снижение способности к восстановить ДНК и это, вероятно, способствует неврологическому спаду.[15]
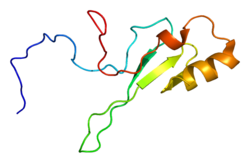
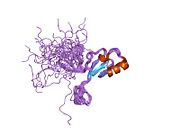
Структура
MECP2 является частью семейства белков метил-CpG-связывающих доменов (MBD), но обладает собственными уникальными различиями, которые помогают выделить его из группы. Он имеет два функциональных домена:
- метил-цитозин -связывающий домен (MBD) состоит из 85 аминокислоты; и
- домен репрессии транскрипции (TRD), состоящий из 104 аминокислот
Домен MBD образует клин и прикрепляется к метилированным сайтам CpG на цепях ДНК. Затем область TRD реагирует с SIN3A, рекрутируя гистоновые деацетилазы (HDAC).[16] Есть также необычные повторяющиеся последовательности, обнаруженные на карбоксильном конце. Эта область на аминокислотном уровне тесно связана с семейством головок вилки.[17]
Роль в болезни
Роль MECP2 в заболевании в первую очередь связана либо с потерей функции (недостаточной экспрессии) гена MECP2, как в Синдром Ретта или в усилении функции (сверх выражения), как в Синдром дублирования MECP2. Многие мутации были связаны с потерей экспрессии гена MECP2 и были идентифицированы у пациентов с синдромом Ретта. Эти мутации включают изменения в одной ДНК. пар оснований (SNP ), вставки или делеции ДНК в MECP2 ген и изменения, влияющие на то, как информация гена преобразуется в белок (Сплайсинг РНК ). Мутации в гене изменяют структуру белка MeCP2 или приводят к уменьшению количества белка. В результате белок не может связываться с ДНК или включать или выключать другие гены. Гены, которые обычно репрессируются MeCP2, остаются активными, когда их продукты не нужны. Другие гены, которые обычно активируются MeCP2, остаются неактивными, что приводит к недостатку генного продукта. Этот дефект, вероятно, нарушает нормальное функционирование нервных клеток, что приводит к появлению признаков и симптомов синдрома Ретта.
Синдром Ретта в основном встречается у девочек с распространенность примерно 1 на каждые 10 000. Пациенты рождаются с очень трудно обнаруживаемыми признаками расстройства, но примерно через шесть месяцев или полтора года речевые и двигательные функции начинают снижаться. Далее следует припадки, задержка роста и когнитивные и двигательные нарушения.[18] Локус MECP2 Х-связанный и вызывающие болезнь аллели доминирующий. Из-за того, что он распространен у женщин, он был связан с мужской летальностью или с преимущественной передачей через отцовскую Х-хромосому; тем не менее, в редких случаях некоторые мужчины также могут быть поражены синдромом Ретта.[19] Мужчины с дупликациями генов MECP-2 в локусе Xq28 также подвержены риску рецидивирующих инфекций и менингита в младенчестве.
Мутации в гене MECP2 также были выявлены у людей с несколькими другими заболеваниями, влияющими на центральную нервную систему. Например, мутации MECP2 связаны с некоторыми случаями от умеренной до тяжелой Х-связанной умственной отсталости. Мутации в гене также были обнаружены у мужчин с тяжелой дисфункцией головного мозга (неонатальная энцефалопатия ) которые доживают до раннего детства. Кроме того, несколько человек с признаками синдрома Ретта и Синдром ангельмана (состояние, характеризующееся умственной отсталостью, проблемами с движением, неуместным смехом и возбудимостью) имеют мутации в гене MECP2. Наконец, в некоторых случаях сообщалось о мутациях MECP2 или изменениях активности гена. аутизм (нарушение развития, которое влияет на общение и социальное взаимодействие).[20]
Более поздние исследования сообщили о генетическом полиморфизме генов MeCP2 у пациентов с системная красная волчанка (СКВ).[21] СКВ - системное аутоиммунное заболевание, которое может поражать несколько органов. О полиморфизмах MeCP2 до сих пор сообщалось у пациентов с волчанкой европейского и азиатского происхождения.
Генетическая потеря MECP2 была идентифицирована как изменение свойств клеток в locus ceruleus эксклюзивный источник норадренергической иннервации для кора головного мозга и гиппокамп.[22]
Исследователи пришли к выводу, что «поскольку эти нейроны являются основным источником норэпинефрина в стволе и переднем мозге и участвуют в регуляции различных функций, нарушаемых при синдроме Ретта, таких как дыхание и познание, мы предполагаем, что голубое пятно является критическим местом в потеря MECP2 приводит к дисфункции ЦНС ».[22]
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы просмотреть статьи по теме. [§ 1]
Взаимодействия
MECP2 был показан взаимодействовать с SKI протеин[23] и Корепрессор ядерного рецептора 1.[23] Считается, что в нейрональных клетках мРНК MECP2 взаимодействует с miR-132, который подавляет экспрессию белка. Это является частью гомеостатического механизма, который может регулировать уровни MECP2 в головном мозге.[24]
MeCP2 и гормоны
MeCP2 в развивающемся мозге крысы регулирует важное социальное развитие сексуально диморфным образом. Уровни MeCP2 у мужчин и женщин в развивающемся мозге крысы различаются через 24 часа после рождения в пределах миндалина и гипоталамус, но эта разница уже не наблюдается через 10 дней после рождения. В частности, мужчины экспрессируют меньше MeCP2, чем женщины,[25] и это совпадает с чувствительным к стероидам периодом времени мозга новорожденных крыс. Уменьшение MeCP2 с Малая интерферирующая РНК (siRNA) в течение первых нескольких дней жизни снижает уровень социального игрового поведения подростков до типичных для женщин уровней, но не влияет на игровое поведение девочек-подростков.[26]
MeCP2 важен для организации гормонально-зависимого поведения и половых различий в развивающейся миндалине крысы. MeCP2, по-видимому, регулирует аргинин вазопрессин (AVP) и рецептор андрогенов (AR) продукция у самцов крыс, но не у самок. Известно, что вазопрессин регулирует многие виды социального поведения, включая создание парных связей.[27] и общественное признание.[28] В то время как самцы крыс обычно имеют более высокий уровень вазопрессина в миндалине,[29] Снижение MeCP2 в течение первых 3 дней жизни вызывает стойкое снижение уровня вазопрессина до типичных для женщин уровней в этой области мозга, которое сохраняется на протяжении всей взрослой жизни. Самцы крыс со сниженным уровнем MeCP2 также демонстрируют значительное снижение AR через две недели после инфузии, но этот эффект исчезает к взрослому состоянию.[30]
Стресс в молодости
MeCP2 отслеживает реакцию на стресс в раннем возрасте. Стресс в раннем детстве коррелирует с гиперфосфорилированием белка MeCP2 в паравентрикулярное ядро гипоталамуса.[31] Таким образом, это приводит к уменьшению занятости MeCP2 в промоторной области гена AVP и, следовательно, к повышению уровней AVP. Вазопрессин - это первичный гормон, участвующий в оси гипотальм-гипофиз-надпочечники, связности мозга, которая регулирует обработку стресса и реакцию на него. Таким образом, сниженное функционирование белка MeCP2 усиливает стрессовую реакцию нейронов.
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000169057 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000031393 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Амир Р.Э., Ван ден Вейвер И.Б., Ван М., Тран CQ, Франк У., Зогби HY (Октябрь 1999 г.). «Синдром Ретта вызван мутациями в X-сцепленном MECP2, кодирующем метил-CpG-связывающий белок 2». Nat. Genet. 23 (2): 185–8. Дои:10.1038/13810. PMID 10508514. S2CID 3350350.
- ^ Льюис Дж. Д., Михан Р. Р., Хензель В. Дж., Маурер-Фоги И., Джеппесен П., Кляйн Ф., Берд А. (июнь 1992 г.). «Очистка, последовательность и клеточная локализация нового хромосомного белка, который связывается с метилированной ДНК». Клетка. 69 (6): 905–14. Дои:10.1016 / 0092-8674 (92) 90610-О. PMID 1606614. S2CID 6825994.
- ^ Чахрур М. и др. (2008). «MECP2, ключевой фактор, вызывающий неврологические заболевания, активирует и подавляет транскрипцию». Наука. 320 (5880): 1224–9. Дои:10.1126 / science.1153252. ЧВК 2443785. PMID 18511691.
- ^ «Ген Entrez: MECP2-метил-CpG-связывающий белок 2 (синдром Ретта)».
- ^ а б Коэн С., Чжоу З., Гринберг М.Э. (май 2008 г.). «Лекарство. Активация репрессора». Наука. 320 (5880): 1172–3. Дои:10.1126 / science.1159146. ЧВК 2857976. PMID 18511680.
- ^ Luikenhuis S, Giacometti E, Beard CF, Jaenisch R (апрель 2004 г.). «Экспрессия MeCP2 в постмитотических нейронах спасает синдром Ретта у мышей». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 101 (16): 6033–8. Дои:10.1073 / pnas.0401626101. ЧВК 395918. PMID 15069197.
- ^ Ясуи Д.Х., Педдада С., Биеда М.С., Валлеро Р.О., Хогарт А., Нагараджан Р.П., Тэтчер К.Н., Фарнхэм П.Дж., Ласалле Дж.М. (декабрь 2007 г.). «Комплексный эпигеномный анализ нейронального MeCP2 выявил роль дальнодействующего взаимодействия с активными генами». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 104 (49): 19416–21. Дои:10.1073 / pnas.0707442104. ЧВК 2148304. PMID 18042715.
- ^ Chahrour M, Jung SY, Shaw C, Zhou X, Wong ST, Qin J, Zoghbi HY (май 2008 г.). «MeCP2, ключевой фактор, вызывающий неврологические заболевания, активирует и подавляет транскрипцию». Наука. 320 (5880): 1224–9. Дои:10.1126 / science.1153252. ЧВК 2443785. PMID 18511691.
- ^ Георгель П.Т., Горовиц-Шерер Р.А., Адкинс Н., Вудкок К.Л., Уэйд П.А., Хансен Дж.С. (август 2003 г.). «Компакция хроматина человеческим MeCP2. Сборка новых вторичных структур хроматина в отсутствие метилирования ДНК». J. Biol. Chem. 278 (34): 32181–8. Дои:10.1074 / jbc.M305308200. PMID 12788925.
- ^ LaSalle JM (2007). «Одиссея MeCP2 и родительского импринтинга». Эпигенетика. 2 (1): 5–10. Дои:10.4161 / epi.2.1.3697. ЧВК 1866173. PMID 17486180.
- ^ а б c Алессио Н., Риччиелло Ф., Сквилларо Т., Капассо С., Дель Гаудио С., Ди Бернардо Дж., Чиполларо М., Мелоне МАБ, Пелусо Дж., Галдериси Ю. (март 2018 г.). «Нервные стволовые клетки из мышиной модели синдрома Ретта склонны к старению, демонстрируют пониженную способность справляться с генотоксическим стрессом и нарушены в процессе дифференцировки». Exp. Мол. Med. 50 (3): 1. Дои:10.1038 / с12276-017-0005-х. ЧВК 6118406. PMID 29563495.
- ^ Уэйкфилд Р.И., Смит Б.О., Нэн Х, Фри А., Сотериу А., Урин Д., Берд А.П., Барлоу П.Н. (сентябрь 1999 г.). «Структура раствора домена MeCP2, который связывается с метилированной ДНК». J. Mol. Биол. 291 (5): 1055–65. Дои:10.1006 / jmbi.1999.3023. PMID 10518942.
- ^ Пол А. Уэйд (декабрь 2001 г.). «Метил CpG-связывающие белки и репрессия транскрипции» (PDF). BioEssays. 23 (12): 1131–1137. Дои:10.1002 / bies.10008. PMID 11746232. S2CID 37525856. Архивировано из оригинал (PDF) на 2007-08-14.
- ^ Кабальеро И.М., Хендрих Б. (апрель 2005 г.). «MeCP2 в нейронах: закрытие причин синдрома Ретта». Гм. Мол. Genet. 14 Спец. № 1: Р19–26. Дои:10.1093 / hmg / ddi102. PMID 15809268.
- ^ Samaco RC, Nagarajan RP, Braunschweig D, LaSalle JM (март 2004 г.). «Множественные пути регулируют экспрессию MeCP2 при нормальном развитии мозга и обнаруживают дефекты при расстройствах аутистического спектра». Гм. Мол. Genet. 13 (6): 629–39. Дои:10.1093 / hmg / ddh063. PMID 14734626.
- ^ Хант, Кэти (12 января 2016 г.). «Китайские ученые создают обезьян с геном аутизма». Новости CNN. Получено 2016-01-27.
- ^ Савальха А.Х., Уэбб Р., Хан С., Келли Дж.А., Кауфман К.М., Кимберли Р.П., Аларкон-Рикельме М.Э., Джеймс Дж.А., Вайз Т.Дж., Гилкесон Г.С., Чой С.Б., Скофилд Р.Х., Бэ СК, Нат СК, Харли Дж.Б. (2008). Джин Д. (ред.). «Общие варианты в MECP2 связаны с риском системной красной волчанки». PLOS ONE. 3 (3): e1727. Дои:10.1371 / journal.pone.0001727. ЧВК 2253825. PMID 18320046.

- ^ а б Танежа П., Ожир М., Брукс-Харрис Г., Шмид Д.А., Кац Д.М., Нельсон С.Б. (2009). «Патофизиология нейронов Locus Ceruleus в мышиной модели синдрома Ретта». Журнал неврологии. 29 (39): 12187–12195. Дои:10.1523 / JNEUROSCI.3156-09.2009. ЧВК 2846656. PMID 19793977.
- ^ а б Кокура К., Каул С.К., Вадхва Р., Номура Т., Хан М.М., Синагава Т., Ясукава Т., Кольменарес К., Исии С. (сентябрь 2001 г.). «Семейство белков Ski требуется для репрессии транскрипции, опосредованной MeCP2». J. Biol. Chem. 276 (36): 34115–21. Дои:10.1074 / jbc.M105747200. PMID 11441023.
- ^ Klein ME, Lioy DT, Ma L, Impey S, Mandel G, Goodman RH (декабрь 2007 г.). «Гомеостатическая регуляция экспрессии MeCP2 с помощью CREB-индуцированной микроРНК». Nat. Неврологи. 10 (12): 1513–4. Дои:10.1038 / nn2010. PMID 17994015. S2CID 29308441.
- ^ Куриан Дж. Р., Форбс-Лорман Р. М., Аугер А. П. (сентябрь 2007 г.). «Половые различия в экспрессии mecp2 в критический период развития мозга крысы». Эпигенетика. 2 (3): 173–8. Дои:10.4161 / epi.2.3.4841. PMID 17965589.
- ^ Kurian JR, Bychowski ME, Forbes-Lorman RM, Auger CJ, Auger AP (июль 2008 г.). «Mecp2 организует социальное поведение подростков в зависимости от пола». J. Neurosci. 28 (28): 7137–42. Дои:10.1523 / JNEUROSCI.1345-08.2008. ЧВК 2569867. PMID 18614683.
- ^ Уинслоу Дж. Т., Гастингс Н., Картер С. С., Харбо CR, Инсел Т. Р. (октябрь 1993 г.). «Роль центрального вазопрессина в парном соединении у моногамных степных полевок». Природа. 365 (6446): 545–8. Дои:10.1038 / 365545a0. PMID 8413608. S2CID 4333114.
- ^ Bielsky IF, Hu SB, Szegda KL, Westphal H, Young LJ (март 2004 г.). «Глубокое нарушение социального признания и снижение тревожного поведения у мышей с нокаутом рецептора вазопрессина V1a». Нейропсихофармакология. 29 (3): 483–93. Дои:10.1038 / sj.npp.1300360. PMID 14647484.
- ^ Де Фрис Г.Дж., Панзика Г.К. (2006). «Половая дифференциация центральной системы вазопрессина и вазотоцина у позвоночных: разные механизмы, схожие конечные точки». Неврология. 138 (3): 947–55. Дои:10.1016 / j.neuroscience.2005.07.050. ЧВК 1457099. PMID 16310321.
- ^ Форбс-Лорман Р.М., Раутио Дж. Дж., Куриан Дж. Р., Аугер А. П., Оже С. Дж. (Март 2012 г.). «Неонатальный MeCP2 важен для организации половых различий в экспрессии вазопрессина». Эпигенетика. 7 (3): 230–8. Дои:10.4161 / epi.7.3.19265. ЧВК 3335947. PMID 22430799.
- ^ Murgatroyd C, Patchev AV, Wu Y, Micale V, Bockmühl Y, Fischer D, Holsboer F, Wotjak CT, Almeida OF, Spengler D (декабрь 2009 г.). «Динамическое метилирование ДНК программирует стойкие неблагоприятные эффекты стресса в раннем возрасте». Nat. Неврологи. 12 (12): 1559–66. Дои:10.1038 / № 2436. PMID 19898468. S2CID 3328884.
дальнейшее чтение
- Chahrour M, Zoghbi HY (2007). «История синдрома Ретта: от клиники к нейробиологии». Нейрон. 56 (3): 422–37. Дои:10.1016 / j.neuron.2007.10.001. PMID 17988628. S2CID 16266882.
- Карни Р.М., Вольперт С.М., Раван С.А., Шахбазиан М., Эшли-Кох А., Куккаро М.Л., Вэнс Дж. М., Перикак-Ванс М.А. (2003). «Идентификация мутаций MeCP2 в серии женщин с аутичным расстройством». Педиатр Neurol. 28 (3): 205–11. Дои:10.1016 / S0887-8994 (02) 00624-0. PMID 12770674.
- Керр А.М., Овраг Д. (2003). «Обзорная статья: новые пути с синдромом Ретта». J Интеллект Disabil Res. 47 (Пт 8): 580–7. Дои:10.1046 / j.1365-2788.2003.00506.x. PMID 14641805.
- Neul JL, Zoghbi HY (2004). «Синдром Ретта: прототипное расстройство психического развития». Нейробиолог. 10 (2): 118–28. Дои:10.1177/1073858403260995. PMID 15070486. S2CID 9617631.
- Шанен С., Хаувинк Э.Дж., Доррани Н., Лейн Дж., Эверетт Р., Фенг А., Кантор Р.М., Перси А. (2004). «Фенотипические проявления мутаций MECP2 при классическом и атипичном синдроме Ретта». Am J Med Genet A. 126 (2): 129–40. Дои:10.1002 / ajmg.a.20571. PMID 15057977. S2CID 32897044.
- Ван ден Вейвер И.Б., Zoghbi HY (2001). «Мутации в гене, кодирующем метил-CpG-связывающий белок 2, вызывают синдром Ретта». Brain Dev. 23 (Приложение 1): S147–51. Дои:10.1016 / S0387-7604 (01) 00376-X. PMID 11738862. S2CID 26138178.
- Уэбб Т., Латиф Ф (2001). «Синдром Ретта и ген MECP2». J Med Genet. 38 (4): 217–23. Дои:10.1136 / jmg.38.4.217. ЧВК 1734858. PMID 11283201.
- Шахбазян MD, Zoghbi HY (2003). «Синдром Ретта и MeCP2: связь эпигенетики и нейрональной функции». Являюсь. J. Hum. Genet. 71 (6): 1259–72. Дои:10.1086/345360. ЧВК 378559. PMID 12442230.
- Moog U, Smeets EE, van Roozendaal KE и др. (2003). «Расстройства нервного развития у мужчин, связанные с геном, вызывающим синдром Ретта у женщин (MECP2)». Евро. J. Paediatr. Neurol. 7 (1): 5–12. Дои:10.1016 / S1090-3798 (02) 00134-4. PMID 12615169.
- Мильтенбергер-Мильтеньи G, Laccone F (2004). «Мутации и полиморфизмы в человеческом метил-CpG-связывающем белке MECP2». Гм. Мутат. 22 (2): 107–15. Дои:10.1002 / humu.10243. PMID 12872250.
- Weaving LS, Ellaway CJ, Gécz J, Christodoulou J (2006). «Синдром Ретта: клинический обзор и генетическое обновление». J. Med. Genet. 42 (1): 1–7. Дои:10.1136 / jmg.2004.027730. ЧВК 1735910. PMID 15635068.
- Бапат С., Галанде С. (2005). «Ассоциация по вине: идентификация DLX5 как мишени для MeCP2 обеспечивает молекулярную связь между геномным импринтингом и синдромом Ретта». BioEssays. 27 (7): 676–80. Дои:10.1002 / bies.20266. PMID 15954098.
- Златанова Ж (2005). «MeCP2: хроматиновые связи и не только». Biochem. Cell Biol. 83 (3): 251–62. Дои:10.1139 / o05-048. PMID 15959553.
- Кауфманн В.Е., Джонстон М.В., Blue ME (2006). «Экспрессия MeCP2 и функция во время развития мозга: последствия для патогенеза и клинической эволюции синдрома Ретта». Brain Dev. 27 (Приложение 1): S77 – S87. Дои:10.1016 / j.braindev.2004.10.008. PMID 16182491. S2CID 702975.
- Армстронг Д.Д. (2006). «Можем ли мы связать дефицит MeCP2 со структурными и химическими аномалиями в мозге Ретта?». Brain Dev. 27 (Приложение 1): S72 – S76. Дои:10.1016 / j.braindev.2004.10.009. PMID 16182497. S2CID 45587850.
- Сантос М., Коэльо PA, Maciel P (2006). «Ремоделирование хроматина и функция нейронов: интересные ссылки». Гены, мозг и поведение. 5 (Дополнение 2): 80–91. Дои:10.1111 / j.1601-183X.2006.00227.x. PMID 16681803.
- Бьенвеню Т., Челли Дж. (2006). «Молекулярная генетика синдрома Ретта: когда метилирование ДНК остается нераспознанным». Природа Обзоры Генетика. 7 (6): 415–26. Дои:10.1038 / nrg1878. PMID 16708070. S2CID 28215286.
- Франк У (2007). «Механизмы заболевания: нейрогенетика дефицита MeCP2». Природа Клиническая Практика Неврология. 2 (4): 212–21. Дои:10.1038 / ncpneuro0148. PMID 16932552. S2CID 22710951.
внешняя ссылка
- Международный фонд синдрома Ретта
- Rett UK Support and Research Charity
- Фонд исследований синдрома Ретта
- Ансамбль Ген ссылка Протеин ссылка
- GeneCard
- RettBASE: База данных вариаций IRSA MECP2
- Запись GeneReview / NIH / UW о заболеваниях, связанных с MECP2
- GeneReviews / NCBI / NIH / UW запись о синдроме дупликации MECP2
- Британский сайт для семей, пострадавших от MECP2.
- Сайт для семей, пострадавших от MECP2.
- Французский официальный сайт по дублированию MeCP2