Периодировать - Periodate
 Метапериодат-ион | |
 Ортопериодат-ион | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК тетраоксойодат (1-) гексаоксойодат (5-) | |
| Идентификаторы | |
| |
3D модель (JSmol ) |
|
| ChemSpider | |
PubChem CID | |
| UNII |
|
| |
| |
| Характеристики | |
| IO4− или же IO65- | |
| Конъюгированная кислота | Периодическая кислота |
| Родственные соединения | |
Другой анионы | Перхлорат Пербромат Перманганат |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Периодировать /пəˈраɪ.ədeɪт/ является анион состоит из йод и кислород. Это один из многих оксианионы йода и является самым высоким в серии, йод присутствует в степень окисления +7. В отличие от других пергалогенатов, таких как перхлорат, он может существовать в двух формах: метапериодат IO−
4 и ортопериодат IO5−
6. В этом отношении он сопоставим с теллурировать ион из соседнего группа. Может сочетаться с рядом противоионы формировать периоды, которые также можно рассматривать как соли периодная кислота.
Периодаты были открыты Генрих Густав Магнус и К. Ф. Аммермюллер; кто первым синтезировал периодическую кислоту в 1833 году.[1]
Синтез
Классически периодат чаще всего производился в форме гидроперидата натрия (Na3ЧАС2IO6).[2] Это коммерчески доступно, но также может быть получено окислением йодаты с хлор и едкий натр.[3] Или, аналогично, из йодиды окислением бром и гидроксид натрия:
- NaIO3 + Cl2 + 4 NaOH → Na3ЧАС2IO6 + 2 NaCl + H2О
- NaI + 4 Br2 + 10 NaOH → Na3ЧАС2IO6 + 8 NaBr + 4 H2О
Современное промышленное производство включает в себя электрохимический окисление йодатов на PbO2 анод, со следующими стандартный электродный потенциал:
Метапериодаты обычно получают дегидратацией гидропериодата натрия с азотная кислота,[2] или путем дегидратации ортопериодной кислоты путем ее нагревания до 100 ° C в вакууме.
- Na3ЧАС2IO6 + 2 HNO3 → NaIO4 + 2 NaNO3 + 2 часа2О
- ЧАС5IO6 → HIO4 + 2 часа2О
Они также могут быть получены непосредственно из йодатов путем обработки другими сильными окислителями, такими как гипохлориты:
Формы и взаимопревращение
Периодат может существовать в различных формах в водной среде, с pH являясь контролирующим фактором. Ортопериодат имеет ряд константы кислотной диссоциации.[5][6]
ЧАС5IO6 ⇌ ЧАС
4IO−
6+ H+ пKа = 3.29 ЧАС
4IO−
6⇌ ЧАС
3IO2−
6+ H+ пKа = 8.31 ЧАС
3IO2−
6⇌ ЧАС
2IO3−
6+ H+ пKа = 11.60
Орто- и метапериодатные формы также существуют в равновесии.
- ЧАС
4IO−
6 ⇌ IO−
4 + 2 часа2О, K = 29
По этой причине ортопериодат иногда называют дигидрат метапериодата,[7] написано IO−
4· 2H2О; однако это описание не совсем точное, так как Рентгеновская кристаллография из H5IO6 показывает 5 эквивалентных групп I – OH.[8]
При экстремальных значениях pH могут образовываться дополнительные виды. В основных условиях может происходить реакция дегидратации с образованием дипериодата (иногда называемого мезопериодатом).
- 2 ЧАС
3IO2−
6 ⇌ ЧАС
2я
2О4−
10 + 2 часа2О, K = 820
В сильнокислых условиях периодическая кислота может быть протонирована с образованием ортопериодоний катион.[9]
- ЧАС
6IO+
6 ⇌ H5IO6 + H+, пKа = −0.8
Структура и склеивание
Как в орто-, так и в метапериодате йод присутствует в гипервалентный, поскольку он образует больше облигаций, чем разрешено классически. Это было объяснено с точки зрения дативные облигации, что подтверждает отсутствие двойной связи в этих молекулах.[10]
Точные структуры различаются в зависимости от противоионов, однако в среднем ортопериодаты принимают слегка деформированную октаэдрическую геометрию с дифракция рентгеновских лучей показывает длину связи I – O 1,89Å.[11][8] Метапериодаты имеют искаженную тетраэдрическую геометрию со средним расстоянием I – O 1,78 Å.[12][13]
Реакции
Реакции расщепления
Периодаты могут расщеплять углерод-углеродные связи на различных 1,2-дифункциональных алканах.[14][15] Самый распространенный пример этого: расщепление диола, который также был обнаружен первым (Реакция Малапрада ).[16]В добавление к диолы, периодаты могут расщеплять 1,2-гидроксикетоны, 1,2-дикетоны, α-кетокислоты, α-гидроксикислоты, аминокислоты,[17] 1,2-аминоспирты,[18] 1,2-диамины,[19] и эпоксиды[20] с образованием альдегидов, кетонов и карбоновых кислот.

Алкены также могут окисляться и расщепляться в Окисление Лемье-Джонсона. При этом используется каталитическая загрузка четырехокись осмия который регенерируется in situ периодатом. Общий процесс эквивалентен процессу озонолиз.
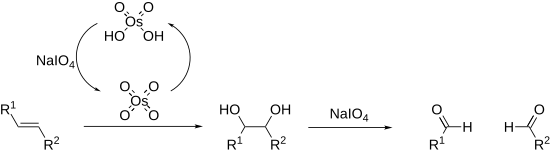
Реакции расщепления протекают через циклический промежуточный продукт, называемый сложным эфиром периодата. На его образование могут влиять pH и температура.[21] но наиболее сильно зависит от геометрии подложки, с СНГ -диолы реагируют значительно быстрее, чем транс -диолы.[22] Реакции экзотермические и обычно проводятся при 0 ° C. Поскольку соли периодата легко растворимы в воде, реакции обычно проводят в водной среде. Если растворимость является проблемой, может использоваться периодическая кислота, так как она растворима в спиртах; катализаторы межфазного переноса также эффективны в двухфазный реакционные смеси. В крайнем случае периодат можно обменять на тетраацетат свинца который реагирует аналогичным образом и растворим в органических растворителях (Криджи окисление ).

Расщепление периодатом часто используется в молекулярной биохимии с целью модификации сахарид кольца, так как многие пяти- и шестичленные сахара имеют вицинальные диолы. Исторически его также использовали для определения структуры моносахаридов.[23][24]
Расщепление периодатом можно проводить в промышленных масштабах с образованием диальдегидный крахмал который используется в производство бумаги.[25]
Реакции окисления
Периодаты сильные окислители. Они могут окислять катехол к 1,2-бензохинон и гидрохинон к 1,4-бензохинон.[26] Сульфиды может быть эффективно окислен до сульфоксиды.[27] Периодаты являются достаточно мощными, чтобы генерировать другие сильные неорганические окислители, такие как перманганат,[28] четырехокись осмия[29]и четырехокись рутения.
Ниша использует
Периодаты являются высокоселективными травителями для определенных рутений оксиды на основе.[30]
Несколько окрашивание агенты используют в микроскопия основаны на периодате (например, периодная кислота – краситель Шиффа и Пятно Джонса )
Периодаты также использовались в качестве окислителей для использования в пиротехника.[31] В 2013 г. Армия США объявил, что заменит экологически вредные химические вещества нитрат бария и перхлорат калия с метапериодат натрия для использования в их трассирующих боеприпасах.[32]
Другие оксианионы
Периодат является частью ряда оксианионов, в которых йод могу предположить состояния окисления из −1, +1, +3, +5 или +7. Ряд нейтральных оксиды йода также известны.
| Степень окисления йода | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | йодид | гипойодит | йодит | йодат | периодировать |
| Формула | я− | IO− | IO− 2 | IO− 3 | IO− 4 или же IO5− 6 |
| Структура |  |
Смотрите также
Рекомендации
- ^ Ammermüller, F .; Магнус, Г. (1833). "Ueber eine neue Verbindung des Jods mit Sauerstoff, die Ueberjodsäure". Annalen der Physik und Chemie (на немецком). 104 (7): 514–525. Bibcode:1833АнП ... 104..514А. Дои:10.1002 / andp.18331040709.
- ^ а б Райли, под редакцией Георга Брауэра; переведен Scripta Technica, Inc. Редактор переводов Рид Ф. (1963). Справочник по препаративной неорганической химии. Том 1 (2-е изд.). Нью-Йорк, Нью-Йорк: Academic Press. С. 323–324. ISBN 012126601X.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Хилл, Артур Э. (октябрь 1928 г.). "Тройные системы. VII. Периоды щелочных металлов". Журнал Американского химического общества. 50 (10): 2678–2692. Дои:10.1021 / ja01397a013.
- ^ Парсонс, Роджер (1959). Справочник электрохимических констант. Butterworths Scientific Publications Ltd. стр.71.
- ^ Aylett, основанная А.Ф. Холлеманом; продолжение Эгон Виберг; переведены Мэри Иглсон, Уильямом Брюером; переработано Бернхардом Дж. (2001). Неорганическая химия (1-е английское изд., [Отредактировано] Нильсом Вибергом. Ред.). Сан-Диего, Калифорния: Берлин: Academic Press, W. de Gruyter. п. 454. ISBN 0123526515.
- ^ Бурго, Жан-Луи (30 марта 2012 г.). Ионные равновесия в аналитической химии. Нью-Йорк: Спрингер. п. 358. ISBN 978-1441983824.
- ^ Ропп, Ричард К. (31 декабря 2012 г.). Энциклопедия щелочноземельных соединений. Оксфорд: Elsevier Science. п. 96. ISBN 978-0444595539.
- ^ а б Фейкема, Ю. Д. (1966). «Кристаллические структуры двух оксикислот йода. I. Исследование ортопериодовой кислоты, H5IO6, методом нейтронографии ». Acta Crystallographica. 20 (6): 765–769. Дои:10.1107 / S0365110X66001828.
- ^ Greenwood, N.N .; Эрншоу, А. (2006). Химия элементов (2-е изд.). Оксфорд: Баттерворт-Хайнеманн. п.874. ISBN 0750633654.
- ^ Иванов, А .; Попов, А .; Болдырев, А .; Жданкин, В. (2014). «Двойная связь I = X (X = O, N, C) в соединениях гипервалентного йода: это реально?». Энгью. Chem. Int. Эд. 53 (36): 9617–9621. Дои:10.1002 / anie.201405142. PMID 25045143.
- ^ Tichý, K .; Rüegg, A .; Бенеш, Дж. (1980). "Нейтронографическое исследование трехводородного периодата диаммония (NH4)2ЧАС3IO6, и его дейтериевый аналог (ND4)2D3IO6". Acta Crystallographica Раздел B. 36 (5): 1028–1032. Дои:10.1107 / S0567740880005225.
- ^ Levason, W .; Вебстер, М. (15 июня 1999 г.). «Тетраоксойодат аммония (VII)». Acta Crystallographica Раздел C. 55 (6): IUC9900052. Дои:10.1107 / S0108270199099394.
- ^ Kálmán, A .; Круикшанк, Д. В. Дж. (1970). «Уточнение структуры NaIO4". Acta Crystallographica Раздел B. 26 (11): 1782–1785. Дои:10.1107 / S0567740870004880.
- ^ Скларц, Б. (1967). «Органическая химия периодатов». Ежеквартальные обзоры, Химическое общество. 21 (1): 3. Дои:10.1039 / QR9672100003.
- ^ Bamford, под редакцией C.H .; Самосвал, C.F.H. (1972). Реакции неметаллических неорганических соединений. Амстердам: паб Elsevier. Co. p. 435. ISBN 9780080868011.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Л. Малапраде, Бык. Soc. Чим. Пт. 3, 1, 833 (1934)
- ^ Зажим, J.R .; Хаф, Л. (январь 1965 г.). «Периодатное окисление аминокислот со ссылкой на исследования гликопротеинов». Биохимический журнал. 94: 17–24. Дои:10.1042 / bj0940017. ЧВК 1206400. PMID 14342227.
- ^ Николет, Бен Х .; Шинн, Лео А. (июнь 1939 г.). «ДЕЙСТВИЕ ПЕРИОДИЧЕСКОЙ КИСЛОТЫ НА α-АМИНО СПИРТЫ». Журнал Американского химического общества. 61 (6): 1615. Дои:10.1021 / ja01875a521.
- ^ Марош, Ласло; Мольнар-Перл, Иболя; Шиссель, Энико; Зердахелий, Вильмос (1980). «Механизм периодатного окисления этан-1,2-диамина». N,N'-Диметилэтан-1,2-диамин и 2-аминоэтанол ». Журнал химического общества, Perkin Transactions 2 (1): 39–45. Дои:10.1039 / P29800000039.
- ^ Telvekar, Vikas N .; Patel, Dharmeshkumar J .; Мишра, Санкет Дж. (2008). «Окислительное расщепление эпоксидов с использованием водного парапериодата натрия». Синтетические коммуникации. 39 (2): 311–315. Дои:10.1080/00397910802372574. S2CID 97403497.
- ^ Buist, G.J .; Bunton, C.A .; Хипперсон, У. С. П. (1971). «Механизм окисления α-гликолей периодической кислотой. Часть X. Окисление пинакола и общее обсуждение стабильности эфиров периодата и их роли в механизме окисления». Журнал химического общества B: Physical Organic: 2128–2142. Дои:10.1039 / J29710002128.
- ^ Макмерри, Джон (2012). Органическая химия (8-е изд., [Международное изд.] Изд.). Сингапур: Brooks / Cole Cengage Learning. п.312. ISBN 978-0840054531.
- ^ Джексон, Эрнест Л .; Хадсон, С.С. (июнь 1937 г.). «Исследования расщепления углеродной цепи гликозидов путем окисления. Новый метод определения кольцевых структур и альфа- и бета-конфигураций гликозидов». Журнал Американского химического общества. 59 (6): 994–1003. Дои:10.1021 / ja01285a010.
- ^ Робит, Джон Ф. (1998). Основы химии углеводов. Нью-Йорк: Спрингер. ISBN 0387949518.
- ^ Ю, Цзюгао; Чанг, Питер Р .; Ма, Сяофэй (январь 2010 г.). «Получение и свойства диальдегидного крахмала и термопластичного диальдегидного крахмала». Углеводные полимеры. 79 (2): 296–300. Дои:10.1016 / j.carbpol.2009.08.005.
- ^ Weidman, S.W .; Кайзер, Э. Т. (декабрь 1966 г.). "Механизм периодата окисления ароматических систем. III. Кинетическое исследование периодатного окисления катехола". Журнал Американского химического общества. 88 (24): 5820–5827. Дои:10.1021 / ja00976a024.
- ^ Леонард, Нельсон Дж .; Джонсон, Карл Р. (январь 1962 г.). "Периодатное окисление сульфидов до сульфоксидов. Объем реакции". Журнал органической химии. 27 (1): 282–284. Дои:10.1021 / jo01048a504.
- ^ Lemieux, R.U .; Рудлофф, Э. Фон (ноябрь 1955 г.). «Периодатно-перманганатное окисление: I. Окисление олефинов». Канадский химический журнал. 33 (11): 1701–1709. Дои:10.1139 / v55-208.
- ^ Pappo, R .; Allen, Jr., D. S .; Lemieux, R.U .; Джонсон, В. С. (1956). «Примечания - Окисление олефиновых связей, катализируемое тетроксидом осмия, периодатом». Журнал органической химии. 21 (4): 478–479. Дои:10.1021 / jo01110a606. ISSN 0022-3263.
- ^ Дитер Вебер, Роза Вёфели, Юэхуа Чен, Юлия Мурзина, Ульрих Поппе: Переменный резистор, изготовленный путем повторяющихся этапов эпитаксиального осаждения и литографического структурирования оксидных слоев с использованием влажных химических травителей.. Тонкие твердые пленки (2013) DOI: 10.1016 / j.tsf.2012.11.118
- ^ Моретти, Джаред Д .; Сабатини, Джесси Дж .; Чен, Гэри (9 июля 2012 г.). «Соли периодата как пиротехнические окислители: разработка зажигательных составов, не содержащих бария и перхлоратов». Angewandte Chemie International Edition. 51 (28): 6981–6983. Дои:10.1002 / anie.201202589. PMID 22639415.
- ^ «Пикатинни для выведения тонны токсинов из смертельных патронов». Армия США. Получено 31 октября 2013.
