Фотооксигенация - Photooxygenation
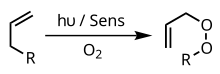
А фотооксигенация реакция окисления под действием света, при которой молекулярный кислород входит в состав продукта (ов).[1][2] Первоначальный исследовательский интерес к реакциям фотооксигенации возник после наблюдений Оскара Рааба в 1900 году о том, что сочетание света, кислорода и фотосенсибилизаторов очень токсично для клеток.[3] Ранние исследования фотооксигенации были сосредоточены на окислительном повреждении ДНК и аминокислот,[2] но недавние исследования привели к применению фотооксигенации в органическом синтезе и фотодинамическая терапия.[4]
Реакции фотооксигенации инициируются фотосенсибилизатор, которая представляет собой молекулу, которая входит в возбужденное состояние при воздействии света определенной длины волны (например, красителей и пигментов). Затем возбужденный сенсибилизатор реагирует либо с субстратом, либо с молекулярным кислородом в основном состоянии, запуская каскад передачи энергии, который в конечном итоге приводит к оксигенированной молекуле. Следовательно, реакции фотооксигенации классифицируются по типу и порядку этих промежуточных продуктов (как тип I, тип II или тип III.[5] реакции).[2][3]
Фон
Терминология
Реакции фотооксигенации легко спутать с рядом процессов, имеющих похожие названия (например, фотосенсибилизированное окисление). Четкие различия можно провести по трем признакам: окисление, участие света и включение молекулярного кислорода в продукты:

Сенсибилизаторы

Сенсибилизаторы (обозначаемые «Sens») представляют собой соединения, такие как флуоресцеиновые красители, метиленовый синий, и полициклические ароматические углеводороды, которые способны поглощать электромагнитное излучение (обычно в видимом диапазоне спектра) и в конечном итоге передают эту энергию молекулярному кислороду или субстрату процесса фотооксигенации. Многие сенсибилизаторы, как естественные, так и синтетические, зависят от обширного ароматические системы поглощать свет в видимом спектре.[4] Когда сенсибилизаторы возбуждаются светом, они достигают синглетное состояние, 1Sens *. Этот синглет затем преобразуется в триплетное состояние (что более стабильно), 3Sens *, через межсистемный переход. В 3Sens * - это то, что реагирует либо с субстратом, либо с 3О2 в трех типах реакций фотооксигенации.[6]
Состояния молекулярного кислорода
В классическом Структуры Льюиса, молекулярный кислород, O2, изображается как имеющий двойную связь между двумя атомами кислорода. Однако молекулярные орбитали O2 на самом деле более сложны, чем предполагают структуры Льюиса. В самая высокая занятая молекулярная орбиталь (ВЗМО) из O2 пара вырожденных разрушение π орбитали, π2 пикселя* и π2py*, которые оба заняты спиновыми неспаренными электронами.[4] Эти электроны являются причиной O2 быть триплет бирадикал в основном состоянии (обозначен как 3О2).
В то время как HOMO многих стабильных молекул состоят из связывающих молекулярных орбиталей и, следовательно, требуют умеренного скачка энергии от связывания к разрыхлению для достижения своего первого возбужденного состояния, антисвязывающая природа ВЗМО молекулярного кислорода позволяет уменьшить энергетический зазор между его основным состоянием и первым возбужденным состоянием. . Это делает возбуждение O2 менее энергетически ограничительный процесс. В первом возбужденном состоянии O2, при увеличении энергии на 22 ккал / моль по сравнению с основным состоянием, оба электрона в разрыхляющих орбиталях занимают вырожденную π * -орбиталь, а кислород теперь находится в синглет состояние (обозначено как 1О2).[3] 1О2 очень реактивен со сроком службы 10–100 мкс.[4]
Типы фотооксигенации
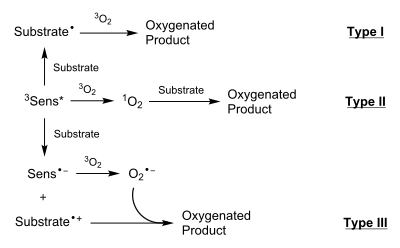
Три типа реакций фотооксигенации различаются механизмами, через которые они протекают, поскольку они способны давать разные или похожие продукты в зависимости от условий окружающей среды. Реакции типа I и II протекают через нейтральные промежуточные соединения, тогда как реакции типа III протекают через заряженные частицы. Отсутствие или наличие 1О2 это то, что отличает реакции типа I и типа II соответственно.[1]
Тип I
При реакциях типа I фотоактивированные 3Sens * взаимодействует с субстратом, образуя радикальный субстрат, обычно через гомолитический разрыв водородной связи на подложке. Этот радикал субстрата затем взаимодействует с 3О2 (основное состояние) для получения субстрата-O2 радикальный. Такой радикал обычно гасят, отводя водород от другой молекулы субстрата или от растворителя. Этот процесс позволяет цепному распространению реакции.
Пример: захват кислорода бирадикальными промежуточными продуктами
Реакции фотооксигенации типа I часто используются в процессе образования и улавливания. бирадикал разновидность. Мирбах и др. сообщил об одной такой реакции, в которой азосоединение лизируется через фотолиз с образованием бирадикального углеводорода, который затем поэтапно захватывается молекулярным кислородом:[7]

Тип II
В реакциях типа II 3Sens * передает свою энергию напрямую 3О2 через безызлучательный переход для создания 1О2. 1О2 затем добавляет к субстрату различными способами, включая: циклоприсоединения (чаще всего [4 + 2]), добавление к двойным связям для получения 1,2-диоксетаны, и ее реакции с олефины.[2]
Пример: предшественник синтеза простагландинов.
[4 + 2] циклоприсоединение синглетного кислорода к циклопентадиен создавать СНГ-2-циклопентен-1,4-диол - это обычная стадия синтеза простагландины.[8] Первоначальное добавление синглетного кислорода через согласованное [4 + 2] циклоприсоединение образует нестабильный эндопероксид. Последующее уменьшение пероксидной связи дает две спиртовые группы.

Тип III
В реакциях III типа наблюдается перенос электронов что происходит между 3Sens * и субстратом, что приводит к анионный Sens и a катионный субстрат. Затем происходит другой перенос электрона, когда анионный сенсор переносит электрон на 3О2 сформировать супероксид-анион, O2−. Эта передача возвращает Sens в его основное состояние. Затем супероксид-анион и катионный субстрат взаимодействуют с образованием насыщенного кислородом продукта.
Пример: фотооксигенация индолизина
Фотооксигенация индолизины (гетероциклические ароматические производные индола) были исследованы как в механистическом, так и в синтетическом контексте. Вместо того, чтобы действовать по механизму фотооксигенации типа I или типа II, некоторые исследователи решили использовать 9,10-дицианоантрацен (DCA) в качестве фотосенсибилизатора, что привело к реакции производного индолизина с супероксид-анион-радикалом. Обратите внимание, что реакция протекает через промежуточный катион-радикал индолизина, который не был выделен (и поэтому не показан):[9]

Приложения
Органический синтез
Все 3 типа фотооксигенации были применены в контексте органического синтеза. В частности, фотооксигенация типа II оказалась наиболее широко используемой (из-за низкого количества энергии, необходимой для генерации синглетного кислорода) и была описана как «один из самых мощных методов фотохимической оксифункционализации органических соединений».[10] Эти реакции могут протекать во всех обычных растворителях и с широким спектром сенсибилизаторов.
Многие из применений фотооксигенации типа II в органическом синтезе исходят из исследований Вальдемара Адама по еновой реакции синглетного кислорода с ациклическими алкенами.[10] Сквозь цис-эффект и наличие соответствующих управляющих групп реакция может даже обеспечить высокий региоселективно и диастереоселективность - два ценных стереохимических контроля.[11]

Фотодинамическая терапия
Фотодинамическая терапия (ФДТ) использует фотооксигенацию для разрушения раковая ткань.[12] В опухоль вводят фотосенсибилизатор, а затем на ткань воздействуют светом определенной длины волны для возбуждения Sens. Возбужденный Sens обычно следует механизму фотооксигенации типа I или II, что приводит к окислительное повреждение в клетки. Обширное окислительное повреждение опухолевых клеток убивает опухолевые клетки. Кроме того, окислительное повреждение близлежащих кровеносных сосудов вызывает локальную агломерацию и прекращает поступление питательных веществ в опухоль, что приводит к голоду опухоли.[13]
Важным фактором при выборе Sens для использования в PDT является определенная длина волны света, которую Sens будет поглощать, чтобы перейти в возбужденное состояние. Поскольку максимальное проникновение в ткани достигается в диапазоне длин волн 800 нм, выбор Sens, которые поглощают в этом диапазоне, является преимуществом, поскольку он позволяет ФДТ воздействовать на опухоли под самым внешним слоем дермы. Окно света 800 нм наиболее эффективно для проникновения в ткани, потому что на длинах волн короче 800 нм свет начинает рассеиваться макромолекулами клеток, а на длинах волн более 800 нм молекулы воды начинают поглощать свет и превращать его в тепло. .[4]
Рекомендации
- ^ а б ИЮПАК (1997). А. Д. Макнот и А. Уилкинсон (ред.). Сборник химической терминологии. Научные публикации Блэквелла, Оксфорд. Дои:10.1351 / goldbook. ISBN 978-0-9678550-9-7.
- ^ а б c d M. R. Iesce; и другие. (2005). «Фотооксигенация гетероциклов». Curr. Орг. Chem. 9 (2): 109–139. Дои:10.2174/1385272053369222.
- ^ а б c К.С. Фут (1968). «Механизмы фотосенсибилизированного окисления». Наука. 162 (3857): 963–970. Bibcode:1968Sci ... 162..963F. Дои:10.1126 / science.162.3857.963.
- ^ а б c d е И. Дж. Макдональд и Т. Дж. Догерти (2001). «Основные принципы фотодинамической терапии». Журнал порфиринов и фталоцианинов. 5 (2): 105–129. Дои:10.1002 / jpp.328.
- ^ Большая часть новейшей литературы (после 2000 г.) включает классификацию «Тип III»; однако более старые статьи признают только Тип I и Тип II как названные классы реакций фотооксигенации.
- ^ К.С. Фут (1987). Механизмы фотодинамического действия типа I и типа II. Серия симпозиумов ACS. 339. С. 22–38. Дои:10.1021 / bk-1987-0339.ch002. ISBN 978-0-8412-1026-4.
- ^ Мирбах, Марлис; М. Манфред; А. Саус (1982). «Фотохимия высокого давления и ультрафиолетовая спектроскопия в системах газ – жидкость». Химические обзоры. 82 (1): 59–76. Дои:10.1021 / cr00047a003.
- ^ Аист, Гилберт; П. Шер; Х. Чен (октябрь 1986 г.). «Радикальная циклизация-улавливание при синтезе натуральных продуктов. Простой стереоконтролируемый путь к простагландину Fza». Варенье. Chem. Soc. 108 (20): 6384–6385. Дои:10.1021 / ja00280a043.
- ^ Ли, Юнь; Х. Ху; J. Ye; H. Fun; Х. Ху; Дж. Сюй (2004). «Режимы и механизм реакций в реакциях фотооксигенации индолизина». Журнал органической химии. 69 (7): 2332–2339. Дои:10.1021 / jo035070d.
- ^ а б Румбах, отредактированный Йохеном Маттеем и Акселем Г. Грисбеком в сотрудничестве с Кристианом Штаммелем, Иоахимом Хиртом и Томасом (1994). Йохен Маттай и Аксель Грисбек (ред.). Ключевые шаги фотохимии в органическом синтезе: экспериментальный учебник. Вайнхайм: ВЧ. ISBN 978-3-527-29214-1.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Адам, Вальдемар; В. Бруенкер (1993). «Диастереоселективная и региоселективная фотооксигенация хирального аллильного амина и его ацильных производных: стереохимическое доказательство регулирующего эффекта аминогруппы в еновой реакции синглетного кислорода». Варенье. Chem. Soc. 115 (7): 3008–3009. Дои:10.1021 / ja00060a072.
- ^ Догерти, Томас (май 1987). «Фотосенсибилизаторы: терапия и выявление злокачественных опухолей». Фотохимия и фотобиология. 45 (445): 879–889. Дои:10.1111 / j.1751-1097.1987.tb07898.x.
- ^ Чен, Цюнь; З. Хуанг; Х. Чен; Х. Шапиро; Дж. Бекерс; Ф. Хетцель (август 2002 г.). «Улучшение ответа опухоли за счет манипулирования оксигенацией опухоли во время фотодинамической терапии». Фотохимия и фотобиология. 76 (2): 197–203. Дои:10.1562 / 0031-8655 (2002) 0760197IOTRBM2.0.CO2.

![{ displaystyle { ce {Sens -> [hv] {^ {1} Sens ^ { ast}} -> {^ {3} Sens ^ { ast}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6215cad829b7f70ab6da195d2ccda72164afd506)
