Пресенилин - Presenilin
| Пресенилин | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Символ | Пресенилин | ||||||||
| Pfam | PF01080 | ||||||||
| Pfam клан | CL0130 | ||||||||
| ИнтерПро | IPR001108 | ||||||||
| МЕРОПЫ | A22 | ||||||||
| TCDB | 1.A.54 | ||||||||
| OPM суперсемейство | 244 | ||||||||
| Белок OPM | 4хиг | ||||||||
| |||||||||
| пресенилин 1 (Болезнь Альцгеймера 3) | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | PSEN1 | ||||||
| Альт. символы | AD3 | ||||||
| Ген NCBI | 5663 | ||||||
| HGNC | 9508 | ||||||
| OMIM | 104311 | ||||||
| RefSeq | NM_000021 | ||||||
| UniProt | P49768 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 3.4.23.- | ||||||
| Locus | Chr. 14 q24.3 | ||||||
| |||||||
| пресенилин 2 (Болезнь Альцгеймера 4) | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | PSEN2 | ||||||
| Альт. символы | AD4 | ||||||
| Ген NCBI | 5664 | ||||||
| HGNC | 9509 | ||||||
| OMIM | 600759 | ||||||
| RefSeq | NM_000447 | ||||||
| UniProt | P49810 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 3.4.23.- | ||||||
| Locus | Chr. 1 q31-q42 | ||||||
| |||||||
Пресенилины представляют собой семейство родственных многопроходных трансмембранных белков, которые составляют каталитические субъединицы гамма-секретаза внутримембранная протеаза сложный. Впервые они были идентифицированы при скрининге мутаций, вызывающих ранние формы семейного Болезнь Альцгеймера к Питер Сент-Джордж-Хислоп на Центр исследований нейродегенеративных заболеваний на Университет Торонто, а теперь и на Кембриджский университет.[3] У позвоночных есть два пресенилина. гены, называется PSEN1 (расположен на хромосома 14 у человека), который кодирует пресенилин 1 (PS-1) и PSEN2 (на хромосома 1 у человека), который кодирует пресенилин 2 (PS-2).[4] Оба гена сохраняются у разных видов, с небольшими различиями между пресенилинами крысы и человека. Червь нематода C. elegans имеет два гена, которые напоминают пресенилины и кажутся функционально подобными, сел-12 и хмель-1.[5]
Пресенилины расщепляются в альфа-спиральной области одной из петель цитоплазмы с образованием большого N-концевой и меньший C-терминал фрагмент, который вместе составляет часть функционального белка.[1] Расщепление пресенилина 1 можно предотвратить с помощью мутация что вызывает потерю экзона 9 и приводит к потере функции. Пресенилины играют ключевую роль в модуляции внутриклеточного Ca2+ участвует в высвобождении пресинаптического нейротрансмиттера и индукции долгосрочной потенциации.[6]
Структура
Структура пресенилин-1 до сих пор остается спорным, хотя недавние исследования привели к более широко принятой модели. При первом обнаружении PSEN1 Ген был подвергнут анализу гидрофобности, который предсказал, что белок будет содержать десять трансмембранных доменов. Все предыдущие модели согласились с тем, что первые шесть предполагаемых межмембранных областей пересекают мембрану. Эти области соответствуют N-концевому фрагменту PS-1, но структура C-концевого фрагмента оспаривается. Недавняя статья Spasic et al.[7] предоставляет убедительные доказательства наличия девяти трансмембранных структур с расщеплением и сборкой в гамма-секретазу сложный перед вставкой в плазматическая мембрана. Однако, поскольку это белок с большим количеством гидрофобных участков, маловероятно, что рентгеновская кристаллография предоставит окончательное доказательство структуры.
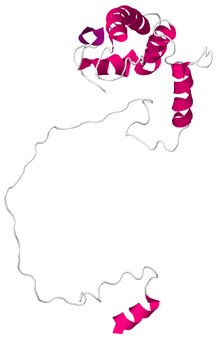
Строение С-концевого каталитического фрагмента пресенилина-1 определяли с помощью растворного ЯМР. Он состоит из альфа-спиралей и имеет длину 176 аминокислот.[1]
Функция
Большинство случаев болезни Альцгеймера не передаются по наследству. Тем не менее, существует небольшая группа случаев, у которых более ранний возраст начала заболевания и которые имеют сильный генетический элемент. У пациентов, страдающих Болезнь Альцгеймера (аутосомно-доминантный наследственный), мутации в пресенилине белки (PSEN1; PSEN2) или белок-предшественник амилоида (APP) можно найти. В большинстве этих случаев присутствуют мутантные гены пресенилина. Важной частью болезненного процесса при болезни Альцгеймера является накопление Амилоид бета (Aβ) белок. Для образования Aβ необходимо разрезать APP на два ферменты, бета-секреты и гамма-секретаза. Пресенилин - это субкомпонент гамма-секретазы, который отвечает за разрезание APP.
Гамма-секретаза может разрезать APP в нескольких точках в пределах небольшой области белка, что приводит к Aβ различной длины. Длина, связанная с болезнью Альцгеймера, составляет 40 и 42 аминокислоты. Aβ 42 с большей вероятностью будет агрегировать с образованием бляшек в головном мозге, чем Aβ 40. Мутации пресенилина приводят к увеличению отношения продуцируемого Aβ 42 по сравнению с Aβ 40, хотя общее количество продуцируемого Aβ остается постоянным.[8] Это может происходить из-за различных эффектов мутаций на гамма-секретазу.[9] Пресенилины также участвуют в переработке выемка, важный белок развития. Мыши, у которых был отключен ген PS1, умирают на раннем этапе развития от аномалий развития, аналогичных тем, которые обнаруживаются при нарушении метки.[10]
Гены пресенилинов были обнаружены в ходе исследований сцепления с использованием мутаций, присутствующих в семейных случаях болезни Альцгеймера в 1995 году.[3]
Генетическая инактивация пресенилинов в гиппокамп синапсов показало, что это избирательно влияет на долгосрочное потенцирование вызванный тета с инактивацией в пресинапсе, но не в постсинапсе, ухудшающем краткосрочную пластичность и синаптическое облегчение.[6] Высвобождение глутамата также снижалось в пресинаптических окончаниях за счет процессов, которые включают модуляцию внутриклеточного Ca2+ релиз.[6] Было высказано предположение, что это «представляет собой общий конвергентный механизм, ведущий к нейродегенерации».[6]
Рекомендации
- ^ а б c Собханифар, S; Шнайдер, Б; Löhr, F; Gottstein, D; Икея, Т; Млынарчик, К; Пулавски, В; Ghoshdastider, U; Колинский, М; Филипек, S; Güntert, P; Бернхард, Ф; Дёч, V (2010). «Структурное исследование С-концевого каталитического фрагмента пресенилина 1». Труды Национальной академии наук. 107 (21): 9644–9. Bibcode:2010PNAS..107.9644S. Дои:10.1073 / pnas.1000778107. ЧВК 2906861. PMID 20445084.
- ^ PDB: 2KR6; Doetsch V (2010). «Структура раствора субъединицы CTF пресенилина-1». Будут опубликованы. Дои:10.2210 / pdb2kr6 / pdb.
- ^ а б Шеррингтон Р., Рогаев Е.И., Лян Ю., Рогаева Е.А., Левеск Дж., Икеда М., Чи Х., Лин Ц., Ли Г., Холман К. (июнь 1995 г.). «Клонирование гена, несущего миссенс-мутации, при семейной болезни Альцгеймера с ранним началом». Природа. 375 (6534): 754–60. Bibcode:1995Натура.375..754S. Дои:10.1038 / 375754a0. PMID 7596406.
- ^ Леви-Лахад Э, Васко В., Пуркадж П., Романо Д.М., Осима Дж., Петтингелл У.Х., Ю. CE, Джондро П.Д., Шмидт С.Д., Ван К., Кроули А.С., Фу Й.Х., Генетт С.Ю., Галас Д., Неменс Э., Вийсман Е. Bird TD, Schellenberg GD, Tanzi RE (сентябрь 1995 г.). «Ген-кандидат в семейный локус болезни Альцгеймера на хромосоме 1». Наука. 269 (5226): 973–977. Bibcode:1995Научный ... 269..973L. Дои:10.1126 / science.7638622. PMID 7638622.
- ^ Smialowska A, Baumeister R (2006). «Функция пресенилина у Caenorhabditis elegans». Neurodegener Dis. 3 (4–5): 227–32. Дои:10.1159/000095260. PMID 17047361.
- ^ а б c d Чжан К., Ву Б., Беглопулос В., Вин-Самуэльсон М., Чжан Д., Драгацис И., Зюдхоф ТК, Шен Дж. (Июль 2009 г.). «Пресенилины необходимы для регулирования высвобождения нейротрансмиттеров». Природа. 460 (7255): 632–6. Bibcode:2009Натура.460..632Z. Дои:10.1038 / природа08177. ЧВК 2744588. PMID 19641596.
- ^ Спасич Д., Толик А., Диллен К., Баерт В., Де Строопер Б., Фрайенс С., Аннаерт В. (сентябрь 2006 г.). «Пресенилин-1 поддерживает топологию девяти трансмембран по всему секреторному пути». J. Biol. Chem. 281 (36): 26569–77. Дои:10.1074 / jbc.M600592200. PMID 16846981.
- ^ Citron M, Westaway D, Xia W, Carlson G, Diehl T, Levesque G, Johnson-Wood K, Lee M, Seubert P, Davis A, Kholodenko D, Motter R, Sherrington R, Perry B, Yao H, Strome R, Либербург I, Ромменс Дж., Ким С., Шенк Д., Фрейзер П., Сент-Джордж Хислоп П., Селкое Д. Д. (январь 1997 г.). «Мутантные пресенилины при болезни Альцгеймера увеличивают продукцию бета-белка амилоида с 42 остатками как в трансфицированных клетках, так и в трансгенных мышах». Nat. Med. 3 (1): 67–72. Дои:10,1038 / нм0197-67. PMID 8986743.
- ^ Bentahir M, Nyabi O, Verhamme J, Tolia A, Horré K, Wiltfang J, Esselmann H, De Strooper B (февраль 2006 г.). «Клинические мутации пресенилина могут влиять на активность гамма-секретазы по разным механизмам». J. Neurochem. 96 (3): 732–42. Дои:10.1111 / j.1471-4159.2005.03578.x. PMID 16405513.
- ^ Шен Дж., Бронсон Р. Т., Чен Д. Ф., Ся В., Селкое Д. Д., Тонегава С. (май 1997 г.). «Дефекты скелета и ЦНС у мышей с дефицитом пресенилина-1». Клетка. 89 (4): 629–39. Дои:10.1016 / S0092-8674 (00) 80244-5. PMID 9160754.
внешняя ссылка
- В МЕРОПЫ онлайн-база данных пептидаз и их ингибиторов: Пресенилин 1 A22.001, Пресенилин 2 A22.002
- Сеть доминантно наследуемой болезни Альцгеймера (ДИАН)
- Расширенный реестр доминантно наследуемой сети Альцгеймера (DIAN)
- Пресенилины в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
