Адсорбция - Adsorption

Адсорбция это адгезия из атомы, ионы или же молекулы от газа, жидкости или растворенного твердого вещества до поверхность.[1] Этот процесс создает фильм адсорбат на поверхности адсорбент. Этот процесс отличается от поглощение, в котором жидкость (в впитывать) является растворенный по или проникает жидкое или твердое ( абсорбент), соответственно.[2] Адсорбция - это поверхностное явление, в то время как абсорбция охватывает весь объем материала, хотя адсорбция часто предшествует абсорбции.[3] Период, термин сорбция охватывает оба процесса, а десорбция это наоборот.
Примечание 1. Адсорбция белков имеет большое значение, когда материал находится в контакте с кровью или биологическими жидкостями. В случае с кровью альбумин, который в значительной степени преобладает, обычно сначала адсорбируется, а затем происходят перегруппировки в пользу других второстепенных белков в соответствии с поверхностным сродством против отбора по закону масс (Эффект Вромана ).
Примечание 2: Адсорбированные молекулы - это те молекулы, которые устойчивы к промывке той же самой растворительной средой в случае адсорбции из растворов. Таким образом, условия стирки могут изменять результаты измерения, особенно при низкой энергии взаимодействия.[4]Похожий на поверхностное натяжение адсорбция является следствием поверхностная энергия. В сыпучем материале все требования к склеиванию (будь то ионный, ковалентный или же металлический ) составляющей атомы материала заполнены другими атомами в материале. Однако атомы на поверхности адсорбента не полностью окружены другими атомами адсорбента и поэтому могут притягивать адсорбаты. Точный характер связывания зависит от деталей участвующих частиц, но процесс адсорбции обычно классифицируется как физическая адсорбция (характеристика слабого силы Ван дер Ваальса ) или хемосорбция (характеристика ковалентной связи). Это также может произойти из-за электростатического притяжения.[5]
Адсорбция присутствует во многих природных, физических, биологических и химических системах и широко используется в промышленных приложениях, таких как гетерогенные катализаторы,[6][7] активированный уголь, захват и использование отходящее тепло для обеспечения холодной водой для кондиционирования воздуха и других технологических требований (адсорбционные чиллеры ), синтетические смолы, увеличивая емкость хранения карбидный углерод и очистка воды. Адсорбция, ионный обмен и хроматография представляют собой сорбционные процессы, в которых определенные адсорбаты избирательно переносятся из жидкой фазы на поверхность нерастворимых твердых частиц, взвешенных в сосуде или упакованных в колонку. Применения в фармацевтической промышленности, в которых адсорбция используется как средство продления неврологического воздействия определенных лекарств или их частей,[нужна цитата ] менее известны.
Слово «адсорбция» было придумано в 1881 году немецким физиком. Генрих Кайзер (1853–1940).[8]
Изотермы
Адсорбция газов и растворенных веществ обычно описывается с помощью изотерм, то есть количества адсорбата на адсорбенте как функции его давления (для газа) или концентрации (для растворенных веществ в жидкой фазе) при постоянной температуре. Адсорбированное количество почти всегда нормируется на массу адсорбента, чтобы можно было сравнивать различные материалы. На сегодняшний день разработано 15 различных моделей изотерм.[9]
Линейный
Freundlich
Первая математическая аппроксимация изотермы была опубликована Фрейндлихом и Кустером (1906) и представляет собой чисто эмпирическую формулу для газообразных адсорбатов:
куда - масса адсорбированного адсорбата, - масса адсорбента, - давление адсорбата (его можно изменить на концентрацию, если исследуется раствор, а не газ), и и - эмпирические константы для каждой пары адсорбент – адсорбат при данной температуре. Эта функция неадекватна при очень высоком давлении, потому что в действительности имеет асимптотический максимум при неограниченном увеличении давления. С повышением температуры постоянные и изменение, чтобы отразить эмпирическое наблюдение, что адсорбированное количество растет медленнее и требуется более высокое давление для насыщения поверхности.
Langmuir
Ирвинг Ленгмюр был первым, кто получил научно обоснованную изотерму адсорбции в 1918 году.[10] Модель применима к газам, адсорбированным на твердых поверхностях. Это полуэмпирическая изотерма с кинетической основой, полученная на основе статистической термодинамики. Это наиболее распространенное уравнение изотермы из-за его простоты и способности соответствовать различным данным адсорбции. Он основан на четырех предположениях:
- Все сайты адсорбции эквивалентны, и каждый сайт может вместить только одну молекулу.
- Поверхность энергетически однородна, адсорбированные молекулы не взаимодействуют.
- Фазовых переходов нет.
- При максимальной адсорбции образуется только монослой. Адсорбция происходит только на локализованных участках поверхности, а не с другими адсорбатами.
Эти четыре предположения редко бывают верными: всегда есть дефекты на поверхности, адсорбированные молекулы не обязательно инертны, и механизм, очевидно, не тот, что самые первые молекулы адсорбируются на поверхность, как для последних. Четвертое условие является наиболее неприятным, поскольку часто на монослой адсорбируется больше молекул; эта проблема решается Изотерма БЭТ для относительно плоских (не-микропористый ) поверхностей. Тем не менее изотерма Ленгмюра является первым выбором для большинства моделей адсорбции и имеет множество приложений в поверхностной кинетике (обычно называемой Кинетика Ленгмюра – Хиншелвуда ) и термодинамика.
Ленгмюр предположил, что адсорбция происходит по такому механизму: , куда А - молекула газа, а S адсорбционный сайт. Прямая и обратная константы скорости равны k и k−1. Если мы определим покрытие поверхности, , как доля занятых адсорбционных центров, в равновесии имеем:
или же
куда - парциальное давление газа или молярная концентрация раствора. Для очень низких давлений , а при высоких давлениях .
Значение сложно измерить экспериментально; обычно адсорбатом является газ, и адсорбированное количество указывается в молях, граммах или объемах газа при стандартная температура и давление (STP) на грамм адсорбента. Если мы позвоним vпн объем адсорбата STP, необходимый для образования монослоя на адсорбенте (на грамм адсорбента), тогда , и получаем выражение для прямой:
Через его склон и у перехват мы можем получить vпн и K, которые являются константами для каждой пары адсорбент – адсорбат при заданной температуре. vпн связано с количеством сайтов адсорбции через закон идеального газа. Если мы предположим, что количество центров - это просто вся площадь твердого тела, разделенная на поперечное сечение молекул адсорбата, мы можем легко вычислить площадь поверхности адсорбента. Площадь поверхности адсорбента зависит от его структуры: тем больше пор, тем больше площадь, которая имеет большое влияние на реакции на поверхности.
Если на поверхности адсорбируется более одного газа, мы определяем как доля пустых сайтов, и мы имеем:
Также мы можем определить как доля площадок, занятых j-й газ:
куда я - это каждый из газов, которые адсорбируют.
Примечания:
1) Чтобы выбрать между уравнениями Ленгмюра и Фрейндлиха, необходимо исследовать энтальпии адсорбции.[11] В то время как модель Ленгмюра предполагает, что энергия адсорбции остается постоянной с заполнением поверхности, уравнение Фрейндлиха выводится с предположением, что теплота адсорбции непрерывно уменьшается по мере заполнения мест связывания. [12] Выбор модели на основе наилучшего соответствия данных - распространенное заблуждение.[13]
2) Использование линеаризованной формы модели Ленгмюра больше не является обычной практикой. Прогресс в вычислительной мощности позволил выполнять нелинейную регрессию быстро и с большей уверенностью, поскольку преобразование данных не требуется.
ДЕРЖАТЬ ПАРИ
Часто молекулы действительно образуют многослойные слои, то есть некоторые из них адсорбируются на уже адсорбированных молекулах, и изотерма Ленгмюра недействительна. В 1938 г. Стивен Брунауэр, Пол Эммет, и Эдвард Теллер разработал модельную изотерму, которая учитывает эту возможность. Их теория называется Теория ставок, после инициалов в их фамилиях. Они модифицировали механизм Ленгмюра следующим образом:
- А(грамм) + S ⇌ AS,
- А(грамм) + AS ⇌ A2S,
- А(грамм) + А2S ⇌ A3S и так далее.

Вывод формулы более сложен, чем формула Ленгмюра (см. Ссылки для полного вывода). Мы получаем:
куда Икс давление, деленное на давление газа для адсорбата при этой температуре (обычно обозначается ), v - STP объем адсорбированного адсорбата, vпн - STP-объем количества адсорбата, необходимого для образования монослоя, и c константа равновесия K мы использовали изотерму Ленгмюра, умноженную на давление пара адсорбата. Ключевое предположение, использованное при выводе уравнения БЭТ, заключается в том, что последовательные теплоты адсорбции для всех слоев, кроме первого, равны теплоте конденсации адсорбата.
Изотерма Ленгмюра обычно лучше подходит для хемосорбции, а изотерма БЭТ лучше подходит для физадсорбции для немикропористых поверхностей.
Кислюк

В других случаях молекулярные взаимодействия между молекулами газа, ранее адсорбированными на твердой поверхности, образуют значительные взаимодействия с молекулами газа в газовых фазах. Следовательно, адсорбция молекул газа на поверхность с большей вероятностью происходит вокруг молекул газа, которые уже присутствуют на твердой поверхности, что делает изотерму адсорбции Ленгмюра неэффективной для целей моделирования. Этот эффект был изучен в системе, где азот был адсорбатом, а вольфрам был адсорбентом, Пол Кислюк (1922–2008) в 1957 году.[14] Чтобы компенсировать повышенную вероятность адсорбции, происходящей вокруг молекул, присутствующих на поверхности подложки, Кислюк разработал теорию состояния предшественника, согласно которой молекулы переходят в состояние предшественника на границе раздела между твердым адсорбентом и адсорбатом в газовой фазе. Отсюда молекулы адсорбата будут либо адсорбироваться на адсорбенте, либо десорбироваться в газовую фазу. Вероятность адсорбции, происходящей из состояния предшественника, зависит от близости адсорбата к другим молекулам адсорбата, которые уже были адсорбированы. Если молекула адсорбата в состоянии предшественника находится в непосредственной близости от молекулы адсорбата, которая уже образовалась на поверхности, вероятность ее прилипания отражается размером SE константа и будет либо адсорбироваться из состояния предшественника со скоростью kЕС или будет десорбироваться в газовую фазу со скоростью kES. Если молекула адсорбата переходит в состояние предшественника в месте, удаленном от любых других ранее адсорбированных молекул адсорбата, вероятность прилипания отражается размером SD постоянный.
Эти факторы были включены как часть единой константы, называемой «коэффициент прилипания», kE, описано ниже:
Поскольку SD диктуется факторами, которые учитываются моделью Ленгмюра, SD можно принять за константу скорости адсорбции. Однако константа скорости для модели Кислюка (р’) Отличается от модели Ленгмюра, поскольку р’Используется для представления влияния диффузии на формирование монослоя и пропорционален квадратному корню из коэффициента диффузии системы. Изотерма адсорбции Кислюка записывается следующим образом, где Θ(т) - частичное покрытие адсорбента адсорбатом, и т время погружения:
Решение для Θ(т) дает:
Энтальпия адсорбции
Константы адсорбции равны константы равновесия, поэтому они подчиняются уравнение Ван 'т Гоффа:
Как видно из формулы, вариация K должен быть изостерическим, то есть с постоянным охватом. Если мы начнем с изотермы БЭТ и предположим, что изменение энтропии одинаково для сжижения и адсорбции, мы получим
то есть адсорбция более экзотермична, чем сжижение.
Одномолекулярное объяснение
Адсорбцию ансамбля молекул на поверхности или границе раздела можно разделить на два процесса: адсорбцию и десорбцию. Если скорость адсорбции превосходит скорость десорбции, со временем молекулы будут накапливаться, образуя кривую адсорбции с течением времени. Если скорость десорбции больше, количество молекул на поверхности со временем будет уменьшаться. Скорость адсорбции зависит от температуры, скорости диффузии растворенного вещества и энергетического барьера между молекулой и поверхностью. Диффузию и ключевые элементы скорости адсорбции можно рассчитать, используя Законы диффузии Фика и Соотношение Эйнштейна (кинетическая теория). Десорбция молекулы с поверхности зависит от энергии связи молекулы с поверхностью и температуры.
Квантовая механика - термодинамическое моделирование площади поверхности и пористости
С 1980 года разрабатывались две теории, объясняющие адсорбцию и получающие работающие уравнения. Эти две категории называются гипотезой ци, квантово-механическим выводом, и избыточной работой поверхности, ESW.[15] Обе эти теории приводят к одному и тому же уравнению для плоских поверхностей:
Где U - функция единичного шага. Определения других символов следующие:
где «адс» означает «адсорбированный», «m» означает «монослойный эквивалент», а «vap» относится к давлению пара жидкого адсорбтива при той же температуре, что и твердый образец. Единичная функция определяет молярную энергию адсорбции для первой адсорбированной молекулы с помощью:
Сюжет о адсорбированный по сравнению с называется сюжетом ци. Для плоских поверхностей наклон графика ци дает площадь поверхности. Эмпирически было отмечено, что этот график очень хорошо соответствует изотерме Поланьи.[16][17][18] а также де Боэром и Цвиккером[19] но не преследовали. Это произошло из-за критики в первом случае Эйнштейном, а во втором - Брунауэром. Это уравнение плоской поверхности можно использовать в качестве «стандартной кривой» в обычных условиях кривых сравнения, за исключением того, что ранняя часть пористого образца на графике против действует как стандарт. С помощью этого метода можно анализировать ультрамикропористые, микропористые и мезопористые состояния. Типичные стандартные отклонения для полной изотермы, включая пористые образцы, обычно составляют менее 2%.
Обратите внимание, что в этом описании физической адсорбции энтропия адсорбции согласуется с термодинамическим критерием Дубинина, то есть энтропия адсорбции из жидкого состояния в адсорбированное состояние приблизительно равна нулю.
Адсорбенты
Характеристики и общие требования

Адсорбенты обычно используются в виде сферических гранул, стержней, отливок или монолитов с гидродинамический радиус от 0,25 до 5 мм. У них должен быть высокий истирание сопротивление, высокое термостойкость и малый диаметр пор, что приводит к увеличению площади открытой поверхности и, следовательно, к высокой адсорбционной способности. Адсорбенты также должны иметь отчетливую пористую структуру, обеспечивающую быстрый перенос газообразных паров.
Большинство промышленных адсорбентов делятся на три класса:
- Кислородсодержащие соединения - обычно гидрофильные и полярные, включая такие материалы, как силикагель и цеолиты.
- Соединения на основе углерода - обычно гидрофобны и неполярны, включая такие материалы, как Активированный уголь и графит.
- Соединения на основе полимеров - полярные или неполярные, в зависимости от функциональных групп в полимерной матрице.
Силикагель

Силикагель представляет собой химически инертную, нетоксичную, полярную и стабильную по размерам (<400 ° C или 750 ° F) аморфную форму SiO.2. Его получают реакцией между силикатом натрия и уксусной кислотой, за которой следует ряд процессов дополнительной обработки, таких как старение, травление и т. Д. Эти методы дополнительной обработки приводят к различному распределению пор по размерам.
Кремнезем используется для осушки технологического воздуха (например, кислорода, природного газа) и адсорбции тяжелых (полярных) углеводородов из природного газа.
Цеолиты
Цеолиты представляют собой природные или синтетические кристаллические алюмосиликаты, которые имеют повторяющуюся сеть пор и выделяют воду при высокой температуре. Цеолиты имеют полярную природу.
Их производят путем гидротермального синтеза алюмосиликата натрия или другого источника кремнезема в автоклаве с последующим ионным обменом с определенными катионами (Na+, Ли+, Ca2+, К+, NH4+). Диаметр канала цеолитных каркасов обычно составляет от 2 до 9. Å. За процессом ионного обмена следует сушка кристаллов, которые можно гранулировать со связующим для образования макропористых гранул.
Цеолиты применяются при сушке технологического воздуха, CO2 удаление из природного газа, удаление CO из газа риформинга, разделение воздуха, каталитический крекинг, каталитический синтез и риформинг.
Неполярные (кремнистые) цеолиты синтезируются из источников кремнезема, не содержащего алюминия, или деалюминированием алюминийсодержащих цеолитов. Процесс деалюминирования осуществляется путем обработки цеолита паром при повышенных температурах, обычно выше 500 ° C (930 ° F). Эта высокотемпературная термообработка разрушает связи алюминий-кислород, и атом алюминия выталкивается из каркаса цеолита.
Активированный уголь
Активированный уголь представляет собой высокопористое аморфное твердое вещество, состоящее из микрокристаллитов с графитовой решеткой, обычно приготовленное в виде небольших гранул или порошка. Это неполярно и дешево. Одним из основных недостатков является то, что он реагирует с кислородом при умеренных температурах (более 300 ° C).

Активированный уголь может быть произведен из углеродистого материала, включая уголь (битуминозный, полубитуминозный и лигнит), торф, древесину или скорлупу орехов (например, кокосовый орех). Производственный процесс состоит из двух этапов: карбонизации и активации.[20] Процесс карбонизации включает сушку, а затем нагрев для отделения побочных продуктов, включая смолы и другие углеводороды, от сырья, а также для удаления любых образующихся газов. Процесс завершается нагреванием материала до температуры выше 400 ° C (750 ° F) в бескислородной атмосфере, которая не может поддерживать горение. Затем карбонизированные частицы «активируют», подвергая их воздействию окислителя, обычно пара или двуокиси углерода, при высокой температуре. Этот агент сжигает структуры, блокирующие поры, созданные во время фазы карбонизации, и, таким образом, они образуют пористую трехмерную структуру решетки графита. Размер пор, образовавшихся во время активации, зависит от времени, которое они проводят на этой стадии. Более продолжительное время выдержки приводит к увеличению размера пор. Наиболее популярные угли в водной фазе имеют битуминозную основу из-за их твердости, устойчивости к истиранию, распределения пор по размеру и низкой стоимости, но их эффективность необходимо проверять при каждом применении для определения оптимального продукта.
Активированный уголь используется для адсорбции органических веществ. [21]и неполярные адсорбаты, а также обычно используется для очистки отходящих газов (и сточных вод). Это наиболее широко используемый адсорбент, поскольку большинство его химических (например, поверхностных групп) и физических свойств (например, распределение пор по размеру и площадь поверхности) можно настроить в соответствии с потребностями. Его полезность также определяется его большим объемом микропор (а иногда и мезопор) и, как следствие, большой площадью поверхности.
Адсорбция воды
Адсорбция воды на поверхностях имеет большое значение в химическая инженерия, материаловедение и катализ. Также называемое поверхностной гидратацией, присутствие физически или химически адсорбированной воды на поверхности твердых тел играет важную роль в управлении свойствами интерфейса, путями химических реакций и каталитическими характеристиками в широком диапазоне систем. В случае физически адсорбированной воды поверхностная гидратация может быть устранена просто путем сушки в условиях температуры и давления, допускающих полное испарение воды. Для химически адсорбированной воды гидратация может быть в форме диссоциативной адсорбции, где H2Молекулы O диссоциируют на поверхностно адсорбированные -H и -OH или молекулярную адсорбцию (ассоциативная адсорбция), при которой отдельные молекулы воды остаются нетронутыми. [22]
Адсорбционное солнечное отопление и хранение
Низкая стоимость (200 долларов за тонну) и высокая частота цикла (2000 ×) синтетических цеолитов, таких как Linde 13X с водным адсорбатом, в последнее время вызвали большой академический и коммерческий интерес для использования для хранения тепловой энергии (TES), в частности, низкосортных солнечных и отходящее тепло. С 2000 г. по настоящее время (2020 г.) в ЕС было профинансировано несколько пилотных проектов.[нужна цитата ] Основная идея заключается в хранении солнечной тепловой энергии в виде скрытой химической энергии в цеолите. Обычно горячий сухой воздух из плоских солнечных коллекторов пропускается через слой цеолита, так что любой присутствующий адсорбат воды удаляется. Хранение может быть дневным, еженедельным, ежемесячным или даже сезонным, в зависимости от объема цеолита и площади солнечных тепловых панелей. Когда требуется тепло ночью, в часы без солнца или зимой, через цеолит проходит увлажненный воздух.По мере того как цеолит поглощает влагу, тепло передается воздуху, а затем и помещению здания. Эта форма TES с конкретным использованием цеолитов была впервые предложена Герра в 1978 году.[23]
Улавливание и хранение углерода
Типовые адсорбенты, предлагаемые для улавливание и хранение углерода находятся цеолиты и MOF.[24] Индивидуальная настройка адсорбентов делает их потенциально привлекательной альтернативой абсорбции. Поскольку адсорбенты можно регенерировать за счет колебаний температуры или давления, этот этап может быть менее энергоемким, чем поглощение методы регенерации.[25] Основные проблемы, связанные со стоимостью адсорбции при улавливании углерода, включают: регенерацию адсорбента, массовое соотношение, растворитель / MOF, стоимость адсорбента, производство адсорбента, срок службы адсорбента.[26]
Адсорбция белков и поверхностно-активных веществ
Адсорбция белка - это процесс, который играет фундаментальную роль в области биоматериалы. Действительно, поверхности биоматериалов, контактирующие с биологическими средами, такими как кровь или сыворотка, немедленно покрываются белками. Следовательно, живущие клетки взаимодействуют не напрямую с поверхностью биоматериала, а со слоем адсорбированных белков. Этот белковый слой обеспечивает взаимодействие между биоматериалами и клетками, переводя физические и химические свойства биоматериала на «биологический язык».[27] По факту, клеточная мембрана рецепторы связываются с биоактивными сайтами белкового слоя, и эти события связывания рецептор-белок передаются через клеточную мембрану таким образом, чтобы стимулировать специфические внутриклеточные процессы, которые затем определяют адгезию, форму, рост и дифференцировку клеток. На адсорбцию протеина влияют многие свойства поверхности, такие как поверхность. смачиваемость, химический состав поверхности [28] и морфология поверхности в нанометровом масштабе.[29]Адсорбция поверхностно-активного вещества - подобное явление, но с использованием молекул поверхностно-активного вещества вместо белков.[30]
Адсорбционные чиллеры
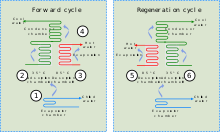
Сочетание адсорбента с хладагентом, адсорбционные чиллеры используйте тепло для создания охлаждающего эффекта. Это тепло в виде горячей воды может поступать из любого числа промышленных источников, включая отходящее тепло промышленных процессов, первичное тепло от солнечных тепловых установок или тепло выхлопных газов или водяной рубашки поршневого двигателя или турбины.
Хотя адсорбционные чиллеры и абсорбционное охлаждение, первый основан на взаимодействии газов и твердых тел. Адсорбционная камера чиллера заполнена твердым материалом (например, цеолитом, силикагелем, оксидом алюминия, активированным углем или некоторыми типами солей металлов), который в своем нейтральном состоянии адсорбировал хладагент. При нагревании твердое вещество десорбирует (выпускает) пар хладагента, который затем охлаждается и сжижается. Затем этот жидкий хладагент обеспечивает охлаждающий эффект в испарителе от его энтальпия испарения. На заключительной стадии пар хладагента (повторно) адсорбируется твердым телом.[31] Поскольку адсорбционный чиллер не требует компрессора, он относительно тихий.
Адсорбция, опосредованная сайтом портала
Адсорбция, опосредованная портальным участком, представляет собой модель сайт-селективной адсорбции активированного газа в металлических каталитических системах, которые содержат множество различных участков адсорбции. В таких системах дефектоподобные участки "края и угол" с низкой координацией могут иметь значительно более низкие энтальпии адсорбции, чем высококоординированные (базисная плоскость ) места. В результате эти участки могут служить «порталами» для очень быстрой адсорбции на остальной поверхности. Это явление основано на обычном «побочном» эффекте (описанном ниже), когда определенные адсорбированные частицы проявляют высокую подвижность на некоторых поверхностях. Модель объясняет, казалось бы, противоречивые наблюдения термодинамики и кинетики адсорбции газа в каталитических системах, где поверхности могут существовать в ряде координационных структур, и она была успешно применена к биметаллическим каталитическим системам, где наблюдается синергетическая активность.
В отличие от чистого перетока, адсорбция на портальном участке относится к поверхностной диффузии к соседним участкам адсорбции, а не к неадсорбционным опорным поверхностям.
Модель, по-видимому, была впервые предложена Брандтом для оксида углерода на платине, нанесенной на кремнезем. и другие. (1993).[32] Похожая, но независимая модель была разработана Кингом с сотрудниками.[33][34][35] для описания адсорбции водорода на биметаллических катализаторах из рутения, серебра-рутения и меди-рутения, нанесенных на кремнезем. Эта же группа применила модель к гидрированию CO (синтез Фишера-Тропша).[36] Zupanc и другие. (2002) впоследствии подтвердили ту же модель адсорбции водорода на биметаллических цезий-рутениевых катализаторах, нанесенных на оксид магния.[37] Trens и другие. (2009) аналогичным образом описали поверхностную диффузию CO на углеродных частицах Pt различной морфологии.[38]
Адсорбционный побочный эффект
В случае каталитических или адсорбционных систем, в которых частицы металла диспергированы на материале носителя (или носителе) (часто квазиинертные оксиды, такие как оксид алюминия или диоксид кремния), адсорбирующие частицы могут косвенно адсорбироваться на поверхности носителя под воздействием условия, при которых такая адсорбция термодинамически невыгодна. Присутствие металла служит более низкоэнергетическим путем для газообразных частиц, которые сначала адсорбируются на металле, а затем диффундируют на поверхности носителя. Это возможно, потому что адсорбированные частицы достигают более низкого энергетического состояния после того, как они адсорбируются на металл, тем самым снижая активационный барьер между частицами газовой фазы и частицами, адсорбированными на носителе.
Перетекание водорода является наиболее распространенным примером адсорбционного перетока. В случае водорода адсорбция чаще всего сопровождается диссоциацией молекулярного водорода (H2) до атомарного водорода (H) с последующим перетеканием присутствующих атомов водорода.
Эффект побочного эффекта использовался для объяснения многих наблюдений в гетерогенный катализ и адсорбция.[39]
Полимерная адсорбция
Адсорбция молекул на поверхности полимера является центральной для ряда приложений, включая разработку антипригарных покрытий и в различных биомедицинских устройствах. Полимеры также могут адсорбироваться на поверхности через адсорбция полиэлектролита.
Адсорбция в вирусах
Адсорбция это первый шаг в вирусный жизненный цикл. Следующие шаги - проникновение, снятие покрытия, синтез (транскрипция, если необходимо, и трансляция) и высвобождение. В этом отношении цикл репликации вирусов одинаков для всех типов вирусов. Такие факторы, как транскрипция, могут потребоваться или не потребоваться, если вирус способен интегрировать свою геномную информацию в ядро клетки или если вирус может реплицироваться непосредственно в цитоплазме клетки.
В популярной культуре
Игра Тетрис это игра-головоломка, в которой блоки из 4 адсорбируются на поверхность во время игры. Ученые использовали блоки тетриса «в качестве заменителя молекул сложной формы» и их «адсорбции на плоской поверхности» для изучения термодинамика из наночастицы.[40][41]
Смотрите также
- Адатом
- Криоадсорбция
- Двухполяризационная интерферометрия
- Концентратор псевдоожиженного слоя
- Зондовый силовой микроскоп Кельвина
- Микромеритика
- Молекулярная решетка
- Адсорбция Поланьи
- Адсорбция при переменном давлении
- Случайная последовательная адсорбция
Рекомендации
- ^ «Глоссарий». Центр поддержки технологий восстановления заброшенных месторождений и земель. Архивировано из оригинал на 2008-02-18. Получено 2009-12-21.
- ^ «абсорбция (химия)». Словарь / тезаурус Memidex (WordNet). Архивировано из оригинал на 2018-10-05. Получено 2010-11-02.
- ^ Аткинс, П. У .; Де Паула, Хулио; Киллер, Джеймс (2018). Физическая химия Аткинса (Одиннадцатое изд.). Оксфорд, Великобритания. ISBN 978-0-19-876986-6. OCLC 1020028162.
- ^ Глоссарий терминов по химии атмосферы (Рекомендации 1990 г.). Чистая и прикладная химия. 62. 1990. стр. 2167. Дои:10.1351 / goldbook.A00155. ISBN 978-0-9678550-9-7.
- ^ Ferrari, L .; Kaufmann, J .; Winnefeld, F .; Планк, Дж. (2010). «Взаимодействие модельных систем цемента с суперпластификаторами исследовано с помощью атомно-силовой микроскопии, дзета-потенциала и измерений адсорбции». J. Colloid Interface Sci. 347 (1): 15–24. Bibcode:2010JCIS..347 ... 15F. Дои:10.1016 / j.jcis.2010.03.005. PMID 20356605.
- ^ Chelej, K .; Cwieka, K .; Курзыдловски, К.Дж. (Май 2016). "CO2 стабильность на поверхностях с низким показателем преломления Ni: DFT-анализ с поправкой Ван-дер-Ваальса ". Catalysis Communications. 80 (5): 33–38. Дои:10.1016 / j.catcom.2016.03.017.
- ^ Chelej, K .; Cwieka, K .; Colmenares, J.C .; Курзыдловски, К.Дж. (2016). "Понимание взаимодействия метанол-селективных промежуточных продуктов окисления с Au- или / и Pd-содержащими монометаллическими и биметаллическими катализаторами Core @ Shell". Langmuir. 32 (30): 7493–7502. Дои:10.1021 / acs.langmuir.6b01906. PMID 27373791.
- ^ Кайзер, Генрих (1881). "Über die Verdichtung von Gasen an Oberflächen in ihrer Abhängigkeit von Druck und Temperatur". Annalen der Physik und Chemie. 248 (4): 526–537. Bibcode:1881АнП ... 248..526К. Дои:10.1002 / andp.18812480404.. В этом исследовании адсорбции газов древесным углем слово «адсорбция» впервые встречается на странице 527: "Schon Saussure kannte die beiden für die Grösse der Adsorption massgebenden Factoren, den Druck und die Temperatur, da er Erniedrigung des Druckes или Erhöhung der Temperatur zur Befreiung der porösen Körper von Gasen benutzte." («Соссоре уже знал два фактора, которые определяют количество адсорбции - [а именно] давление и температуру - поскольку он использовал понижение давления или повышение температуры, чтобы освободить пористые вещества от газов».)
- ^ Foo, K. Y .; Хамид, Б. Х. (2010). «Взгляды на моделирование систем изотермы адсорбции». Журнал химической инженерии. 156 (1): 2–10. Дои:10.1016 / j.cej.2009.09.013. ISSN 1385-8947.
- ^ Czepirski, L .; Балыс, М. Р .; Коморовская-Чепирска, Э. (2000). «Некоторое обобщение изотермы адсорбции Ленгмюра». Интернет-журнал химии. 3 (14). ISSN 1099-8292.
- ^ Burke GM, Wurster DE, Buraphacheep V, Berg MJ, Veng-Pedersen P, Schottelius DD. Выбор модели адсорбции фенобарбитала активированным углем. Pharm Res. 1991; 8 (2): 228-231. DOI: 10.1023 / а: 1015800322286
- ^ Физическая химия поверхностей. Артур В. Адамсон. Interscience (Wiley), Нью-Йорк, 6-е изд.
- ^ Burke GM, Wurster DE, Buraphacheep V, Berg MJ, Veng-Pedersen P, Schottelius DD. Выбор модели адсорбции фенобарбитала активированным углем. Pharm Res. 1991; 8 (2): 228-231. DOI: 10.1023 / а: 1015800322286
- ^ Кислюк П. П. (1957). «Вероятности прилипания газов, хемосорбированных на поверхности твердых тел». Журнал физики и химии твердого тела. 3 (1–2): 95–101. Bibcode:1957JPCS .... 3 ... 95 тыс.. Дои:10.1016/0022-3697(57)90054-9.
- ^ Кондон, Джеймс (2020). Площадь поверхности и определение пористости с помощью физсорбции, измерения, классической теории и квантовой теории, 2-е издание. Amsterdam.NL: Эльзевир. С. Главы 3, 4 и 5. ISBN 978-0-12-818785-2.
- ^ Поланьи, М. (1914). Verk. Deutsch. Physik, газ. 16: 1012. Отсутствует или пусто
| название =(помощь)[требуется полная цитата ] - ^ Поланьи, М. (1920). "Neueres über Adsorption und Ursache der Adsorptionskräfte". Zeitschrift für Elektrochemie. 26: 370–374.
- ^ Поланьи, М. (1929). "Grundlagen der Potentialtheorie der Адсорбция". Zeitschrift für Elektrochemie. 35: 431–432.
- ^ deBoer, J.H .; Цвиккер, К. (1929). "Адсорбция на основе поляризации Фольге фон". Zeitschrift für Physikalische Chemie. B3: 407–420.
- ^ Spessato, L. et al. KOH-суперактивированный уголь из отходов биомассы: понимание механизма адсорбции парацетамола и циклов термической регенерации. Журнал опасных материалов, Vol. 371, страницы 499-505, 2019.
- ^ Мальхотра, Милан; Суреш, Сумати; Гарг, Анураг (2018). «Активированный уголь, полученный из отходов чая, для адсорбции диклофенака натрия из сточных вод: характеристики адсорбента, изотермы адсорбции, кинетика и термодинамика». Экология и исследования загрязнения окружающей среды. 25 (32): 32210–32220. Дои:10.1007 / s11356-018-3148-у. PMID 30221322. S2CID 52280860.
- ^ Адсорбция воды на TiO2 самолеты, диссоциативная и молекулярная адсорбция воды.
- ^ Патент США №4 269 170 "Адсорбционное солнечное отопление и хранение"; Изобретатель: Джон М. Герра; Выдан 26 мая 1981 г.
- ^ Беренд, Смит; Реймер, Джеффри А; Ольденбург, Кертис М; Бург, Ян С. (2014). Введение в улавливание и связывание углерода. Imperial College Press. ISBN 9781306496834.
- ^ Д'Алессандро, Дина М .; Смит, Беренд; Лонг, Джеффри Р. (16 августа 2010 г.). «Улавливание углекислого газа: перспективы новых материалов». Angewandte Chemie International Edition. 49 (35): 6058–82. Дои:10.1002 / anie.201000431. ISSN 1521-3773. PMID 20652916.
- ^ Сатре, Роджер; Масанет, Эрик (2013-03-18). «Перспективное моделирование жизненного цикла системы улавливания и хранения углерода с использованием металлоорганических структур для улавливания CO2». RSC Advances. 3 (15): 4964. Дои:10.1039 / C3RA40265G. ISSN 2046-2069.
- ^ Уилсон, CJ; Клегг, RE; Ливсли, Д.И. Пирси, MJ (2005). "Посредничество биоматериалов-клеточных взаимодействий адсорбированными белками: обзор". Тканевая инженерия. 11 (1): 1–18. Дои:10.1089 / десять.2005.11.1. PMID 15738657.
- ^ Sivaraman B .; Страхов К.П .; Латур Р.А. (2009). «Исследование влияния химии поверхности и концентрации раствора на конформацию адсорбированных белков с использованием улучшенного метода кругового дихроизма». Langmuir. 25 (5): 3050–6. Дои:10.1021 / la8036814. ЧВК 2891683. PMID 19437712.
- ^ Скопеллити, Паскуале Эмануэле; Боргоново, Антонио; Индриери, Марко; Джорджетти, Лука; Бонджорно, Геро; Карбоне, Роберта; Подеста, Алессандро; Милани, Паоло (2010). Чжан, Шугуан (ред.). «Влияние морфологии поверхности в нанометровом масштабе на адсорбцию белка». PLoS ONE. 5 (7): e11862. Bibcode:2010PLoSO ... 511862S. Дои:10.1371 / journal.pone.0011862. ЧВК 2912332. PMID 20686681.
- ^ Черагян, Гоштасп (2017). «Оценка наночастиц глины и коллоидального диоксида кремния на адсорбцию поверхностно-активного полимера во время увеличения нефтеотдачи». Журнал Японского института нефти. 60 (2): 85–94. Дои:10.1627 / jpi.60.85.
- ^ Пилатовский, И .; Romero, R.J .; Isaza, C.A .; Gamboa, S.A .; Себастьян, П.Дж .; Ривера, В. (2011). «Глава 5: Сорбционные холодильные системы». Когенерационные топливные элементы - сорбционные системы кондиционирования воздуха. Зеленая энергия и технологии. Springer. С. 99, 100. Дои:10.1007/978-1-84996-028-1_5. ISBN 978-1-84996-027-4.
- ^ Brandt, R.K .; Hughes, M. R .; Bourget, L.P .; Truszkowska, K .; Гринлер, Р. Г. (1993). "Интерпретация СО, адсорбированного на Pt / SiO.2 двух различных гранулометрических составов ». Наука о поверхности. 286 (1–2): 15–25. Bibcode:1993СурСк.286 ... 15Б. Дои:10.1016 / 0039-6028 (93) 90552-У.
- ^ Uner, D. O .; Savargoankar, N .; Пруски, М .; Кинг, Т. С. (1997). Влияние щелочных промоторов на динамику хемосорбции водорода и кинетику реакции синтез-газа на Ru / SiO2 катализаторы. Исследования в области наук о поверхности и катализа. 109. С. 315–324. Дои:10.1016 / S0167-2991 (97) 80418-1. ISBN 9780444826091.
- ^ Narayan, R.L .; Кинг, Т. С. (1998). «Состояния адсорбции водорода на биметаллических катализаторах Ru-Ag и Ru-Cu, нанесенных на кремнезем, исследованы с помощью микрокалориметрии». Термохимика Акта. 312 (1–2): 105–114. Дои:10.1016 / S0040-6031 (97) 00444-9.
- ^ VanderWiel, D.P .; Пруски, М .; Кинг, Т. С. (1999). «Кинетическое исследование адсорбции и реакции водорода на рутениевых и серебряно-рутениевых биметаллических катализаторах на основе диоксида кремния во время гидрирования окиси углерода». Журнал катализа. 188 (1): 186–202. Дои:10.1006 / jcat.1999.2646.
- ^ Унер, Д. О. (1998). "Разумный механизм промотирования щелочью в синтезе Фишера-Тропша: подвижности адсорбата". Исследования в области промышленной и инженерной химии. 37 (6): 2239–2245. Дои:10.1021 / ie970696d.
- ^ Zupanc, C .; Hornung, A .; Hinrichsen, O .; Мюлер, М. (2002). «Взаимодействие водорода с катализаторами Ru / MgO». Журнал катализа. 209 (2): 501–514. Дои:10.1006 / jcat.2002.3647.
- ^ Trens, P .; Durand, R .; Coq, B .; Coutanceau, C .; Rousseau, S .; Лами, К. (2009). «Отравление катализаторов Pt / C CO и его последствия для кинетики хемосорбции водорода». Прикладной катализ B: Окружающая среда. 92 (3–4): 280–4. Дои:10.1016 / j.apcatb.2009.08.004.
- ^ Розанов, В. В .; Крылов, О. В. (1997). «Распространение водорода при гетерогенном катализе». Российские химические обзоры. 66 (2): 107–119. Bibcode:1997RuCRv..66..107R. Дои:10.1070 / RC1997v066n02ABEH000308.
- ^ Термодинамика тетриса, Ars Technica, 2009.
- ^ Барнс, Брайан Ч .; Siderius, Daniel W .; Гелб, Лев Д. (2009). «Структура, термодинамика и растворимость в тетроминовых жидкостях». Langmuir. 25 (12): 6702–16. Дои:10.1021 / la900196b. PMID 19397254.
дальнейшее чтение
- Касслер, Э. Л. (1997). Диффузия: массоперенос в жидкостных системах (2-е изд.). Нью-Йорк: Издательство Кембриджского университета. С. 308–330. ISBN 978-0-521-45078-2.
внешняя ссылка
- Вывод изотерм Ленгмюра и БЭТ, на JHU.edu
- Адсорбция углерода, на MEGTEC.com































