Brainbow - Brainbow
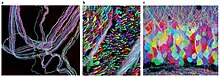
Brainbow это процесс, посредством которого отдельные нейроны в мозг можно отличить от соседних нейронов с помощью флуоресцентных белков. Случайным образом выражая различные соотношения красных, зеленых и синих производных зеленый флуоресцентный белок в отдельных нейронах можно пометить каждый нейрон отличительным цветом. Этот процесс стал важным вкладом в сферу коннектомика, традиционно известная как годология, изучающая нейронные связи в головном мозге.
Методика была первоначально разработана в 2007 году командой во главе с Джефф В. Лихтман и Джошуа Р. Санес, оба в Гарвардский университет.[1] Оригинальный метод был недавно адаптирован для использования с другими модельными организмами, включая Drosophila melanogaster, Caenorhabditis elegans[нужна цитата ], и Arabidopsis thaliana.[2]
В то время как более ранние методы маркировки позволяли отображать только несколько нейронов, этот новый метод позволяет одновременно и по-разному освещать более 100 нейронов с различным картированием. Полученные в результате изображения могут быть довольно яркими и завоевали награды на конкурсах научной фотографии.[нужна цитата ].
История и развитие
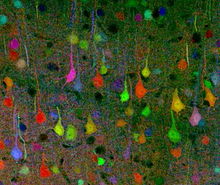
Методика нейровизуализации головного мозга была первоначально разработана группой исследователей из Гарвардский университет в 2007.[1] В то время они работали в Вашингтонском университете в Сент-Луисе. Эту конкретную группу ученых возглавляли профессора Джефф В. Лихтман и Джошуа Р. Сэнс, оба из которых специализируются на молекулярной и клеточной биологии и широко известны своей работой. Команда построила Brainbow, используя двухэтапный процесс: во-первых, конкретный генетический Была создана конструкция, которая могла быть рекомбинирована в нескольких компоновках для получения одного из трех или четырех цветов в зависимости от конкретных применяемых флуоресцентных белков (XFP).[3] Затем несколько копий одного и того же трансгенный конструкция была вставлена в геном целевых видов, что приводит к случайной экспрессии различных соотношений XFP и впоследствии вызывает разные клетки отображать множество красочных оттенков.[3]
Изначально Brainbow был создан как усовершенствование более традиционных нейровизуализация такие методы, как окрашивание по Гольджи и инъекция красителя, оба из которых представляли серьезные ограничения для исследователей в их способности визуализировать сложную архитектуру нейронная схема в мозг.[1] В то время как более старые методы могли окрашивать клетки только в ограниченный диапазон цветов, часто используя двух- и трехцветные трансгенные мыши Чтобы раскрыть ограниченную информацию о нейронных структурах, Brainbow гораздо более гибок, поскольку он может флуоресцентно маркировать отдельные нейроны примерно до 100 различных оттенков, чтобы ученые могли идентифицировать и даже различать дендритный и аксональный процессы.[3] Раскрывая такую подробную информацию о нейронных связях и паттернах, иногда даже in vivo, ученые часто могут вывести информацию о взаимодействии нейронов и их последующем влиянии на поведение и функции. Таким образом, Brainbow заполнили пустоту, оставленную предыдущими методами нейровизуализации.
С недавним появлением Brainbow в нейробиология Теперь исследователи могут создавать конкретные карты нейронных цепей и лучше исследовать, как они соотносятся с различными умственными действиями и их взаимосвязанным поведением (то есть Brainbow раскрывает информацию о взаимосвязях между нейронами и их последующими взаимодействиями, которые влияют на общую функциональность мозга). Таким образом, в качестве дальнейшей экстраполяции этого метода Brainbow можно использовать для изучения как неврологических, так и психологических расстройств путем анализа различий в нейронных картах.[3]
Методы


Приемы работы с мозгом полагаются на Cre-Lox рекомбинация, в котором белок Cre рекомбиназа диски инверсия или удаление ДНК между сайтами loxP. Оригинальный метод Brainbow включает как Brainbow-1, так и Brainbow-2, в которых используются различные формы рекомбинации cre / lox. Brainbow-3, модифицированная версия Brainbow-1, была разработана в 2013 году.[4] Для всех подтипов Brainbow выражение данного XFP является стохастическим или случайным событием.
Brainbow-1 использует Конструкции ДНК с разными генами флуоресцентных белков (XFP), разделенными мутантными и каноническими формами loxP. Это создает набор взаимоисключающих возможностей удаления, поскольку рекомбинация происходит только между идентичными сайтами loxP.[1] После рекомбинации флуоресцентный белок, который остается сразу после промоутер выражается однозначно. Таким образом, конструкция с четырьмя XFP, разделенными тремя разными сайтами loxP, тремя событиями вырезания и исходной конструкцией, может продуцировать четыре разных флуоресцентных белка.[3]
Brainbow-2 использует вырезание и инверсию Cre, чтобы обеспечить несколько возможностей выражения в данной конструкции. В одном сегменте ДНК с двумя противоположно ориентированными XFP Cre будет вызывать случайное событие инверсии, которое оставляет один флуоресцентный белок в правильной ориентации для экспрессии. Если две из этих обратимых последовательностей выровнены, возможны три различных события инверсии. Когда также учитываются события вырезания, один из четырех флуоресцентных белков будет экспрессироваться для данной комбинации вырезаний и инверсий Cre.
Brainbow-3 сохраняет формат loxP Brainbow-1, но заменяет гены RFP, YFP и CFP на mOrange2, EGFP и mKate2. mO2, EGFP и mK2 были выбраны как потому, что их флуоресцентные спектры возбуждения и излучения минимально перекрываются, так и потому, что они имеют минимальную гомологию последовательностей, что позволяет создать селективные антитела, которые можно использовать для их обнаружения в иммуногистохимический протоколы. Brainbow-3 также решает проблему неравномерного заполнения нейронов XFP за счет использования фарнезилированных производных XFP, которые более равномерно передаются на мембраны нейронов.[4]
Brainbow реализован in vivo путем пересечения двух трансгенный штаммы организмов: один, экспрессирующий белок Cre, и другой, трансфицированный несколькими версиями конструкции loxP / XFP. Использование нескольких копий трансген позволяет сочетать XFP таким образом, чтобы можно было получить один из примерно 100 разных цветов.[3] Таким образом, каждый нейрон помечен другим оттенком, основанным на заданной комбинаторной и стохастической экспрессии флуоресцентных белков.
Чтобы выявить паттерны дифференциальной экспрессии XFP в видимой форме, срезы мозга визуализируются с помощью конфокальная микроскопия. При воздействии фотон со своей длиной волны возбуждения, каждый флуорофор излучает сигнал, который собирается в красный, зеленый или синий канал, и полученная комбинация света анализируется с помощью программного обеспечения для анализа данных.[1] Наложение нейронов разного цвета позволяет визуально распутать сложные нейронные цепи.
На сегодняшний день Brainbow преимущественно тестировался на мышах; однако описанный выше базовый метод также был модифицирован для использования в более поздних исследованиях с момента появления оригинального метода, представленного в 2007 году.
мышей

В мозг мыши имеет 75000000 нейроны и больше похож на человеческий мозг, чем дрозофила и другие часто используемые организмы для моделирования этого метода, такие как C. elegans. Мыши были первыми организмами, в которых был успешно применен метод нейровизуализации Brainbow.[1] Livet et al. (2007) разработали две версии мышей Brainbow с использованием Brainbow-1 и Brainbow-2, которые описаны выше.[1] При использовании этих методов для создания полной карты и отслеживания аксонов мышцы мыши необходимо собрать десятки тысяч изображений и скомпилировать их в стеки для создания полной схемы.[3] Затем можно проследить каждый моторный аксон и его синаптические контакты, чтобы построить полную коннектом мышцы.
Больше примеров нейронов, исследованных с помощью техники Brainbow в трансгенный мыши располагаются в двигательном нерве, иннервирующем мышцы уха, в аксональных трактах мозговой ствол, а зубчатая извилина гиппокампа.[3]
Дрозофила
Сложность мозга дрозофилы, состоящего из примерно 100 000 нейронов, делает его отличным кандидатом для применения таких методов нейрофизиологии и нейробиологии, как Brainbow. Фактически, Стефани Хэмпел и др. (2011) объединили Brainbow в сочетании с инструментами генетического нацеливания для идентификации отдельных нейронов в головном мозге дрозофилы и различных нейрональных клонов.[5] Одним из инструментов генетического нацеливания был GAL4 / UAS бинарная система экспрессии, которая контролирует экспрессию UAS-Brainbow и нацеливает экспрессию на небольшие группы нейронов. Использование методов «Flip Out» увеличило клеточное разрешение репортерной конструкции. Экспрессия флуоресцентных белков, как и в оригинальном Brainbow, зависела от рекомбинации Cre, соответствующей совпадающим сайтам lox. Hampel et al. (2011) также разработали свой собственный вариант Brainbow (dBrainbow), основанный на маркировке антителами эпитопов, а не на эндогенной флуоресценции.[5] Две копии их конструкции дают шесть ярких, разборчивых цветов. Это, наряду с упрощением назначения цветов, позволило им наблюдать траектории каждого нейрона на больших расстояниях. В частности, они проследили двигательные нейроны от антеннальной доли до нервно-мышечных соединений, что позволило им идентифицировать конкретные мышечные мишени отдельных нейронов.
В конечном итоге этот метод дает возможность эффективно отображать нейронные цепи у дрозофилы, чтобы исследователи могли получить больше информации о структуре мозга этого беспозвоночного и о том, как она связана с его последующим поведением.
Ограничения
Как и любой нейровизуализация Brainbow имеет ряд ограничений, связанных с методами, необходимыми для его выполнения. Например, процесс выведения по крайней мере двух линий трансгенных животных из эмбриональных стволовых клеток занимает много времени и является сложным. Даже если два трансгенный виды успешно созданы, не все их потомки покажут рекомбинацию. Таким образом, это требует тщательного планирования перед проведением эксперимента.[3]
Кроме того, из-за случайного характера экспрессии флуоресцентных белков ученые не могут точно контролировать маркировку нейронных цепей, что может привести к плохой идентификации конкретных нейронов.
Использование головного мозга в млекопитающее популяциям также препятствует невероятное разнообразие нейронов Центральная нервная система. Чистая плотность нейроны в сочетании с наличием длинных трактов аксонов затрудняет просмотр больших участков ЦНС с высоким разрешением. Brainbow наиболее полезен при изучении разрешения отдельных клеток на фоне сложной многоклеточной среды. Однако из-за пределов разрешения оптическая микроскопия, окончательное определение синаптических связей между нейронами не так просто. Этой проблемы можно несколько избежать, используя синаптические маркеры в дополнение к использованию оптической микроскопии при наблюдении синаптических связей.[6]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм Livet, J .; Weissman, T. A .; Kang, H .; Проект, R.W .; Lu, J .; Bennis, R.A .; Sanes, J. R .; Лихтман, Дж. У. (2007). «Трансгенные стратегии комбинаторной экспрессии флуоресцентных белков в нервной системе». Природа. 450 (7166): 56–62. Bibcode:2007Натура 450 ... 56л. Дои:10.1038 / природа06293. PMID 17972876.
- ^ Мах, Дженнифер (01.07.2011). "Клональный анализ с помощью системы Brainbow". Растительная клетка. 23 (7): 2471. Дои:10.1105 / tpc.111.230710. ISSN 1532–298X. ЧВК 3226220.
- ^ а б c d е ж грамм час я Лихтман, Джефф; Жан Ливе; Джошуа Санес (июнь 2008 г.). «Яркий подход к коннектомуу». Обзоры природы Неврология. 9 (6): 417–422. Дои:10.1038 / nrn2391. ЧВК 2577038. PMID 18446160.
- ^ а б Cai, D .; Коэн, К. Б .; Luo, T .; Lichtman, J. W .; Санес, Дж. Р. (2013). «Улучшенные инструменты для набора инструментов Brainbow». Методы природы. 10 (6): 540–547. Дои:10.1038 / nmeth.2450. ЧВК 3713494. PMID 23817127.
- ^ а б Стефани Хэмпел; Phuong Chung; Клэр МакКеллар; Дональд Холл; Лорен Лугер; Джули Симпсон (февраль 2011 г.). "Drosophila Brainbow: метод флуоресцентного мечения на основе рекомбиназы для разделения паттернов нервной экспрессии". Методы природы. 8 (3): 253–260. Дои:10.1038 / nmeth.1566. ЧВК 3077945. PMID 21297621.
- ^ Дхавале, А; Бхалла (2008). «Сеть и синапс: 100 лет после Кахала». Журнал HFSP. 2 (1): 12–16. Дои:10.2976/1.2835214. ЧВК 2640997. PMID 19404449.
