Фракционирование изотопов углерода в кислородном фотосинтезе - Fractionation of carbon isotopes in oxygenic photosynthesis
Фотосинтез обращает углекислый газ к углеводы через несколько метаболические пути которые обеспечивают организм энергией и предпочтительно реагируют с определенными стабильные изотопы из углерод.[1] Селективное обогащение одного стабильного изотопа другим создает отчетливые изотопное фракционирование которые можно измерить и сопоставить с кислородсодержащими фототрофы. На степень фракционирования изотопов углерода влияет несколько факторов, включая метаболизм, анатомию, скорость роста и условия окружающей среды организма. Понимание этих различий в фракционировании углерода между видами полезно для биогеохимический исследования, в том числе реконструкция палеоэкология, эволюция растений, а характеристика пищевые цепи.[2][3]

Кислородный фотосинтез это метаболический путь при содействии автотрофы, включая растения, водоросли и цианобактерии. Этот путь превращает неорганический диоксид углерода из атмосферы или водной среды в углеводы, используя воду и энергию света, затем выделяет молекулярный кислород в качестве продукта. Органический углерод содержит меньше стабильного изотопа Углерод-13, или же 13C по сравнению с исходным неорганическим углеродом из атмосферы или воды, потому что фотосинтетическая фиксация углерода включает несколько реакций фракционирования с кинетические изотопные эффекты.[4] Эти реакции претерпевают кинетический изотопный эффект, потому что они ограничено преодолевая энергия активации барьер. Более легкий изотоп имеет более высокую энергетическое состояние в квантовая яма химической связи, что позволяет предпочтительно формировать продукты. Разные организмы связывают углерод с помощью разных механизмов, которые отражаются в различных изотопных составах фотосинтетических путей (см. Таблицу ниже и пояснения к обозначениям в разделе «Измерение изотопов углерода»). В следующих разделах будут описаны различные пути оксигенного фотосинтеза и то, что влияет на связанные с ними значения дельты.

| Путь | δ13С (‰) |
|---|---|
| C3 | От -20 до -37[2] |
| C4 | От -12 до -16[5] |
| CAM | От -10 до -20[6] |
| Фитопланктон | От -18 до -25[4][7] |
Измерение изотопов углерода
Углерод на Земле в природе встречается в виде двух стабильных изотопов, 98,9% которых находятся в форме 12C и 1,1% в 13C.[1][8] Соотношение между этими изотопами варьируется в биологических организмах из-за метаболических процессов, которые избирательно используют один изотоп углерода по сравнению с другим, или «фракционируют» углерод посредством кинетических или термодинамических эффектов.[1] Кислородный фотосинтез происходит у растений и микроорганизмов разными химическими путями, поэтому разные формы органического материала отражают разные соотношения 13C изотопы. Понимание этих различий в фракционировании углерода между видами применяется в изотопная геохимия и экологические изотопные исследования для понимания биохимических процессов, установления пищевых цепочек или моделирования углеродного цикла в геологическом времени.[5]
Фракционирование изотопов углерода выражается в дельта-обозначении δ13C («дельта тринадцать C»), которая указывается в частях на тысячу (промилле, ‰).[9] δ13C определяется по отношению к Венскому Пи Ди Белемнит (VPDB, 13C /12C = 0,01118) как установленный эталонный стандарт.[8][10] Это называется «дельта-значением», и его можно рассчитать по следующей формуле:
Фотосинтез реакции
Химический путь оксигенного фотосинтеза исправляет углерод в две стадии: светозависимые реакции и светонезависимые реакции.
Светозависимые реакции захватывают световую энергию для переноса электронов из воды и преобразования НАДФ+, ADP, и неорганический фосфат в молекулы-аккумуляторы НАДФН и АТФ. Общее уравнение светозависимых реакций обычно выглядит следующим образом:[11]
2 ч2O + 2 НАДФ+ + 3 ADP + 3 Pя + свет → 2 НАДФ + 2 Н+ + 3 АТФ + O2
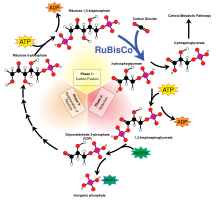
В светонезависимый реакции проходят Цикл Кальвина-Бенсона, в котором энергия НАДФН и АТФ используется для преобразования углекислый газ и вода в органические соединения через фермент RuBisCO Общее общее уравнение для светонезависимых реакций следующее:[11]
3 CO2 + 9 АТФ + 6 НАДФН + 6 Н+ → С3ЧАС6О3-фосфат + 9 АДФ + 8 Pя + 6 НАДФ+ + 3 часа2О
3-углеродные продукты (C3ЧАС6О3-фосфат) цикла Кальвина позже превращаются в глюкоза или другие углеводы, такие как крахмал, сахароза, и целлюлоза.
Фракционирование через RuBisCO

Большое фракционирование 13C в фотосинтезе происходит из-за реакции карбоксилирования, которая осуществляется ферментом рибулозо-1,5-бисфосфаткарбоксилазой оксигеназой, или RuBisCO.[5] RuBisCO катализирует реакцию между пятиуглеродной молекулой rибулоза-1,5-бисфосфат (сокращенно RuBP) и CO2 образовать две молекулы 3-фосфоглицериновая кислота (сокращенно PGA). PGA реагирует с NADPH с образованием 3-фосфоглицеральдегид.[4]
Согласно прогнозам, фракционирование изотопов только за счет карбоксилирования Rubsico (форма I) будет в среднем на 28%.[12][5] Однако значения фракционирования у разных организмов различаются, начиная от истощения 11 ‰, наблюдаемого в кокколитофорид водорослей до истощения 29 ‰, наблюдаемого в шпинат.[13][14] RuBisCO вызывает кинетический изотопный эффект потому что 12CO2 и 13CO2 конкурировать за один и тот же активный сайт и 13C имеет более низкую скорость реакции.[15]
13Модель фракционирования C
В дополнение к различающим эффектам ферментативных реакций диффузия CO2 Газ к месту карбоксилирования в растительной клетке также влияет на изотопное фракционирование.[16] В зависимости от типа установки (см. Разделы ниже) внешний CO2 должны транспортироваться через пограничный слой и устьица и во внутреннее газовое пространство растительной клетки, где он растворяется и диффундирует в хлоропласт.[5] В диффузионность газа обратно пропорционально квадратному корню из его молекулярного уменьшенная масса, вызывая 13CO2 быть на 4,4% менее диффузным, чем 12CO2.
Преобладающая модель фракционирования атмосферного CO2 в растениях сочетает изотопные эффекты реакции карбоксилирования с изотопными эффектами от диффузия газа в растение в следующем уравнении:[16]
Где:
- δ13Cобразец это дельта-значение организма для 13C состав
- δ13Cбанкомат - дельта-значение атмосферного CO2, что составляет = -7,8 ‰
- дискриминация из-за диффузии а = 4.4%
- дискриминация карбоксилирования б = 30‰
- cа парциальное давление CO2 во внешней атмосфере, и
- cя парциальное давление CO2 в межклеточных пространствах.
Эта модель, производная ab initio, в целом описывает фракционирование углерода в большинстве растений, которое способствует Фиксация углерода C3. На основании эмпирических данных в эту модель были внесены изменения.[17] Однако несколько дополнительных факторов, не включенных в эту общую модель, будут увеличиваться или уменьшаться. 13Фракционирование углерода по видам. К таким факторам относятся конкурирующая реакция оксигенации RuBisCO, анатомическая и временная адаптация к активности фермента, а также вариации роста и геометрии клеток. Изотопное фракционирование различных путей фотосинтеза однозначно характеризуется этими факторами, как описано ниже.
На заводах C3

Завод C3 использует Фиксация углерода C3, один из трех путей метаболического фотосинтеза, которые также включают C4 и CAM (описано ниже). Эти растения получили название «C3» из-за трехуглеродного соединения (3-фосфоглицериновая кислота, или 3-PGA) производятся CO2 механизм фиксации в этих растениях. Этот механизм C3 является первым этапом цикла Кальвина-Бенсона, который преобразует CO2 и RuBP в 3-ПГА.
Растения C3 являются наиболее распространенным типом растений и обычно хорошо растут при умеренной интенсивности солнечного света и температуре, CO2 концентрации выше 200 частей на миллион и обильные грунтовые воды.[18] Растения C3 плохо растут в очень жарких или засушливых регионах, в которых растения C4 и CAM лучше адаптированы.
Изотопное фракционирование при связывании углерода C3 является результатом комбинированного воздействия CO2 диффузия газа через устьица растения, и карбоксилирование через RuBisCO.[1] Устьичная проводимость дискриминирует более тяжелые 13C на 4,4 ‰.[1] Карбоксилирование RuBisCO способствует большей дискриминации 27 ‰.[1]
Фермент RuBisCO катализирует карбоксилирование CO2 и 5-углеродный сахар, RuBP, в 3-фосфоглицерат, 3-углеродное соединение по следующей реакции:
- CO2 + H2O + RuBP →RuBisCO 2(3-фосфоглицерат)
Продукт 3-фосфоглицерат истощен в 13C из-за кинетический изотопный эффект вышеуказанной реакции. Общая 13C-фракционирование для фотосинтеза C3 находится в диапазоне от -20 до -37 ‰.[2]
Широкий диапазон изменений значений дельты, выраженных в растениях C3, модулируется устьичная проводимость, или скорость CO2 попадание или выход водяного пара в маленькие поры эпидермиса листа.[1] Δ13C растений C3 зависит от взаимосвязи между устьичной проводимостью и скоростью фотосинтеза, что является хорошим показателем эффективности использования воды листьями.[19] Установки C3 с высокой эффективностью использования воды, как правило, меньше фракционируются в 13C (т.е. δ13C относительно менее отрицательный) по сравнению с установками C3 с низкой эффективностью использования воды.[19]
В растениях C4

Растения C4 разработали Фиксация углерода C4 способ сохранить потери воды, поэтому они более распространены в жарком, солнечном и сухом климате.[20] Эти растения отличаются от растений C3, потому что CO2 изначально превращается в четырехуглеродную молекулу, малат, который направляется в связку клеток оболочки, высвобождается обратно в виде CO2 и только после этого входит в цикл Кальвина. Напротив, растения C3 непосредственно выполняют цикл Кальвина в клетках мезофилла, без использования CO2 метод концентрации. Малат, четырехуглеродное соединение, является тезкой фотосинтеза "C4". Этот путь позволяет фотосинтезу C4 эффективно перемещать CO2 к ферменту RuBisCO и поддерживать высокие концентрации CO2 в связка клеток оболочки. Эти клетки являются частью характерного анатомия листа Кранца, который пространственно разделяет типы фотосинтетических клеток концентрическим образом для накопления CO2 возле RuBisCO.[21]
Эти химические и анатомические механизмы улучшают способность RuBisCO связывать углерод, а не выполнять его расточительную работу. оксигеназа Мероприятия. Активность оксигеназы RuBisCO, называемая фотодыхание, вызывает потерю субстрата RuBP из-за окисления и потребляет при этом энергию. Адаптация растений C4 дает преимущество перед путем C3, который теряет эффективность из-за фотодыхания.[22] Соотношение фотодыхания и фотосинтеза в растении зависит от условий окружающей среды, так как снижение CO2 и повышенный O2 концентрации повысили бы эффективность фотодыхания.[20] Атмосферный CO2 на Земле в период между 32-25 миллионами лет назад резко уменьшилось. Это дало избирательное преимущество эволюции пути C4, который может ограничивать частоту фотодыхания, несмотря на снижение концентрации CO в окружающей среде.2.[23] Сегодня растения C4 составляют примерно 5% растительной биомассы на Земле, но около 23% земной фиксации углерода.[24][25][26] Типы растений, которые используют фотосинтез C4, включают: травы и экономически важные культуры, такие как кукуруза, сахарный тростник, просо, и сорго.[22][27]
Изотопное фракционирование различается между Фиксация углерода C4 и C3, из-за пространственного разделения в растениях C4 CO2 захват (в клетках мезофилла) и цикл Кальвина (в клетках оболочки пучка). В растениях C4 углерод превращается в бикарбонат, закрепленный в оксалоацетат через фермент фосфоенолпируват (PEP) карбоксилаза, а затем преобразуется в малат.[4] Малат транспортируется из мезофилл к связка ножен клетки, непроницаемые для CO2. Внутренний СО2 концентрируется в этих клетках, поскольку малат повторно окисляется, а затем декарбоксилируется обратно в CO2 и пируват. Это позволяет RuBisCO проводить катализ, в то время как внутренний CO2 достаточно высока, чтобы избежать конкурирующей реакции фотодыхания. Значение дельты в пути C4 составляет от -12 до -16 ‰, обеднен 13C из-за комбинированного действия карбоксилазы PEP и RuBisCO.
Изотопная дискриминация в пути C4 варьируется относительно пути C3 из-за дополнительных стадий химического превращения и активности PEP-карбоксилазы. После диффузии в устьица конверсия CO2 к бикарбонатным концентратам тяжелее 13C. Последующая фиксация карбоксилазой PEP, таким образом, меньше истощается 13C, чем у Rubsico: около 2 ‰ обедненных PEP карбоксилазой по сравнению с 29 в RuBisCO.[1][5] Однако часть изотопно-тяжелого углерода, который фиксируется карбоксилазой PEP, выходит из ячеек оболочки пучка. Это ограничивает доступный для RuBisCO углерод, что, в свою очередь, снижает его эффект фракционирования.[4] Это объясняет, что общее значение дельты для растений C4 составляет от -12 до -16 ‰.[4]
На заводах CAM
Растения, которые используют Метаболизм крассуловой кислоты, также известный как фотосинтез CAM, временно разделяют свои химические реакции между днем и ночью. Эта стратегия модулирует устьичную проводимость для повышения эффективности использования воды, поэтому хорошо адаптирована для засушливого климата.[28] Ночью растения CAM открывают устьица, чтобы CO2 проникать в клетку и фиксироваться в органических кислотах, которые хранятся в вакуолях. Этот углерод выделяется в цикл Кальвина в течение дня, когда устьицы закрыты, чтобы предотвратить потерю воды, и световые реакции могут управлять необходимой выработкой АТФ и НАДФН.[29] Этот путь отличается от фотосинтеза C4, потому что растения CAM отделяют углерод, сохраняя фиксированный CO2 в пузырьках ночью, а затем транспортировать для использования в течение дня. Таким образом, растения CAM временно концентрируют CO2 для повышения эффективности RuBisCO, тогда как установки C4 пространственно концентрируют CO2 в клетках-оболочках пучка. Распространение растений, использующих фотосинтез САМ, включает: эпифиты (например., орхидеи, бромелии ) и ксерофиты (например., суккуленты, кактусы ).[30]
В метаболизме крассуловой кислоты изотопное фракционирование объединяет эффекты пути C3 в дневное время и пути C4 в ночное время. Ночью, когда температура и потеря воды ниже, CO2 диффундирует через устьица и продуцирует малат через фосфенолпируваткарбоксилазу.[4][6] На следующий день устьица закрываются, малат декарбоксилируется, CO2 фиксируется RuBisCO. Сам по себе этот процесс аналогичен процессу для растений C4 и дает характерные значения фракционирования C4 примерно -11.[6] Однако во второй половине дня растения CAM могут открывать устьица и выполнять фотосинтез C3.[6] Только в дневное время растения CAM имеют фракционирование примерно -28 ‰, характерное для растений C3.[6] Эти комбинированные эффекты обеспечивают δ13C значения для CAM-растений в диапазоне от -10 до -20 ‰.
В 13C к 12Соотношение C в CAM-растениях может указывать на временное разделение CO2 фиксация, которая представляет собой степень биомассы, полученной из ночного CO2 фиксация относительно суточного СО2 фиксация.[31] Это различие может быть сделано потому, что карбоксилаза PEP, фермент, ответственный за чистый CO2 поглощение ночью, различает 13C меньше, чем RuBisCO, который отвечает за дневную CO2 поглощение. CAM-установки, которые фиксируют CO2 в основном ночью будет предсказано показать δ13C значения больше похожи на растения C4, тогда как дневной CO2 фиксация покажет δ13C значения больше похожи на растения C3.
В фитопланктоне
В отличие от наземных растений, где CO2 диффузия в воздухе относительно быстрая и обычно не ограничивает, диффузия растворенного CO2 в воде происходит значительно медленнее и часто может ограничивать связывание углерода в фитопланктоне.[5] В виде газообразного CO2 (г) растворяется в водном CO2 (водн.), он фракционируется как кинетическим, так и эффекты равновесия которые зависят от температуры.[32] По отношению к растениям растворенный CO2 источник фитопланктона может быть обогащен 13C примерно на 8 ‰ от атмосферного CO2.[33]
Изотопное фракционирование 13C пользователем фитопланктон на фотосинтез влияет диффузия внеклеточного водного CO2 в клетку, скорость роста клеток, зависящую от RuBisCO, а также геометрию клетки и площадь поверхности.[7] Использование механизмов бикарбоната и концентрации углерода в фитопланктоне отличает изотопное фракционирование от путей фотосинтеза растений.
Разница между внутриклеточным и внеклеточным CO2 концентрации отражает CO2 потребность клетки фитопланктона, которая зависит от скорости ее роста. Отношение спроса на углерод к предложению определяет диффузию CO.2 в клетку и отрицательно коррелирует с величиной фракционирования углерода фитопланктоном.[34] В совокупности эти отношения позволяют фракционировать CO2 (водн.) и биомасса фитопланктона, которая будет использоваться для оценки темпов роста фитопланктона.[35]
Однако одна только скорость роста не учитывает наблюдаемое фракционирование. Поток CO2 (водн.) вход и выход из клетки примерно пропорционален площади поверхности клетки, а углеродная биомасса клетки варьируется в зависимости от объема клетки. Геометрия фитопланктона, которая увеличивает площадь поверхности до объема, должна иметь большее фракционирование изотопов в результате фотосинтеза.[36]
Биохимические характеристики фитопланктона аналогичны растениям C3, тогда как характеристики газообмена больше напоминают стратегию C4.[37] Более конкретно, фитопланктон повышает эффективность своего основного фермента, связывающего углерод, RuBisCO, с помощью механизмов концентрации углерода (CCM), так же как растения C4 накапливают CO2 в клетках оболочки пучка. Различные формы CCM в фитопланктоне включают активное поглощение бикарбоната и CO.2 через клеточную мембрану активный транспорт неорганического углерода от клеточной мембраны в хлоропласты, а также активное однонаправленное превращение CO2 бикарбонат.[38] Параметры, влияющие на 13Фракционирование углерода в фитопланктоне способствует δ13C значения от -18 до -25 ‰.[4][7]
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час Г. Д. Фаркуар; Дж. Р. Элерингер; Хубик и К. Т. (1989). «Дискриминация изотопов углерода и фотосинтез». Ежегодный обзор физиологии растений и молекулярной биологии растений. 40 (1): 503–537. Дои:10.1146 / annurev.pp.40.060189.002443.
- ^ а б c Кон, Мэтью Дж. (16 ноября 2010 г.). «Изотопный состав углерода наземных растений C3 как индикаторы (палео) экологии и (палео) климата». Труды Национальной академии наук. 107 (46): 19691–19695. Дои:10.1073 / pnas.1004933107. ISSN 0027-8424. ЧВК 2993332. PMID 21041671.
- ^ Фрай, Б .; Шерр, Э. Б. (1989). Стабильные изотопы в экологических исследованиях. Нью-Йорк, штат Нью-Йорк: Springer New York. С. 196–229. Дои:10.1007/978-1-4612-3498-2_12. ISBN 9781461281276.
- ^ а б c d е ж грамм час Хейс, Джон (01.01.2001). «Фракционирование изотопов углерода и водорода в биосинтетических процессах». Обзоры в Минералогии и геохимии. 43: 225–277. Дои:10.2138 / gsrmg.43.1.225.
- ^ а б c d е ж грамм О'Лири, Мэрион Х. (май 1988 г.). «Изотопы углерода в фотосинтезе». Бионаука. 38 (5): 328–336. Дои:10.2307/1310735. ISSN 0006-3568. JSTOR 1310735.
- ^ а б c d е О'Лири, Мэрион Х. (1988). «Изотопы углерода в фотосинтезе». Бионаука. 38 (5): 328–336. Дои:10.2307/1310735. JSTOR 1310735.
- ^ а б c Попп, Брайан Н .; Законы, Эдвард А.; Бидигар, Роберт Р .; Доре, Джон Э .; Hanson, Kristi L .; Уэйкхэм, Стюарт Г. (январь 1998 г.). «Влияние геометрии клеток фитопланктона на изотопное фракционирование углерода». Geochimica et Cosmochimica Acta. 62 (1): 69–77. Bibcode:1998GeCoA..62 ... 69P. Дои:10.1016 / S0016-7037 (97) 00333-5. ISSN 0016-7037.
- ^ а б Гонфиантини, Роберто (апрель 1984 г.). «Заседание консультативной группы I.A.E.A. по эталонным образцам стабильных изотопов для геохимических и гидрологических исследований». Химическая геология. 46 (1): 85. Дои:10.1016/0009-2541(84)90167-0. ISSN 0009-2541.
- ^ МакКоун, Гарольд Т. (сентябрь 1992 г.). "Введение в морскую биогеохимию (Либес, Сьюзан М.)". Журнал химического образования. 69 (9): A251. Дои:10.1021 / ed069pa251.2. ISSN 0021-9584.
- ^ Макклинток, Барбара М. (март 1977 г.). «Биологическая океанография». Американский учитель биологии. 39 (3): 186. Дои:10.2307/4445858. HDL:2027 / umn.31951d01800724l. ISSN 0002-7685. JSTOR 4445858.
- ^ а б Х., Ворон, Питер (2005). Биология растений. Эверт, Рэй Франклин., Эйххорн, Сьюзен Э. (7-е изд.). Нью-Йорк: W.H. Фриман и Ко. ISBN 978-0716710073. OCLC 56051064.
- ^ Табита, Ф. Р .; Satagopan, S .; Hanson, T. E .; Kreel, N.E .; Скотт, С. С. (19 июня 2007 г.). «Отличные формы белков Rubisco I, II, III и IV из трех царств жизни дают ключ к разгадке эволюции Rubisco и взаимосвязей между структурой и функцией». Журнал экспериментальной ботаники. 59 (7): 1515–1524. Дои:10.1093 / jxb / erm361. ISSN 0022-0957. PMID 18281717.
- ^ Скотт, Кэтлин М .; Шведок, Джули; Schrag, Daniel P .; Кавано, Коллин М. (декабрь 2004 г.). «Влияние формы IA RubisCO и растворенного в окружающей среде неорганического углерода на дельта13С симбиоза моллюск-хемоавтотроф Solemya velum». Экологическая микробиология. 6 (12): 1210–1219. Дои:10.1111 / j.1462-2920.2004.00642.x. ISSN 1462-2912. PMID 15560819.
- ^ Guy, R.D .; Fogel, M. L .; Берри, Дж. А. (1993-01-01). «Фотосинтетическое фракционирование стабильных изотопов кислорода и углерода». Физиология растений. 101 (1): 37–47. Дои:10.1104 / стр.101.1.37. ISSN 0032-0889. ЧВК 158645. PMID 12231663.
- ^ МакНевин, Деннис Б .; Badger, Murray R .; Whitney, Spencer M .; Каеммерер, Сюзанна фон; Tcherkez, Guillaume G.B .; Фаркуар, Грэм Д. (2007-12-07). «Различия в различении изотопов углерода трех вариантов D-рибулозо-1,5-бисфосфаткарбоксилазы / оксигеназы отражают различия в их каталитических механизмах». Журнал биологической химии. 282 (49): 36068–36076. Дои:10.1074 / jbc.M706274200. ISSN 0021-9258. PMID 17925403.
- ^ а б Фаркуар, Грэм; О'Лири, M.H .; Берри, Джозеф (1982-01-01). «О связи между дискриминацией изотопов углерода и межклеточной концентрацией диоксида углерода в листьях». Австралийский журнал физиологии растений. 13 (2): 281–292. Дои:10.1071 / PP9820121.
- ^ Шуберт, Брайан А .; Джарен, А. Хоуп (ноябрь 2012 г.). «Влияние концентрации CO2 в атмосфере на фракционирование изотопов углерода в наземных растениях C3». Geochimica et Cosmochimica Acta. 96: 29–43. Bibcode:2012GeCoA..96 ... 29S. Дои:10.1016 / j.gca.2012.08.003. ISSN 0016-7037.
- ^ Уайтхед, Марк (2017-03-06). Окружающая среда и государство. Международная энциклопедия географии: люди, земля, окружающая среда и технологии. Оксфорд, Великобритания: John Wiley & Sons, Ltd., стр. 1–11. Дои:10.1002 / 9781118786352.wbieg0920. ISBN 9780470659632.
- ^ а б Морено-Гутьеррес, Кристина; Доусон, Тодд Э .; Николас, Эмилио; Керехета, Хосе Игнасио (23 августа 2012 г.). «Изотопы раскрывают контрастирующие стратегии водопользования среди сосуществующих видов растений в средиземноморской экосистеме». Новый Фитолог. 196 (2): 489–496. Дои:10.1111 / j.1469-8137.2012.04276.x. ISSN 0028-646X. PMID 22913668.
- ^ а б Ehleringer, James R .; Sage, Rowan F .; Фланаган, Лоуренс Б .; Пирси, Роберт В. (1991-03-01). «Изменение климата и эволюция фотосинтеза C4». Тенденции в экологии и эволюции. 6 (3): 95–99. Дои:10.1016 / 0169-5347 (91) 90183-Х. ISSN 0169-5347. PMID 21232434.
- ^ Кеннеди, Роберт А. (23 апреля 1976 г.). «Фотодыхание в культурах тканей растений C3 и C4». Физиология растений. 58 (4): 573–575. Дои:10.1104 / pp.58.4.573. ЧВК 543284. PMID 16659720.
- ^ а б C₄ биология растений. Сейдж, Роуэн Фредерик, Монсон, Р.К. (Рассел К.), 1954-. Сан-Диего: Academic Press. 1999 г. ISBN 9780080528397. OCLC 176630229.CS1 maint: другие (связь)
- ^ Sage, Rowan F .; Сейдж, Тэмми Л .; Кочачинар, Ферит (2012). "Фотодыхание и эволюция фотосинтеза C4 | Ежегодный обзор биологии растений". Ежегодный обзор биологии растений. 63 (1): 19–47. Дои:10.1146 / annurev-arplant-042811-105511. PMID 22404472. S2CID 24199852.
- ^ Bond, W. J .; Woodward, F. I .; Мидгли, Г. Ф. (2004-11-12). «Глобальное распределение экосистем в мире без огня». Новый Фитолог. 165 (2): 525–538. Дои:10.1111 / j.1469-8137.2004.01252.x. ISSN 0028-646X. PMID 15720663.
- ^ Osborne, C.P .; Бирлинг, Д. Дж. (29 января 2006 г.). «Зеленая революция природы: выдающийся эволюционный рост растений C4». Философские труды Королевского общества B: биологические науки. 361 (1465): 173–194. Дои:10.1098 / rstb.2005.1737. ISSN 0962-8436. ЧВК 1626541. PMID 16553316.
- ^ Келлог, Элизабет А. (июль 2013 г.). «С4 фотосинтез». Текущая биология. 23 (14): R594 – R599. Дои:10.1016 / j.cub.2013.04.066. ISSN 0960-9822. PMID 23885869.
- ^ Чжу, Синь-Гуан; Лонг, Стивен П.; Орт, Дональд Р. (апрель 2008 г.). «Какова максимальная эффективность, с которой фотосинтез может преобразовывать солнечную энергию в биомассу?». Текущее мнение в области биотехнологии. 19 (2): 153–159. Дои:10.1016 / j.copbio.2008.02.004. ISSN 0958-1669. PMID 18374559.
- ^ Тинг, ИП (июнь 1985 г.). «Кислотный метаболизм у крассулейных». Ежегодный обзор физиологии растений. 36 (1): 595–622. Дои:10.1146 / annurev.pp.36.060185.003115. HDL:10150/552219. ISSN 0066-4294.
- ^ Тинг, И. (1 января 1985 г.). «Кислотный метаболизм у крассулейных». Ежегодный обзор физиологии растений и молекулярной биологии растений. 36 (1): 595–622. Дои:10.1146 / annurev.pp.36.060185.003115. HDL:10150/552219. ISSN 1040-2519.
- ^ Smith, J. A. C .; Уинтер, К. (1996). Кислотный метаболизм крассулейных. Берлин, Гейдельберг: Springer Berlin Heidelberg. С. 427–436. Дои:10.1007/978-3-642-79060-7_27. ISBN 9783642790621.
- ^ Зима, Клаус; Холтум, Джозеф А. М. (2002-08-01). «Насколько близко значения δ13C у растений, ответственных за метаболизм жирных водорослей, отражают долю CO2, зафиксированную в течение дня и ночи?». Физиология растений. 129 (4): 1843–1851. Дои:10.1104 / стр.002915. ISSN 0032-0889. ЧВК 166772. PMID 12177497.
- ^ Zhang, J .; Quay, P.D .; Уилбур, Д.О. (1995-01-01). «Фракционирование изотопов углерода при газо-водном обмене и растворении СО2». Geochimica et Cosmochimica Acta. 59 (1): 107–114. Дои:10.1016 / 0016-7037 (95) 91550-Д. ISSN 0016-7037.
- ^ Köhler, P .; Fischer, H .; Шмитт, Дж. (Март 2010 г.). «Атмосферная δ13CO2 и ее связь с CO2 и глубинными океанскими δ13C в конце плейстоцена» (PDF). Палеоокеанография. 25 (1). Дои:10.1029 / 2008pa001703. ISSN 0883-8305.
- ^ Законы, Эдвард А.; Попп, Брайан Н .; Кассар, Николас; Танимото, Джейми (2002). «Модели дискриминации 13C в океаническом фитопланктоне: вероятное влияние механизмов концентрации CO2 и последствия для палеореконструкций». Функциональная биология растений. 29 (3): 323–333. Дои:10.1071 / pp01183. ISSN 1445-4416.
- ^ Законы, Эдвард А.; Попп, Брайан Н .; Бидигар, Роберт Р .; Kennicutt, Mahlon C .; Макко, Стивен А. (1995-03-01). «Зависимость изотопного состава углерода фитопланктона от скорости роста и [CO2) водн .: теоретические соображения и экспериментальные результаты». Geochimica et Cosmochimica Acta. 59 (6): 1131–1138. Bibcode:1995GeCoA..59.1131L. Дои:10.1016/0016-7037(95)00030-4. ISSN 0016-7037.
- ^ Попп, Брайан Н .; Законы, Эдвард А.; Бидигар, Роберт Р .; Доре, Джон Э .; Hanson, Kristi L .; Уэйкхэм, Стюарт Г. (1 января 1998 г.). «Влияние геометрии клеток фитопланктона на изотопное фракционирование углерода». Geochimica et Cosmochimica Acta. 62 (1): 69–77. Bibcode:1998GeCoA..62 ... 69P. Дои:10.1016 / S0016-7037 (97) 00333-5. ISSN 0016-7037.
- ^ Законы, Эдвард А.; Бидигар, Роберт Р .; Попп, Брайан Н. (ноябрь 1997 г.). «Влияние скорости роста и концентрации СО2 на фракционирование изотопов углерода морской диатомей Phaeodactylum tricornutum». Лимнология и океанография. 42 (7): 1552–1560. Дои:10.4319 / lo.1997.42.7.1552. ISSN 0024-3590.
- ^ Кассар, Николас; Законы, Эдвард А.; Попп, Брайан Н. (ноябрь 2006 г.). «Изотопное фракционирование углерода морской диатомей Phaeodactylum tricornutum в условиях роста, ограниченного питательными веществами и светом». Geochimica et Cosmochimica Acta. 70 (21): 5323–5335. Дои:10.1016 / j.gca.2006.08.024. ISSN 0016-7037.


