Галогениды индия - Википедия - Indium halides
Есть три набора Галогениды индия, тригалогениды, моногалогениды и несколько промежуточных галогениды. В моногалогенидах степень окисления индия равен +1, а их собственные названия - фторид индия (I), хлорид индия (I), бромид индия (I) и иодид индия (I).
Промежуточные галогениды содержат индий с степени окисления, +1, +2 и +3.
Тригалогениды индия
Во всех тригалогенидах степень окисления индия равен +3, а их собственные названия - фторид индия (III), хлорид индия (III), бромид индия (III) и иодид индия (III). Тригалогениды Льюис кислый. Трихлорид индия является отправной точкой в производстве триметилиндий который используется в полупроводниковой промышленности.
Фторид индия (III)
InF3 белый кристаллическое твердое вещество с т.пл. 1170 ° С. В его состав входит 6-координатный индий.
Хлорид индия (III)
InCl3 представляет собой белое кристаллическое твердое вещество, т.пл. 586 ° C. Он имеет ту же структуру, что и AlCl3.
Бромид индия (III)
InBr3 представляет собой бледно-желтое кристаллическое твердое вещество, т.пл. 435 ° С. Он имеет ту же структуру, что и AlCl3. InBr3 находит применение в органический синтез как водостойкая кислота Льюиса.[1]
Иодид индия (III)
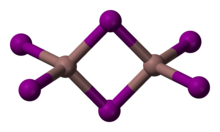
InI3 представляет собой окрашенное кристаллическое твердое вещество, обычно обозначаемое как оранжевый. Известны отчетливые желтые и красные формы. Красная форма превращается в желтую при 57 ° C. Структура красной формы не определена Рентгеновская кристаллография, однако спектроскопические данные указывают на то, что индий может иметь шести координаты.[2] Желтая форма состоит из В2я6 с 4-мя координатными индиевыми центрами. Он используется в качестве «геттера йодида» в Cativa процесс.
Промежуточные галогениды
Известно удивительное количество промежуточных хлоридов и бромидов, но только один йодид, а не дифторид. Вместо кажущейся степени окисления +2 эти соединения содержат индий в степенях окисления +1 и +3. Таким образом, дииодид описывается как InяВIIIИкс4. Спустя некоторое время существование соединений, содержащих анион In2
Br2−
были подтверждены, которые содержат индий-индийскую связь. Ранние работы по хлоридам и бромидам включали исследования бинарных фазовых диаграмм тригалогенидов и родственного моногалогенида. Многие из соединений были изначально неправильно идентифицированы, поскольку многие из них неконгруэнтны и разлагаются перед плавлением. Существование большинства хлоридов и бромидов, о которых ранее сообщалось, в настоящее время либо подтверждено рентгеновскими дифракционными исследованиями, либо их структура уже оставлена историей. Возможно, самым неожиданным случаем ошибочной идентификации стал неожиданный результат: тщательное повторное исследование InCl / InCl3 бинарная фазовая диаграмма не обнаружила InCl2.[3]
Причина такого обилия соединений заключается в том, что индий образует 4- и 6-координатные анионы, содержащие индий (III), например. В
Br−
, В
Cl3−
а также анион В2
Br2−
что удивительно содержит индий-индийскую связь.
В7Cl9 И в7Br9
В7Cl9 представляет собой твердое вещество желтого цвета, стабильное до 250 ° C, которое входит в составя6(ВIIICl6) Cl3[4]
В7Br9 имеет структуру, аналогичную In7Cl9 и может быть сформулирован как Inя6(ВIIIBr6) Br3[5]
В5Br7
В5Br7 представляет собой бледно-желтое твердое вещество. Он сформулирован вя3(ВII2Br6) Br. ВII2Br6 анион имеет затмеваемую этаноподобную структуру с длиной связи металл-металл 270 мкм.[6]
В2Cl3 И в2Br3
В2Cl3 бесцветен и сформулирован вя3 ВIIICl6[7] В отличие от2Br3 содержит In2Br6 анион, присутствующий в In5Br7, и сформулирована вя(ВII2Br6) со структурой, подобной Ga2Br3.[8]
В4Br7
В4Br7 почти бесцветный с бледно-зеленовато-желтым оттенком. Он светочувствителен (как TlCl и TlBr), распадаясь на InBr.2 и в металле. Это смешанная соль, содержащая In
Br−
И в
Br3−
анионы, сбалансированные In+ катионы. Он сформулирован вя5(ВIIIBr4)2(ВIIIBr6Причины искаженной решетки были приписаны разрыхляющей комбинации между дважды заполненными ненаправленными 5s-орбиталями индия и соседними гибридными 4p-орбиталями брома.[9]
В5Cl9
В5Cl9 формулируется как Inя3ВIII2Cl9. В2
Cl3−
анион имеет два 6-координированных атома индия с 3-мя мостиковыми атомами хлора, грани которых разделяют биоктаэдры, со структурой, аналогичной Cr2
Cl2−
и Tl2
Cl2−
.[10]
InBr2
InBr2 представляет собой зеленовато-белое кристаллическое твердое вещество, содержащееся вяВIII Br4. Имеет ту же структуру, что и GaCl.2. InBr2 растворим в ароматических растворителях и некоторых соединениях, содержащих η6-ареновые комплексы In (I). (Видеть осязание для объяснения связи в таких комплексах арен-ион металла). С некоторыми лигандами InBr2 образует нейтральные комплексы, содержащие индий-индийскую связь.[11]
InI2
InI2 представляет собой твердое вещество желтого цвета, содержащееся вяВIIIя4.
Моногалогениды
Твердые моногалогениды InCl, InBr и InI все нестабильны по отношению к воде, разлагаясь на частицы металла и индия (III). Они находятся между соединениями галлия (I), которые являются более активными, и таллием (I), которые устойчивы по отношению к воде. InI самый стабильный. До относительно недавнего времени моногалогениды были научным курьезом, однако с открытием того, что их можно использовать для получения кластерных и цепочечных соединений индия, они теперь вызывают гораздо больший интерес.
InF
InF известен только как нестабильное газообразное соединение.
InCl
Форма InCl при комнатной температуре - желтая, с кубической искаженной структурой NaCl.[12] Красная высокая температура (> 390 ° C) имеет структура.[13]
InBr
InBr представляет собой красное кристаллическое твердое вещество, т.пл. 285 ° C. Он имеет ту же структуру, что и , с ромбической искаженной структурой каменной соли. Его можно приготовить из металлического индия и InBr.3.
InI
InI - темно-красное пурпурное кристаллическое твердое вещество. Он имеет ту же структуру, что и . Это может быть получено путем прямого сочетания составляющих его элементов при высокой температуре. В качестве альтернативы его можно приготовить из InI.3 и металлический индий в кипящих ксилолах.[14] Это наиболее устойчивый из твердых моногалогенидов и растворим в некоторых органических растворителях. Растворы InI в смеси пиридин / м-ксилол стабильны ниже 243 К.[15]
Анионогалогенидные комплексы In (III)
Тригалогениды Кислоты Льюиса и образуют аддитивные соединения с лигандами. Для InF3 Однако известно несколько примеров других галогенидно-аддитивных соединений с тетраэдрической, тригонально-бипирамидальной и октаэдрической координационной геометриями. С галогенид-ионами есть примеры всех этих геометрических форм наряду с некоторыми анионами с октаэдрически координированным индием и с мостиковыми атомами галогена.2
Икс3−
с тремя мостиковыми атомами галогена и In2
Икс−
с одним.Кроме того, в InX есть примеры индия с квадратной плоской геометрией.52− ион. Квадратная плоская геометрия In
Cl2−
был первым найденным элементом основной группы.
В
Икс−
И в
Икс3−
Соли В
Cl−
, В
Br−
И в
я−
известны. Соль LiInF4 был подготовлен [16] однако он не содержит тетраэдрических анионов, но имеет необычную слоистую структуру с октаэдрически координированными атомами индия. Соли InF63−, В
Cl3−
И в
Br3−
[17] все было сделано.
В
Cl2−
И в
Br2−
В
Cl2−
ион оказался квадратно-пирамидальным в соли (NEt4)2InCl5, с той же структурой, что и (NEt4)2 TlCl5, но является тригонально-бипирамидным в сольвате ацетонитрила пентахлориндата тетрафенилфосфония.[18]
В
Br2−
ион аналогичным образом обнаружен в форме квадратной пирамиды, хотя и искаженной, в соли бис (4-хлорпиридиния) [19] и тригонально-бипирамидный [20] в Би37InBr48.
В2
Икс−
В2
Икс−
ионы содержат единственный мостиковый атом галогена. Изогнутый или линейный мостик не может быть определен по спектрам. Хлорид и бромид были обнаружены с помощью масс-спектрометрии с электрораспылением. В2
я−
ион был приготовлен в соли CsIn2я7.[21]
В2
Икс3−
Цезиевые соли In2
Cl3−
И в2
Br3−
оба содержат биядерные анионы с октаэдрически координированными атомами индия.[22]
Анионные галогенидные комплексы In (I) и In (II)
Вя
Икс−
И вя
Икс2−
ВяИкс2− производится, когда In2Икс62− ион непропорционально. Соли, содержащие Inя
Икс2−
ионы, и их колебательные спектры интерпретированы как показывающие, что они имеют C3в симметрия тригонально-пирамидальный геометрия со структурой, аналогичной изоэлектронной Sn
Икс−
ионы.
В2
Cl2−
, В2
Br2−
И в2
я2−
Соли хлорид-, бром- и иодид-ионов (Bu4N)2В2Икс6 были подготовлены. В неводных растворителях этот ион непропорционально уступатья
Икс−
И вIII
Икс−
.
Аддукты нейтрального галогенида индия (II)
После открытия In2Br62− ряд родственных нейтральных соединений, содержащих InII2Икс4 ядра образовались в результате реакции дигалогенидов индия с нейтральными лигандами.[23] Некоторые химики называют эти аддукты, когда они используются в качестве отправной точки для синтеза кластерных соединений, как «In2Икс4’Например то TMEDA аддукт.[24]
Рекомендации
- Таблица Менделеева WebElements »Индий» информация о соединениях
- Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Коттон, Ф. Альберт; Уилкинсон, Джеффри; Мурильо, Карлос А .; Бохманн, Манфред (1999), Продвинутая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ Zhan-Hui Zhang Thieme Connect Synlett 2005 711
- ^ Тейлор М. Дж., Клоо Л. А. Журнал рамановской спектроскопии 31, 6, (2000), 465
- ^ Мейер Г., Блахник Р.З. Анорг. Allg. Chem. 1983, 503, 126
- ^ H.P. Бек Д. Вильгельм Ангью. Chem. Int. Эд. Англ., 30 (7) (1991) 824-25
- ^ Dronskowski R Z Kristallogr. 210 (1995) 920
- ^ M Ruck, H Bärnighausen Z. Anorg. allg. Chem. 625, выпуск 4, (1999), 577
- ^ Мейер. Г. З. Анорг. Allgem. Chem. 479 (1981) 7 39
- ^ Staffel. Т., Мейер. G., Z Anorg Allgem Chem 552 9 113
- ^ Р. Дронсковский, Angew. Chem. Int. Эд. Англ. 34 (1995) 1126.
- ^ Мейер. Г. З. Анорг. Allgem. Chem. 1978 445140,
- ^ Синклер И., Уорролл И. Дж. Кан. J. Chem./Rev. может. чим. 60 (6): 695-698 (1982).
- ^ Дж. М. Ван ден Берг Acta Crystallogr 20 (1966) 905
- ^ К. П. Дж. М. ван дер Ворст, Г. К. Вершур, В. Дж. А. Мааскант, Acta Crystallogr. 1978, B34, 3333.
- ^ Organic Syntheses, Coll. Vol. 10, стр.170 (2004); Vol. 79, стр.59 (2002).
- ^ Дженнифер А. Дж. Пардо Дж. Эй Джей, Коули А. Р. , Даунс А.Дж. , Грин Т. Acta Crystallogr. (2005). C61, 200
- ^ Gravereau P, Chaminade J.P, Gaewdang., T., Grannec J., Pouchard M., Hagenmuller P. Acta Crystallogr. (1992). C48, 769
- ^ Spiro Inorg Chem 4 1290 (1965)
- ^ Бубенхайм В., Френзен Г., Мюллер У. Acta Crystallogr. С, 51, 6, (1995), 1120.
- ^ Исихара Х., Доу С., Гесинг Т.М., Паулюс Х., Фюсс Х., Вайс А. Журнал молекулярной структуры 471, 1 (1998) 175
- ^ Дубенский В., Рук М., З. Анорг. Allgem. Chemie, 629, (2003), 3, 375
- ^ Тейлор М. Дж. Клоо Л. А. Журнал рамановской спектроскопии 31, 6, (2000), 465
- ^ . Мейер З. Анорг. allgem. Chem. 1978, 445, 140
- ^ Синклер И., Уорролл И.Дж. Может. J. Chem./Rev. может. чим. 60 (6): 695-698 (1982).
- ^ Xiao-Wang Li, Robinson G, Pennington W.T. Основная группа химии 1, (1996) 301

