Минимально сознательное состояние - Minimally conscious state
| Минимально сознательное состояние | |
|---|---|
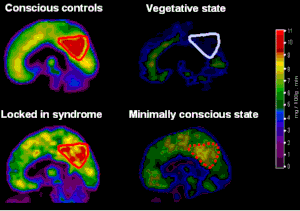 | |
| Сканирование мозга при различных нарушениях сознания, в том числе минимально сознательном состоянии |
А минимально сознательное состояние (MCS) это расстройство сознания в отличие от стойкое вегетативное состояние и синдром запертости. В отличие от стойкого вегетативного состояния у пациентов с MCS наблюдается частичное сохранение сознательной осведомленности.[1] MCS - относительно новая категория расстройств сознания. Естественное течение и отдаленные результаты MCS еще не изучены. Распространенность MCS оценивается от 112 000 до 280 000 взрослых и педиатрический случаи.[2]
Патофизиология
Нейровизуализация
Поскольку состояние минимального сознания является относительно новым критерием диагностики, существует очень мало исследований функциональной визуализации пациентов с этим состоянием. Предварительные данные показали, что общий церебральный метаболизм ниже, чем у людей с осознанным осознанием (20-40% от нормы).[3]) и немного выше, но сопоставимы с таковыми в вегетативных состояниях. Активация в медиальном теменная кора и прилегающий задний поясная извилина это области мозга, которые, по-видимому, различаются между пациентами с MCS и пациентами с вегетативным состоянием. Эти области наиболее активны в периоды сознательного бодрствования и наименее активны в измененных состояниях сознания, таких как Общая анестезия, пропофол, гипнотический государственный, слабоумие, и Синдром Вернике – Корсакова. Слуховая стимуляция вызывала более выраженную активацию в первичных и префронтальных ассоциативных областях у пациентов с MCS, чем у пациентов с вегетативным состоянием. Также было больше кортиокортикальной функциональной связи между слуховая кора и большая сеть временный и префронтальная кора в MCS, чем в вегетативных состояниях. Эти результаты стимулируют лечение, основанное на терапевтических стратегиях нейромодуляции и когнитивной ревалидации для пациентов с MCS.[4]


Использовано одно исследование диффузионная тензорная визуализация (DTI) в двух тематических исследованиях. Они обнаружили, что у обоих пациентов была широко распространенная церебральная атрофия. В боковые желудочки были увеличены в размерах, а мозолистое тело и перивентрикулярный белое вещество были уменьшены. Карты DTI показали, что наблюдалось значительное уменьшение объема медиального мозолистого тела и других частей мозга по сравнению с нормальными субъектами. Они также обнаружили заметно более низкие значения диффузии в белом веществе и увеличение спинномозговая жидкость отсеки. Корковые травмы на этом уровне создают особенно благоприятную среду для прорастания новых аксоны возникать в неповрежденных областях коры головного мозга, что может объяснить некоторые из более высоких показателей выздоровления у пациентов с минимальным сознанием. Рост аксонов коррелировал с функциональным восстановлением моторики. Повторный рост и изменение маршрута аксонов может объяснить некоторые изменения в структуре мозга. Эти результаты подтверждают попытки проспективно и продольно охарактеризовать нейропластичность как в структуре, так и в функции мозга после тяжелых травм. Использование DTI и других нейровизуализация Эти методы могут пролить свет на дебаты о перестройке кортикального слоя на большие расстояния и могут привести к лучшим стратегиям реабилитации.[5]
Некоторые области мозга, которые связаны с субъективным ощущением боли, были активированы у пациентов с MCS, когда вредная стимуляция присутствовал. Позитронно-эмиссионная томография (ПЭТ) сканирование показало усиление кровотока во вторичную сенсорную кору, задний теменная кора, премоторная кора, и начальник височная кора. Паттерн активации, однако, имел меньшую пространственную протяженность. Некоторые части мозга были менее активированы, чем нормальные пациенты, во время обработки ядовитых стимулов. Это были задняя поясная извилина, медиальный префронтальная кора, а затылочная кора. Несмотря на то, что функциональная визуализация мозга может объективно измерить изменения функции мозга во время вредной стимуляции, роль различных областей мозга в обработке боли изучена лишь частично. Кроме того, все еще существует проблема субъективного опыта. Пациенты с MCS по определению не могут последовательно и надежно сообщать о своем опыте. Даже если бы они смогли ответить на вопрос «Вам больно?», Не было бы надежного ответа. Необходимы дальнейшие клинические испытания, чтобы определить целесообразность использования обезболивание у пациентов с MCS.[6]
Остаточная языковая функция
А функциональная магнитно-резонансная томография Исследование (фМРТ) показало, что пациенты с минимально сознательным состоянием проявляли активацию в слуховых сетях, когда они слышали рассказы с личным значимым содержанием, которые читались знакомым голосом. Эти активации не наблюдались при обратном чтении повествования.[7]
В другом исследовании сравнивали способность распознавать язык пациентов в вегетативном состоянии и состоянии минимального сознания. Они обнаружили, что некоторые пациенты в состоянии минимального сознания демонстрировали некоторые доказательства сохраненной обработки речи. В ответ на предложения было больше активации по сравнению с белым шумом.[8]
Диагностический
Медицинское определение
Состояние минимального сознания (MCS) определяется как состояние сильно измененного сознания, при котором демонстрируются минимальные, но определенные поведенческие свидетельства самосознания или осведомленности об окружающей среде.[1]
Диагностика
Хотя пациенты с MCS могут демонстрировать когнитивно-опосредованное поведение, они возникают непоследовательно. Однако они воспроизводимы или могут сохраняться достаточно долго, чтобы отличить их от рефлексивного поведения. Из-за этого несоответствия может потребоваться расширенная оценка, чтобы определить, произошла ли простая реакция (например, движение пальца или моргание) из-за определенного события окружающей среды (например, команда переместить палец или моргнуть) или была просто случайным поведением. .[1] Различить VS и MCS часто бывает трудно, потому что диагноз зависит от наблюдения за поведением, которое демонстрирует самосознание или осведомленность об окружающей среде, и потому, что эти поведенческие реакции заметно снижаются. Одна из наиболее распространенных диагностических ошибок, связанных с расстройствами сознания, - это принятие MCS за VS, что может привести к серьезным последствиям, связанным с клиническим ведением.[9]
Giacino et al. предложили продемонстрировать следующее поведение, чтобы поставить диагноз MCS.
- Следуя простым командам.
- Жестовые или вербальные ответы да / нет (независимо от точности).
- Разборчивая вербализация.
- Целенаправленное поведение, например, обусловленное соответствующими стимулами окружающей среды и не являющееся рефлексивным. Вот некоторые примеры целенаправленного поведения:
- уместная улыбка или плач в ответ на лингвистическое или визуальное содержание эмоционального, но не на нейтральные темы или стимулы.
- вокализации или жесты, которые происходят в прямом ответе на лингвистическое содержание вопросов.
- достижение объектов, демонстрирующее четкую взаимосвязь между местоположением объекта и направлением досягаемости.
- прикосновение к предметам или удерживание их таким образом, чтобы соответствовать размеру и форме предмета.
- преследовать движение глаз или устойчивую фиксацию, которая происходит в прямом ответе на движущиеся или заметные раздражители.[1]
Уход
В настоящее время нет убедительных доказательств, подтверждающих изменение курса восстановления минимально сознательного состояния. В настоящее время существует несколько клинические испытания ведутся исследования потенциальных методов лечения.[10]В одном случае стимуляция таламуса с использованием глубокая стимуляция мозга (DBS) привела к некоторым улучшениям в поведении. Пациент был 38-летним мужчиной, который оставался в минимальном сознании после тяжелого травматическое повреждение мозга. Он не реагировал на постоянное подчинение командам или коммуникативные способности и оставался невербальным в течение двух лет на стационарной реабилитации. фМРТ сканирование показало сохранение крупномасштабной двухполушарной церебральной языковой сети, что указывает на возможность дальнейшего восстановления. Позитронно-эмиссионная томография показали, что общий уровень церебрального метаболизма у пациента значительно снизился. Ему были имплантированы электроды DBS с двух сторон в его центральную часть. таламус. В частности, электроды DBS нацелены на переднюю интраламинарные ядра таламуса и соседние параламинарные области ядер таламической ассоциации. Оба электрода располагались в центральном латеральном ядре, параламинарных областях срединной спинной мышцы и в задне-медиальной части комплекса центромедианного / парафасикулярного ядра. Это позволило максимально охватить таламические тела. Стимуляция DBS проводилась таким образом, что пациент подвергался различным моделям стимуляции, чтобы помочь определить оптимальные поведенческие реакции. Примерно через 140 дней после начала стимуляции проявились качественные изменения в поведении. Были более длительные периоды открытия глаз и повышенная реакция на командные стимулы, а также более высокие баллы по шкале восстановления комы (CRS) JFK. Также наблюдались функциональное использование предметов и внятная вербализация. Наблюдаемые улучшения в уровне возбуждения, моторном контроле и последовательности поведения могут быть результатом прямой активации лобных корковых и базальный ганглий системы, которые были иннервируются нейроны внутри ядер таламической ассоциации. Эти нейроны действуют как ключевые коммуникационные реле и образуют путь между мозговой ствол системы возбуждения и лобная доля регионы. Этот путь важен для многих исполнительные функции Такие как рабочая память, регулирование усилия, избирательное внимание, и фокус.[11]
В другом исследовании с участием 50-летней женщины, у которой были симптомы, соответствующие MCS, введение золпидем, а успокаивающее гипнотический препарат значительно улучшил состояние пациента. Без лечения у пациента появились признаки мутизм, атетоид движения конечностей и полная зависимость от всех средств личной гигиены. Через 45 минут после введения 5-10 мг золпидема пациент прекратил атетоид движений, восстановила способность говорить и могла самостоятельно питаться. Эффект длился 3-4 часа, после чего она вернулась в прежнее состояние. Эффекты повторялись ежедневно. ДОМАШНИЙ ПИТОМЕЦ Сканирование показало, что после введения золпидема наблюдалось заметное увеличение кровотока в областях мозга, прилегающих к поврежденным тканям или удаленных от них. В данном случае эти области были ипсилатеральный полушария головного мозга и мозжечок. Считается, что эти области были заблокированы местом повреждения из-за ГАМК -опосредованный механизм, и ингибирование было изменено золпидемом, который является ГАМК агонист. Тот факт, что золпидем является успокаивающее лекарство, которое вызывает сон у нормальных людей, но вызывает возбуждение у пациента с MCS, парадоксально. Механизмы возникновения этого эффекта не совсем ясны.[12]
Есть недавние доказательства того, что транскраниальная стимуляция постоянным током (tDCS), метод, обеспечивающий подачу небольшого электрического тока в мозг с помощью неинвазивных электродов, может улучшить клиническое состояние пациентов с MCS. В одном исследовании с 10 пациентами с нарушениями сознания (7 в VS, 3 в MCS), tDCS применялась в течение 20 минут каждый день в течение 10 дней и показала клиническое улучшение у всех 3 пациентов, которые находились в MCS, но не у пациентов с ПРОТИВ. Эти результаты остались при 12-месячном наблюдении. Двое из пациентов с MCS, у которых был инсульт мозга менее 12 месяцев, пришли в сознание в следующие месяцы. Один из этих пациентов прошел второй курс лечения tDCS через 4 месяца после его первоначального лечения, и у него было дальнейшее выздоровление и он пришел в сознание без изменения клинического статуса между двумя курсами лечения.[13] Более того, в двойном слепом перекрестном исследовании с фиктивным контролем было показано, что немедленные эффекты одного сеанса tDCS временно улучшают клинический статус 13 из 30 пациентов с MCS, но не у пациентов с VS[14]
Прогноз
Одной из определяющих характеристик состояния минимального сознания является более постоянное улучшение и значительно более благоприятные исходы после травмы по сравнению с вегетативным состоянием. В одном исследовании приняли участие 100 пациентов с тяжелой черепно-мозговой травмой. В начале исследования все пациенты не могли последовательно выполнять команды или надежно общаться. Этим пациентам был поставлен диагноз MCS или вегетативное состояние на основании результатов теста JFK. Кома Шкала восстановления и диагностические критерии MCS, рекомендованные рабочей группой Aspen Consensus Conference. Обе группы пациентов были дополнительно разделены на тех, кто страдал от травматическое повреждение мозга и те, кто получил нетравматические повреждения головного мозга (аноксия, опухоль, гидроцефалия, инфекционное заболевание ). Пациентов оценивали несколько раз в течение 12 месяцев после травмы с использованием шкалы оценки инвалидности (DRS), которая варьируется от 30 = мертвые до 0 = нет инвалидности. Результаты показывают, что баллы DRS для подгрупп MCS показали наибольшее улучшение и предсказали наиболее благоприятные исходы через 12 месяцев после травмы. Среди пациентов с диагнозом MCS показатели DRS были значительно ниже у пациентов с нетравматическими повреждениями головного мозга по сравнению с пациентами с вегетативным состоянием с черепно-мозговой травмой. Показатели DRS также были значительно ниже в группе с нетравматическим повреждением головного мозга MCS по сравнению с группой с черепно-мозговой травмой MCS. Парные сравнения показали, что баллы по DRS были значительно выше у пациентов с нетравматическими повреждениями головного мозга, чем у пациентов с черепно-мозговыми травмами. Для пациентов в вегетативных состояниях не было достоверных различий между пациентами с нетравматическим повреждением головного мозга и пациентами с черепно-мозговой травмой. Из 100 изученных пациентов 3 пациента полностью выздоровели (имели 0 баллов по шкале DRS). Этим трем пациентам был поставлен диагноз MCS, и они страдали черепно-мозговой травмой.[9]
Таким образом, люди с минимальным сознанием и нетравматическими повреждениями головного мозга не будут прогрессировать так же хорошо, как пациенты с черепно-мозговой травмой, в то время как у тех, кто находится в вегетативном состоянии, вероятность выздоровления ниже или ниже.
Из-за существенных различий в прогнозах, описанных в этом исследовании, крайне важно правильно диагностировать MCS. Неправильная диагностика MCS как вегетативного состояния может привести к серьезным последствиям, связанным с клиническим ведением.
История
До середины 1990-х гг. У клиницистов и исследователей не было рабочих определений для проведения дифференциальной диагностики среди расстройства сознания. В результате пациенты были разделены на широкие категории, часто в зависимости от тяжести инвалидности (например, умеренная, тяжелая, чрезвычайно тяжелая). Эти диагнозы были поставлены без учета существенных различий в поведенческих и патологических характеристиках. За трехлетний период, охватывающий 1994–1996 гг., Были опубликованы три позиционных заявления относительно диагностических критериев расстройства сознания. «Медицинские аспекты Стойкое вегетативное состояние »Была опубликована Американская академия неврологии (AAN) в 1994 году. В 1995 году «Рекомендации по использованию единой номенклатуры, относящиеся к пациентам с тяжелыми нарушениями сознания» были опубликованы Американский конгресс реабилитационной медицины (ACRM). В 1996 г. «Международная рабочая группа по управлению вегетативным состоянием: краткий отчет» была опубликована группой международных делегатов из неврология, реабилитация, нейрохирургия, и нейропсихология. Однако, поскольку диагностические критерии были опубликованы независимо друг от друга, окончательные рекомендации сильно отличались друг от друга. Для изучения основных причин этих различий была созвана рабочая группа по нейроповеденческим исследованиям в Аспене. В конце концов, рабочая группа Aspen представила консенсусное заявление относительно определений и диагностических критериев расстройства сознания, которые включают вегетативное состояние (VS) и состояние минимального сознания (MCS).[15]
Этические вопросы
Одна из основных этических проблем пациентов с тяжелым поражением головного мозга - их неспособность общаться. По определению, пациенты, находящиеся без сознания или находящиеся в минимальном сознании, не могут дать информированное согласие, необходимое для участия в клинических исследованиях. Обычно письменное разрешение получают от членов семьи или законных представителей. Невозможность получить информированное согласие привело к тому, что многим исследованиям было отказано в грантах, одобрении этического комитета или публикациях исследований. Это подвергает пациентов в этих условиях риску быть лишенным лечения, которое может спасти жизнь.[4]
Право на смерть
В право умереть у пациентов со временем развились тяжелые когнитивные нарушения из-за тяжелого неврологического состояния и кажущейся бесполезности продолжения лечения. Такие дела активно обсуждались в прошлом, как и в случае с Терри Скьяво у которого диагностировано стойкое вегетативное состояние. В случае пациентов с минимальным сознанием они не находятся в бессознательном состоянии постоянно и не обязательно безнадежно повреждены. Таким образом, эти пациенты требуют дополнительного обследования.[16] С одной стороны, некоторые утверждают, что возможность вмешательства у некоторых пациентов может подорвать моральное обязательство «право на смерть». И наоборот, существует также опасение, что люди могут ассоциировать отношения с высокофункциональными людьми в состоянии минимального сознания с людьми в устойчивом вегетативном состоянии, тем самым сводя к минимуму ценность их жизни.[17]
Регулирующий терапевтический нигилизм
В настоящее время, предотвращение риска доминирует в этическом ландшафте, когда в исследованиях участвуют люди с ограниченными способностями принимать решения.[16] Опасения терапевтического авантюризма привели к непропорционально высокому мнению о недооценке потенциальных преимуществ и переоценке рисков.[требуется разъяснение ]. Таким образом, признание этого искажения важно для расчета правильного баланса между защитой уязвимых групп населения, которые не могут предоставить автономное согласие, и потенциально восстановительными клиническими испытаниями.[16]
Рекомендации
- ^ а б c d Джачино Дж. Т., Эшвал С., Чайлдс Н., Крэнфорд Р., Дженнет Б., Кац Д. И. и др. (Февраль 2002 г.). «Состояние минимального сознания: определение и диагностические критерии». Неврология. 58 (3): 349–53. Дои:10.1212 / wnl.58.3.349. PMID 11839831.
- ^ Штраус, диджей; Ashal S; Day SM; и другие. (2000). «Продолжительность жизни детей в вегетативном и минимально сознательном состояниях». Детская неврология. 23 (4): 1–8. CiteSeerX 10.1.1.511.2986. Дои:10.1016 / S0887-8994 (00) 00194-6. PMID 11068163.
- ^ Schiff, ND; Родригес-Морено Д; Камаль А; Ким К; Джачино JT; Слива F; и другие. (2005). «ФМРТ выявляет крупномасштабную активацию сети у пациентов с минимальным сознанием». Неврология. 64 (3): 514–523. Дои:10.1212 / 01.WNL.0000150883.10285.44. PMID 15699384.
- ^ а б c d Лаурис С., Оуэн А.М., Шифф Н.Д. (2004). «Работа мозга при коме, вегетативном состоянии и родственных расстройствах» (PDF). Ланцетная неврология. 3 (9): 537–546. Дои:10.1016 / S1474-4422 (04) 00852-X. PMID 15324722.
- ^ Voss, H.U .; Uluç, A. M .; Dyke, J. P .; Watts, R .; Kobylarz, E.J .; McCandliss, B.D .; Heier, L.A .; Битти, Б. Дж .; Hamacher, K. A .; Vallabhajosula, S .; Goldsmith, S.J .; Ballon, D .; Giacino, J. T .; Шифф, Н. Д. (2006). «Возможный рост аксонов при позднем выходе из состояния минимального сознания». Журнал клинических исследований. 116 (7): 2005–2011. Дои:10.1172 / JCI27021. ЧВК 1483160. PMID 16823492.
- ^ Boly, M. L .; Faymonville, M.E .; Schnakers, C .; Peigneux, P .; Lambermont, B .; Phillips, C .; Lancellotti, P .; Luxen, A .; Lamy, M .; Moonen, G .; Maquet, P .; Лаурис, С. (2008). «Восприятие боли в состоянии минимального сознания при активации ПЭТ: обсервационное исследование». Ланцетная неврология. 7 (11): 1013–1020. Дои:10.1016 / S1474-4422 (08) 70219-9. PMID 18835749.
- ^ Schiff, ND; Слива F; Резай А.Р. (2002). «Разработка протезов для лечения когнитивных нарушений в результате приобретенных травм головного мозга». Neurol Res. 24 (2): 166–24. Дои:10.1179/016164102101199576. PMID 11877893.
- ^ Коулман, MR; и другие. (2007). «Сохраняют ли вегетативные пациенты аспекты языка? Данные фМРТ». Мозг. 130 (Pt 10): 2494–2507. Дои:10.1093 / мозг / awm170. PMID 17827174.
- ^ а б Джачино, JT; Кальмар К. (1997). «Вегетативное и минимально сознательное состояния: сравнение клинических характеристик и функционального результата». J Head Trauma Rehabil. 12 (4): 36–51. Дои:10.1097/00001199-199708000-00005.
- ^ НАЦИОНАЛЬНЫЕ ИНСТИТУТЫ ЗДРАВООХРАНЕНИЯ США. "Clinicaltrials.gov".
- ^ Лаурис С., Оуэн А.М., Шифф Н.Д. (август 2007 г.). «Поведенческие улучшения с таламической стимуляцией после тяжелой черепно-мозговой травмы». Природа. 448 (7153): 600–603. Дои:10.1038 / природа06041. PMID 17671503.
- ^ Shames, J. L .; Ринг, Х. (2008). «Временное изменение состояния минимального сознания, связанного с аноксической травмой головного мозга, после введения золпидема: отчет о болезни». Архивы физической медицины и реабилитации. 89 (2): 386–388. Дои:10.1016 / j.apmr.2007.08.137. PMID 18226667.
- ^ Ангелакис Э., Лиута Э., Андредис Н., Корфиас С., Ктонас П., Страньялис Г., Сакас Д.Э. (2014). «Эффекты транскраниальной стимуляции постоянным током (tDCS) при расстройствах сознания». Arch Phys Med Rehabil. 95 (2): 283–9. Дои:10.1016 / j.apmr.2013.09.002. PMID 24035769.
- ^ Тибо А., Бруно М.А., Леду Д., Демерци А., Лаурейс С. (2014). «tDCS у пациентов с нарушениями сознания: фиктивное рандомизированное двойное слепое исследование». Неврология. 82 (13): 1112–8. Дои:10.1212 / wnl.0000000000000260. PMID 24574549.
- ^ Джачино Дж. Т., Уайт Дж. (2005). «Вегетативные и минимально сознательные состояния». J Head Trauma Rehabil. 20 (1): 30–50. Дои:10.1097/00001199-200501000-00005. PMID 15668569.
- ^ а б c Fins JJ (апрель 2003 г.). «Построение этической стереотаксии тяжелой черепно-мозговой травмы: баланс между рисками, преимуществами и доступом». Обзоры природы Неврология. 4 (4): 323–327. Дои:10.1038 / nrn1079. PMID 12671648.
- ^ Коулман, Д. (2002). «Минимально сознательное состояние: определение и диагностические критерии». Неврология. 58 (3): 506–507. Дои:10.1212 / wnl.58.3.506.
внешняя ссылка
| Классификация |
|---|
