Эми Розенцвейг - Amy Rosenzweig
Профессор Эми Розенцвейг | |
|---|---|
| Родившийся | Питтсбург, Пенсильвания |
| Национальность | Американец |
| Образование | Б.А. Химия, Амхерстский колледж, 1988; доктор философии. Химия, Массачусетский технологический институт, 1994 г. |
| Награды | Стипендия Макартура |
| Научная карьера | |
| Поля | Биохимия и химия |
Эми К. Розенцвейг профессор химии и молекулярных биологических наук в Северо-Западный университет.[1] Она родилась в 1967 году в Питтсбурге, штат Пенсильвания. Она получила степень бакалавра в химия из Амхерст Колледж в 1988 г. и ее докторская степень. из Массачусетский Институт Технологий в 1994 году. В Массачусетском технологическом институте Розенцвейг работал под руководством Стивен Дж. Липпард где она была пионером в структурных исследованиях гидроксилаза компонент метанмонооксигеназа из метилоккозная капсула. В настоящее время ее исследовательские интересы включают: структурная биология и биоинорганическая химия, поглощение и транспорт металлов, активация кислорода металлоферменты, и характеристика мембранный белок. За свою работу она была отмечена рядом национальных и международных наград, в том числе Премия Макартура "Гений" в 2003 г.
Биологическое окисление метана
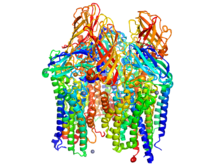
Розенцвейг определил молекулярные структуры основного метана Природы. окисление катализаторы. Монооксигеназы метана (MMO ) являются металлоферментами, входящими в семейство метанотрофные бактерии. Эти ферменты относятся к оксидоредуктаза учебный класс. Они активируют углеродно-водородные связи, чтобы селективно переносить кислород на субстрат. Существуют два основных вида MMO - растворимые MMO (sMMO) и твердые частицы MMO (пММО). Несмотря на то, что они опосредуют одну и ту же химическую реакцию, структура и механизм этих двух ферментов существенно различаются.
С начала 1990-х годов Розенцвейг изучал ферменты MMO в различных биологических системах. Ее команда первой решила Кристальная структура твердых частиц MMO в 1993 году. В последующие годы она добилась значительных успехов в определении ферментов биологическая активность и химическое строение, в том числе огромный вклад в исследования в области координации металлов активный сайт.[2][3]
Предлагаемый в настоящее время механизм для sMMO включает Утюг (II) координационный комплекс который дважды окисляется с образованием металлопероксид разновидность. Затем этот вид подвергается восстановлению в присутствии субстрата. метан чтобы получить окисленный алкил метанол. Определена кристаллическая структура белкового комплекса sMMO.[3][4]

В настоящее время остается загадкой прямое понимание взаимодействия pMMO-субстрат, особенно при диагностике сложного механизма. По словам Розенцвейга, эта неуловимая проблема остается «одной из основных нерешенных проблем в биоинорганической химии».[1]
Металлический транспорт
В своей работе с pMMOs Розенцвейг выяснила молекулярные основы безопасного обращения с потенциально опасными веществами. токсичный ионы металлов посредством прямой передачи между белковыми партнерами. Метанотрофы выделяют метанобактин. Метанобактин хелатный с высокой близостью к медь, и образует комплекс (CuMbn), который может быть повторно интернализован клеткой посредством активного транспорта. Между CuMbn и белками MbnT и MbnE существуют специфические взаимодействия. Эти находки раскрывают механизмы распознавания и транспорта CuMbn.[2]
Металлопротеиновая функция
Розенцвейг определил структуры важных металлопротеинов, оказывающих устойчивое влияние на область биоинорганической химии. Конкретные белки, структуру которых она определила, - это E. coli Mn (II) 2-NrdF и Fe (II) 2-NrdF, которые имеют разные координационные сайты. Это предполагает наличие различных начальных участков связывания оксидантов во время активации кофактора с помощью E. coli и нуклеотидов.[5]
Награды
- Избранный член, Национальная Академия Наук, 2017[6]
- Избранный сотрудник, Американская академия искусств и наук, 2014[7]
- Королевское химическое общество Премия Джозефа Чатта, 2014 г.[8]
- Премия Ивано Бертини, 2014 г.[9]
- Американское химическое общество Подпись лауреата Нобелевской премии в области последипломного образования, 2006 г.[10]
- Почетная степень, доктор наук, Амхерст Колледж, 2005[11]
- Сотрудник Макартура, 2003 г.[1]
Работает
- Либерман, Р. Л. и Розенцвейг, А. С. "Кристаллическая структура мембраносвязанного металлофермента, который катализирует биологическое окисление метана", Природа 2005, 434, 177-182.
- Либерман, Р.Л., Кондапалли, К.К., Шреста, Д.Б., Хакемиан, А.С., Смит, С.М., Телсер, Дж., Кузелка, Дж., Гупта, Р., Боровик, А.С., Липпард, С.Дж., Хоффман, Б.М., Розенцвейг, А.К. , & Стеммлер, Т.Л. "Характеристика металлических центров метанмонооксигеназы в виде частиц в нескольких окислительно-восстановительных состояниях с помощью спектроскопии поглощения рентгеновских лучей". Неорг. Chem. 2006, 45, 8372-8381.
- Сазинский, М. Х., Мандал, А. Л., Аргуэлло, Дж. М., и Розенцвейг, А. С. «Структура АТФ-связывающего домена из Cu1 + -АТФазы Archaeglobus fulgidus». J. Biol. Chem.. 2006, 281, 11161-11166.
- Яцуник, Л. А. и Розенцвейг, А. С. "Связывание и перенос меди N-концом белка болезни Вильсона", J. Biol. Chem.. 2007, 282, 8622-8631.
- Розенцвейг, Липпард, "Структура и биохимия ферментных систем метанмонооксигеназы", Переходные металлы в микробном метаболизме, Редакторы Гюнтер Винкельманн, Карл Дж. Каррано, CRC Press, 1997, ISBN 978-90-5702-220-3
- Розенцвейг, Фен, Липпард, «Исследования модельных комплексов метанмонооксигеназы и окисления алканов», Применение ферментной биотехнологии, Редакторы Джеффри В. Келли, Томас О. Болдуин, Springer, 1991, ISBN 978-0-306-44095-3
Рекомендации
- ^ а б c "Добро пожаловать в Rosenzweig Group!". groups.molbiosci.northwestern.edu. Получено 2017-06-08.
- ^ а б Сираджуддин, Сара; Розенцвейг, Эми К. (14 апреля 2015 г.). «Ферментативное окисление метана». Биохимия. 54 (14): 2283–2294. Дои:10.1021 / acs.biochem.5b00198. ISSN 0006-2960. ЧВК 5257249. PMID 25806595.
- ^ а б Розенцвейг, Эми С.; Фредерик, Кристин А .; Липпард, Стивен Дж .; П & Аумл; Нордлунд, Р. (1993-12-09). «Кристаллическая структура бактериальной негемовой гидроксилазы железа, которая катализирует биологическое окисление метана». Природа. 366 (6455): 537–543. Bibcode:1993Натура.366..537R. Дои:10.1038 / 366537a0. PMID 8255292. S2CID 4237249.
- ^ Лотон, Томас Дж; Розенцвейг, Эми К. (2016-12-01). «Биокатализаторы конверсии метана: большой прогресс в разрушении небольшого субстрата». Современное мнение в области химической биологии. Энергетическая механистическая биология. 35: 142–149. Дои:10.1016 / j.cbpa.2016.10.001. ЧВК 5161620. PMID 27768948.
- ^ Boal, Amie K .; Котруво, Джозеф А .; Стуббе, Джоанна; Розенцвейг, Эми К. (17 сентября 2010 г.). «Структурная основа активации рибонуклеотидредуктазы Ib класса». Наука. 329 (5998): 1526–1530. Bibcode:2010Sci ... 329.1526B. Дои:10.1126 / science.1190187. ISSN 0036-8075. ЧВК 3020666. PMID 20688982.
- ^ "Эми Розенцвейг". Национальная Академия Наук. Получено 2018-03-22.
- ^ «Индекс активных участников» (PDF).
- ^ «Победитель премии Джозефа Чатта 2014 года». www.rsc.org. Получено 2018-04-05.
- ^ "Резюме Эми К. Розенцвейг" (PDF). Октябрь 2017 г.
- ^ "Подпись лауреата Нобелевской премии за высшее образование в области химии - Американское химическое общество". Американское химическое общество. Получено 2018-03-22.
- ^ "Почетные ученые степени и награды | Имя получателя | Колледж Амхерста". www.amherst.edu. Получено 2018-03-23.
внешняя ссылка
- "Эми Розенцвейг", Факультет 1000
