Арогенатдегидратаза - Arogenate dehydratase
| Арогенатдегидратаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Кристаллическая структура предшественника циклогексадиенилдегидратазы из Pseudomonas aeruginosa PA01. Вторичная структура отображается на изображении, а остатки, важные для катализа, были выделены. | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.2.1.91 | ||||||||
| Количество CAS | 76600-70-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
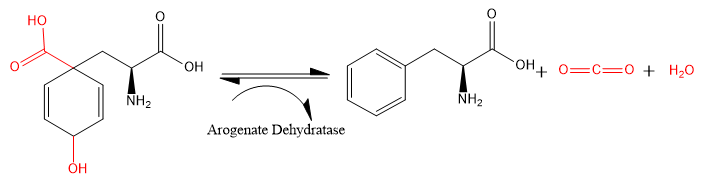
Арогенатдегидратаза (ADT) (EC 4.2.1.91) - фермент, катализирующий химическую реакцию
- L-арогенат → L-фенилаланин + H2O + CO2
Следовательно, у этого фермента есть один субстрат, L-арогенат, но 3 продукта:L-фенилаланин, H2O и CO2. Некоторые формы белка могут катализировать вторую реакцию,[1]
L-префенат → L-фенилпируват + H2O + CO2
Этот фермент участвует в фенилаланин, тирозин, и триптофан биосинтез (пример структуры показан справа.[2]
Номенклатура
Этот фермент принадлежит к семейству лиасы в частности гидролазы, которые разрывают углерод-кислородные связи. В систематическое название этого класса ферментов L-арогенат гидролаза (декарбоксилирование; образование L-фенилаланина). Другие широко используемые имена включают:
- арогенатдегидратаза
- L-арогенат гидролаза (декарбоксилирование)
- циклогексадиенилдегидратаза
- карбоциклогексадиенилдегидратаза
- pheC
- ADT
Реакция
В карбоксил и гидроксид группы (показаны красным), присоединенные к 2,5-циклогексеновому кольцу, удаляются из L-арогената, оставляя как углекислый газ и воды. 2,5-циклогексеновое кольцо превращается в фенильное кольцо, и образуется L-фенилаланин.
Было показано, что определенные формы ADT демонстрируют некоторые префенатдегидратаза (PDT) в дополнение к стандартной активности ADT, описанной выше.[1] Известные как циклогексадиенилдегидратазы или карбоциклогексадиенилдегидратазы (перечисленные выше),[1] эти формы фермента катализируют реакции одного типа ( декарбоксилирование и обезвоживание ) на префенат. Карбоксильные и гидроксидные группы (отмечены красным), присоединенные к 2,5-циклогексеновому кольцу, удаляются, оставляя фенилпируват.

Функция
ADT катализирует реакцию, классифицируемую по двум основным изменениям в структуре субстрат, это декарбоксилирование и обезвоживание; фермент удаляет карбоксильная группа и молекула воды (соответственно).[1] Оба потенциальных продукта этой реакции (L-арогенат и фенилпируват) возникают в конце или почти в конце пути биосинтеза. Сообщается о полном синтезе L-арогената.[3][4]
Структура
Структура арогенатдегидратаз описывается как имеющая по большей части три основных раздела. ADT содержат N-концевой транзитный пептид, а Тихоокеанское летнее время -подобный домен и ДЕЙСТВОВАТЬ (Аспартокиназа, cхоризмат мутаза, ТyrA) домен.[5]
Гомологи
Гомологи для ADT были изолированы в Arabidopsis thaliana (кресс-салат из кроличьих ушей),[5] Nicotiana sylvestris (табак),[6] Spinacia oleracea (шпинат),[6] Петуния гибридная,[7] Сорго двухцветное,[8] и Oryza sativa,[9] которые все считаются растениями более высокого порядка. Эрвиния гербикола[10] и Синегнойная палочка[11] известны гомологи циклогексадиенилдегидратазы. Из растений с гомологами ADT оба Arabidopsis thaliana и Петуния гибридная известны паралоги гена (шесть и три соответственно).[5][7]
Рекомендации
- ^ а б c d Фишер, Р. Дженсен, Р. (1987). Арогенатдегидратаза. Методы Энзимол. Методы в энзимологии. 142. С. 495–502. Дои:10.1016 / S0076-6879 (87) 42061-2. ISBN 9780121820428. PMID 3600377.
- ^ Бак.; Marshall, N .; Бак, К .; Иоахимиак, А. (2009). «Кристаллическая структура предшественника циклогексадиенилдегидратазы из Pseudomonas aeruginosa PA01». Дои:10.2210 / pdb3kbr / pdb. Цитировать журнал требует
| журнал =(помощь) - ^ Кроссли, Максвелл Дж .; Рид, Роберт С. (1994). «Краткий синтез арогената. Биосинтетический предшественник фенилаланина и тирозина». Журнал химического общества, химические коммуникации. 0 (19): 2237–2238. Дои:10.1039 / c39940002237.
- ^ Данишефский, Самуэль; Моррис, Джоэл; Клизбе, Лейн А. (01.05.2002). «Полный синтез претирозина (арогената)». Журнал Американского химического общества. 103 (6): 1602–1604. Дои:10.1021 / ja00396a070.
- ^ а б c Чо, Ман-Хо; Кориа, Оливер Р. А .; Ян, Хун; Бедгар, Диана Л .; Laskar, Dhrubojyoti D .; Anterola, Aldwin M .; и другие. (2007). «Биосинтез фенилаланина в Arabidopsis thaliana- идентификация и характеристика арогенатдегидратаз ». J. Biol. Chem. 282 (42): 30827–35. Дои:10.1074 / jbc.m702662200. PMID 17726025.
- ^ а б Юнг Э, Замир Л.О., Дженсен Р.А. (1986). «Хлоропласты высших растений синтезируют L-фенилаланин через L-арогенат». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 83 (19): 7231–5. Дои:10.1073 / пнас.83.19.7231. ЧВК 386689. PMID 3463961.
- ^ а б Maeda, H .; Шасаны, А. К .; Schnepp, J .; Орлова, И .; Taguchi, G .; Купер, Б. Р .; и другие. (2010). "РНКи подавление Арогенат дегидратаза 1 показывает, что фенилаланин синтезируется преимущественно через арогенатный путь в лепестках петунии ». Растительная клетка. 22 (3): 832–849. Дои:10.1105 / tpc.109.073247. ЧВК 2861463. PMID 20215586.
- ^ Siehl, DL; Conn, EE (1988). «Кинетические и регуляторные свойства арогенатдегидратазы в проростках Sorghum bicolor (L.) Moench». Arch. Biochem. Биофизы. 260 (2): 822–9. Дои:10.1016/0003-9861(88)90513-9. PMID 3124763.
- ^ Yamada, T .; Matsuda, F .; Kasai, K .; Fukuoka, S .; Kitamura, K .; Tozawa, Y .; и другие. (2008). «Мутация гена риса, кодирующего фермент биосинтеза фенилаланина, приводит к накоплению фенилаланина и триптофана». Растительная клетка. 20 (5): 1316–1329. Дои:10.1105 / tpc.107.057455. ЧВК 2438470. PMID 18487352.
- ^ Ся, Т; Ахмад, S; Чжао, G; Дженсен, Р.А. (1991). «Одна циклогексадиенилдегидратаза определяет компоненты префенатдегидратазы и арогенатдегидратазы двух независимых путей к L-фенилаланину у Erwinia herbicola». Arch. Biochem. Биофизы. 286 (2): 461–465. Дои:10.1016 / 0003-9861 (91) 90066-р. PMID 1897969.
- ^ Чжао, G; Ся, Т; Фишер, RS; Дженсен, Р.А. (1992). «Циклогексадиенилдегидратаза из Pseudomonas aeruginosa. Молекулярное клонирование гена и характеристика продукта гена». J. Biol. Chem. 267 (4): 2487–2493. PMID 1733946.
