Катехол 1,2-диоксигеназа - Catechol 1,2-dioxygenase
| Катехол 1,2-диоксигеназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 1.13.11.1 | ||||||||
| Количество CAS | 9027-16-1 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Катехол 1,2-диоксигеназа (EC 1.13.11.1, 1,2-CTD, катехол-кислород 1,2-оксидоредуктаза, 1,2-пирокатегаз, катехиза, катехол 1,2-оксигеназа, катехолдиоксигеназа, пирокатегаз, пирокатехол 1,2-диоксигеназа, CD I, CD II)[1][2][3][4] является фермент который катализирует окислительное расщепление кольца катехол формировать СНГ, СНГ-муконовая кислота:[5]

В частности, 1,2-CTD представляет собой интрадиол-диоксигеназа, семейство катехолдиоксигеназ, которые расщепляют связь между фенольными гидроксильными группами катехола с помощью Fe3+ кофактор.
К настоящему времени 1,2-CTD обнаружен в следующих видах почвенных бактерий и грибов: Pseudomonas sp.,[6] Pseudomonas fluorescens,[7] Aspergillus niger,[8] Brevibacterium fuscum,[9][10] Acinetobacter calcoaceticus,[11] Trichosporon cutaneum,[12] Родококк красный,[13] Frateuria sp.,[14] Rhizobium trifolii,[15] Pseudomonas putida,[16] Candida tropicalis,[17] Кандида мальтоза,[18] Rhizobium leguminosarum,[19] и Nocardia sp..[20] Эти бактерии впоследствии используют 1,2-CTD на последней стадии разложения ароматических соединений до алифатических продуктов.[21]
История
Осаму Хаяиши и Кизо Хашимото в 1950 году открыли два семейства диоксигеназ: катехол-1,2-диоксигеназы и катехол-2,3-диоксигеназа (2,3-CTD).[22] Эти два фермента были идентифицированы как часть двух отдельных семейств катехолдиоксигеназ: 1,2-CTD был классифицирован как интрадиолдиоксигеназа, а 2,3-CTD был классифицирован как экстрадиолдиоксигеназа. Эти два фермента можно различить по продуктам их реакции и кофакторам. 1,2-CTD использует Fe3+ в качестве кофактора для разрыва углерод-углеродной связи между фенольными гидроксильными группами катехола, в результате чего получается муконовая кислота в качестве его продукта. Напротив, 2,3-CTD использует Fe2+ в качестве кофактора для расщепления углерод-углеродной связи, соседней с фенольными гидроксильными группами катехола, с получением 2-гидроксимукональдегида в качестве его продукта.[23]
Структура фермента
Почти все представители семейства 1,2-CTD являются гомодимеры; фермент 1,2-CTD, продуцируемый Pseudomonas arvilla является исключением из этого правила, он содержит две высокогомологичные субъединицы, которые могут образовывать либо гомо-, либо гетеродимер.[24]Фермент по форме напоминает бумеранг, и поэтому его можно четко разделить на три домена: два каталитических домена на каждом конце «бумеранга» и линкерный домен в центре.
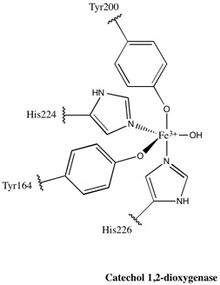
Каждый каталитический домен состоит из двух составных частей смешанной топологии. β листы и несколько случайные катушки. Эти листы и спирали впоследствии охватывают активный центр: негемовый комплекс железа (III). Без гема железо должно быть перевязанный до четырех аминокислотных остатков (Tyr200, His226, Tyr164, His224) для поддержания каталитически активной конформации. Когда Tyr200 и His226 действуют как аксиальные лиганды, а Tyr164, His224 и молекула воды-растворителя действуют как экваториальные лиганды, Fe3+ сложные дисплеи тригонально-бипирамидный геометрия. Поскольку активные центры каждого каталитического домена разделены расстоянием 40 Å, считается, что они не оказывают аллостерического влияния друг на друга.
Напротив, линкерный домен состоит из α спирали обеспечивается двумя каталитическими доменами: каждый домен вносит пять спиралей от своих N-концов и одну спираль, которая охватывает как каталитический домен, так и линкерный домен. В центре линкерного домена находится гидрофобный туннель 8 на 35 Å с двумя фосфолипидами, связанными на каждом конце. Головка каждого фосфолипида направлена наружу в сторону раствора, в то время как хвосты заключены в фермент. Функция этого гидрофобного туннеля неизвестна, хотя были высказаны две гипотезы относительно его полезности. Во-первых, связывание концевых фосфолипидов изменяет конформацию активных центров, подразумевая, что туннель действует как эффектор, позволяя ферменту быть активным только в определенных областях клетки. Вторая гипотеза постулирует, что туннель регулирует жесткость липидной мембраны за счет деградации фенольных углеводородов и способности связываться с другими липидами. Исследования показали, что фенольные углеводороды влияют на функциональные и структурные свойства клеточных мембран.[25] 1,2-CTD разлагает фенольные углеводороды, необходимые для синтеза липидных мембран. Следовательно, 1,2-CTD может связываться с липидной мембраной клетки через свои терминальные фосфолипиды и, таким образом, иметь больший доступ к фенольным углеводородам, важным для структуры липидной мембраны.[26]
Ферментный механизм

Каталитический механизм катехол-1,2-диоксигеназы был выяснен с использованием комбинации O18 маркировка экспериментов и кристаллография.[27][28][29] При входе в активный центр гидроксильная группа на четвертом атоме углерода (C4) катехола связывается с Fe3+; это связывание облегчается гидроксидным лигандом, который депротонирует гидроксильную группу C4. Вторая гидроксильная группа катехина на углероде 3 (C3) координирована с Fe3+ после его депротонирования лигандом Tyr200. В процессе депротонирования гидроксильной группы C3 Tyr200 диссоциирует от каталитического комплекса.
Кислород связывается с субстратом через серию транс влияет и стабилизация водородной связи между субстратом и другими аминокислотными остатками активного сайта. His226 принимает электронную плотность от подложки, следовательно, уменьшая связь между Fe3+ и C4-гидроксил. В то же время связь между гидроксилом С3 и Fe3+ увеличивается из-за электроноакцепторных эффектов Tyr164. Эти искажения в сочетании с водородной связью между Arg221 и гидроксилом C3 индуцируют кетонизацию гидроксильной группы C3 и усиливают карбанионный характер C4. Вновь образованный карбанион C4 атакует O2, связывая его с субстратом.
Другой транс влияние следует за вышеупомянутым этапом, что приводит к расщеплению O2 и последующее введение одной из молекул кислорода между C3 и C4. За этой реакцией следует быстрый гидролиз с образованием праймированного активного центра и продукта.
Рекомендации
- ^ Hayaishi O, Lardy H, Myrbäck K (1963). «Прямая оксигенация O2, оксигеназы ». В Boyer PD (ed.). Ферменты. 8 (2-е изд.). Нью-Йорк: Academic Press. С. 353–371.
- ^ Хаяиси О., Катагири М., Ротберг С. (декабрь 1957 г.). "Исследования по оксигеназам; пирокатехазе". Журнал биологической химии. 229 (2): 905–20. PMID 13502352.
- ^ Sistrom WR, Stanier RY (октябрь 1954 г.). «Механизм образования бета-кетоадипиновой кислоты бактериями». Журнал биологической химии. 210 (2): 821–36. PMID 13211620.
- ^ Зейер Дж., Кочер HP, Тиммис К.Н. (август 1986 г.). «Влияние пара-заместителей на окислительный метаболизм о-нитрофенолов Pseudomonas putida B2». Прикладная и экологическая микробиология. 52 (2): 334–9. Дои:10.1128 / AEM.52.2.334-339.1986. ЧВК 203526. PMID 3752997.
- ^ Шомбург Д., Шомбург I (2006). «Катехол 1,2-диоксигеназа». Оксидоредуктазы класса I X. Справочник по ферментам Springer. 25 (2-е изд.). Springer Berlin Heidelberg. С. 382–394. Дои:10.1007/3-540-37704-2_47. ISBN 978-3-540-37704-7.
- ^ Дорн Э., Knackmuss HJ (июль 1978 г.). «Химическая структура и способность к биоразложению галогенированных ароматических соединений. Две катехол-1,2-диоксигеназы из псевдомонады, выращенной на 3-хлорбензоате». Биохимический журнал. 174 (1): 73–84. Дои:10.1042 / bj1740073. ЧВК 1185887. PMID 697765.
- ^ Хаяиси С., Катагири М., Ротберг С. (1957). "Пионерская работа в области оксигеназ посредством изучения метаболизма триптофана: работа Осаму Хаяиши" (PDF). J. Biol. Chem. 229: 905–920.
- ^ Ниннекар Х., Вайдьянатан С. (1981). «Катехол 1,2-диоксигеназа из Aspergillus niger: Очищение и свойства ». J. Indian Inst. Наука. 63C: 131–136.
- ^ Накадзава Х, Иноуэ Х, Такеда Й (1963). «Характеристики катехолоксигеназы из Brevibacterium fuscum". J. Biochem. 54 (1): 65–74. Дои:10.1093 / oxfordjournals.jbchem.a127748. PMID 14056355.
- ^ Hou CT, Patel R, Lillard MO (март 1977 г.). «Экстрадиольное расщепление 3-метилкатехола катехол-1,2-диоксигеназой различных микроорганизмов». Прикладная и экологическая микробиология. 33 (3): 725–7. Дои:10.1128 / AEM.33.3.725-727.1977. ЧВК 170750. PMID 16345232.
- ^ Patel RN, Hou CT, Felix A, Lillard MO (июль 1976 г.). «Катехол 1,2-диоксигеназа из Acinetobacter calcoaceticus: очистка и свойства». Журнал бактериологии. 127 (1): 536–44. Дои:10.1128 / JB.127.1.536-544.1976. ЧВК 233087. PMID 58860.
- ^ Ито, М. (1981). «Характеристики новой катехол-1,2-оксигеназы из Trichosporon cutaneum WY2-2 ". Agric. Биол. Chem. 45 (1): 2787–2796.
- ^ Аоки К., Конохана Т., Шинке Р., Нишира Х. (1984). «Классификация семейства катехол-1,2-диоксигеназ: анализ последовательности гена катехол 1,2-диоксигеназы, демонстрирующий высокую специфичность к метилкатехинам из Gram +, ассимилирующих анилин. Родококк красный Ан-13 ». Agric. Биол. Chem. 48 (1): 2087–2095. Дои:10.1016 / S0378-1119 (96) 00629-4. PMID 9034312.
- ^ Аоки К., Конохана Т., Шинке Р., Нишира Х. (1984). «Две катехол-1,2-диоксигеназы из ассимилирующей анилин бактерии, Frateuria вид АНА-18 ". Agric. Биол. Chem. 48 (1): 2097–2104.
- ^ Чен Ю., Гленн А., Дилворт М. (1985). «Ароматический обмен в Rhizobium trifolii-катехол 1,2-диоксигеназа ». Arch. Микробиол. 141 (1): 225–228. Дои:10.1007 / BF00408063.
- ^ Паскаль Р.А., Хуанг Д.С. (июль 1986 г.). «Реакции 3-этилкатехола и 3- (метилтио) катехола с катехолдиоксигеназами». Архивы биохимии и биофизики. 248 (1): 130–7. Дои:10.1016/0003-9861(86)90409-1. PMID 3015028.
- ^ Круг М, Штраубе Г (1986). «Разложение фенольных соединений дрожжами Candida tropicalis HP 15. II. Некоторые свойства первых двух ферментов пути разложения». Журнал базовой микробиологии. 26 (5): 271–81. Дои:10.1002 / jobm.3620260505. PMID 3783431.
- ^ Гоми К., Хоригучи (1988). "Очистка и характеристика пирокатехазы из ассимилирующих катехол дрожжей Кандида мальтоза". Agric. Биол. Chem. 52 (2): 585–587. Дои:10.1271 / bbb1961.52.585.
- ^ Чен Ю.П., Ловелл CR (июнь 1990 г.). «Очистка и свойства катехол 1,2-диоксигеназы из Rhizobium leguminosarum biovar Viceae USDA 2370». Прикладная и экологическая микробиология. 56 (6): 1971–3. Дои:10.1128 / AEM.56.6.1971-1973.1990. ЧВК 184541. PMID 16348234.
- ^ Смит М., Рэтледж С., Крук С. (1990). "Свойства цианогенбромид-активированной, иммобилизованной на агарозе катехол 1,2-диоксигеназы из лиофилизированных экстрактов Nocardia sp. NCIB 10503 ". Enzyme Microb. Technol. 12 (12): 945–949. Дои:10.1016/0141-0229(90)90114-6.
- ^ Que L, Ho RY (ноябрь 1996 г.). «Активация кислорода ферментами с мононуклеарными негемовыми железными активными сайтами». Химические обзоры. 96 (7): 2607–2624. Дои:10.1021 / cr960039f. PMID 11848838.
- ^ Хаяиси О, Хашимото К. (1950). «Пирокатеказа - новый фермент, катализирующий окислительное разложение пирокатехина» (PDF). J. Biochem. 37 (3): 371–374. Дои:10.1093 / oxfordjournals.jbchem.a126205.
- ^ Багг, Тимоти (2003). «Ферменты диоксигеназы: каталитические механизмы и химические модели». Тетраэдр. 59 (36): 7075–7101. Дои:10.1016 / S0040-4020 (03) 00944-X.
- ^ Накаи К., Кагамияма Х, Саеки Й, Нодзаки М. (июнь 1979 г.). «Неидентичные субъединицы пирокатехазы из Pseudomonas arvilla C-1». Архивы биохимии и биофизики. 195 (1): 12–22. Дои:10.1016/0003-9861(79)90322-9. HDL:2433/222081. PMID 475379.
- ^ Сиккема Дж., Де Бонт Дж. А., Пулмен Б. (март 1994 г.). «Взаимодействие циклических углеводородов с биологическими мембранами» (PDF). Журнал биологической химии. 269 (11): 8022–8. PMID 8132524.[постоянная мертвая ссылка ]
- ^ Vetting MW, Ohlendorf DH (апрель 2000 г.). «Кристаллическая структура 1,8 А катехол 1,2-диоксигеназы раскрывает новую гидрофобную спиральную застежку-молнию в качестве линкера субъединицы». Структура. 8 (4): 429–40. Дои:10.1016 / S0969-2126 (00) 00122-2. PMID 10801478.
- ^ Хаяиси О, Хашимото К. (1950). «Пирокатеказа - новый фермент, катализирующий окислительное разложение пирокатехина» (PDF). J. Biochem. 37 (3): 371–374. Дои:10.1093 / oxfordjournals.jbchem.a126205.
- ^ Орвилл А.М., Липскомб Д.Д., Олендорф Д.Х. (август 1997 г.). «Кристаллические структуры субстрата и комплексов аналогов субстрата протокатехуат-3,4-диоксигеназы: эндогенное смещение лиганда Fe3 + в ответ на связывание субстрата». Биохимия. 36 (33): 10052–66. Дои:10.1021 / bi970469f. PMID 9254600.
- ^ Липскомб Дж., Орвилл А. (1992). Ионы металлов в биологических системах. 28. Марсель Деккер, Инк., Стр. 243–298.
внешняя ссылка
- Катехол + 1,2-диоксигеназа в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
