Деферасирокс - Deferasirox
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | de FER a sir ox |
| Торговые наименования | Exjade, Jadenu |
| Другие имена | CGP-72670, ICL-670A, IC L670 |
| AHFS /Drugs.com | Монография |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 70% |
| Связывание с белками | 99% |
| Метаболизм | Печеночный глюкуронизация |
| Устранение период полураспада | От 8 до 16 часов |
| Экскреция | Фекальный (84%) и почечный (8%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.211.077 |
| Химические и физические данные | |
| Формула | C21ЧАС15N3О4 |
| Молярная масса | 373.368 г · моль−1 |
| 3D модель (JSmol ) | |
| Плотность | 1,4 ± 0,1 г / см3 [1] |
| |
| |
| | |
Деферасирокс, продается под торговой маркой Exjade среди прочего, это устный утюг хелатор. Его основное использование - уменьшить хроническая перегрузка железом у пациентов, длительно получающих переливание крови для таких условий, как бета-талассемия и другие хронические анемии.[2][3] Это первое пероральное лекарство, одобренное для этой цели в США.[4]
Он был одобрен США.Управление по контролю за продуктами и лекарствами (FDA) в ноябре 2005 г.[2][4]По данным FDA (май 2007 г.), почечная недостаточность и цитопении Сообщалось о пациентах, получающих пероральные таблетки суспензии деферазирокс. Он одобрен в Европейском Союзе Европейское агентство по лекарствам (EMA) для детей от шести лет и старше при хронической перегрузке железом при повторных переливаниях крови.[5][6][7]
В июле 2020 года Тева решила прекратить прием деферасирокса.[8] Он доступен как универсальный препарат.[9]
Свойства
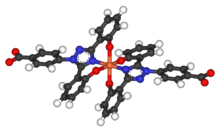
Период полувыведения деферазирокса составляет от 8 до 16 часов, что позволяет принимать его один раз в день. Две молекулы деферасирокса способны связываться с 1 атомом железа, которые впоследствии выводятся с калом. Его низкая молекулярная масса и высокая липофильность позволяют принимать препарат внутрь в отличие от дефероксамин который необходимо вводить внутривенно (внутривенная инфузия). Вместе с деферипрон, деферазирокс, по-видимому, способен удалять железо из клеток (сердечных миоцитов и гепатоцитов), а также удалять железо из крови.
Синтез
Деферасирокс можно получить из простых коммерчески доступных исходных материалов (салициловая кислота, салициламид и 4-гидразинобензойная кислота) в следующей двухстадийной последовательности синтеза:

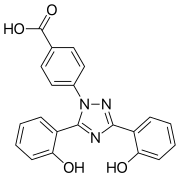
Конденсация салицилоилхлорида (образуется на месте из салициловой кислоты и тионилхлорида) с салициламидом в условиях реакции дегидратации приводит к образованию 2- (2-гидроксифенил) -1,3 (4ЧАС) -бензоксазин-4-он. Этот промежуточный продукт выделяют и подвергают взаимодействию с 4-гидразинобензойной кислотой в присутствии основания с получением 4- (3,5-бис (2-гидроксифенил) -1,2,4-триазол-1-ил) бензойной кислоты (деферазирокс).[10]
Риски
Деферазирокс был лекарством №2 в списке «Наиболее частые подозреваемые лекарства в зарегистрированных случаях смерти пациентов», составленном Институтом безопасной медицинской практики в 2009 году. Сообщалось о 1320 случаях смерти, что, возможно, объясняется обновлением данных ADE Novartis, и новое предупреждение в рамке о желудочно-кишечном кровотечении, а также о почечной и печеночной недостаточности.[11]
использованная литература
- ^ «Паспорт безопасности материала (MSDS): Деферазирокс». ChemSrc. 2018.
- ^ а б Чоудри В.П., Найтани Р. (август 2007 г.). «Текущее состояние перегрузки железом и хелатирования деферасирокса». Индийский журнал педиатрии. 74 (8): 759–64. Дои:10.1007 / s12098-007-0134-7. PMID 17785900. S2CID 19930076. Бесплатный полный текст В архиве 2014-04-29 в Wayback Machine
- ^ Ян LP, Ким SJ, Китинг GM (2007). «Деферасирокс: обзор его использования в лечении хронической перегрузки железом при переливании крови». Наркотики. 67 (15): 2211–30. Дои:10.2165/00003495-200767150-00007. PMID 17927285.
- ^ а б «FDA одобрило первое пероральное лекарство от хронической перегрузки железом» (Пресс-релиз). Соединенные Штаты Управление по контролю за продуктами и лекарствами. 9 ноября 2005 г.. Получено 2007-10-31.
- ^ «Эксиджад - деферасирокс» (PDF). Европейское агентство по лекарственным средствам. 2018.
- ^ Kontoghiorghes GJ (апрель 2013 г.). «Закрывать глаза на токсичность деферасирокса?». Ланцет. 381 (9873): 1183–4. Дои:10.1016 / S0140-6736 (13) 60799-0. PMID 23561999. S2CID 27794849.
- ^ «Обзор: побочные эффекты Exjade».
- ^ «Прекращение приема Деферасирокса». НАС. Управление по контролю за продуктами и лекарствами (FDA). Получено 20 июля 2020.
- ^ «Лекарства @ FDA: лекарства, одобренные FDA». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 15 августа 2020.
- ^ Steinhauser S, Heinz U, Bartholomä M, Weyhermüller T, Nick H, Hegetschweiler K (2004). «Комплексное образование ICL670 и родственных лигандов с FeIII и FeII". Европейский журнал неорганической химии. 2004 (21): 4177–4192. Дои:10.1002 / ejic.200400363.]
- ^ ISMP (2010). "ISMP QuarterWatch (TM)". 15 (12). Предупреждение о безопасности лекарств ISMP. С. 1–3.
внешние ссылки
- «Деферасирокс». Портал информации о наркотиках. Национальная медицинская библиотека США.
