Талассемия - Thalassemia
| Талассемия | |
|---|---|
| Другие имена | Талассемия, средиземноморская анемия |
 | |
| Мазок периферической крови человека с дельта-бета-талассемией | |
| Произношение | |
| Специальность | Гематология |
| Симптомы | Чувство усталый, бледная кожа, увеличенная селезенка, желтоватая кожа, темная моча[1] |
| Причины | Генетический (аутосомно-рецессивный )[2] |
| Диагностический метод | Анализы крови, генетические тесты[3] |
| Уход | Переливание крови, хелатирование железа, фолиевая кислота[4] |
| Частота | 280 миллионов (2015)[5] |
| Летальные исходы | 16,800 (2015)[6] |
Талассемии унаследованы заболевания крови характеризуется уменьшением гемоглобин производство.[7] Симптомы зависят от типа и могут варьироваться от отсутствия до тяжелых.[1] Часто бывает от легкой до тяжелой анемия (низкий красные кровяные тельца или гемоглобин).[1] Анемия может вызвать чувство усталый и бледная кожа.[1] Также могут быть проблемы с костями, увеличенная селезенка, желтоватая кожа и темная моча.[1] У детей может наблюдаться медленный рост.[1]
Талассемии бывают генетические нарушения унаследовано от родителей человека.[2] Есть два основных типа: альфа-талассемия и бета-талассемия.[7] Тяжесть альфа- и бета-талассемии зависит от того, сколько из четырех генов альфа-глобин или два гена для бета-глобин не хватает.[2] Диагноз обычно ставится на основании анализа крови, включая полный анализ крови, специальные тесты на гемоглобин, и генетические тесты.[3] Диагноз может быть поставлен до рождения через пренатальное тестирование.[8]
Лечение зависит от типа и степени тяжести.[4] Лечение людей с более тяжелым заболеванием часто включает регулярные переливание крови, хелатирование железа, и фолиевая кислота.[4] Хелатирование железа может быть выполнено с дефероксамин, деферазирокс или же деферипрон.[4][9] Иногда пересадка костного мозга может быть вариант.[4] Осложнения могут включать: железная перегрузка от переливаний с последующим сердце или же болезнь печени, инфекции, и остеопороз.[1] Если селезенка становится чрезмерно увеличенным, хирургическое удаление может потребоваться.[1] Больные талассемией, которые плохо реагируют на переливание крови, могут принимать гидроксимочевину или талидомид, а иногда и их комбинацию.[10] Гидроксимочевина - единственный одобренный FDA препарат для лечения талассемии. Пациенты, которые принимали 10 мг / кг гидроксимочевины каждый день в течение года, имели значительно более высокий уровень гемоглобина, и это было хорошо переносимым лечением для пациентов, которые плохо реагировали на переливание крови.[11] Другой индуктор гемоглобина включает талидомид, хотя он не тестировался в клинических условиях. Комбинация талидомида и гидроксимочевины привела к значительному повышению уровня гемоглобина у пациентов, зависимых от трансфузий и не зависимых от трансфузий [12]
По состоянию на 2015 год талассемия встречается примерно у 280 миллионов человек, из которых около 439000 страдают тяжелыми заболеваниями.[13] Это наиболее распространено среди людей итальянского, греческого, Ближневосточный, Южная Азия, и африканского происхождения.[7] У мужчин и женщин одинаковая частота заболеваний.[14] В 2015 году в результате этого погибло 16 800 человек по сравнению с 36 000 в 1990 году.[6][15] Те, у кого есть незначительная степень талассемии, аналогичная тем, у кого серповидно-клеточная характеристика, есть некоторая защита от малярия, объясняя, почему они более распространены в регионах мира, где существует малярия.[16]
Признаки и симптомы

- Железная перегрузка: Люди с талассемией могут получить избыток железа в организме либо из-за самого заболевания, либо из-за частых переливаний крови. Слишком много железа может привести к повреждению сердца, печени и эндокринная система, в состав которого входят железы, вырабатывающие гормоны, регулирующие процессы во всем организме. Повреждение характеризуется чрезмерным отложением железа. Без адекватной терапии хелатированием железа почти у всех пациентов с бета-талассемией накапливается потенциально смертельный уровень железа.[17]
- Инфекция: люди с талассемией имеют повышенный риск заражения. Это особенно актуально, если была удалена селезенка.[18]
- Деформации костей: талассемия может вызвать расширение костного мозга, что приводит к расширению костей. Это может привести к аномальной структуре костей, особенно на лице и черепе. Расширение костного мозга также делает кости тонкими и ломкими, что увеличивает риск перелома костей.[19]
- Увеличенная селезенка: Селезенка помогает бороться с инфекциями и фильтрует нежелательные вещества, такие как старые или поврежденные клетки крови. Талассемия часто сопровождается разрушением большого количества красных кровяных телец, и задача удаления этих клеток приводит к увеличению селезенки. Спленомегалия может усугубить анемию и сократить срок жизни перелитых эритроцитов. Сильное увеличение селезенки может потребовать ее удаления.[20]
- Замедленные темпы роста: анемия может замедлить рост ребенка. Половое созревание также может задерживаться у детей с талассемией.[21]
- Проблемы с сердцем: такие заболевания, как застойная сердечная недостаточность и нарушение сердечного ритма, могут быть связаны с тяжелой талассемией.[22]
Причина
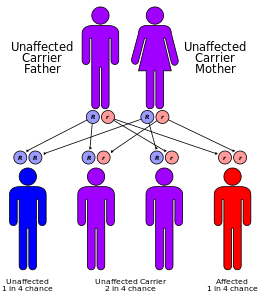
Как α-, так и β-талассемия часто передается по наследству аутосомный рецессивный манера. Случаи преимущественно Сообщалось о наследственных α- и β-талассемии, первая из которых была в ирландском семействе с двумя делециями 4 и 11 п.н. в экзоне 3, прерванных вставкой 5 п.н. в ген β-глобина. Для аутосомно-рецессивных форм заболевания оба родителя должны быть носителями, чтобы ребенок был поражен. Если оба родителя имеют признак гемоглобинопатии, риск для пораженного ребенка составляет 25% для каждой беременности.
Эволюция
Наличие единственного генетического варианта талассемии может защитить от малярии и таким образом может быть преимуществом.[23]
Люди с диагнозом гетерозиготный (носитель) β-талассемия имеет некоторую защиту от ишемическая болезнь сердца.[24]
Патофизиология
Обычно большая часть взрослого гемоглобина (HbA ) состоит из четырех белковых цепей, двух α и двух β-глобиновых цепей, расположенных в виде гетеротетрамер. При талассемии пациенты имеют дефекты в цепи альфа- или бета-глобина, вызывающие выработку аномальных эритроцитов (In серповидноклеточная анемия, которая является гемоглобинопатией, а не талассемией, мутация специфична для β-глобина).
Талассемии классифицируются в зависимости от того, какая цепь молекулы гемоглобина поражена. В α-талассемии, производство α-глобиновой цепи нарушается, а в β-талассемия, это влияет на продукцию цепи β-глобина.
Цепи β-глобина кодируются одним геном на хромосома 11; Цепи α-глобина кодируются двумя тесно связанными генами на хромосома 16.[25] Таким образом, у нормального человека с двумя копиями каждой хромосомы два локуса кодируют β-цепь, а четыре локуса кодируют α-цепь. Делеция одного из α-локусов широко распространена у лиц африканского или азиатского происхождения, что увеличивает вероятность их развития. α-талассемия. β-талассемии распространены не только в Африканцы, но и в Греки и Итальянцы.
Альфа-талассемии
В α-талассемии вовлечены гены HBA1[26] и HBA2,[27] унаследован в Менделирующий рецессивный мода. Два генные локусы Итак, существует четыре аллеля. Для α-глобина существует два генетических локуса, таким образом, четыре аллеля находятся в диплоидных клетках. Два аллеля являются материнскими, а два - отцовскими. Тяжесть α-талассемии коррелирует с количеством пораженного α-глобина; аллели: чем больше, тем тяжелее будут проявления болезни.[28] Альфа-талассемия приводит к снижению продукции альфа-глобина; следовательно, образуется меньше альфа-глобиновых цепей, что приводит к избытку β-цепей у взрослых и избытку γ-цепей у новорожденных. Избыточные β-цепи образуют нестабильные тетрамеры (называемые гемоглобином H или HbH 4 β-цепей), которые имеют аномальные кривые диссоциации кислорода. Альфа-талассемии часто встречаются у людей из Юго-Восточной Азии, Ближнего Востока, Китая и лиц африканского происхождения.[29]
| # отсутствующих аллелей | Типы альфа-талассемии[28] | Симптомы |
|---|---|---|
| 1 | Бесшумный носитель | Нет симптомов |
| 2 | Признак альфа-талассемии | Незначительная анемия |
| 3 | Болезнь гемоглобина H | Анемия легкой или средней степени может вести нормальный образ жизни |
| 4 | Водянка плода | Смерть плода обычно наступает при рождении. |
Бета-талассемия
Бета-талассемии возникают из-за мутаций в Ген HBB на хромосоме 11,[30] также наследуется по аутосомно-рецессивному типу. Тяжесть заболевания зависит от характера мутации и от наличия мутации в одном или обоих аллелях.
Мутировавшие аллели называются β+ когда частичная функция сохраняется (либо белок имеет пониженную функцию, либо он функционирует нормально, но вырабатывается в пониженном количестве) или βо, когда не вырабатывается функционирующий белок.
Положение обоих аллелей определяет клиническую картину:
- β-талассемия большая (Средиземноморье анемия или Кули анемия) вызывается βо/ βо генотип. Функциональные β-цепи не образуются, и поэтому сборка гемоглобина А невозможна. Это самая тяжелая форма β-талассемии;
- Промежуточная β-талассемия вызывается β-+/ βо или β+/ β+ генотип. В этой форме вырабатывается гемоглобин А;
- Малая β-талассемия вызывается β / βо или β / β+ генотип. Только один из двух аллелей β-глобина содержит мутацию, поэтому образование β-цепи не сильно нарушено, и пациенты могут быть относительно бессимптомными.
Бета-талассемия чаще всего встречается у людей средиземноморского происхождения. В меньшей степени могут пострадать китайцы, выходцы из Азии и афроамериканцы.[29]
Дельта-талассемия
Помимо альфа- и бета-цепей, присутствующих в гемоглобине, около 3% взрослого гемоглобина состоит из альфа- и дельта-цепей. Как и в случае с бета-талассемией, могут возникать мутации, которые влияют на способность этого гена продуцировать дельта-цепи.[нужна цитата ]
Комбинированные гемоглобинопатии
Талассемия может сосуществовать с другими гемоглобинопатии. Самые распространенные из них:
- Гемоглобин E / талассемия: часто встречается у Камбоджа, Таиланд, и части Индия, он клинически подобен большой β-талассемии или промежуточной талассемии.[нужна цитата ]
- Гемоглобин S / талассемия: часто встречается у Африканский и Средиземноморье популяций, клинически похож на серповидноклеточная анемия, с дополнительной функцией спленомегалия.[нужна цитата ]
- Гемоглобин С / талассемия: часто встречается у Средиземноморье и Африканский популяции, гемоглобин C / βо талассемия вызывает гемолитическую анемию средней степени тяжести со спленомегалией; гемоглобин C / β+ талассемия вызывает более легкое заболевание.[нужна цитата ]
- Гемоглобин D / талассемия: распространена в северо-западных частях Индия и Пакистан (Пенджаб регион ).[31]
Диагностика
Талассемию можно диагностировать с помощью полный анализ крови, электрофорез гемоглобина, и ДНК-тестирование.[32]Электрофорез гемоглобина не так широко доступен в развивающихся странах, поэтому индекс Ментцера также можно использовать для диагностики талассемии. Хотя это не диагностический тест, но он может дать четкое представление о возможности талассемии. Индекс Ментцера можно рассчитать на основании отчета об общем анализе крови. Для этого также можно использовать калькуляторы индекса Ментцера.[33].
Профилактика
В Американский колледж акушеров и гинекологов рекомендует всем людям, которые думают о беременности, пройти обследование на наличие талассемии.[34] Генетическое консультирование и генетическое тестирование рекомендуются семьям с признаками талассемии.
Политика проверки существует в Кипр снизить заболеваемость талассемией, которая с момента реализации программы в 1970-х годах (которая также включает пренатальный скрининг и аборты) снизила количество детей, рожденных с этим заболеванием, с одного из 158 рождений почти до нуля.[35] В Греции также действует программа скрининга для выявления носителей.[36]
В Иран в качестве добрачного скрининга в первую очередь проверяются показатели эритроцитов мужчины. Если у него есть микроцитоз (средний клеточный гемоглобин <27 пг или средний объем эритроцитов <80 эт), женщина проходит тестирование. Когда оба микроцитарные, их гемоглобин А2 концентрации измеряются. Если оба имеют концентрацию выше 3,5% (диагностика признака талассемии), их направляют в местный специальный медпункт. генетическое консультирование.[37]
Широкомасштабные информационные кампании организуются в Индия[38] как правительственными, так и неправительственными организациями в пользу добровольного добрачного скрининга для выявления носителей талассемии, и вступление в брак между обоими носителями категорически не рекомендуется.
Управление
Легкая талассемия: люди с талассемией черты не требуют медицинского или последующего ухода после постановки первоначального диагноза.[39] Людей с признаками β-талассемии следует предупредить, что их состояние может быть ошибочно признано более распространенным. железодефицитная анемия. Им следует избегать рутинного использования добавки железа; Однако дефицит железа может развиться во время беременности или в результате хронического кровотечения.[40] Консультирование показано всем людям с генетическими нарушениями, особенно когда семья подвержена риску тяжелой формы заболевания, которую можно предотвратить.[41]
Анемия
Людям с тяжелой формой талассемии требуется медицинская помощь. Режим переливания крови был первой мерой, способной продлить жизнь.[39]
Гормональная терапия роста
Есть некоторые свидетельства того, что заместительная терапия гормоном роста может помочь увеличить скорость роста детей с талассемией.[42]
Железная перегрузка
Многократные переливания крови могут привести к перегрузке железом. Перегрузку железом, связанную с талассемией, можно лечить: хелатотерапия с лекарствами дефероксамин, деферипрон, или же деферасирокс.[43] Эти методы лечения привели к увеличению продолжительности жизни у больных большой талассемией.[43]
Дефероксамин эффективен только при ежедневных инъекциях, что затрудняет его длительное применение. Его преимущество заключается в том, что он недорогой и приличный в долгосрочном плане безопасности. Побочные эффекты - это первичные кожные реакции вокруг места инъекции и потеря слуха.[43]
Деферасирокс является пероральным препаратом. Общие побочные эффекты включают: тошноту, рвоту и диарею. Однако он эффективен не для всех и, вероятно, не подходит тем, у кого серьезные проблемы с сердцем, связанные с перегрузкой железом. Стоимость тоже значительна.[43]
Деферипрон - это лекарство, которое принимают внутрь. При его использовании относительно часто наблюдаются тошнота, рвота и диарея.[43] Он доступен как в Европе, так и в США.[43][44] Это самый эффективный агент, когда сильно поражено сердце.[43]
Нет никаких доказательств от рандомизированное контролируемое исследование для поддержки приема цинка при талассемии.[45]
Трансплантация костного мозга
Трансплантация костного мозга может предложить возможность излечения у молодых людей, у которых HLA -подобный донор.[46] Показатели успеха находятся в диапазоне 80–90%.[46] Летальность от процедуры около 3%.[47] Нет рандомизированных контролируемых испытаний, которые проверяли бы безопасность и эффективность неидентичный донор трансплантация костного мозга людям с β-талассемией, которым требуется переливание крови.[48]
Заболевания трансплантата против хозяина (GvHD) - один из побочных эффектов трансплантации костного мозга. Необходимы дальнейшие исследования, чтобы оценить, можно ли использовать мезенхимальные стромальные клетки в качестве профилактики или лечения РТПХ.[49]
Если у человека нет HLA-совместимого совместимого донора, можно использовать другой метод, называемый трансплантацией костного мозга (BMT) от гаплоидентичной матери ребенку (несовместимый донор). В исследовании с участием 31 человека выживаемость без талассемии составила 70%, отторжение - 23%, а смертность - 7%. Лучшие результаты у очень молодых людей.[50]
Эпидемиология
Бета-форма талассемии особенно распространена среди Средиземноморье народов, и это географическое объединение несет ответственность за свое первоначальное название.[51] В 2013 году талассемия унесла жизни 25000 человек по сравнению с 36000 в 1990 году.[15]
В Европе самые высокие концентрации заболевания обнаруживаются в Греция, прибрежные районы в индюк (особенно Эгейский регион Такие как Измир, Балыкесир, Айдын, Мугла, и Средиземноморский регион Такие как Анталия, Адана, Мерсин ), в части Италия, особенно южная италия и нижняя долина реки По. Основные средиземноморские острова (кроме Балеарские острова ) Такие как Сицилия, Сардиния, Мальта, Корсика, Кипр, и Крит особенно сильно страдают. Другие жители Средиземноморья, а также жители его окрестностей также имеют высокий уровень талассемии, в том числе люди из Западная Азия и Северная Африка. Вдали от Средиземного моря, Выходцы из Южной Азии также затронуты, при этом самая высокая концентрация носителей в мире (16–18% населения) находится в Мальдивы.[52]
В настоящее время он встречается у популяций, живущих в Африке, Америке и в других странах. Люди тару в Тераи регион Непал и Индия.[53] Считается, что на его долю приходится гораздо меньшее количество заболеваний и смертей от малярии,[54] это объясняет историческую способность Тараса выживать в районах с сильным заражением малярией, где другие не могли. Талассемии особенно связаны с людьми средиземноморского происхождения, арабами (особенно Палестинцы и люди палестинского происхождения) и азиаты.[55] На Мальдивах самый высокий уровень заболеваемости талассемией в мире - 18% населения. По оценкам, распространенность составляет 16% у людей из Кипр, 1%[56] в Таиланд и 3–8% в популяциях из Бангладеш, Китай, Индия, Малайзия и Пакистан. Талассемии также встречаются у потомков людей из стран Средиземноморья (например, Греции, Италии, Испания, и др.), в Латинская Америка.
По оценкам, примерно 1,5% населения мира (80–90 миллионов человек) являются носителями β-талассемии.[57] Однако точные данные о частоте носителей среди многих групп населения отсутствуют, особенно в развивающихся регионах мира, которые, как известно, или как ожидается, сильно пострадают.[58][59] Из-за того, что заболевание широко распространено в странах, мало осведомленных о талассемии, доступ к надлежащему лечению и диагностике может быть затруднен.[60] Хотя в развивающихся странах есть некоторые диагностические и лечебные учреждения, в большинстве случаев они не предоставляются государственными службами и доступны только пациентам, которые могут себе это позволить. В целом, более бедные слои населения имеют доступ только к ограниченным диагностическим средствам вместе с переливаниями крови. В некоторых развивающихся странах практически отсутствуют средства для диагностики или лечения талассемии.[60]
Этимология и синоним
Слово талассемия (/θæлɪˈsямяə/) происходит от Греческий таласса (θάλασσα), «море»,[61] и Новая латынь -емия (от греч. сложный корень -Аймия (-αιμία), из Хайма (αἷμα), «кровь»).[62] Он был придуман, потому что состояние под названием «средиземноморская анемия» было первым описанный в людях Средиземноморье национальности. «Средиземноморская анемия» переименована. большая талассемия однажды генетика была лучше понята. Слово талассемия впервые был использован в 1932 году.[51]:877[63]
Общество и культура
В 2008 году в Испании родился ребенок. выборочно имплантированный быть лекарство от талассемии его брата. Ребенок родился от эмбриона, который был проверен на отсутствие болезни перед имплантацией in vitro оплодотворение. Запас иммунологически совместимой пуповинной крови ребенка был сохранен для трансплантации брату. Трансплантация признана успешной.[64] В 2009 году группа врачей и специалистов в Ченнаи и Коимбатур зарегистрировали успешное лечение талассемии у ребенка с использованием пуповинной крови здорового брата или сестры.[65]
Исследование
Генная терапия
Генная терапия изучается на талассемию.[66] Процедура предполагает сбор гемопоэтические стволовые клетки (HSC) из крови пострадавшего. Затем к HSC добавляется ген бета-глобина с использованием лентивирусный вектор. После разрушения костного мозга пораженного человека дозой химиотерапии (режим миелоаблативного кондиционирования) измененные HSC вливаются обратно в пострадавшего человека, где они приживаются в костном мозге, где они размножаются. Это потенциально приводит к прогрессивному увеличению синтеза гемоглобина А2 во всех последующих развивающихся эритроцитах, что приводит к разрешению анемии.[67]
Хотя одному человеку с бета-талассемией больше не требовалось переливание крови после лечения в рамках исследовательского исследования, по состоянию на 2018 год это лечение не было одобрено.[66][68]
Индукция HbF
Индукция HbF - это попытка реактивации транскрипции гена глобина плода.[69] Усилия включают попытки нарушить промотор гена глобина плода.[69]
Рекомендации
- ^ а б c d е ж грамм час «Каковы признаки и симптомы талассемии?». NHLBI. 3 июля 2012 г. В архиве из оригинала 16 сентября 2016 г.. Получено 5 сентября 2016.
- ^ а б c "Что вызывает талассемию?". NHLBI. 3 июля 2012 г. В архиве из оригинала 26 августа 2016 г.. Получено 5 сентября 2016.
- ^ а б «Как диагностируют талассемии?». NHLBI. 3 июля 2012 г. В архиве из оригинала 16 сентября 2016 г.. Получено 5 сентября 2016.
- ^ а б c d е "Как лечат талассемии?". NHLBI. 3 июля 2012 г. В архиве из оригинала 16 сентября 2016 г.. Получено 5 сентября 2016.
- ^ ГББ 2015 Заболеваемость и травматизм, частота и распространенность, соавторы. (8 октября 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 310 заболеваний и травм, 1990–2015 годы: систематический анализ для исследования глобального бремени болезней 2015». Ланцет. 388 (10053): 1545–1602. Дои:10.1016 / S0140-6736 (16) 31678-6. ЧВК 5055577. PMID 27733282.
- ^ а б ГББ 2015 Смертность и причины смерти, соавторы. (8 октября 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 гг .: систематический анализ для исследования глобального бремени болезней 2015 г.». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / с0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ а б c "Что такое талассемия?". NHLBI. 3 июля 2012 г. В архиве из оригинала 26 августа 2016 г.. Получено 5 сентября 2016.
- ^ «Как можно предотвратить талассемию?». NHLBI. 3 июля 2012 г. В архиве из оригинала 16 сентября 2016 г.. Получено 5 сентября 2016.
- ^ «Железное хелатирование». Получено 15 июля 2020.
- ^ Шах, Сандип; Шет, Радхика; Шах, Камлеш; Патель, Киннари (февраль 2020 г.). «Безопасность и эффективность комбинации талидомида и гидроксимочевины при промежуточной и основной β-талассемии: ретроспективное пилотное исследование». Британский журнал гематологии. 188 (3). Дои:10.1111 / bjh.16272. ISSN 0007-1048.
- ^ Кейхаи, Биджан (2015). «Клинические и гематологические эффекты гидроксимочевины у пациентов с промежуточной β-талассемией». ЖУРНАЛ КЛИНИКО-ДИАГНОСТИЧЕСКИХ ИССЛЕДОВАНИЙ. Дои:10.7860 / JCDR / 2015 / 14807.6660.
- ^ Мазера, Николетта; Тавеккья, Луиза; Капра, Мариетта; Каззанига, Джованни; Вимеркати, Кьяра; Поцци, Лорена; Бионди, Андреа; Мазера, Джузеппе (2010). «Оптимальный ответ на талидомид у пациента с большой талассемией, резистентной к традиционной терапии». Переливание крови. Дои:10.2450/2009.0102-09. ISSN 1723-2007. ЧВК 2809513. PMID 20104280.
- ^ Исследование глобального бремени болезней, 2013 г., соавторы (22 августа 2015 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 301 острого и хронического заболевания и травмы в 188 странах, 1990–2013 гг .: систематический анализ для исследования глобального бремени болезней 2013». Ланцет. 386 (9995): 743–800. Дои:10.1016 / с0140-6736 (15) 60692-4. ЧВК 4561509. PMID 26063472.
- ^ Clin. Методы в пед. Издательство Jaypee Brothers. 2005. с. 21. ISBN 9788171798087.
- ^ а б ГББ 2013 Смертность и причины смерти, соавторы (17 декабря 2014 г.). «Глобальная, региональная и национальная смертность от всех причин и причин смерти с разбивкой по возрасту и полу от 240 причин смерти, 1990–2013 гг .: систематический анализ для исследования глобального бремени болезней 2013 г.». Ланцет. 385 (9963): 117–71. Дои:10.1016 / S0140-6736 (14) 61682-2. ЧВК 4340604. PMID 25530442.
- ^ Уизералл, Д. Дж. (2015). «Талассемии: нарушения синтеза глобина». Гематология Вильямса (9e изд.). McGraw Hill Professional. п. 725. ISBN 9780071833011.
- ^ Чианчиулли П. (октябрь 2008 г.). «Лечение перегрузки железом при талассемии». Педиатр Эндокринол Рев. 6 (Приложение 1): 208–13. PMID 19337180.
- ^ «Талассемия - симптомы и причины». В архиве из оригинала от 20 ноября 2016 г.. Получено 4 апреля 2017.
- ^ Вогиаци, Мария Г; Маклин, Эрик А; Фанг, Эллен Б.; Cheung, Angela M; Вичинский, Эллиот; Оливьери, Нэнси; Кирби, Мелани; Квятковски, Джанет Л; Каннингем, Мелоди; Холм, Ингрид А; Лейн, Джозеф; Шнайдер, Роберт; Флейшер, Мартин; Грэди, Роберт В. Петерсон, Чарльз С; Джардина, Патрисия Дж (март 2009 г.). «Болезнь костей при талассемии: частая и до сих пор нерешенная проблема». Журнал исследований костей и минералов. 24 (3): 543–557. Дои:10.1359 / jbmr.080505. ISSN 0884-0431. ЧВК 3276604. PMID 18505376.
- ^ «Симптомы и причины - Увеличенная селезенка (спленомегалия) - Клиника Мэйо». www.mayoclinic.org. В архиве из оригинала 19 ноября 2016 г.. Получено 2 февраля 2017.
- ^ Солиман, Ашраф Т; Калра, Санджай; Де Санктис, Винченцо (1 ноября 2014 г.). «Анемия и рост». Индийский журнал эндокринологии и метаболизма. 18 (7): S1–5. Дои:10.4103/2230-8210.145038. ЧВК 4266864. PMID 25538873.
- ^ «Осложнения талассемии». Талассемия. Открытая публикация. В архиве из оригинала от 3 октября 2011 г.. Получено 27 сентября 2011.
- ^ Вамбуа S; Mwangi, Tabitha W .; Корток, Моисей; Уйога, Софи М .; Macharia, Alex W .; Mwacharo, Jedidah K .; Weatherall, Дэвид Дж .; Сноу, Роберт В .; Марш, Кевин; Уильямс, Томас Н. (май 2006 г.). «Влияние α + -талассемии на заболеваемость малярией и другими заболеваниями у детей, живущих на побережье Кении». PLOS Медицина. 3 (5): e158. Дои:10.1371 / journal.pmed.0030158. ЧВК 1435778. PMID 16605300.
- ^ Tassiopoulos S; Дефтереос, Спирос; Константопулос, Костас; Фармакис, Димитрис; Цирони, Мария; Кириакидис, Михалис; Эссопос, Афанасий (2005). «Обеспечивает ли гетерозиготная бета-талассемия защиту от ишемической болезни сердца?». Летопись Нью-Йоркской академии наук. 1054: 467–70. Дои:10.1196 / летопись.1345.068. PMID 16339699.
- ^ Базовая патология Роббинса, Страница №: 428
- ^ Онлайн-менделевское наследование в человеке (OMIM): Гемоглобин - Альфа-локус 1; HBA1 - 141800
- ^ Онлайн-менделевское наследование в человеке (OMIM): Гемоглобин - Альфа-локус 2; HBA2 - 141850
- ^ а б Галанелло, Ренцо; Цао, Антонио (5 января 2011 г.). «Альфа-талассемия». Генетика в медицине. 13 (2): 83–88. Дои:10.1097 / GIM.0b013e3181fcb468. ISSN 1098-3600. PMID 21381239.
- ^ а б «Основы анемии». WebMD. Получено 9 мая 2019.
- ^ Онлайн-менделевское наследование в человеке (OMIM): Гемоглобин - бета-локус; HBB - 141900
- ^ Torres Lde S (март 2015 г.). «Гемоглобин D-Пенджаб: происхождение, распространение и лабораторная диагностика». Revista Brasileira de Hematologia e Hemoterapia. Дои:10.1016 / j.bjhh.2015.02.007. PMID 25818823. Получено 16 октября 2020. Цитировать журнал требует
| журнал =(помощь) - ^ «Как диагностируют талассемии? - NHLBI, NIH». www.nhlbi.nih.gov. В архиве из оригинала 28 июля 2017 г.. Получено 6 сентября 2017.
- ^ https://play.google.com/store/apps/details?id=com.gmail.sarahtinmaswala.challenge
- ^ «Скрининг носителей в эпоху геномной медицины - ACOG». www.acog.org. В архиве из оригинала 25 февраля 2017 г.. Получено 24 февраля 2017.
- ^ Leung TN; Лау ТК; Чунг ТХ (апрель 2005 г.). «Скрининг талассемии при беременности». Текущее мнение в области акушерства и гинекологии. 17 (2): 129–34. Дои:10.1097 / 01.gco.0000162180.22984.a3. PMID 15758603. S2CID 41877258.
- ^ Лукопулос, Д. (октябрь 2011 г.). «Гемоглобинопатии в Греции: программа профилактики за последние 35 лет». Индийский журнал медицинских исследований. 134: 572–6. ЧВК 3237258. PMID 22089622.
- ^ Самават А, Модель Б (ноябрь 2004 г.). «Иранская национальная программа скрининга на талассемию». BMJ (под ред. Клинических исследований). 329 (7475): 1134–7. Дои:10.1136 / bmj.329.7475.1134. ЧВК 527686. PMID 15539666.
- ^ Петру, Мэри (1 января 2010 г.). «Скрининг на бета-талассемию». Индийский журнал генетики человека. 16 (1): 1–5. Дои:10.4103/0971-6866.64934. ЧВК 2927788. PMID 20838484.[постоянная мертвая ссылка ]
- ^ а б Детская талассемия ~ лечение в eMedicine
- ^ Burdick CO; Ntaios, G .; Ратод, Д. (март 2009 г.). «Разделение признака талассемии и дефицита железа простым осмотром». Являюсь. J. Clin. Патол. 131 (3): 444, ответ автора 445. Дои:10.1309 / AJCPC09VRAXEASMH. PMID 19228649. Архивировано из оригинал 22 сентября 2014 г.
- ^ Принципы внутренней медицины Харрисона (17-е изд.). Макгроу-Хилл медицинский. Сентябрь 2008. с. 776. ISBN 978-0-07-164114-2.
- ^ Ngim, CF; Лай, Нью-Мексико; Хонг, JY; Tan, SL; Рамадас, А; Muthukumarasamy, P; Тонг, МК (28 мая 2020 г.). «Терапия гормоном роста для больных талассемией». Кокрановская база данных систематических обзоров. 5: CD012284. Дои:10.1002 / 14651858.CD012284.pub3. PMID 32463488.
- ^ а б c d е ж грамм Neufeld, EJ (2010). «Обновленная информация о хелаторах железа при талассемии». Гематология. 2010: 451–5. Дои:10.1182 / asheducation-2010.1.451. PMID 21239834.
- ^ «Феррипрокс». Drugs.com. Американское общество фармацевтов систем здравоохранения. В архиве из оригинала 20 сентября 2016 г.. Получено 5 сентября 2016.
- ^ Кай Мон Мин Све (2013). «Добавки цинка для лечения талассемии и серповидноклеточной анемии». Кокрановская база данных систематических обзоров (6): CD009415. Дои:10.1002 / 14651858.CD009415.pub2. PMID 23807756.
- ^ а б Газиев, Дж; Лукарелли, Г. (июнь 2011 г.). «Трансплантация гемопоэтических стволовых клеток при талассемии». Текущие исследования стволовых клеток и терапия. 6 (2): 162–9. Дои:10.2174/157488811795495413. PMID 21190532.
- ^ Саблов, М; Чанди, М; Ван, З; Логан, BR; Гавамзаде, А; Лизать; Ирфан, С.М.; Бредесон, CN; и другие. (2011). «Трансплантация HLA-совместимого костного мозга брату и сестре при большой β-талассемии». Кровь. 117 (5): 1745–50. Дои:10.1182 / blood-2010-09-306829. ЧВК 3056598. PMID 21119108.
- ^ Джаганнатх, Ванита А .; Федорович, Збыс; Аль-Хаджери, Амани; Шарма, Акшай (30 ноября 2016 г.). «Трансплантация гемопоэтических стволовых клеток людям с большой ß-талассемией». Кокрановская база данных систематических обзоров. 11: CD008708. Дои:10.1002 / 14651858.CD008708.pub4. ISSN 1469-493X. ЧВК 6492419. PMID 27900772.
- ^ Фишер, Шейла А; Катлер, Антоний; Дори, Кэролайн; Бранскилл, Сьюзен Дж; Стэнворт, Саймон Дж; Наваррете, Кристина; Гердлстон, Джон (30 января 2019 г.). Кокрановская группа по гематологическим злокачественным новообразованиям (ред.). «Мезенхимальные стромальные клетки как лечение или профилактика острого или хронического заболевания трансплантат против хозяина у реципиентов гемопоэтических стволовых клеток (HSCT) с гематологическим заболеванием». Кокрановская база данных систематических обзоров. 1: CD009768. Дои:10.1002 / 14651858.CD009768.pub2. ЧВК 6353308. PMID 30697701.
- ^ Sodani, P; Isgrò, A; Газиев, Дж; Paciaroni, K; Марзиали, М; Simone, MD; Роведа, А; Де Анжелис, G; и другие. (2011). «Трансплантация гла-гаплоидентичных стволовых клеток с истощенными Т-клетками у молодых пациентов с талассемией». Педиатрические отчеты. 3 (Приложение 2): e13. Дои:10.4081 / pr.2011.s2.e13. ЧВК 3206538. PMID 22053275.
- ^ а б Джон П. Грир JP, Арбер Д.А., Глэдер Б., и другие. Клиническая гематология Винтроба 2013. ISBN 9781451172683
- ^ Вахид, Фазила; Фиштер, Коллин; Авофесо, Авонийи; Стэнли, Дэвид (июль 2016 г.). «Скрининг носителей бета-талассемии на Мальдивах: мнение родителей пострадавших детей, которые не принимали участие в скрининге, и его последствия». Журнал общественной генетики. 7 (3): 243–253. Дои:10.1007 / s12687-016-0273-5. ЧВК 4960032. PMID 27393346.
- ^ Модиано, G .; Морпурго, G; Терренато, L; Новеллетто, А; Ди Риенцо, А; Коломбо, B; Пурпура, M; Мариани, М; и другие. (1991). «Защита от заболеваемости малярией: почти фиксация гена α-талассемии у населения Непала». Американский журнал генетики человека. 48 (2): 390–7. ЧВК 1683029. PMID 1990845.
- ^ Терренато, L; Шреста, S; Диксит, штат Калифорния; Луццатто, L; Модиано, G; Морпурго, G; Арезе, П. (февраль 1988 г.). «Снижение заболеваемости малярией среди народа тару по сравнению с симпатичным населением в Непале». Анналы тропической медицины и паразитологии. 82 (1): 1–11. Дои:10.1080/00034983.1988.11812202. PMID 3041928.
- ^ Э. Гольян, Патология, 2-е изд. Мосби Эльзевир, Серия быстрых обзоров.[страница нужна ]
- ^ «Талассемия» (на тайском языке). Департамент медицинских наук. Сентябрь 2011. Архивировано с оригинал 25 сентября 2011 г.
- ^ Галанелло, Ренцо; Орига, Рафаэлла (2010). «Бета-талассемия». Журнал редких заболеваний Orphanet. 5 (1): 11. Дои:10.1186/1750-1172-5-11. ЧВК 2893117. PMID 20492708.
- ^ Галанелло, Ренцо; Орига, Рафаэлла (2010). «Бета-талассемия». Журнал редких заболеваний Orphanet. 5 (1): 11. Дои:10.1186/1750-1172-5-11. ЧВК 2893117. PMID 20492708.
- ^ Вичинский, Эллиотт П. (1 ноября 2005 г.). «Изменение моделей талассемии во всем мире». Летопись Нью-Йоркской академии наук. 1054 (1): 18–24. Bibcode:2005НЯСА1054 ... 18В. Дои:10.1196 / Анналы.1345.003. ISSN 1749-6632. PMID 16339647.
- ^ а б WEATHERALL, ДЭВИД Дж. (Ноябрь 2005 г.). «Основной доклад: проблема талассемии для развивающихся стран». Летопись Нью-Йоркской академии наук. 1054 (1): 11–17. Bibcode:2005НЯСА1054 ... 11Вт. Дои:10.1196 / летопись.1345.002. PMID 16339646.
- ^ θάλασσα. Лидделл, Генри Джордж; Скотт, Роберт; Греко-английский лексикон на Проект Персей.
- ^ αἷμα в Liddell и Скотт.
- ^ Уиппл Г. Х., Брэдфорд Висконсин. Ам Дж. Дис Чайлд 1932; 44: 336
- ^ "Испанский ребенок, созданный, чтобы вылечить брата". Архивировано из оригинал 15 октября 2008 г.
- ^ Хранитель его сестры: кровь брата - благо жизни В архиве 22 сентября 2009 г. Wayback Machine, Времена Индии, 17 сентября 2009 г.
- ^ а б Негре, Оливье; Эггиманн, Энн-Вирджини; Бёзар, Ив; Рибей, Жан-Антуан; Бурже, Филипп; Борворнпиньо, Супарек; Хонгэн, Сурадей; Хасейн-бей, Салима; Каваззана, Марина; Лебулш, Филипп; Пайен, Эммануэль (февраль 2016 г.). «Генная терапия β-гемоглобинопатий лентивирусным переносом β-гена». Генная терапия человека. 27 (2): 148–165. Дои:10.1089 / hum.2016.007. ЧВК 4779296. PMID 26886832.
- ^ Биффи, А (19 апреля 2018 г.). «Генная терапия как средство лечения β-талассемии». Медицинский журнал Новой Англии. 378 (16): 1551–1552. Дои:10.1056 / NEJMe1802169. PMID 29669229.
- ^ Lidonnici, MR; Ferrari, G (май 2018 г.). «Генная терапия и стратегии редактирования генов при гемоглобинопатиях». Клетки, молекулы и болезни крови. 70: 87–101. Дои:10.1016 / j.bcmd.2017.12.001. PMID 29336892.
- ^ а б Винерт, В; Мартын, GE; Фаннелл, APW; Куинлан, КГР; Кроссли, М. (1 октября 2018 г.). «Пробуждающий сонный ген: реактивация фетального глобина для β-гемоглобинопатий». Тенденции в генетике. 34 (12): 927–940. Дои:10.1016 / j.tig.2018.09.004. PMID 30287096.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
- Талассемия в Керли
- Изучение талассемии опубликовано Национальным институтом исследования генома человека.
