Феррицианид - Ferricyanide
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК гексацианид железа (3+) | |
| Систематическое название ИЮПАК гексацианидоферрат (III) | |
| Другие имена гексацианид железа; гексацианидоферрат (3-); гексацианоферрат (III) | |
| Идентификаторы | |
3D модель (JSmol ) | |
PubChem CID | |
| |
| Свойства | |
| [Fe (CN)6]3− | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
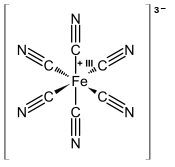
Феррицианид это анион [Fe (CN)6]3−. Его еще называют гексацианоферрат (III) и редко, но систематическая номенклатура, гексацианидоферрат (III). Самая распространенная соль этого аниона - феррицианид калия, красный кристаллический материал, который используется в качестве окислитель в органическая химия.[1]
Свойства
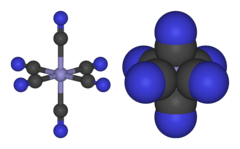
[Fe (CN)6]3− состоит из Fe3+ центр привязан в октаэдрическая геометрия до шести цианид лиганды. В комплексе есть Oчас симметрия. Утюг низкое вращение и легко сводится к ферроцианид ион [Fe (CN)6]4−, который представляет собой железо (Fe2+) производная. Эта окислительно-восстановительная пара обратима и не влечет за собой образования или разрыва связей Fe – C:
- [Fe (CN)6]3− + е− ⇌ [Fe (CN)6]4−
Эта редокс пара стандарт в электрохимия.
По сравнению с нормальным цианиды любить цианистый калий, феррицианиды гораздо менее токсичны из-за плотного удержания CN− к Fe3+. Однако они реагируют с минеральными кислотами с выделением высокотоксичных веществ. цианистый водород газ.
Использует
Обработка феррицианида солями железа (II) дает блестящий, стойкий пигмент. Берлинская лазурь, традиционный цвет чертежи.
Смотрите также
использованная литература
- ^ Gail, E .; Гос, С .; Kulzer, R .; Lorösch, J .; Rubo, A .; Sauer, M .; Kellens, R .; Редди, Дж .; Штайер, Н. "Циано-соединения, неорганические". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a08_159.pub3.
