Нановолокно - Nanofiber

Нановолокна волокна с диаметрами в нанометр ассортимент. Нановолокна могут быть получены из разных полимеры и, следовательно, имеют разные физические свойства и возможности применения. Примеры природных полимеров включают коллаген, целлюлоза, фиброин шелка, кератин, желатин и полисахариды такие как хитозан и альгинат.[1][2] Примеры синтетических полимеров включают поли (молочная кислота) (PLA), поликапролактон (PCL), полиуретан (PU), поли (молочно-гликолевая кислота) (PLGA), поли (3-гидроксибутират-со-3-гидроксивалерат) (PHBV) и сополимер этилена и винилацетата (PEVA).[1][2] Полимерные цепи соединяются через ковалентные связи.[3] Диаметр нановолокон зависит от типа используемого полимера и метода производства.[4] Все полимерные нановолокна уникальны своим большим отношением площади поверхности к объему, высокой пористостью, значительной механической прочностью и гибкостью в функционализации по сравнению с их микрофибра аналоги.[1][2][5]
Существует множество различных методов изготовления нановолокон, в том числе рисование, электроспиннинг, самосборка, темплатный синтез и термическое разделение фаз. Электропрядение - это наиболее часто используемый метод для создания нановолокон из-за простоты настройки, возможности массового производства непрерывных нановолокон из различных полимеров и способности создавать ультратонкие волокна с регулируемыми диаметром, составом и ориентацией.[5] Такая гибкость позволяет контролировать форму и расположение волокон, чтобы различные структуры (т.е. полые, плоские и ленточные) могут изготавливаться в зависимости от предполагаемого применения. Используя инновационный метод обработки расплава, который подходит для промышленного массового производства, ученые и инженеры из Университета Миннесоты смогли сделать нановолокна толщиной всего 36 нм.[6]
Нановолокна имеют множество возможных технологических и коммерческих применений. Они используются в тканевой инженерии,[1][2][7] Доставка наркотиков,[8][9][10] материал покрытия семян,[11][12][13][14] диагностика рака,[15][16][17] литий-воздушная батарея,[18][19][20] оптические датчики[21][22][23] и фильтрация воздуха.[24][25][26]
История производства нановолокна
Нановолокна сначала производились через электроспиннинг более четырех веков назад.[27][28] Начиная с развития метода электроспиннинга, английский физик Уильям Гилберт (1544-1603) впервые задокументировал электростатическое притяжение между жидкостями, подготовив эксперимент, в котором он наблюдал, как сферическая капля воды на основе сухой поверхности превращается в конус, когда она находится под электрически заряженным янтарем.[29] Эта деформация позже стала известна как Конус Тейлора.[30] В 1882 г. английский физик Лорд Рэйли (1842-1919) проанализировали нестабильное состояние жидких капель, которые были электрически заряжены, и отметили, что жидкость выбрасывалась крошечными струями, когда равновесие была создана между поверхностное натяжение и электростатическая сила.[31] В 1887 г. британский физик Чарльз Вернон Бойз (1855-1944) опубликовал рукопись о разработке и производстве нановолокна.[32] В 1900 году американский изобретатель Джон Фрэнсис Кули (1861–1903) подал первый патент на современное электропрядение.[33]
Антон Формхалс был первым, кто попытался произвести нановолокно между 1934 и 1944 годами и опубликовал первый патент, описывающий экспериментальное производство нановолокон.[28] В 1966 году Гарольд Саймонс опубликовал патент на устройство, которое могло производить тонкие и легкие ткани из нановолокна с разнообразными мотивами.[34]
Только в конце 20 века слова электропрядение и нановолокно стали общим языком ученых и исследователей.[27][28] Электроспиннинг продолжает развиваться и сегодня.
Методы синтеза
Существует множество химических и механических методов получения нановолокон.
Электропрядение


Электропрядение это наиболее часто используемый метод изготовления нановолокон.[35][5] [36][37]Инструменты, необходимые для электроспиннинга, включают источник высокого напряжения, капиллярная трубка пипеткой или иглой небольшого диаметра и металлическим улавливающим экраном. Один электрод помещается в раствор полимера, а другой электрод присоединяется к коллектору. An электрическое поле наносится на конец капиллярной трубки, которая содержит раствор полимера, удерживаемый его поверхностным натяжением, и формирует заряд на поверхности жидкости. По мере увеличения напряженности электрического поля полусферическая поверхность жидкости на конце капиллярной трубки удлиняется, образуя коническую форму, известную как Конус Тейлора. Критическое значение достигается при дальнейшем увеличении электрического поля, в котором отталкивающая электростатическая сила преодолевает поверхностное натяжение, и заряженная струя жидкости выбрасывается из кончика конуса Тейлора. Выбрасываемая струя раствора полимера нестабильна и в результате удлиняется, в результате чего струя становится очень длинной и тонкой. Заряженные полимерные волокна затвердевают при испарении растворителя.[5][38] На коллекторе собираются случайно ориентированные нановолокна. Нановолокна также могут быть собраны строго согласованным способом с использованием специализированных коллекционеров, таких как вращающийся барабан,[39] металлический каркас,[40] или система двух параллельных пластин.[41] Для производства нановолокон с одинаковым диаметром и морфологией необходимо контролировать такие параметры, как движение струи и концентрация полимера.[42]
Технология электропрядения превращает многие типы полимеров в нановолокна. Сеть из электропряденого нановолокна напоминает внеклеточный матрикс (ECM) хорошо.[5][43][44] Это сходство является основным преимуществом электроспиннинга, поскольку оно открывает возможность имитации ECM в отношении диаметра волокна, высокой пористости и механических свойств. Электропрядение получает дальнейшее развитие для массового производства отдельных непрерывных нановолокон.[43]
Термическое разделение фаз
Разделение фаз, вызванное термическим воздействием, разделяет гомогенный полимерный раствор на многофазную систему через термодинамический изменения.[1][7][45] Процедура состоит из пяти этапов: полимер растворение, разделение фаз жидкость-жидкость или жидкость-твердая фаза, полимер гелеобразование, добыча растворителя из геля с водой, и замораживание и сублимационной сушки под вакуумом.[1][7] Метод термического разделения фаз широко используется для создания каркасов для регенерации тканей.[45]
Гомогенный раствор полимера на первом этапе является термодинамически нестабильным и имеет тенденцию к разделению на фазы с высоким содержанием полимера и фазы с низким содержанием полимера при соответствующей температуре. В конечном итоге после удаления растворителя фаза, богатая полимером, затвердевает с образованием матрицы, а фаза с низким содержанием полимера превращается в поры.[нужна цитата ] Затем в растворе полимера можно провести два типа разделения фаз в зависимости от желаемой структуры. Разделение жидкость-жидкость обычно используется для образования бинепрерывных фазовых структур, в то время как разделение твердой и жидкой фаз используется для образования кристаллических структур. Стадия гелеобразования играет решающую роль в регулировании пористой морфологии нановолоконных матриц. На гелеобразование влияют температура, концентрация полимера и свойства растворителя.[45] Температура регулирует структуру волоконной сети: низкая температура гелеобразования приводит к образованию наноразмерных волоконных сетей, а высокая температура гелеобразования приводит к образованию пластинчатой структуры.[1] Концентрация полимера влияет на свойства волокна: увеличение концентрации полимера снижает пористость и увеличивает механические свойства, такие как прочность на разрыв. Свойства растворителя влияют на морфологию каркасов. После гелеобразования гель помещают в дистиллированную воду для замены растворителя. Затем гель вынимают из воды и подвергают замораживанию и сушке вымораживанием. Затем он хранится в эксикаторе до определения характеристик.
Рисование
Метод вытяжки позволяет создавать длинные отдельные нити нановолокон по одной. Процесс вытягивания сопровождается затвердеванием, которое превращает растворенный прядильный материал в твердое волокно.[43][46] Этап охлаждения необходим в случае формования из расплава и испарения растворителя в случае сухого формования. Ограничение, однако, состоит в том, что только вязкоупругий материал, который может подвергаться обширным деформациям, но при этом обладает достаточной когезией, чтобы выдерживать напряжения, возникающие при растяжении, с помощью этого процесса можно превратить в нановолокна.[43][47]
Синтез шаблона
В методе синтеза шаблона используется шаблон нанопористой мембраны, состоящий из цилиндрических пор одинакового диаметра, чтобы сделать фибриллы (твердое нановолокно) и трубочки (полое нановолокно).[48][49] Этот метод можно использовать для получения фибрилл и канальцев из многих типов материалов, включая металлы, полупроводники и электронопроводящие полимеры.[48][49] Однородные поры позволяют контролировать размеры волокон, поэтому с помощью этого метода можно производить нановолокна с очень маленькими диаметрами. Однако недостатком этого метода является то, что он не может производить непрерывные нановолокна по одному.
Самостоятельная сборка
Метод самосборки используется для создания пептид нановолокна и пептидные амфифилы. Этот метод был вдохновлен естественным процессом складывания аминокислота остатки для образования белков с уникальной трехмерной структурой.[50] Процесс самосборки пептидных нановолокон включает в себя различные движущие силы, такие как гидрофобные взаимодействия, электростатические силы, водородная связь и силы Ван дер Ваальса и находится под влиянием внешних условий, таких как ионная сила и pH.[51]
Полимерные материалы

Благодаря своей высокой пористости и большому соотношению площади поверхности к объему, нановолокна широко используются для создания каркасов для биологических применений.[1][2] Основными примерами природных полимеров, используемых в производстве строительных лесов, являются: коллаген, целлюлоза, фиброин шелка, кератин, желатин и полисахариды такие как хитозан и альгинат. Коллаген является естественным внеклеточным компонентом многих соединительной ткани. Его фибриллярная структура, диаметр которой варьируется от 50 до 500 нм, важна для распознавания, прикрепления, пролиферации и дифференцировки клеток.[2] С помощью коллаген I типа нановолокна, полученные методом электроспиннинга, Shih et al. обнаружили, что сконструированный коллагеновый каркас показал увеличение клеточной адгезии и уменьшение миграции клеток с увеличением диаметра волокна.[52] Используя шелковые каркасы в качестве ориентира роста для регенерации костной ткани, Kim et al. наблюдали полное сращение кости через 8 недель и полное заживление дефектов через 12 недель, тогда как в контроле, в котором кость не имела каркаса, наблюдали ограниченное исправление дефектов за тот же период времени.[53] Так же, кератин, желатин, хитозан и альгинат продемонстрировать отличный биосовместимость и биологическая активность в строительных лесах.[2]
Однако клеточное распознавание природных полимеров может легко вызвать иммунный ответ.[2][44] Следовательно, синтетические полимеры, такие как поли (молочная кислота) (PLA), поликапролактон (PCL), полиуретан (PU), поли (молочно-гликолевая кислота) (PLGA), поли (L-лактид) (PLLA) и сополимер этилена и винилацетата (PEVA) были разработаны в качестве альтернативы интеграции в каркасы. Эти синтетические полимеры, биоразлагаемые и биосовместимые, могут использоваться для образования матриц с диаметром волокна в нанометровом диапазоне. Из этих синтетических полимеров PCL вызвал значительный энтузиазм среди исследователей.[54] PCL - это тип биоразлагаемого полиэфира, который может быть получен полимеризацией с раскрытием кольца ε-капролактона с использованием катализаторы. Он показывает низкую токсичность, низкую стоимость и медленную деградацию. PCL можно комбинировать с другими материалами, такими как желатин, коллаген, хитозан и фосфат кальция, для улучшения способности к дифференцировке и пролиферации (2, 17).[2][54] PLLA - еще один популярный синтетический полимер. PLLA хорошо известен своими превосходными механическими свойствами, биоразлагаемостью и биосовместимостью. Он демонстрирует способность к эффективной миграции клеток благодаря высокой пространственной взаимосвязи, высокой пористости и контролируемому выравниванию.[55] Смесь матрицы каркаса PLLA и PLGA показала правильную биомиметическую структуру, хорошую механическую прочность и благоприятную биоактивность.
Приложения
Тканевая инженерия
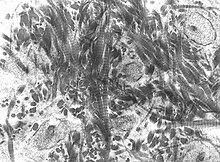
В тканевой инженерии необходим высокопористый искусственный внеклеточный матрикс для поддержки и направления роста клеток и регенерации тканей.[1][2][56][57] Для создания таких каркасов использовались природные и синтетические биоразлагаемые полимеры.[1][2]
Саймон в отчете о гранте NIH SBIR за 1988 год показал, что электроспиннинг может быть использован для производства полистирольных и поликарбонатных волокнистых матов нано- и субмикронного масштаба, специально предназначенных для использования в качестве субстратов клеток in vitro. Это раннее использование электропряденых фиброзных решеток для клеточных культур и тканевой инженерии показало, что фибробласты крайней плоти человека (HFF), трансформированная карцинома человека (HEp-2) и эпителий легкого норки (MLE) будут прилипать к волокнам и размножаться на них.[58][59]
Каркасы из нановолокна используются в инженерии костной ткани для имитации естественного внеклеточного матрикса костей.[7] Костная ткань располагается либо в компактный или трабекулярный узор и состоит из организованных структур, длина которых варьируется от сантиметрового диапазона до нанометрового масштаба. Неминерализованный органический компонент (т.е. коллаген 1 типа ), минерализованный неорганический компонент (т.е. гидроксиапатит ), и многие другие неколлагеновые матричные белки (т.е. гликопротеины и протеогликаны ) составляют нанокомпозитную структуру костного ВКМ.[56] Волокна органического коллагена и неорганические минеральные соли придают ЭЦМ гибкость и прочность, соответственно.
Хотя кость представляет собой динамическую ткань, которая может самовосстанавливаться при незначительных травмах, она не может восстанавливаться после возникновения крупных дефектов, таких как опухоль кости. резекции и тяжелые несращенные переломы из-за отсутствия соответствующего шаблона.[1][7] В настоящее время стандартным лечением является аутотрансплантация который включает в себя получение донорской кости из незначительного и легкодоступного участка (т.е. гребень подвздошной кости ) в собственном теле пациента и пересадив его на дефектный участок. Трансплантация аутологичной кости дает наилучший клинический результат, поскольку она надежно интегрируется с костью хозяина и позволяет избежать осложнений для иммунной системы.[60] Но его использование ограничено его дефицитом и заболеваемостью донорских участков, связанных с процедурой сбора урожая.[56] Кроме того, кости с автографом бессосудистый и, следовательно, зависят от распространение на питательные вещества, что влияет на их жизнеспособность в организме хозяина.[60] Трансплантаты также можно рассасывать перед остеогенез является полным из-за высокой скорости ремоделирования в организме.[56][60] Еще одна стратегия лечения серьезных повреждений костей: аллотрансплантация который пересаживает кости, извлеченные из трупа человека. Однако аллотрансплантаты создают у хозяина риск заболевания и инфекции.[60]
Инженерия костной ткани представляет собой универсальный способ лечения травм и деформаций костей. Нановолокна, полученные с помощью электропрядения, особенно хорошо имитируют архитектуру и характеристики естественного внеклеточного матрикса. Эти каркасы можно использовать для доставки биоактивных агентов, способствующих регенерации тканей.[2] Эти биоактивные материалы в идеале должны быть остеоиндуктивный, остеокондуктивный, и остеоинтегрируемый.[56] Материалы для замены костной ткани, предназначенные для замены аутологичной или аллогенной кости, состоят из биоактивной керамики, биоактивных стекол, а также биологических и синтетических полимеров. Основа инженерии костной ткани заключается в том, что материалы будут рассасываться и со временем заменяться собственной недавно регенерированной биологической тканью организма.[57]
Тканевая инженерия не ограничивается только костью: большое количество исследований посвящено хрящам,[61] связка[62] скелетная мышца,[63] кожа[64] кровеносный сосуд,[65] и инженерия нервной ткани[66] также.
Доставка наркотиков

Успешная доставка терапевтических средств к намеченной цели во многом зависит от выбора носителя лекарственного средства. Критерии идеального препарат, средство, медикамент носитель включает максимальный эффект при доставке лекарственного средства к целевому органу, уклонение от иммунной системы организма в процессе достижения органа, удержание терапевтических молекул от подготовительных стадий до конечной доставки лекарственного средства и правильное высвобождение препарат для оказания намеченного терапевтического эффекта.[8] Нановолокна изучаются как возможные кандидаты в носители лекарственных средств.[9][10][67] Природные полимеры, такие как желатин и альгинат, являются хорошими производственными биоматериалами для нановолокон-носителей из-за их биосовместимость и биоразлагаемость в результате не причиняется вреда ткани хозяина и не происходит накопления токсинов в организме человека, соответственно. Благодаря цилиндрической морфологии нановолокна обладают высоким отношением площади поверхности к объему. В результате волокна обладают высокой способностью загружать лекарственное средство и могут высвобождать терапевтические молекулы на большой площади поверхности.[8][44] В то время как отношение площади поверхности к объему можно контролировать только путем регулирования радиуса сферических везикул, нановолокна имеют больше степеней свободы в управлении соотношением за счет изменения как длины, так и радиуса поперечного сечения. Эта возможность регулирования важна для их применения в системах доставки лекарств, в которых необходимо точно контролировать функциональные параметры.[8]
Предварительные исследования показывают, что антибиотики и противоопухолевые препараты могут быть инкапсулированы в нановолокна, полученные методом электропрядения, путем добавления лекарства в раствор полимера перед электропрядением.[68][69] Каркасы из нановолокна с поверхностной нагрузкой полезны в качестве барьеров для адгезии между внутренними органами и тканями после операции.[70][71] Сращение происходит во время процесса заживления и может вызвать такие осложнения, как хроническая боль и неудача повторной операции.[70][71][72]
Диагноз рака
Несмотря на то что патологическое обследование это текущий стандартный метод определения молекулярных характеристик при тестировании на наличие биомаркеры Что касается опухолей, то эти анализы на одном образце не учитывают разнообразную геномную природу опухолей.[15] Учитывая инвазивный характер, психологический стресс и финансовое бремя, возникающее в результате повторных биопсий опухоли у пациентов, биомаркеры, которые можно оценить с помощью минимально инвазивных процедур, таких как забор крови, представляют собой возможность для прогресса в точной медицине.
Жидкая биопсия - вариант, который становится все более популярным в качестве альтернативы биопсии солидной опухоли.[15][16] Это просто анализ крови, содержащий циркулирующие опухолевые клетки (ЦКО), которые попадают в кровоток из солидных опухолей. Пациенты с метастатический рак с большей вероятностью обнаруживают ЦОК в кровотоке, но ЦОК также существуют у пациентов с локализованными заболеваниями. Было обнаружено, что количество ЦКО, присутствующих в кровотоке пациентов с метастатическим раком предстательной железы и колоректальным раком, является прогностическим фактором общей выживаемости опухолей.[17][73] Также было продемонстрировано, что ЦКО влияют на прогноз на более ранних стадиях заболевания.[74]

Недавно Ke et al. разработали чип NanoVelcro, который улавливает ЦОК из образцов крови.[16] Когда кровь проходит через чип, нановолокна, покрытые белковыми антителами, связываются с белками, экспрессируемыми на поверхности раковых клеток, и действуют как липучки, улавливая ЦКО для анализа. Анализы NanoVelcro CTC прошли три поколения развития. Чип NanoVelcro первого поколения был создан для подсчета ЦКО для прогноза, определения стадии и динамического мониторинга рака.[75] NanoVelcro-LCM второго поколения был разработан для выделения одноклеточных ЦКО.[76][77] Индивидуально изолированные ЦОК можно подвергнуть генотипированию по одному ЦКО. Чип Thermoresponsive Chip третьего поколения позволяет очищать CTC.[16][78] Щетки из нановолоконных полимеров претерпевают зависящие от температуры конформационные изменения для захвата и высвобождения CTC.
Литий-воздушный аккумулятор
Среди многих современных электрохимических накопителей энергии, перезаряжаемые литий-воздушные батареи представляют особый интерес из-за их значительной способности аккумулировать энергию и высокой удельной мощности.[18][19] Поскольку батарея используется, литиевая ионы соединяться с кислородом воздуха с образованием частиц оксиды лития, которые прикрепляются к углеродные волокна на электроде. Во время перезарядки оксиды лития снова разделяются на литий и кислород, который возвращается в атмосферу. Эта последовательность преобразования крайне неэффективна, поскольку существует значительная разница напряжений более 1,2 В между выходным напряжением и напряжением зарядки аккумулятора, что означает, что примерно 30% электроэнергии теряется в виде тепла, когда аккумулятор заряжается.[18] Кроме того, большие объемные изменения в результате непрерывного преобразования кислорода между его газообразным и твердым состоянием создают нагрузку на электрод и ограничивают его срок службы.

Производительность этих батарей зависит от характеристик материала, из которого изготовлен катод. Углеродные материалы широко используются в качестве катодов из-за их превосходной электропроводности, большой площади поверхности и химической стабильности.[20][79] Углеродные материалы, особенно актуальные для литий-воздушных батарей, служат подложками для поддержки оксидов металлов. Нановолокна из электропряденого углерода без связующего являются особенно хорошими потенциальными кандидатами для использования в электродах в литий-кислородных батареях, поскольку они не имеют связующих, имеют открытые макропористые структуры, содержат углерод, который поддерживает и катализирует реакции восстановления кислорода, и обладают универсальностью.[80]
Zhu et al. разработали новый катод, который может накапливать литий и кислород в электроде, который они назвали нанолитием, который представляет собой матрицу углеродных нановолокон, периодически заделанных оксид кобальта.[81] Эти оксиды кобальта придают стабильность обычно нестабильному супероксидсодержащему нанолитию. В этой конструкции кислород хранится в виде LiO.2 и не переходит из газообразной формы в твердую во время зарядки и разрядки. Когда батарея разряжается, ионы лития в нанолитии реагируют с супероксидным кислородом матрицы с образованием Li.2О2, и Ли2О. Кислород остается в твердом состоянии при переходе между этими формами. Химические реакции этих переходов дают электрическую энергию. Во время зарядки переходы происходят в обратном порядке.
Оптические датчики
Полимерные оптические волокна вызывают растущий интерес в последние годы.[21][22] Из-за невысокой стоимости, простоты обращения, долгого длина волны Прозрачность, большая гибкость и биосовместимость, полимерные оптические волокна демонстрируют большой потенциал для сетей на малых расстояниях, оптического зондирования и подачи энергии.[23][82]
Нановолокна электроспрядения особенно хорошо подходят для оптических сенсоров, поскольку чувствительность сенсора увеличивается с увеличением площади поверхности на единицу массы. Оптическое зондирование работает путем обнаружения интересующих ионов и молекул через механизм тушения флуоресценции. Wang et al. успешно разработанные нановолоконные тонкопленочные оптические сенсоры для ионов металлов (Fe3+ и Hg2+) и 2,4-динитротолуол (DNT) обнаружение методом электроспиннинга.[21]
Квантовые точки демонстрируют полезные оптические и электрические свойства, включая высокое оптическое усиление и фотохимический стабильность. Разнообразие квантовые точки были успешно включены в полимерные нановолокна.[83] Meng et al. показали, что датчик из полимерного нановолокна с квантовыми точками для определения влажности демонстрирует быстрый отклик, высокую чувствительность и долгосрочную стабильность при низком потреблении энергии.[84]
Kelly et al. разработали датчик, который предупреждает сотрудников службы экстренного реагирования, когда угольные фильтры в их респираторах насыщаются токсичными частицами дыма.[24] Респираторы обычно содержат активированный древесный уголь который задерживает переносимые по воздуху токсины. Когда фильтры насыщаются, через них начинают проходить химические вещества, и респираторы становятся бесполезными. Чтобы легко определить, когда фильтр закончился, Келли и его команда разработали маску, оснащенную датчиком, состоящим из углеродных нановолокон, собранных в повторяющиеся структуры, называемые фотонные кристаллы отражающие световые волны определенной длины. Датчики имеют переливающийся цвет, который меняется, когда волокна поглощают токсины.
Фильтрация воздуха

Нановолокна электропрядения полезны для удаления летучие органические соединения (VOC) из атмосферы. Scholten et al. показали, что адсорбция и десорбция ЛОС с помощью электропряденой нановолоконной мембраны были быстрее, чем у обычного активированного угля.[25]
Загрязнение воздуха в кабинах для персонала горнодобывающего оборудования вызывает озабоченность у горняков, горнодобывающих компаний и государственных учреждений, таких как Управление по безопасности и охране здоровья в шахтах (MSHA). Недавняя работа с производителями горнодобывающего оборудования и MSHA показала, что фильтрующий материал из нановолокна может снизить концентрацию пыли в салоне в большей степени по сравнению со стандартным целлюлоза фильтр СМИ.[26]
Нановолокна могут использоваться в масках для защиты людей от вирусы, бактерии, смог, пыль, аллергены и другие частицы. Эффективность фильтрации составляет около 99,9%, а принцип фильтрации - механический. Частицы в воздухе крупнее пор в полотне из нановолокна, но кислород частицы достаточно малы, чтобы пройти.
Разделение масла и воды
Нановолокна обладают способностью отделять масло от воды, особенно в процессе сорбции, когда используемый материал имеет олеофильные и гидрофобные поверхности. Эти характеристики позволяют использовать нановолокна в качестве средства борьбы либо с масляными сточными водами от бытовых и промышленных предприятий, либо с нефтесодержащей морской водой из-за утечки нефти в океан при транспортировке нефти и очистке нефтяных резервуаров на судне.[36]
Спортивная одежда текстиль
Текстиль для спортивной одежды с мембраной из нановолокна внутри основан на современной технологии нановолокна, в которой ядро мембраны состоит из волокон диаметром в 1000 раз тоньше человеческого волоса. Это чрезвычайно плотное «сито» с более чем 2,5 миллиардами пор на квадратный сантиметр намного эффективнее удаляет пар и обеспечивает лучший уровень водонепроницаемости. Говоря языком цифр, текстиль из нановолокна имеет следующие параметры:
· Паропроницаемость RET 1.0 и 10 000 мм водяного столба (вариант с воздухопроницаемостью)
· Паропроницаемость RET 4.8 и 30 000 мм водяного столба (вариант с большей водонепроницаемостью)
Одежда и обувные мембраны из нановолокна состоят из полиуретан поэтому его производство не наносит вреда природе. Мембраны к спортивной одежде из нановолокна бывают перерабатываемый.
Смотрите также
использованная литература
- ^ а б c d е ж г час я j k Васита Р., Катти Д.С. (2006). «Нановолокна и их применение в тканевой инженерии». Международный журнал наномедицины. 1 (1): 15–30. Дои:10.2147 / нано.2006.1.1.15. ЧВК 2426767. PMID 17722259.
- ^ а б c d е ж г час я j k л Хаджави Р., Аббасипур М., Бахадор А. (2016). «Каркасы из биодеградируемых нановолокон из электропрядения для инженерии костной ткани». J Appl Polym Sci. 133 (3): н / д. Дои:10.1002 / app.42883.
- ^ Тераока I (2002). Полимерные растворы: введение в физические свойства. John Wiley & Sons, Inc. ISBN 978-0-471-22451-8.
- ^ Ренекер Д., Чун И. (1996). «Волокна полимера нанометрового диаметра, полученные методом электроспиннинга». Нанотехнологии. 7 (3): 216–223. Bibcode:1996Nanot ... 7..216R. Дои:10.1088/0957-4484/7/3/009. S2CID 4498522.
- ^ а б c d е Ли Д, Ся Й (2004). «Электроспиннинг нановолокон: изобретать колесо?». Adv Mater. 16 (14): 1151–1170. Дои:10.1002 / adma.200400719.
- ^ Солтани I, Macosko CW (06.06.2018). «Влияние реологии и свойств поверхности на морфологию нановолокон, полученных из нетканых материалов, полученных аэродинамическим способом из расплава на островах в море». Полимер. 145: 21–30. Дои:10.1016 / j.polymer.2018.04.051. ISSN 0032-3861.
- ^ а б c d е Ма П.Х., Чжан Р. (июль 1999 г.). «Синтетический наноразмерный волокнистый внеклеточный матрикс». Журнал исследований биомедицинских материалов. 46 (1): 60–72. Дои:10.1002 / (sici) 1097-4636 (199907) 46: 1 <60 :: aid-jbm7> 3.0.co; 2-ч.. HDL:2027.42/34415. PMID 10357136.
- ^ а б c d Шарифи Ф., Соорияраччи А.С., Алтурал Н, Монтазами Р., Райландер М.Н., Хашеми Н. (2016). «Волоконно-оптические подходы как системы доставки лекарств». ACS Biomater Sci Eng. 2 (9): 1411–1431. Дои:10.1021 / acsbiomaterials.6b00281.
- ^ а б Ан С.Ю., Мун СН, Ли С.Х. (2015). «Микрожидкостное прядение волокнистого альгинатного носителя, имеющего значительно улучшенную способность загрузки лекарственного средства и профиль замедленного высвобождения». RSC Adv. 5 (20): 15172–15181. Дои:10.1039 / C4RA11438H.
- ^ а б Гарг Т., Рат Дж., Гоял А.К. (апрель 2015 г.). «Каркас из нановолокна на основе биоматериалов: целевой и контролируемый носитель для доставки клеток и лекарств». Журнал нацеливания на лекарства. 23 (3): 202–21. Дои:10.3109 / 1061186X.2014.992899. PMID 25539071. S2CID 8398004.
- ^ Кампанья Дж. М., Ариас М (2020-10-28). «Нановолокна как система доставки арбускулярных микоризных грибов». Прикладные полимерные материалы ACS. Дои:10.1021 / acsapm.0c00874.
- ^ Фариас Б.В., Пирзада Т., Мэтью Р., Сит Т.Л., Опперман К., Хан С.А. (2019-12-16). «Электроспряденные полимерные нановолокна в качестве покрытий семян для защиты сельскохозяйственных культур». ACS Устойчивая химия и инженерия. 7 (24): 19848–19856. Дои:10.1021 / acssuschemeng.9b05200.
- ^ Сюй Т., Ма Ц., Айтач З., Ху Х, Нг К.В., Уайт Джей Си, Демокриту П. (2020-06-29). «Улучшение агрохимической доставки и развития рассады с помощью биоразлагаемых, настраиваемых покрытий для семян из нановолокна на основе биополимеров». ACS Устойчивая химия и инженерия. 8 (25): 9537–9548. Дои:10.1021 / acssuschemeng.0c02696.
- ^ Де Грегорио П.Р., Михавила Г., Риккарди Мюллер Л., де Соуза Борхес С., Помарес М.Ф., Сакколь де Са Эль и др. (2017-05-04). «Полезные ризобактерии, иммобилизованные в нановолокнах, для потенциального применения в качестве биоинокулянтов семян сои». PLOS One. 12 (5): e0176930. Дои:10.1371 / journal.pone.0176930. ЧВК 5417607. PMID 28472087.
- ^ а б c Chen JF, Zhu Y, Lu YT, Hodara E, Hou S, Agopian VG и др. (2016). «Клиническое применение анализов редких клеток NanoVelcro для обнаружения и характеристики циркулирующих опухолевых клеток». Тераностика. 6 (9): 1425–39. Дои:10.7150 / thno 15359. ЧВК 4924510. PMID 27375790.
- ^ а б c d Ke Z, Lin M, Chen JF, Choi JS, Zhang Y, Fong A и др. (Январь 2015 г.). «Программирование термореактивности субстратов NanoVelcro позволяет эффективно очищать циркулирующие опухолевые клетки у пациентов с раком легкого». САУ Нано. 9 (1): 62–70. Дои:10.1021 / nn5056282. ЧВК 4310634. PMID 25495128.
- ^ а б Cristofanilli M, Hayes DF, Budd GT, Ellis MJ, Stopeck A, Reuben JM и др. (Март 2005 г.). «Циркулирующие опухолевые клетки: новый прогностический фактор для вновь диагностированного метастатического рака груди». Журнал клинической онкологии. 23 (7): 1420–30. Дои:10.1200 / JCO.2005.08.140. PMID 15735118.
- ^ а б c Чжан Б., Кан Ф., Тараскон Дж. М., Ким Дж. К. (2016). «Последние достижения в области электропряденых углеродных нановолокон и их применение в электрохимическом накоплении энергии». Prog Mater Sci. 76: 319–380. Дои:10.1016 / j.pmatsci.2015.08.002.
- ^ а б «Литий-воздушные батареи: их время пришло». Экономист. 6 августа 2016 г.
- ^ а б Ян Х, Хэ П, Ся Й (2009). «Приготовление мезоячеистой угольной пены и ее применение для литиево-кислородной батареи». Electrochem Commun. 11 (6): 1127–1130. Дои:10.1016 / j.elecom.2009.03.029.
- ^ а б c Ван Х, Дрю С., Ли С.Х., Сенекал К.Дж., Кумар Дж., Самуэльсон Л.А. (2002). «Электроспрядные нановолоконные мембраны для высокочувствительных оптических сенсоров». Nano Lett. 2 (11): 1273–1275. Bibcode:2002NanoL ... 2,1273 Вт. CiteSeerX 10.1.1.459.8052. Дои:10.1021 / nl020216u.
- ^ а б Ян Цзянь, Цзян X, Гу Ф, Ма З, Чжан Дж, Тонг Л. (2008). «Полимерные микро- или нановолокна для применения в оптических устройствах». J Appl Polym Sci. 110 (2): 1080–1084. Дои:10.1002 / app.28716.
- ^ а б Зубиа Дж, Арру Дж (2001). «Пластиковые оптические волокна: введение в их технологические процессы и области применения». Оптоволоконная технология. 7 (2): 101–140. Bibcode:2001OptFT ... 7..101Z. Дои:10.1006 / оф.2000.0355.
- ^ а б Келли Т.Л., Гао Т., Матрос MJ (апрель 2011 г.). «Углеродные и углеродно-кремниевые композиты, используемые в фильтрах ругат для адсорбции и обнаружения органических паров». Передовые материалы. 23 (15): 1776–81. Дои:10.1002 / adma.201190052. PMID 21374740.
- ^ а б Scholten E, Bromberg L, Rutledge GC, Hatton TA (октябрь 2011 г.). «Электропряденые полиуретановые волокна для поглощения летучих органических соединений из воздуха». Прикладные материалы и интерфейсы ACS. 3 (10): 3902–9. Дои:10.1021 / am200748y. HDL:1721.1/81271. PMID 21888418.
- ^ а б Грэм К., Оуян М., Рэтер Т., Граф Т., Макдональд Б., Кнауф П. (2002). «Полимерные нановолокна в системах фильтрации воздуха». Пятнадцатая ежегодная техническая конференция и выставка Американского общества фильтрации и разделения.
- ^ а б Насименто М.Л., Араужу Е.С., Кордейро Э.Р., де Оливейра А.Х., де Оливейра Х.П. (2015). «Литературное исследование электропрядения и нановолокон: исторические тенденции, текущее состояние и будущие задачи». Последние патенты на нанотехнологии. 9 (2): 76–85. Дои:10.2174/187221050902150819151532. PMID 27009122.
- ^ а б c Такер Н., Стангер Дж. Дж., Стайгер МП, Раззак Х, Хофман К. (2012). «История науки и техники электроспиннинга с 1600 по 1995 год» (PDF). J Eng Fiber Fabr. 7: 63–73.
- ^ Гилберт В. (1600). "De magnete, magnetisque corporibus, et de magno magnete tellure". Цитировать журнал требует
| журнал =(Помогите) - ^ Тейлор Г (1964). «Распад капель воды в электрическом поле». Труды Королевского общества А. 280 (1382): 383–39 7. Bibcode:1964RSPSA.280..383T. Дои:10.1098 / rspa.1964.0151. S2CID 15067908.
- ^ Strutt J (1882). «О равновесии жидких проводящих масс, заряженных электричеством, Лондон, Эдинбург и Дублин». Филос. Mag. 14 (87): 184–186. Дои:10.1080/14786448208628425.
- ^ Мальчики С (1887 г.). «О производстве, свойствах и некоторых предлагаемых вариантах использования лучших нитей». Филос. Mag. 23 (145): 489–499. Дои:10.1080/14786448708628043.
- ^ Кули Дж. «Усовершенствованные способы и устройство для электрического отделения относительно летучего жидкого компонента от компонента относительно фиксированных веществ композитных жидкостей». Espacenet.
- ^ Гарольд С. «Способ и устройство для производства узорчатых нетканых материалов». Espacenet.
- ^ Lolla D, Gorse J, Kisielowski C, Miao J, Taylor PL, Chase GG, Reneker DH (январь 2016 г.). «Молекулы поливинилиденфторида в нановолокнах, полученные в атомном масштабе с помощью электронной микроскопии с коррекцией аберраций». Наномасштаб. 8 (1): 120–8. Bibcode:2015Нано ... 8..120л. Дои:10.1039 / C5NR01619C. PMID 26369731.
- ^ а б Сарбатлы Р., Кришнаия Д., Камин З. (май 2016 г.). «Обзор полимерных нановолокон методом электроспиннинга и их применения в разделении нефти и воды для очистки морских разливов нефти». Бюллетень загрязнения морской среды. 106 (1–2): 8–16. Дои:10.1016 / j.marpolbul.2016.03.037. PMID 27016959.
- ^ Сиван М., Мадхесваран Д., Асадиан М., Коулс П., Туккарам М., Ван Дер Воорт П., Морент Р., Де Гейтер Н., Лукас Д. (2020-10-15). «Влияние плазменной обработки на объемные свойства нановолоконных матов из поликапролактона, изготовленных необычным методом электроспиннинга на переменном токе: сравнительное исследование». Технология поверхностей и покрытий. 399: 126203. Дои:10.1016 / j.surfcoat.2020.126203. ISSN 0257-8972.
- ^ Гарг К., Боулин Г.Л. (март 2011 г.). «Электропрядильные форсунки и нановолоконные конструкции». Биомикрофлюидика. 5 (1): 13403. Дои:10.1063/1.3567097. ЧВК 3082340. PMID 21522493.
- ^ Ким К.В., Ли К.Х., Хил М.С., Хо Ю.С., Ким Х.Й. (2004). «Влияние молекулярной массы и линейной скорости поверхности барабана на свойства нетканых материалов из электропряденого полиэтилентерефталата». Волокна Polym. 5 (2): 122–127. Дои:10.1007 / BF02902925. S2CID 137021572.
- ^ Дерш Р., Лю Т., Шапер А. К., Грейнер А., Вендорф Дж. Х. (2003). «Электросрядные нановолокна: внутренняя структура и внутренняя ориентация». Polym Chem. 41 (4): 545–553. Bibcode:2003JPoSA..41..545D. Дои:10.1002 / pola.10609.
- ^ Бичли V, Вен X (апрель 2009 г.). «Влияние параметров электроспиннинга на диаметр и длину нановолокна». Материаловедение и инженерия. C, Материалы для биологических приложений. 29 (3): 663–668. Дои:10.1016 / j.msec.2008.10.037. ЧВК 3065832. PMID 21461344.
- ^ Leach MK, Feng ZQ, Tuck SJ, Corey JM (январь 2011 г.). «Основы электропрядения: оптимизация параметров раствора и аппарата». Журнал визуализированных экспериментов. 47 (47): 2494. Дои:10.3791/2494. ЧВК 3182658. PMID 21304466.
- ^ а б c d Хуанг З.М., Чжан Ю.З., Котаки М., Рамакришна С. (2003). «Обзор полимерных нановолокон методом электроспиннинга и их применения в нанокомпозитах». Compos Sci Technol. 63 (15): 2223–2253. Дои:10.1016 / S0266-3538 (03) 00178-7.
- ^ а б c Ченг Дж., Джун Й., Цинь Дж., Ли Ш. (январь 2017 г.). «Электроспиннинг против микрофлюидного прядения функциональных волокон для биомедицинских приложений». Биоматериалы. 114: 121–143. Дои:10.1016 / j.biomaterials.2016.10.040. PMID 27880892.
- ^ а б c Ма, П. (2004). «Каркасы для изготовления тканей». Материалы сегодня. 7 (5): 30–40. Дои:10.1016 / S1369-7021 (04) 00233-0.
- ^ Рамакришна С. и др. (2005). Введение в электроспиннинг и нановолокна. World Scientific. ISBN 978-981-256-415-3.
- ^ Ондаркуху Т., Иоахим С. (1998). «Нанесение одного нановолокна на сотни микрон». Europhys Lett. 42 (2): 215–220. Bibcode:1998EL ..... 42..215O. Дои:10.1209 / epl / i1998-00233-9.
- ^ а б Мартин С. (1995). «Шаблонный синтез электронопроводящих полимерных наноструктур». Acc Chem Res. 28 (2): 61–68. Дои:10.1021 / ar00050a002.
- ^ а б Мартин ЧР (декабрь 1994 г.). «Наноматериалы: синтетический подход на основе мембран». Наука. 266 (5193): 1961–6. Bibcode:1994Научный ... 266.1961М. Дои:10.1126 / science.266.5193.1961. PMID 17836514. S2CID 45456343.
- ^ Малкар Н.Б., Лауэр-Филдс Дж. Л., Юска Д., Филдс Г. Б. (2003). «Характеристика пептидов-амфифилов, обладающих последовательностями активации клеток». Биомакромолекулы. 4 (3): 518–28. Дои:10.1021 / bm0256597. PMID 12741765.
- ^ Чжан Ц., Сюэ Х, Ло Ц., Ли И, Ян К., Чжуан Х и др. (Ноябрь 2014 г.). «Самособирающиеся пептидные нановолокна, разработанные как биологические ферменты для катализирования гидролиза сложного эфира». САУ Нано. 8 (11): 11715–23. Дои:10.1021 / nn5051344. PMID 25375351.
- ^ Ши Ю. Р., Чен С. Н., Цай С. В., Ван Ю. Дж., Ли ОК (ноябрь 2006 г.). «Рост мезенхимальных стволовых клеток на электропряденых коллагеновых нановолокнах I типа». Стволовые клетки. 24 (11): 2391–7. Дои:10.1634 / стволовые клетки.2006-0253. PMID 17071856.
- ^ Ким К.Х., Чон Л., Пак Х.Н., Шин С.И., Пак У.Х., Ли С.К. и др. (Ноябрь 2005 г.). «Биологическая эффективность мембран из нановолокон из фиброина шелка для направленной регенерации кости». Журнал биотехнологии. 120 (3): 327–39. Дои:10.1016 / j.jbiotec.2005.06.033. PMID 16150508.
- ^ а б Азими Б., Нурпанах П., Раби М., Арбаб С. (2014). «Поли (ε-капролактон) волокно: обзор». J Eng Fiber Fabr. 9 (3): 74–90.
- ^ Хиджази Ф., Мирзаде Х. (сентябрь 2016 г.). «Новый 3D каркас с улучшенными физическими характеристиками и характеристиками клеточного ответа для регенерации костной ткани, изготовленный методом электроспиннинга / электрораспыления». Журнал материаловедения. Материалы в медицине. 27 (9): 143. Дои:10.1007 / s10856-016-5748-8. PMID 27550014. S2CID 23987237.
- ^ а б c d е Бург К.Дж., Портер С., Келлам Дж.Ф. (декабрь 2000 г.). «Разработка биоматериалов для инженерии костной ткани». Биоматериалы. 21 (23): 2347–59. Дои:10.1016 / s0142-9612 (00) 00102-2. PMID 11055282.
- ^ а б Сунь Б., Лонг Й.З., Чжан Х.Д., Ли ММ, Дувайл Д.Л., Цзян XY, Инь Х.Л. (2014). «Достижения в трехмерных нановолоконных макроструктурах с помощью электроспиннинга». Pro Polym Sci. 39 (5): 862–890. Дои:10.1016 / j.progpolymsci.2013.06.002.
- ^ Саймон, Эрик М. (1988). «ИТОГОВЫЙ ОТЧЕТ NIH, ФАЗА I: ВОЛОКОННЫЕ СУБСТРАТЫ ДЛЯ КУЛЬТУРЫ КЛЕТОК (R3RR03544A) (доступна загрузка PDF-файла)». ResearchGate. Получено 2017-05-22.
- ^ Сукумар Великобритания, Packirisamy G (2019-10-08). "Изготовление нанофиброзного каркаса, привитого с помощью микросфер полистирола, функционализированного желатином, для проявления наномеханических сигналов стимулированного растяжением фибробласта". ACS Applied Bio Materials. 2 (12): 5323–5339. Дои:10.1021 / acsabm.9b00580.
- ^ а б c d Бец Р.Р. (май 2002 г.). «Ограничения аутотрансплантата и аллотрансплантата: новые синтетические решения». Ортопедия. 25 (5 Прил.): S561-70. Дои:10.3928/0147-7447-20020502-04. PMID 12038843.
- ^ Тули Р., Ли В. Дж., Туан Р. С. (2003). «Современное состояние инженерии хрящевой ткани». Исследования и лечение артрита. 5 (5): 235–8. Дои:10.1186 / ar991. ЧВК 193737. PMID 12932283.
- ^ Лин В.С., Ли М.К., О'Нил С., Маккин Дж., Сунг К.Л. (октябрь 1999 г.). «Инженерия связочной ткани с использованием каркасов из синтетических биоразлагаемых волокон». Тканевая инженерия. 5 (5): 443–52. Дои:10.1089 / десять.1999.5.443. PMID 10586100.
- ^ Рибольди С.А., Сампаолези М., Нойеншвандер П., Коссу Г., Мантеро С. (август 2005 г.). «Электроспрядные разлагаемые полиэфируретановые мембраны: потенциальные основы для инженерии тканей скелетных мышц». Биоматериалы. 26 (22): 4606–15. Дои:10.1016 / j.biomaterials.2004.11.035. PMID 15722130.
- ^ Мэтьюз Дж. А., Винек Г. Е., Симпсон Д. Г., Боулин Г. Л. (2002). «Электроспиннинг коллагеновых нановолокон». Биомакромолекулы. 3 (2): 232–8. Дои:10.1021 / bm015533u. PMID 11888306.
- ^ Мо XM, Сюй CY, Котаки М., Рамакришна С. (май 2004 г.). «Нановолокно Electrospun P (LLA-CL): биомиметический внеклеточный матрикс для пролиферации гладкомышечных и эндотелиальных клеток». Биоматериалы. 25 (10): 1883–90. Дои:10.1016 / j.biomaterials.2003.08.042. PMID 14738852.
- ^ Ян Ф, Сюй Си, Котаки М, Ван С., Рамакришна С. (2004). «Характеристика нервных стволовых клеток на нановолоконном каркасе из электроспенного поли (L-молочной кислоты)». Журнал науки о биоматериалах. Полимерное издание. 15 (12): 1483–97. Дои:10.1163/1568562042459733. PMID 15696794. S2CID 2990409.
- ^ Fogaça R, Ouimet MA, Catalani LH, Uhrich KE (2013). Поли (ангидрид-эфиры) и смеси на биоактивной основе для контролируемой доставки лекарств. Американское химическое общество. ISBN 9780841227996.
- ^ Ху Х, Лю С., Чжоу Г, Хуан И, Се З, Цзин Х (июль 2014 г.). «Электроспиннинг полимерных нановолокон для приложений доставки лекарств». Журнал контролируемого выпуска. 185: 12–21. Дои:10.1016 / j.jconrel.2014.04.018. PMID 24768792.
- ^ Ю ХС, Ким Т.Г., Пак Т.Г. (октябрь 2009 г.). «Поверхностно-функциональные электропряденые нановолокна для тканевой инженерии и доставки лекарств». Расширенные обзоры доставки лекарств. 61 (12): 1033–42. Дои:10.1016 / j.addr.2009.07.007. PMID 19643152.
- ^ а б Zong X, Li S, Chen E, Garlick B, Kim KS, Fang D и др. (Ноябрь 2004 г.). «Профилактика послеоперационных спаек брюшной полости с помощью электропряденых биоабсорбируемых нановолоконных мембран на основе сополимера лактида и гликолида». Анналы хирургии. 240 (5): 910–5. Дои:10.1097 / 01.sla.0000143302.48223.7e. ЧВК 1356499. PMID 15492575.
- ^ а б Кумбар С.Г., Наир Л.С., Бхаттачарья С., Лоренсин СТ (2006). «Полимерные нановолокна как новые носители для доставки терапевтических молекул». Журнал нанонауки и нанотехнологий. 6 (9–10): 2591–607. Дои:10.1166 / jnn.2006.462. PMID 17048469.
- ^ Игнатова М., Рашков И., Манолова Н. (апрель 2013). «Электропряденые материалы с лекарственными препаратами для перевязки ран и местного лечения рака». Мнение эксперта по доставке лекарств. 10 (4): 469–83. Дои:10.1517/17425247.2013.758103. PMID 23289491. S2CID 24627745.
- ^ Коэн SJ, Punt CJ, Iannotti N, Saidman BH, Sabbath KD, Gabrail NY, et al. (Июль 2008 г.). «Связь циркулирующих опухолевых клеток с опухолевым ответом, выживаемостью без прогрессирования и общей выживаемостью у пациентов с метастатическим колоректальным раком». Журнал клинической онкологии. 26 (19): 3213–21. Дои:10.1200 / JCO.2007.15.8923. PMID 18591556.
- ^ Rack B, Schindlbeck C, Jückstock J, Andergassen U, Hepp P, Zwingers T. и др. (Май 2014 г.). «Циркулирующие опухолевые клетки предсказывают выживаемость у пациентов с раком груди на ранней стадии среднего и высокого риска». Журнал Национального института рака. 106 (5): 1–11. Дои:10.1093 / jnci / dju066. ЧВК 4112925. PMID 24832787.
- ^ Лу Ю.Т., Чжао Л., Шен Кью, Гарсия М.А., Ву Д., Хоу С. и др. (Декабрь 2013). «Чип NanoVelcro для подсчета ЦКО у больных раком простаты». Методы. 64 (2): 144–52. Дои:10.1016 / j.ymeth.2013.06.019. ЧВК 3834112. PMID 23816790.
- ^ Jiang R, Lu YT, Ho H, Li B, Chen JF, Lin M и др. (Декабрь 2015 г.). «Сравнение изолированных циркулирующих опухолевых клеток и биопсий тканей с использованием полногеномного секвенирования при раке простаты». Oncotarget. 6 (42): 44781–93. Дои:10.18632 / oncotarget.6330. ЧВК 4792591. PMID 26575023.
- ^ Zhao L, Lu YT, Li F, Wu K, Hou S, Yu J и др. (Июнь 2013). «Выделение высокочистых циркулирующих опухолевых клеток простаты с помощью микрочипа, встроенного в полимерное нановолокно, для полного секвенирования экзома». Передовые материалы. 25 (21): 2897–902. Дои:10.1002 / adma.201205237. ЧВК 3875622. PMID 23529932.
- ^ Hou S, Zhao H, Zhao L, Shen Q, Wei KS, Suh DY и др. (Март 2013 г.). «Захват и стимулирование высвобождения циркулирующих опухолевых клеток на кремниевых наноструктурах с привитым полимером». Передовые материалы. 25 (11): 1547–51. Дои:10.1002 / adma.201203185. ЧВК 3786692. PMID 23255101.
- ^ Митчелл Р.Р., Галлант Б.М., Томпсон CV, Шао-Хорн Й. (2011). «Электроды из углеродного нановолокна для высокоэнергетических аккумуляторных батарей LiO2». Energy Environ Sci. 4 (8): 2952–2958. Дои:10.1039 / c1ee01496j. S2CID 96799565.
- ^ Сингхал Р., Калра В. (2016). «Не содержащие связующего вещества иерархически пористые углеродные нановолокна, украшенные наночастицами кобальта, в качестве эффективных катодов для литий-кислородных батарей». RSC Adv. 6 (105): 103072–103080. Дои:10.1039 / C6RA16874D.
- ^ Чжу З., Кусима А., Инь З, Ци Л., Амин К., Лу Дж., Ли Дж. (2016). «Анионно-окислительно-восстановительные нанолитовые катоды для литий-ионных аккумуляторов». Энергия природы. 1 (8): 16111. Bibcode:2016 НатЭн ... 116111Z. Дои:10.1038 / nenergy.2016.111. S2CID 366009.
- ^ Петерс К. (2011). «Полимерные оптоволоконные датчики - обзор». Smart Mater Struct. 20 (1): 013002. Bibcode:2011SMaS ... 20a3002P. Дои:10.1088/0964-1726/20/1/013002. S2CID 52238312.
- ^ Лю Х., Эдель Дж. Б., Беллан Л. М., Крейгхед Х. Г. (апрель 2006 г.). «Нановолокна из электропряденого полимера как субволновые оптические волноводы, содержащие квантовые точки». Маленький. 2 (4): 495–9. Дои:10.1002 / smll.200500432. PMID 17193073.
- ^ Мэн Ц., Сяо И, Ван П, Чжан Л., Лю И, Тонг Л. (сентябрь 2011 г.). «Полимерные нановолокна, легированные квантовыми точками, для оптического зондирования». Передовые материалы. 23 (33): 3770–4. Дои:10.1002 / adma.201101392. PMID 21766349.
