Патофизиология астмы - Pathophysiology of asthma
| Патофизиология астмы, | |
|---|---|
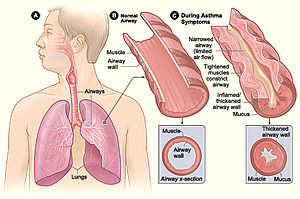 | |
| На рисунке А показано расположение легких и дыхательных путей в организме. На рисунке B показано поперечное сечение нормального дыхательного пути. На рисунке C показано поперечное сечение дыхательных путей во время симптомов астмы. | |
| Специальность | Пульмонология |
Астма является распространенным легочным заболеванием, определяемым хроническим воспалением дыхательных трубок, стягиванием дыхательной гладкой мускулатуры и эпизодами бронхоспазма.[1] По оценкам Центров по контролю и профилактике заболеваний, в Соединенных Штатах Америки астмой болеет 1 из 11 детей и 1 из 12 взрослых.[1] По данным Всемирной организации здравоохранения, астма поражает 235 миллионов человек во всем мире.[2] Есть две основные категории астмы: аллергическая и неаллергическая. В центре внимания этой статьи будет аллергическая астма. В обоих случаях выражен бронхоспазм.[1]
Бронхоспазм


Во время приступа астмы воспалился дыхательные пути реагируют на триггеры окружающей среды, такие как дым, пыль или пыльца. Дыхательные пути сужаются и производят избыток слизь, затрудняющее дыхание. По сути, астма является результатом иммунная реакция в бронхиальный дыхательные пути.[3]
Дыхательные пути больных астмой "сверхчувствительный "для определенных триггеров, также известных как стимулы (Смотри ниже). (Обычно классифицируется как гиперчувствительность I типа.)[4][5] В ответ на воздействие этих триггеров бронхи (крупные воздушные трассы) сокращаются в спазм («приступ астмы»). Воспаление вскоре следует, что приводит к дальнейшему сужению дыхательных путей и чрезмерному слизь производство, которое приводит к кашлю и другим затруднениям дыхания. Бронхоспазм может разрешиться спонтанно через 1–2 часа или примерно у 50% пациентов, он может стать частью «позднего» ответа, когда это начальное поражение следует через 3–12 часов с дальнейшим бронхоспазмом и воспалением.[6]
Нормальный калибр бронхов поддерживается сбалансированным функционированием вегетативной нервной системы, которая действует рефлекторно. В парасимпатический Рефлекторная петля состоит из афферентных нервных окончаний, которые берут начало под внутренней оболочкой бронха. Всякий раз, когда эти афферентные нервные окончания стимулируются (например, пылью, холодным воздухом или парами), импульсы направляются к блуждающему центру ствола головного мозга, а затем вниз по эфферентному пути блуждающего нерва, чтобы снова достичь малых дыхательных путей бронхов. Ацетилхолин высвобождается из эфферентных нервных окончаний. Этот ацетилхолин приводит к избыточному образованию инозитол-1,4,5-трифосфата (IP3) в гладкомышечных клетках бронхов, что приводит к укорочению мышц и вызывает сужение бронхов.
Бронхиальное воспаление
Механизмы аллергической астмы, т. Е. Астмы, возникающей в результате иммунная реакция вдыхать аллергены - наиболее изучены причинные факторы. Как у людей, страдающих астмой, так и у людей, не страдающих этим заболеванием, вдыхаемые аллергены проникают внутрь организма. дыхательные пути находятся проглоченный по типу клетки, известной как антигенпрезентирующие клетки, или БТР. Затем APC «представляют» части аллергена другим иммунная система клетки. У большинства людей эти другие иммунные клетки (ТЧАС0 ячеек ) «проверить» и обычно игнорировать молекулы аллергена. Однако у больных астмой эти клетки преобразовать в клетку другого типа (TЧАС2) по причинам, которые не совсем понятны. Возможной причиной может быть высвобождение интерлейкина-4 тучными клетками, которые вызывают дифференцировку наивных хелперных Т-клеток (Th0-клеток) в Th2-клетки.
Результирующий TЧАС2 клетки активируют важное звено иммунной системы, известное как гуморальная иммунная система. Гуморальная иммунная система производит антитела против вдыхаемого аллергена. Позже, когда пациент вдыхает тот же аллерген, эти антитела «распознают» его и активируют гуморальный ответ. Результат воспаления: вырабатываются химические вещества, которые вызывают утолщение стенки дыхательных путей, клетки, образующие рубцы, размножаются и способствуют дальнейшему `` ремоделированию дыхательных путей '', заставляют продуцирующие слизь клетки увеличиваться в размерах и производить больше и более густой слизи, а клеточно-опосредованные рука иммунной системы активируется. Воспаленные дыхательные пути более гиперреактивны и более подвержены бронхоспазму.
"гипотеза гигиены "постулирует, что дисбаланс в регуляции этих TЧАС Типы клеток в раннем возрасте приводят к долгосрочному преобладанию клеток, участвующих в аллергических реакциях, над теми, которые участвуют в борьбе с инфекцией. Предполагается, что у ребенка, который в раннем возрасте подвергается воздействию микробов, принимает меньше антибиотиков, живет в большой семье и растет в сельской местности, стимулируют TЧАС1 ответ и снизить вероятность развития астмы.[7]
Астма связана с прокоагулянт состояние в бронхоальвеолярном пространстве.[8]
Стимулы
- Аллергены от природы, как правило, вдыхаемые, в том числе отходы от обычных домашних вредителей, клещ домашней пыли и таракан, а также пыльца травы, плесень споры и домашнее животное эпителиальные клетки;[9]
- В помещении загрязнение воздуха из летучие органические соединения, включая парфюмерию и парфюмерию. Примеры включают мыло, посудомоечная жидкость, стиральный порошок, кондиционер для белья, бумажные салфетки, бумажные полотенца, туалетная бумага, шампунь, лак для волос, гель для волос, косметика, крем для лица, крем для загара, дезодорант, одеколон, крем для бритья, лосьон после бритья, освежитель воздуха и свечи, и такие продукты, как масляные краски.[9][10]
- Лекарства, включая аспирин,[11] β-адреноблокаторы (бета-блокаторы),[12] ибупрофен и пенициллин.[13]
- Пищевые аллергии Такие как молоко, арахис, и яйца. Однако астма редко является единственным симптомом, и не все люди с пищевой или другой аллергией страдают астмой. [14]
- Сульфитная чувствительность Астма может возникнуть в результате приема внутрь или вдыхания сульфитов, которые добавляют в пищу и вино в качестве консервантов.[15]
- Чувствительность к салицилатам Салицилаты могут вызывать астму у чувствительных людей. Салицилаты естественным образом содержатся во многих здоровых продуктах питания. Аспирин также является салицилатом.[16]
- Использование ископаемое топливо связанные с аллергенный загрязнение воздуха, Такие как озон, смог, летний смог, диоксид азота, и диоксид серы, что считается одной из основных причин высокой распространенности астмы среди городской области.[10]
- Различные промышленные составы (например, толуолдиизоцианат [17]) и другие химические вещества, в частности сульфиты; хлорированный бассейны генерируют монохлорамин (NH2Cl), дихлорамин (NHCl2) и трихлорамин (NCl3) - в воздухе вокруг них, которые, как известно, вызывают астму.[18]
- Раннее детство инфекции, особенно популярный инфекции верхних дыхательных путей. Дети, страдающие частыми респираторными инфекциями в возрасте до шести лет, подвергаются более высокому риску развития астмы, особенно если у них есть родитель с этим заболеванием. Однако у людей любого возраста астма может быть вызвана: простуды и другие респираторные инфекции, даже если их обычные стимулы могут быть из другой категории (например, пыльца) и отсутствовать во время заражения. Во многих случаях серьезная астма может даже не возникнуть, пока респираторная инфекция не перейдет в стадию угасания и состояние человека, по-видимому, улучшится.[10] У детей наиболее частыми триггерами являются вирусные заболевания, например те, которые вызывают простуда.[19]
- Упражнение или интенсивное использование дыхательной системы - эффекты которых несколько отличаются от эффектов других триггеров, поскольку они кратковременны. Считается, что они возникают в первую очередь в результате воздействия на эпителий дыхательных путей холодного и сухого воздуха.
- Гормональный изменения в подросток девочки и взрослые женщины, связанные с их менструальный цикл может привести к обострению астмы. Некоторые женщины также испытывают обострение астмы во время беременность в то время как другие не находят значительных изменений, а у других женщин астма улучшается во время беременности.[10]
- Психологический стресс. Появляется все больше свидетельств того, что психологический стресс является спусковым крючком. Он может модулировать иммунную систему, вызывая усиленный воспалительный ответ на аллергены и загрязнители.[20]
- Холодная погода может затруднить дыхание пациентам.[21] Вопрос о том, помогает ли большая высота астме или ухудшает ее, остается спорным и может варьироваться от человека к человеку.[22]
- Было показано, что ожирение и системное воспаление ожирения ухудшают функцию легких и увеличивают риск развития обострений астмы.[23]
Патогенез
Основная проблема астмы заключается в следующем: иммунологический: у маленьких детей на ранних стадиях астмы появляются признаки чрезмерного воспаления дыхательных путей. Эпидемиологические данные дать подсказки относительно патогенез: заболеваемость астмой, похоже, растет во всем мире, и теперь астма гораздо более распространена в богатых странах.
В 1968 г. Андор Сентиваньи впервые описал Бета-адренергическая теория астмы; при котором блокада бета-2 рецепторов гладкомышечных клеток легких вызывает астму.[24]Бета-адренергическая теория Сентиваньи - это классика цитирования[25] с использованием Индекс научного цитирования и был процитирован больше раз, чем любая другая статья в истории Журнал аллергии и клинической иммунологии.
В 1995 году Szentivanyi и его коллеги продемонстрировали, что IgE блокирует рецепторы бета-2.[26]Поскольку избыточное производство IgE является центральным фактором всех атопических заболеваний, это был переломный момент в мире аллергии.[27]
Астма и апноэ во сне
Все чаще признается, что пациенты, у которых есть оба обструктивное апноэ во сне и астма часто значительно улучшается, когда апноэ во сне диагностируется и лечится.[28] CPAP не эффективен только у пациентов с ночной астмой.[29]
Астма и гастроэзофагеальная рефлюксная болезнь
Если гастроэзофагеальная рефлюксная болезнь (ГЭРБ), у пациента могут быть повторяющиеся эпизоды аспирации кислоты. ГЭРБ может быть обычным явлением при трудноизлечимой астме, но, согласно одному исследованию, ее лечение не влияет на астму.[30]Когда есть клиническое подозрение на ГЭРБ как на причину астмы, Мониторинг pH пищевода требуется для подтверждения диагноза и установления связи между ГЭРБ и астмой.
Астма и воздействие загрязненного воздуха во время беременности
От астмы страдают от четырех до восьми беременных женщин из ста.[31] Это связано с тем, что во время беременности происходит иммунологический сдвиг из-за гормональных колебаний.[32] В некоторых случаях наблюдается повышение уровня эстрогена, что, в свою очередь, снижает активность естественных клеток-киллеров, выработку воспалительных цитокинов клетками Th1 и выработку противовоспалительных цитокинов.[32] Как мы видели, они играют важную роль в патофизиологии астмы.
Исследователи обнаружили связь между преждевременными родами и воздействием загрязненного воздуха у беременных, страдающих астмой.[33] Результаты показали, что женщины, страдающие астмой, имеют более высокий риск преждевременных родов.[33] Исследователи предположили, что приступы астмы у беременных женщин были связаны с продолжающимся воздействием двуокиси азота и окиси углерода - типов загрязнителей воздуха.[33]
Исследователи также изучали, когда женщины наиболее подвержены развитию астмы. Данные показали, что женщины подвергались более высокому риску развития астмы при воздействии загрязнителей до зачатия и во время беременности.[33] В частности, «увеличение воздействия оксида азота на 30 частей на миллиард (частей на миллиард) за три месяца до беременности увеличило риск преждевременных родов почти на 30 процентов для женщин с астмой по сравнению с 8 процентами для женщин без астмы».[33]
В других исследованиях ученые обнаружили связь между астмой у детей и пренатальным воздействием загрязненного воздуха. Результаты исследования, в котором участвовало 65000 канадских детей, показали, что у детей матерей, живших рядом с шоссе во время беременности, риск развития астмы в возрасте до пяти лет повышен на 25% по сравнению с детьми матерей, которые не жили рядом с шоссе.[34] Автомагистрали являются основным источником загрязнения воздуха, связанного с дорожным движением, так как в непосредственной близости от автомагистралей происходит накопление таких загрязнителей воздуха, как двуокись азота и окись углерода (выбрасываемые транспортными средствами).[34]
В другом исследовании ученые собрали данные о 6000 детей, посещающих государственные школы Калифорнии. Результаты показали, что высокая подверженность пренатальному загрязнению воздуха сильно коррелировала с повышенной предрасположенностью к астме в детстве.[35]
Рекомендации
- ^ а б c Цзян, Лань; Диас, Филип Т .; Бест, Томас М .; Stimpfl, Julia N .; Он, Фэн; Цзо, Ли (2014). «Молекулярная характеристика окислительно-восстановительных механизмов при аллергической астме». Анналы аллергии, астмы и иммунологии. 113 (2): 137–142. Дои:10.1016 / j.anai.2014.05.030. PMID 24986036.

- ^ «Астма». Всемирная организация здоровья. Архивировано из оригинал 29 июня 2011 г.. Получено 2016-03-29.
- ^ Мэддокс Л., Шварц Д.А. (2002). «Патофизиология астмы». Анну. Преподобный Мед. 53: 477–98. Дои:10.1146 / annurev.med.53.082901.103921. PMID 11818486.
- ^ «Лекция 14: Гиперчувствительность». Архивировано из оригинал на 2009-07-21. Получено 2008-09-18.
- ^ «Центр лечения аллергии и астмы: спросите эксперта». Архивировано из оригинал на 2007-02-16. Получено 2008-09-18.
- ^ Учебник респираторной медицины Мюррея и Наделя, 4-е изд. Роберт Дж. Мейсон, Джон Ф. Мюррей, Джей А. Надел, 2005 г., Эльзевир стр.334
- ^ Типпетс Б., Гильбер Т.В. (2009). «Управление астмой у детей: часть 1: постановка диагноза, оценка степени тяжести». Консультант педиатров. 8 (5).
- ^ де Бур Дж. Д., Майор С. Дж., ван 'Т Веер С., Бел Э. Х., ван дер Пол Т. (апрель 2012 г.). «Астма и коагуляция». Кровь. 119 (14): 3236–44. Дои:10.1182 / blood-2011-11-391532. PMID 22262775.
- ^ а б Принципы и практика Миддлтона в отношении аллергии, Н. Ф. Адкинсон, Б. С. Бохнер, В. В. Бусс, С. Т. Холгейт, Р. Ф. Леманске, Ф. Е. Р. Саймонс. Глава 33: «Внутренние аллергены». 2008. Elsevier.
- ^ а б c d Сондерс (2005). «Астма». Мейсон: Учебник респираторной медицины Мюррея и Наделя (Гомер А. Боуши-младший, доктор медицины Дэвид Б. Корри, доктор медицины Джон В. Фахи, доктор медицины, Эстебан Г. Берчард, доктор медицины Прескотт Г. Вудрафф, доктор медицины и другие. (ред.)) (4-е изд.). Эльзевир.
- ^ Дженкинс С., Костелло Дж, Ходж Л. (2004). «Систематический обзор распространенности аспириновой астмы и ее значения для клинической практики». BMJ. 328 (7437): 434. Дои:10.1136 / bmj.328.7437.434. ЧВК 344260. PMID 14976098.
- ^ Болезнь сердца Браунвальда: Учебник сердечно-сосудистой медицины, 8-е изд. Джон М. Миллер, Дуглас П. Зипес. «ГЛАВА 33 - Терапия сердечной аритмии». 2007. Elsevier.
- ^ Принципы и практика Миддлтона в отношении аллергии, Н. Ф. Адкинсон, Б. С. Бохнер, В. В. Бусс, С. Т. Холгейт, Р. Ф. Леманске, Ф. Е. Р. Саймонс. «Глава 42 - Эпидемиология астмы и аллергических заболеваний - факторы риска астмы» 2008. Elsevier.
- ^ Принципы и практика Миддлтона в отношении аллергии, Н. Ф. Адкинсон, Б. С. Бохнер, В. В. Бусс, С. Т. Холгейт, Р. Ф. Леманске, Ф. Е. Р. Саймонс. «Глава 65 - Побочные реакции на пищу: реакции респираторной пищевой гиперчувствительности» 2008. Elsevier.
- ^ Австралазийское общество клинической иммунологии и аллергии (3 мая 2010 г.). «Сульфитная аллергия». ASCIA. Архивировано из оригинал на 2012-03-04.
- ^ Города SJ, Меллис CM (1984). «Роль ацетилсалициловой кислоты и метабисульфита натрия в хронической детской астме». Педиатрия. 73 (5): 631–7. PMID 6718119.
- ^ Mapp CE, Boschetto P, Maestrelli P, Fabbri LM (2005). «Профессиональная астма». Американский журнал респираторной медицины и реанимации. 172 (1): 280–305. Дои:10.1164 / rccm.200311-1575SO. PMID 15860754.
- ^ Немери Б., Хут PH, Новак Д. (2002). «Крытые бассейны, хлорирование воды и здоровье органов дыхания». Евро. Респир. J. 19 (5): 790–3. Дои:10.1183/09031936.02.00308602. PMID 12030714.
- ^ Чжао Дж., Такамура М., Ямаока А., Одадзима Ю., Икура Ю. (февраль 2002 г.). «Измененные уровни эозинофилов в результате вирусной инфекции при обострении астмы в детстве». Педиатр Аллергия Иммунол. 13 (1): 47–50. Дои:10.1034 / j.1399-3038.2002.00051.x. ЧВК 7168121. PMID 12000498.
- ^ Чен Э, Миллер GE (2007). «Стресс и воспаление при обострениях астмы». Brain Behav. Иммунная. 21 (8): 993–9. Дои:10.1016 / j.bbi.2007.03.009. ЧВК 2077080. PMID 17493786.
- ^ Ллойд, Стейси (2008-11-08). «Почему холодный воздух вызывает затруднения дыхания у пациентов с заболеваниями легких». О: Заболевания легких. Архивировано из оригинал на 2007-01-02.
- ^ «Астма и высота». Результаты по телу.
- ^ Питерс, Майкл С; МакГрат, Келли Вонг; Хокинс, Грегори А; Хасти, Аннетт Т; Леви, Брюс Д; Израиль, Эллиот; Филлипс, Бренда Р.; Mauger, Дэвид Т; Comhair, Suzy A; Эрзурум, Серпил С; Йоханссон, Матс В. Джарджур, Низар Н; Coverstone, Андреа М; Кастро, Марио; Ольгин, Фернандо; Венцель, Салли Э; Вудрафф, Прескотт Дж. Бликер, Юджин Р.; Фахи, Джон V (июль 2016 г.). «Концентрации интерлейкина-6 в плазме, метаболическая дисфункция и тяжесть астмы: поперечный анализ двух когорт». Ланцет респираторной медицины. 4 (7): 574–584. Дои:10.1016 / S2213-2600 (16) 30048-0. ЧВК 5007068. PMID 27283230.
- ^ Szentivanyi, Андор (1968). "Бета-адренергическая теория атопической аномалии при астме". J. Аллергия. 42 (4): 203–232. Дои:10.1016 / S0021-8707 (68) 90117-2.
- ^ Локки, Ричард, должное: Андор Сентиваньи, доктор медицины. J. Аллергия и клиническая иммунология, Январь 2006 г.
- ^ Szentivanyi A .; Али К .; Кальдерон EG .; Brooks SM .; Коффи РГ .; Локки РФ. (1993). "The in vitro влияние иммуноглобулина E {IgE} на концентрации циклического АМФ в эпителиальных клетках легких человека A549 с бета-адренергической стимуляцией или без нее ». Журнал аллергии и клинической иммунологии. 91: 379. - Часть аннотаций из:
"50-летие Американской академии аллергии и иммунологии. 49-е ежегодное собрание. Чикаго, Иллинойс, 12-17 марта 1993 г. Тезисы". Журнал аллергии и клинической иммунологии. 91 (1 Пет 2): 141–379. 1993 г. Дои:10.1016 / 0091-6749 (93) 90360-Р. PMID 8421135. - ^ Kowalak JP; Hughes AS; и др., ред. (2001). Профессиональный справочник по болезням (7-е изд.). Springhouse.
- ^ «Нарушения дыхания во время сна часто встречаются у пациентов с астмой, они могут помочь предсказать тяжелую астму» (Пресс-релиз). Система здравоохранения Мичиганского университета. 25 мая 2005 г. Архивировано с оригинал 18 января 2006 г.. Получено 23 сентября, 2006.
- ^ Basner RC (25 июля 2006 г.). «Астма и СОАС». Американская ассоциация апноэ сна. Архивировано из оригинал на 2011-06-15. Получено 23 сентября, 2006.
- ^ Леггетт Дж. Дж., Джонстон Б. Т., Миллс М., Гэмбл Дж., Хини Л. Г. (2005). «Распространенность гастроэзофагеального рефлюкса при тяжелой астме: связь с исходом астмы». Грудь. 127 (4): 1227–31. CiteSeerX 10.1.1.561.3736. Дои:10.1378 / сундук.127.4.1227. PMID 15821199. Архивировано из оригинал на 2007-09-27.
- ^ «Астма при беременности». www.marchofdimes.org. Получено 2016-03-29.
- ^ а б Робинсон, Дионн П .; Кляйн, Сабра Л. (2012-08-01). «Беременность и гормоны, связанные с беременностью, изменяют иммунный ответ и патогенез заболевания». Гормоны и поведение. 62 (3): 263–271. Дои:10.1016 / j.yhbeh.2012.02.023. ISSN 0018-506X. ЧВК 3376705. PMID 22406114.
- ^ а б c d е «ЗАГРЯЗНЕНИЕ ВОЗДУХА ПОВЫШАЕТ РИСК ПРЕЖДЕВЫХ РОЖДЕНИЙ ДЛЯ ЖЕНЩИН С АСТМОЙ». 1 марта 2016 г.. Получено 2016-03-29.
- ^ а б Сбихи, хинд; Тамбурик, Лилиан; Кохорн, Мике; Брауэр, Майкл (09.02.2016). «Воздействие загрязнения воздуха в перинатальном периоде и развитие астмы от рождения до 10 лет». Европейский респираторный журнал. 47 (4): ERJ – 00746–2015. Дои:10.1183/13993003.00746-2015. ISSN 0903-1936. PMID 26862123.
- ^ «Воздействие загрязнения воздуха на младенцев и детей, Институт окружающей среды и устойчивого развития Калифорнийского университета в Лос-Анджелесе». www.environment.ucla.edu. Получено 2016-03-29.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
