Нульвалентное железо - Zerovalent iron

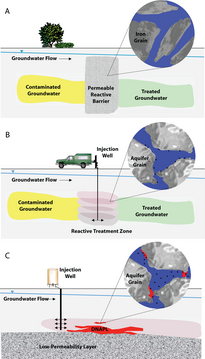
Нульвалентное железо и другие нулевой валент металлы (ZVI и ZVM соответственно) имеют множество применений, начиная от фильтры к электроды к траншеи. Одно из новых применений ZVI - железная стена. восстановление. Эта технология использует ZVI для формирования проницаемый реактивный барьер (PRB), который отфильтровывает загрязнения в грунтовые воды, оставляя только обеззараженные грунтовые воды и растворенное железо на другой стороне PRB.
История
Разработка технологии PRB из гранулированного железа основывалась на двух достижениях: металлическое железо разрушает хлорированные органические соединения и могут протекать реакции. на месте под нормальным грунтовые воды условия.[1] Металлы использовались как катализаторы с 20-го века, с большим количеством доступной литературы, касающейся коррозии металлических транспортных и складских контейнеров.[1] Поскольку эта литература касалась чистых растворителей, а не водный Растворы и процессы часто происходили при высоких температурах и давлениях, и экологическое сообщество не обращало на это внимания.[1] В 1972 году было обнаружено, что металлы с нулевой валентностью эффективны в расщеплении пестицидов и других хлорированных органических соединений в водном растворе.[2] Однако это открытие также не было учтено, возможно, потому, что оно было зафиксировано только в патентах и предшествовало осознанию того, что хлорированные растворители в грунтовых водах представляют собой проблему окружающей среды.[1]
В 1980-х годах студентка Университет Ватерлоо изучили возможность систематической ошибки выборки, вызванной сорбция загрязняющих веществ в обсадные трубы скважин и других материалов, используемых при отборе проб подземных вод.[1] В то время как загрязняющие вещества были потеряны из раствора в результате распространение в полимеры потери загрязняющих веществ наблюдались также при контакте растворов с некоторыми металлами, и эти потери не соответствовали распространение процесс.[1] Восстановительный дехлорирование считалось наиболее вероятной причиной.[2] Это подтвердили тесты, которые показали несколько переходные металлы обладают способностью разлагать многие хлорированные алифатические соединения.[1]
Предпосылки (теория)
Основы химии коррозии железа
В коррозия реакция с участием воды идет медленно, тогда как коррозия Fe0 с растворенным кислородом быстро, если предположить, что есть O2 настоящее время. Это реактивные процессы:
Анаэробный коррозия: Fe0 + 2H2O → Fe2+ + H2 + 2OH−
Аэробика коррозия: 2Fe0 + O2 + 2H2O → 2Fe2+ + 4OH−
Присутствие восстанавливаемого загрязнения может вызвать другую реакцию, которая затем может повлиять на общую скорость коррозии.[3]
Пути уменьшения загрязнения

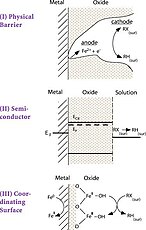
Нулевой валентный металл (обычно гранулированное железо) является объемным восстановителем в этих системах. Однако коррозия металлического железа дает Fe2+ и водород, оба из которых являются возможными восстановителями загрязняющих веществ, таких как хлорированные растворители. А эвристический Модель, состоящая из трех возможных механизмов, оказалась очень полезной.
Путь A представляет собой прямой перенос электронов (ET) для Fe0 к адсорбированному галоидоуглероду (RX) в точке контакта металл / вода, что приводит к дехлорированию и образованию Fe2+. Путь B показывает, что Fe2+ (в результате коррозии Fe0) может также дехлорировать RX с образованием Fe3+. Путь C показывает, что H2 от анаэробный коррозия Fe2+ может реагировать с RX, если присутствует катализатор.
Гидрирование также играет второстепенную роль в большинстве систем, и поверхность железа будет покрыта осадками оксидов (или карбонатов и сульфидов) в большинстве условий окружающей среды. Обеспокоенность, связанная с тем, как оксидный слой обеспечивает перенос электронов от Fe0 к адсорбированному RX привело к формулировке другой эвристической модели, снова состоящей из трех механизмов.
Во второй модели путь I показывает по существу прямую ЭТ от Fe0 к RX в коррозионной яме или аналогичном дефекте оксидной пленки. Путь II показывает оксидную пленку, опосредующую ЭТ из Fe0 к RX, действуя как полупроводник. Путь III показывает оксидную пленку как координирующую поверхность, содержащую центры Fe0 что сложнее и уменьшить RX.[4]
Секвестрация
Улавливание загрязнителя относится к процессу удаления, который не включает разложение загрязнителя. Секвестрация Fe0 обычно происходит через адсорбция, снижение, и соосаждение. Часто адсорбция является лишь прелюдией к другим процессам, которые действительно преобразуют загрязнитель, чтобы гарантировать, что процесс не может быть обращен вспять. Однако бывают случаи, когда адсорбция является процессом секвестрации первостепенной важности, особенно с металлами, которые встречаются в виде растворимых катионы который не может быть восстановлен до нерастворимых форм Fe0. Это также может быть верно для тяжелых металлов, таких как CD, Cu, Hg и т. д., которые существуют преимущественно в виде растворимых катионов, но могут быть восстановлены до нерастворимых веществ с помощью Fe0.[3]
Деградация через сокращение
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Май 2011 г.) |
Разложение путем окисления
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Май 2011 г.) |
Тип металла
Утюг
Чугун, состоящий из строительного лома, использовался в качестве реактивного материала для проницаемые реактивные барьеры за восстановление грунтовых вод. Обычно считается, что реакции происходят на поверхности Fe (оксида); однако было показано, что включения графита также могут служить местом реакции для 2,4-динитротолуол (DNT)[5]
Железо высокой чистоты - еще одна категория, которая указывает на коммерческое гранулированное железо для порошковая металлургия, так далее.
Цинк и другие металлы
Цинк показал гораздо более высокую реакционную способность по отношению к пентахлорфенол чем железо. Это указывает на то, что цинк может использоваться в качестве замены ZVI при дехлорировании хлорированных фенолов. Хлорированные фенолы последовательно дехлорируют, и поэтому менее хлорированные фенолы были идентифицированы как продукт восстановления.[6]
Биметаллические комбинации
Полихлорированные бифенилы (ПХБ) обеззараживают с использованием системы обработки, включающей каталитические частицы ZVM и органический водородный донор растворителя. Растворитель включает воду и алкоголь. Система обработки может содержать второй растворитель, такой как d-лимонен, толуол, или же гексан. Система обработки может содержать загуститель, такой как стеарат кальция или же крахмал. Система обработки может содержать стабилизатор, такой как глицерин, минеральное масло, или же растительное масло. Катализатор состоит из частиц нульвалентного металла, особенно. магний или же утюг, покрытый каталитическим металлом, таким как палладий, никель, или же серебро. Система обработки представляет собой пастообразную систему, которую предпочтительно наносить на естественные среды и структуры ex-situ.[7]
Наноразмерные частицы
Помимо использования «типичного» окалины в PRB, наночастицы (Диаметр 1-100 нм), содержащее нульвалентное железо (nZVI). Существуют неопределенности относительно характеристик этой технологии, которые затрудняют разработку приложений для обеспечения оптимальной производительности или оценки риска для здоровья человека или окружающей среды. Однако было выявлено несколько ключевых фактов, связанных с nZVI, игнорирование которых может привести к неправильному пониманию технологии. Это следующие: 1) nZVI, используемые в восстановление грунтовых вод больше, чем частицы, показывающие "истинное" наноразмерные эффекты 2) высокая реактивность nZVI в основном обусловлена его высокой удельная поверхность и 3) подвижность частиц nZVI почти во всех соответствующих сценариях будет меньше нескольких метров (одним из следствий этой ограниченной мобильности является то, что облучение человека из-за восстановление применение nZVI скорее всего будет минимальным). Однако есть еще много характеристик этой технологии, о которых известно очень мало: например, как быстро nZVI будет преобразован и в какие продукты, будет ли этот остаток обнаруживаться в окружающей среде и как поверхностные модификации nZVI изменят его длительность. - срочная экологическая судьба и эффективность восстановления.[4]
Нисходящий подход к производству нано -ZVM начинается с крупной металлической частицы (гранулированной или микромасштабной) и разрушает ее. Для этого могут использоваться механические или химические средства, которые включают, но не ограничиваются ими, фрезерование, травление и механическую обработку. С другой стороны, подход снизу вверх предполагает «рост». наночастицы посредством химического синтеза, самосборки, позиционной сборки и т. д.[8]
Тип очищаемых загрязнений
Металлы
Хромат является важным компонентом многих шлейфов радиоактивных загрязнений. Один из методов удаления включает добавление металлического лома. Реактивная поверхность ZVI в щелочной воды это железо покрытие типа зеленой ржавчины.[9]
За мышьяк, при выборе реактивного материала ПРБ необходимо учитывать свойства загрязнителя. В случае очистки воды, загрязненной мышьяком, материалы с высоким потенциалом анион адсорбция и соосаждение желательны. Также выгодно иметь высокий потенциал для уменьшения загрязнения до нерастворимого твердого вещества. Для удаления мышьяка используется следующий химический процесс:[10]
FeCl3 + 3H2О + [В качестве] → [Как]Fe (ОН)3 + 3H+ + Cl−
Технеций, радиоактивный материал, вызывает серьезную озабоченность из-за его длительного период полураспада и изобилие коммерческих ядерных отходов. Технеций в состояниях с более низкой валентностью имеет более низкую растворимость и сильнее сорбируется почвами, чем Te7+. ZVI может удалять технеций из грунтовых вод.[11]
К исправить подземные воды загрязнены уран было разработано лечение, чтобы минимизировать подвижность уранил переводя его в стабильную фазу. Поскольку точный механизм процесса дезактивации неизвестен, были синтезированы многочисленные формы ZVI-материалов, включая углеродистую сталь, низколегированную сталь, чугун и все другие железосодержащие сплавы.[12]
Неметаллические неорганические вещества
Хлорамины представляют угрозу для водных экосистем, подверженных сбросу очищенных сточных вод. Дехлорирование сульфит слишком медленно восстанавливает наиболее тугоплавкие органические хлорамины, чтобы производить сточные воды, отвечающие текущим критериям защиты экосистем в Соединенных Штатах. Восстановители водной фазы, которые обеспечивают преимущества в скорости по сравнению с одним сульфитом, включают: дитионит, тиосульфат, и йодид-опосредованный сульфит. Аскорбиновая кислота была даже более реакционной, но было обнаружено, что она медленнее по сравнению с сульфитом. Потенциальная биологическая потребность в кислороде может ограничивать выбор водных восстановителей. Показано, что металлическое железо эффективно восстанавливает неорганические и органические хлорамины.[13]
Стремительный нитрат восстановление железным порошком наблюдается только при pH ≤4. pH контроль серной кислотой продлевает восстановление нитратов и увеличивает удаляемое количество.[14] Аммиак является конечным продуктом восстановления нитратов и составляет весь нитрат, преобразованный в определенных экспериментальных условиях.[14] Однако, используя наноразмерное железо N2 вместо этого продуктом является газ.[15] Железо виды, Fe2+ и Fe (OH)2 вероятно, не участвуют в реакции.[14]
Органика
Доказано, что железо эффективно при дехлорировании пестицидов, таких как ДДТ, DDD, и DDE. Скорость дехлорирования не зависела от количества железа; однако ставки с поверхностно-активное вещество (Triton X-114) присутствующих были намного выше. Скорость дехлорирования ограничивается скоростью растворения в водной фазе.[16]
Вирусы особенно опасны для окружающей среды, поскольку они более подвижны и устойчивы к хлорированию и фильтрации, чем бактерии. Удаление вирусов из подземных вод включает несколько различных форм железа, включая Fe.0, Fe2+, и магнетит. Кроме того, вирусы могут по-разному взаимодействовать с железом и, таким образом, могут быть в разной степени деактивированы.[17]
Режимы применения
Проницаемые реактивные барьеры
Перемешивание почвы
Проницаемые реактивные барьеры могут быть менее эффективными на больших глубинах из-за строительных проблем, так как большинство строительных технологий включают выемку грунта и замену реактивной средой. Технология стенок для смешивания грунта (SMW), при которой устанавливаются разделительные стены и смешиваются цементные растворы непосредственно с грунтом под землей, стала новой технологией в восстановление почвы.[18]
Крышка осадка
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Май 2011 г.) |
Канистры надземные
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Май 2011 г.) |
Примечания
- ^ а б c d е ж грамм Гиллхэм, Роберт, Джон Воган, Лай Гуи, Майкл Дюшен и Дженнифер Сон. «Железные барьерные стены для восстановления хлорированных растворителей». На месте Восстановление шлейфов хлорированных растворителей. Эд. Ханс Ф. Строо и К. Херб Уорд. Нью-Йорк, штат Нью-Йорк: Springer Science + Business Media, 2010.
- ^ а б Reynolds GW, Hoff JT, Gillham R W. 1990. Смещение выборки, вызванное материалами, используемыми для мониторинга галоидоуглеродов в подземных водах. Environ Sci Technol 24: 135-142
- ^ а б Tratnyek, P. G .; М. М. Шерер; Т. Дж. Джонсон; Мэтисон, Л.Дж. (2003). Проницаемые реакционные барьеры из железа и других металлов с нулевой валентностью. В: Tarr M. A. (ed.), Химические методы разложения отходов и загрязнителей; Экологические и промышленные применения. Наука об окружающей среде и борьба с загрязнением, Марсель Деккер, Нью-Йорк, стр. 371-421. Дои:10.1201 / 9780203912553.ch9
- ^ а б Тратник, Пол и Рик Джонсон. «Восстановление железным металлом». Центр исследования подземных вод. Орегонский университет здоровья и науки, 4 февраля 2005 г.
- ^ Jafarpour, B .; Имхофф, П. Т .; Чиу. ПК. 2005. Количественная оценка и моделирование восстановления 2,4-динитротолуола высокочистым чугуном. Журнал гидрологии загрязнителей. 76 (1-2): 87-107. Дои:10.1016 / j.jconhyd.2004.08.001
- ^ Kim, Y.H .; Carraway, E. R. 2003. Дехлорирование хлорированных фенолов нульвалентным цинком. Экологические технологии. 24 (12): 1455-1463. Дои:10.1080/09593330309385690
- ^ Куинн, Дж. У., К. Б. Брукс, К. Л. Гейгер и К. А. Клаузен. 2007. Биметаллическая система очистки и ее применение для удаления и восстановления полихлорированных дифенилов. WO. Патент № 2007021640. Соединенные Штаты Америки, представленные Adm, 20060807.
- ^ Li, X .; Elliot, D.W .; Чжан, В. 2006. Наночастицы нульвалентного железа для борьбы с загрязнителями окружающей среды: материалы и технические аспекты. Критические обзоры в области твердого тела и материаловедения. 31 (4): 111-122. Дои:10.1080/10408430601057611
- ^ Wander, M. C. F .; Rosso, K.M .; Schoonen, M.A. 2006. Восстановление хромата двухвалентным железом и грин раст: сравнение гомогенных и гетерогенных скоростей переноса электронов. 232-е Национальное собрание ACS, Сан-Франциско, Калифорния. Тезисы докладов, 232-е Национальное собрание ACS, COLL-509.
- ^ Это все еще необходимо процитировать, это взято из буклета в ламинатной обложке под названием «Достижения в PRB для очистки грунтовых вод».
- ^ Дин, М .; Schroeder, N.C .; Реймус П.В. 2001. Нульвалентное железо как восстанавливающий «геттер» для иммобилизации технеция. 222-е Национальное собрание ACS, Чикаго, Иллинойс. Тезисы докладов, 222-е Национальное собрание ACS, Чикаго, Иллинойс, США, ENVR-149.
- ^ Багванд, А. 2003. Иммобилизация урана в подземных водах. Журнал экологических исследований. 29 (31): 1-12.
- ^ Беднер, М .; У. А. МакКрехан; Г. Р. Хельц. 2004. Сделать хлор более экологичным: исследование альтернатив сульфиту для дехлорирования. Исследования воды. 38 (10): 2505-2514. Дои:10.1016 / j.watres.2004.03.010
- ^ а б c Хуанг, С .; Wang, H .; Чиу П. 1998. Восстановление нитратов металлическим железом. Исследования воды. 32 (8): 2257-2264. Дои:10.1016 / S0043-1354 (97) 00464-8
- ^ Choe, S .; Chang, Y .; Hwang, K .; Хим, Дж. 1999. Кинетика восстановительной денитрификации наноразмерным нульвалентным железом. Chemosphere. 41 (8): 1307-1311. Дои:10.1016 / S0045-6535 (99) 00506-8
- ^ Sayles, G.D .; Вы г.; Wang, M .; Купферле, М. Дж. 1997. Дехлорирование ДДТ, ДДД и ДДЕ нульвалентным железом. Наука об окружающей среде и технологии. 31 (12): 3448-3454. Дои:10.1021 / es9701669
- ^ Zhang, L .; Chiu, P.C .; Джин, Ю. 2006. Реабилитация и инактивация вирусов элементарным железом. 231-е Национальное собрание ACS, Американское химическое общество, Отдел окружающей среды. Атланта, Джорджия. Тезисы докладов, 231-е Национальное собрание ACS, ENVR-234.
- ^ Ито, Х., С. Хино, К. Окуниси, Ю. Кинрю и Н. Хамамото. 2004. Испытания на строительство PRBS в виде стены для перемешивания грунта. Международная конференция по восстановлению хлорированных и устойчивых соединений, 4-я, Монтерей, Калифорния. Труды Международной конференции по восстановлению хлорированных и устойчивых соединений, 4-я, Монтерей, Калифорния, США, 24–27 мая 2004 г., 3A 04 / 1-3A 04/8.
