Борилирование - Borylation
C – H-борилирование, катализируемое металлами реакции представляют собой органические реакции, катализируемые переходными металлами, которые производят борорганическое соединение посредством функционализации алифатический и ароматный Связи C – H и поэтому являются полезными реакциями активация углеродно-водородной связи.[1] В реакциях борилирования C – H, катализируемых металлами, переходные металлы используются для прямого преобразования связи C – H в связь C – B. Этот путь может быть выгодным по сравнению с традиционными реакциями борилирования за счет использования дешевого и обильного углеводородного исходного материала, ограничения предварительно функционализированных органических соединений, уменьшения токсичных побочных продуктов и оптимизации синтеза биологически важных молекул.[2][3] Бороновые кислоты и сложные эфиры бороновой кислоты представляют собой обычные борильные группы, включенные в органические молекулы посредством реакций борилирования.[4] Бороновые кислоты представляют собой трехвалентные борсодержащие органические соединения, которые имеют один алкильный заместитель и две гидроксильные группы. Точно так же сложные эфиры бороновой кислоты содержат один алкильный заместитель и две сложноэфирные группы. Бороновые кислоты и сложные эфиры классифицируются в зависимости от типа углеродной группы (R), непосредственно связанной с бором, например, алкиловые, алкениловые, алкиниловые и арилбороновые сложные эфиры. Наиболее распространенный тип исходных материалов, которые включают сложные эфиры бороновой кислоты в органические соединения для реакций борилирования, катализируемых переходными металлами, имеют общую формулу (RO)2B-B (ИЛИ)2. Например, бис (пинаколато) диборон (B2Штырь2) и бис (катехолато) диборан (B2Кот2) являются обычными источниками бора этой общей формулы.[5]
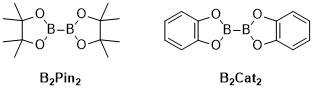
Атом бора боронового эфира или кислоты является sp.2 гибридизированный обладающие вакантной p-орбиталью, что позволяет этим группам действовать как Кислоты Льюиса. Связь C – B бороновых кислот и сложных эфиров немного длиннее типичных одинарных связей C – C в диапазоне 1,55–1,59 Å. Удлинение связи C – B по сравнению с связью C – C приводит к энергии связи, которая также немного меньше, чем энергия связи C – C (323 кДж / моль для C – B по сравнению с 358 кДж / моль для C – C).[6] В связь углерод-водород имеет длину связи около 1,09 Å и энергию связи около 413 кДж / моль. Следовательно, связь C – B является полезным промежуточным звеном в качестве связи, которая заменяет обычно нереактивную связь C – H.
Органоборон соединения - это органические соединения, содержащие связь углерод-бор. Борорганические соединения имеют широкое применение в химическом синтезе, поскольку связь C – B может быть легко преобразована в связь C – X (X = Br, Cl), C – O, C – N или C – C. Из-за универсальности связи C – B были разработаны многочисленные способы их включения в органические соединения.[7] Боровоорганические соединения традиционно синтезированный из Реактивы Гриньяра через гидроборирование, или реакции диборирования.[8] Альтернативой является борилирование.
Катализируемые металлами реакции борилирования C – H
Алифатический C – H борилирование
Как впервые было описано Хартвигом, алканы могут быть селективно борилированы с высокой селективностью по первичной связи C – H с использованием Cp * Rh (η4-C6Мне6) в качестве катализатора.[9] Примечательно, что селективность по первичной связи C – H исключительна даже при наличии гетероатомов в углеродно-водородной цепи. Катализируемое родием борилирование метильных связей C – H происходит селективно, независимо от положения гетероатома. Борилирование происходит селективно по наименее стерически затрудненной и наименее богатой электронами первичной связи C – H в диапазоне ацетали, эфиры, амины, и алкилфториды.[10] Кроме того, показано, что реакция не происходит в отсутствие первичных связей C – H, например, когда циклогексан это субстрат.
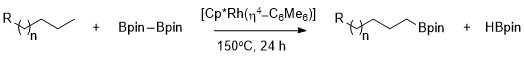
Селективная функционализация первичной алкановой связи обусловлена образованием кинетически и термодинамически благоприятного первичного комплекса алкил-металл по сравнению с образованием вторичного комплекса алкил-металл.[11]

Более высокая стабильность первичных алкильных комплексов по сравнению с вторичными может быть объяснена несколькими факторами. Во-первых, первичный алкильный комплекс стерически предпочтительнее вторичного алкильного комплекса. Во-вторых, частичные отрицательные заряды часто присутствуют на α-углероде металлоалкильного комплекса, а первичный алкильный лиганд поддерживает частичный отрицательный заряд лучше, чем вторичный алкильный лиганд. Причиной селективности алифатического C – H-борилирования с использованием родиевых катализаторов было исследовали с использованием типа механистического исследования, называемого водородно-дейтериевый обмен. Обмен H / D показал, что региоселективность всего процесса, показанного ниже, является результатом селективного расщепления первичных, а не вторичных связей C – H и селективной функционализации первичного металл-алкильного промежуточного соединения по сравнению с вторичным металл-алкильным промежуточным соединением.[12]
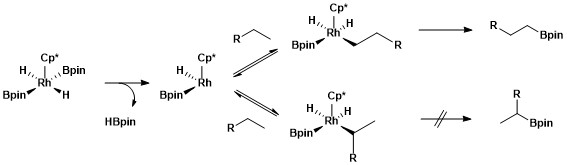
Синтетическая полезность алифатического C – H-борилирования применялась для модификации полимеров посредством борилирования с последующим окислением с образованием гидроксил-функционализированных полимеров.[13]
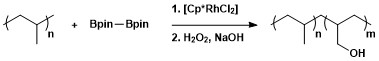
Ароматическое C – H-борилирование
Стерическое направленное C – H -орилирование аренов
О первом примере каталитического C – H-борилирования неактивированного углеводорода (бензола) сообщили Смит и Иверсон с использованием Ir (Cp *) (H) (Bpin) в качестве катализатора. Однако эффективность этой системы была низкой, она обеспечивала всего 3 оборота за 120 ч при 150 ° C.[14] Многочисленные последующие разработки Хартвига и соавторов привели к созданию эффективных практических условий для аренорилирования. Ароматическое C – H-борилирование было разработано Хартвиг и Исияма с использованием диборонового реагента Бис (пинаколато) диборон катализируется 4,4’-ди-трет-бутилбипиридином (dtbpy) и [Ir (COD) (OMe)]2.[15] С этой каталитической системой борилирование ароматических связей C – H происходит с региоселективностью, которая контролируется стерические эффекты стартовой арены. Селективность функционализации ароматических связей C – H регулируется общим правилом, согласно которому реакция не происходит. орто к заместителю, когда связь C – H не имеет орто заместитель имеется.[11] Когда присутствует только одна функциональная группа, борилирование происходит в мета и параграф позиция в статистическом соотношении 2: 1 (мета: пара). В орто изомер не обнаруживается из-за стерических эффектов заместителя.[16]

Добавление Bpin происходит только в одном положении для симметрично замещенных 1,2- и 1,4-замещенных аренов. Симметричные или несимметричные 1,3-замещенные арены также селективно борилируются, поскольку стерически доступна только одна связь C – H.
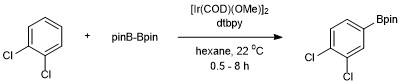
Это в отличие от Электрофильное ароматическое замещение где региоселективность определяется электронными эффектами.[17]
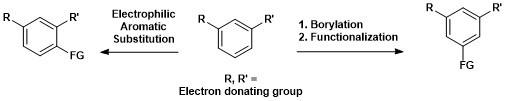
Синтетическое значение ароматического C – H-борилирования показано ниже, где 1,3-дизамещенное ароматическое соединение может быть непосредственно преобразовано в 1,3,5-органоборановое соединение и впоследствии функционализировано.[15]

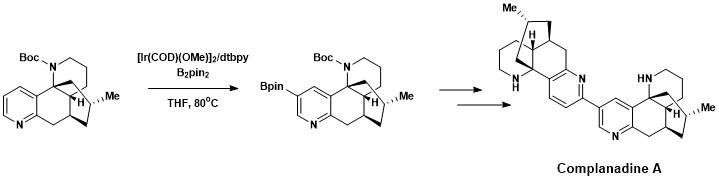
Ароматическая C – H-функционализация была успешно включена в общий синтез компланадина A, a Lycopodium алкалоид что усиливает мРНК выражение для фактор роста нервов (NGF) и производство NGF в организме человека глиальные клетки. Натуральные продукты, способствующие развитию новых нейронных сетей, представляют интерес для лечения таких заболеваний, как Болезнь Альцгеймера.[18] Компланадин A был успешно синтезирован с использованием комбинации прямого ароматического C – H-борилирования, разработанного Hartwig и Ishyiama, с последующим использованием Кросс-муфта Suzuki – Miyaura, затем расщепление Boc защитная группа.
C – H борилирование гетероаренов
Гетероарены также могут подвергаться борилированию в условиях иридиевого катализатора, однако сайт-селективность в этом случае контролируется электронные эффекты, куда фураны, пирролы, и тиофены вступают в реакцию по альфа-связи C – H с гетероатомом. В этом случае предполагается, что селективность происходит через альфа-связь C – H с гетероатомом, потому что это наиболее кислая связь C – H и, следовательно, наиболее реакционная.[11]

Режиссер орто C – H борилирование
Использование одинаковых управляющих групп каталитической системы может быть использовано для достижения региоселективности без заместителей в качестве стерических медиаторов. Например, Бобель и Хартвиг сообщили о методе проведения орто-борилирование, когда диметил-гидросилильная направляющая группа на арене подвергается катализируемому иридием борилированию по связи C – H орто к силан режиссерская группа.[19] Избирательность для орто положение в случае использования гидросилильных направляющих групп объясняется обратимым присоединением связи Si-H к металлическому центру, что приводит к преимущественному разрыву связи C – H орто к гидросилильному заместителю. Несколько других стратегий для достижения орто-Борилирование аренов разработано с использованием различных режиссерских групп.[20][21][22]

Детали механизма C – H борляции аренов.
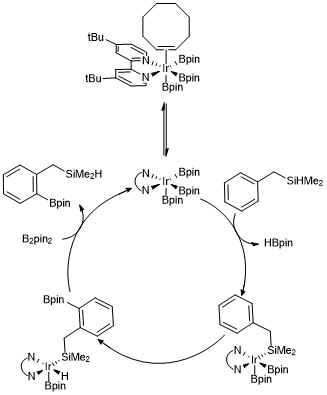
Был предложен комплекс трисборил иридия для облегчения механизма каждой из этих реакций, которые приводят к C – H-борилированию аренов и гетероаренов. Кинетические исследования и изотопная маркировка исследования показали, что Ir (III) triбориловый комплекс реагирует с ареном в каталитическом процессе.[23]Вариант каталитического цикла показан ниже для орто борилирование гидросилановых соединений. Кинетические данные показывают, что наблюдаемый трисборильный комплекс, координированный с циклооктен быстро и обратимо диссоциирует циклооктен с образованием 16-электронного трисборильного комплекса. В случае использования бензилдиметилсилана в качестве направляющей группы предполагается, что бензилдиметилсилан взаимодействует с трисборилиридиевым катализатором посредством обратимого присоединения связи Si-H к металлическому центру с последующим селективным орто-С – Н связь активация через окислительная добавка и восстановительное устранение.[24]
Мета-селективное борилирование: Мета-селективное борилирование C – H является важным синтетическим преобразованием, которое было обнаружено в 2002 году Смитом III из Университета штата Мичиган, США. Однако это метаборилирование было полностью стерически направленным и ограничивалось только 1,3-дизамещенными бензолами. Примерно 12 лет спустя доктор Чаттопадхай и его команда из Центра биомедицинских исследований, США, Индия открыли изящную технологию метаселективной активации и борилирования связей C – H. Команда показала, что, используя тот же субстрат, можно переключать другую позиционную селективность, просто меняя лиганд. Происхождение мета-селективности определялось двумя параметрами, такими как: 1) электростатическое взаимодействие, 2) вторичное взаимодействие B-N.[25]
В то же время команда доктора Канаи из Японии представила удивительную концепцию метаселективного борилирования, основанного на вторичном взаимодействии. Метод охватывает борилирование различных карбонильных соединений.[26]
Реакции восстановления борорганическими соединениями
Редукция Кори – Бакши – Шибата (редукция CBS)
В 1981 году Хирао и его сотрудники обнаружили, что асимметричное восстановление прохиральных ароматических кетонов с хиральный амино- спирты и боран дал соответствующие вторичные спирты с 60% ее. Они выяснили, что хиральная амино спирты будет реагировать с боран с образованием комплексов алоксиламин-боран. Предполагается, что комплексы содержат относительно жесткую пятичленную кольцевую систему, которая делает их термически и гидролитически стабильными и растворимыми в большом количестве протический и апротонные растворители.[27]
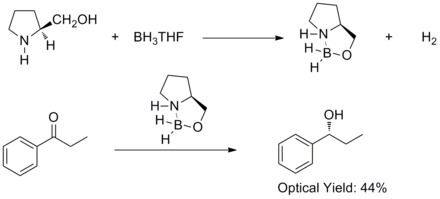
В 1987 г. Э. Дж. Кори и сотрудники обнаружили, что образование оксазаборолидинов из борана и хиральный амино- спирты. Было обнаружено, что оксазаборолидины катализируют быстрое и высокоэнантиоселективное восстановление прохиральных кетонов в присутствии BH3THF. Это энантиоселективное снижение ахирального кетоны с каталитическим оксазаборолидином называется восстановлением Кори – Бакши – Шибата или восстановлением CBS.[28][29]
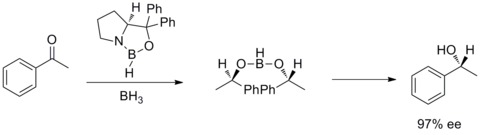
Срединно-альпийское сокращение борана (Срединное сокращение)
В 1977 г. M. M. Midland и его сотрудники сообщили об удивительном наблюдении, что B-3-альфа-пинанил-9-борабицикло [3,3,1] нонан, легко полученный гидроборированием (+) - альфа-пинена с 9-боробицикло [3,3,1] нонан, быстро восстанавливает бензальдегид-альфа-d до (S) - (+) - бензил-альфа-d спирта с по существу количественной асимметричной индукцией.[30]
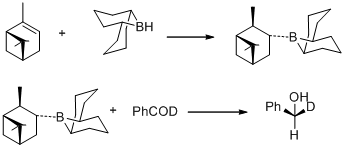
В том же году М. М. Мидленд обнаружил B-3-альфа-пинанил-9-BBN в качестве восстановителя, который может быть легко доступен при взаимодействии (+) - альфа-пинена с 9-BBN. Новый восстановитель позже был коммерциализирован Aldrich Co. под именем Альпийский боран и асимметричное восстановление карбонильных групп любым энантиомером альпийского борана известно как восстановление Мидленд альпийско-боран.[31]
В 2012 году У. Р. Й. Венкатесварлу и его сотрудники сообщили о стереоселективном методе синтеза пектинолида H. Восстановление по Мидленду и реакция дигидроксилирования Шарплесса участвуют в образовании трех хиральных центров на C-4 ’, C-5 и C-1’.[32]
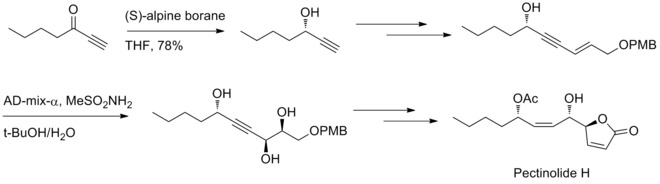
Реакции связывания с борорганическими соединениями
Петазис бороновая кислота-реакция Манниха
В 1993 г. Н. А. Петасис и И. Акрлтопулу сообщили об эффективном синтезе аллильных аминов с модифицированной Реакция Манниха. В этом измененном Реакция Манниха, они обнаружили, что винилбороновые кислоты могут участвовать в качестве нуклеофилы дать геометрически чистые аллиламины. Это измененное Реакция Манниха был известен как реакция Петазиса бороновой кислоты-Манниха.[33][34]
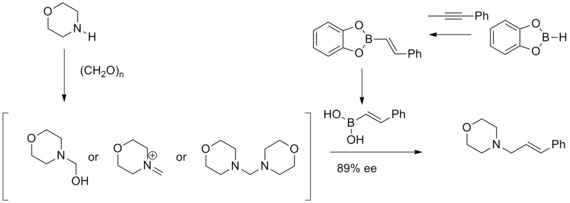
Асимметричное аллилирование Руша
В 1978 г. R. W. Hoffmann и T. Herold сообщили об энантиоселективном синтезе вторичных гомоаллиловых спиртов с помощью хиральных нерацемических аллилборных спиртов. сложные эфиры. Гомоаллиловые спирты образовывались с отличными урожай и умеренная энантиоселективность.[35]
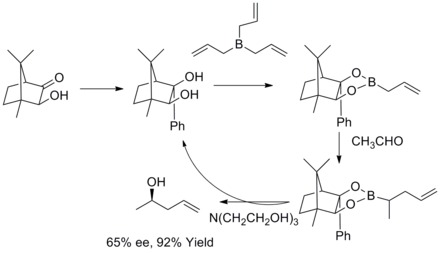
В 1985 году W. R. Roush и его сотрудники обнаружили, что аллильные боронаты, модифицированные тартратом, предлагают простой и очень привлекательный подход к контролю селективности лица в реакциях с хиральными и ахиральными альдегидами. В последующие годы W.R. Roush и его коллеги расширили эту стратегию до синтеза 2-бутен-1,4-диолы и антидиолы. Этот вид реакции известен как асимметричное аллилирование Руша.[36][37][38][39]
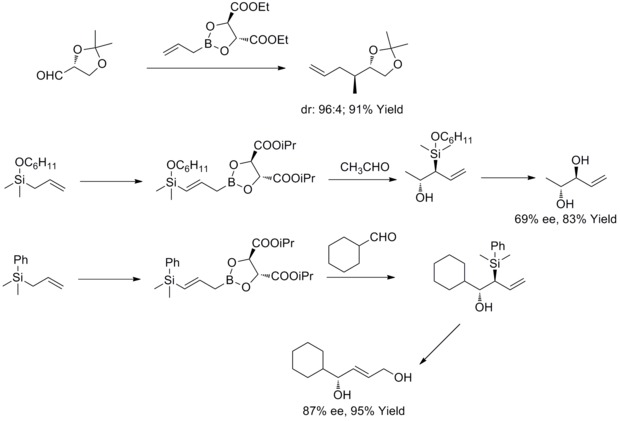
В 2011 г. R. A. Fernandes и P. Kattanguru завершили улучшенный полный синтез диастереомеров (8S, 11R, 12R) - и (8R, 11R, 12R) -топсентолид B2 в восемь стадий. В статье реакция диастереоселективного аллилирования Руша была использована в качестве ключевой реакции в общем синтезе для введения двух хиральных промежуточных продуктов. А затем авторы синтезировали два диастереомера через эти два хиральных промежуточных соединения.[40]

Кросс-муфта Suzuki – Miyaura
В 1979 г. Н. Мияура и А. Судзуки сообщили о синтезе арилированных (E) -алкенов с высоким выходом из арилгалогениды с алкил-1-енилборанами и катализируемый тетракис (трифенилфосфин ) палладий и основания. Затем А. Сузуки и его сотрудники распространяют этот вид реакции на другие борорганические соединения и другие алкенилы, арил, алкилгалогениды и тройной. Борорганические соединения, катализируемые палладием, и эти органические галогениды с образованием углерод-углеродных связей известны как Кросс-муфта Suzuki – Miyaura.[41][42]
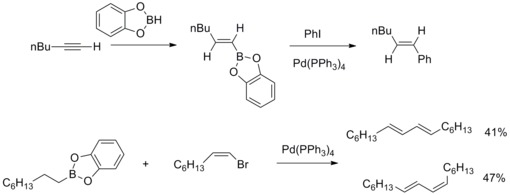
В 2013 году Иоахим Подлех и его сотрудники определили структуру альтенуиновой кислоты III альтернариозного микотоксина с помощью ЯМР-спектроскопического анализа и завершили его полный синтез. В стратегии синтеза использовали реакцию перекрестного связывания Сузуки-Мияура с высокофункциональным боронатом и бутенолидами для синтеза предшественника природного продукта с высоким выходом.[43]

Модифицированный биариловый эфир Ульмана и синтез биариламина
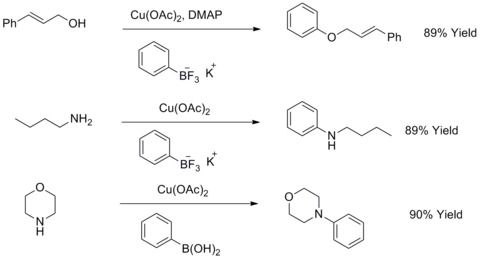
В 1904 г. Фриц Ульманн выяснили, что медный порошок может значительно улучшить реакцию арилгалогенидов с фенолами с образованием биариловых эфиров. Эта реакция известна как Конденсация Ульмана. В 1906 г. И. Голдберг расширил эту реакцию, чтобы синтезировать ариламин путем взаимодействия арилгалогенидов с амидом в присутствии карбоната калия и CuI. Эта реакция известна как модифицированная Гольдбергом конденсация Ульмана.[44] В 2003 году Р. А. Бэйти и Т. Д. Квач модифицировали этот тип реакций, используя калий. органотрифторбораты соли для реакции с алифатическими спиртами, алифатическими аминами или анилинами для синтеза простых ариловых эфиров или ариламинов.[45][46]
Смотрите также
- Борорганическая химия
- Реакции органоборатов и боранов
- Редукция Кори – Ицуно
- Срединно-альпийское сокращение борана
- Петазис реакция
- Сузуки реакция
Рекомендации
- ^ Хартвиг, Джон Ф. (2012). "Борилирование и силилирование связей C – H: платформа для разнообразных функционализаций связи C – H". Отчеты о химических исследованиях. 45 (6): 864–873. Дои:10.1021 / ar200206a. ISSN 0001-4842. PMID 22075137.
- ^ Cho, J. Y .; Це, М.К .; Холмс, Д .; Maleczka, R.E .; Младший; Смит, М. Р. (2001). «Замечательно селективные иридиевые катализаторы для разработки ароматических связей C-H». Наука. 295 (5553): 305–8. Дои:10.1126 / science.1067074. PMID 11719693. S2CID 21096755.
- ^ Ishiyama, T .; Nobuta, Y .; Hartwig, J. F .; Мияура, Н. Chem. Commun. 2003, 2924.
- ^ Brown, H.C .; Kramer, G.W .; Леви, А. Б .; Мидленд, М. М. Органический синтез через боран; Wiley-Interscience: Нью-Йорк, 1975; Vol. 1.
- ^ Брауншвейг, H .; Гетлейн, Ф. (2011). "Синтез диборанов, катализируемый переходными металлами (4)". Angewandte Chemie International Edition. 50 (52): 12613–12616. Дои:10.1002 / anie.201104854. PMID 22057739.
- ^ Холл, Д. Г. (2011) Структура, свойства и получение производных бороновой кислоты в бороновых кислотах: получение и применение в органическом синтезе, медицине и материалах (Том 1 и 2), Второе издание (под ред. Д. Г. Холла), Wiley-VCH Verlag GmbH & Co. KGaA, Вайнхайм, Германия. Дои:10.1002 / 9783527639328.ch1
- ^ Mkhalid, Ibraheem A. I .; Барнард, Джонатан Х .; Мардер, Тодд Б.; Мерфи, Жаклин М .; Хартвиг, Джон Ф. (2010). «Активация C – H для создания облигаций C – B». Химические обзоры. 110 (2): 890–931. Дои:10.1021 / cr900206p. PMID 20028025.
- ^ Уэйд, Л. Г., Органическая химия. Верхняя река Сэдл: Pearson Education, Inc., 2010.
- ^ Chen, H .; Schlecht, S .; Семпл, Т. С .; Хартвиг, Дж. Ф. (2000). «Термическая, каталитическая, региоспецифическая функционализация алканов». Наука. 287 (5460): 1995–1997. Bibcode:2000Sci ... 287.1995C. Дои:10.1126 / science.287.5460.1995. PMID 10720320.
- ^ Lawrence, J.D .; Takahashi, M .; Bae, C .; Хартвиг, Дж. Ф. (2004). «Региоспецифическая функционализация метил-C-H-связей алкильных групп в реагентах с гетероатомной функциональностью». Варенье. Chem. Soc. 126 (47): 15334–15335. Дои:10.1021 / ja044933x. PMID 15563132.
- ^ а б c Хартвиг, Дж. Ф. (2011). «Региоселективность борилирования алканов и аренов». Chem. Soc. Rev. 40 (4): 1992–2002. Дои:10.1039 / C0CS00156B. PMID 21336364.
- ^ Wei, C. S .; Jimenez-Hoyos, C.A .; Videa, M.F .; Hartwig, J. F .; Холл, М. Б. (2010). «Истоки селективности для борилирования первичных по вторичным связям C-H, катализируемым комплексами Cp * -родия». Варенье. Chem. Soc. 132 (9): 3078–91. Дои:10.1021 / ja909453g. PMID 20121104.
- ^ Кондо, Й .; Garcia-Cuadrado, D .; Hartwig, J.F .; Boaen, N.K .; Вагнер, Н.Л .; Хиллмайер, М.А. (2002). "Катализируемая родием региоспецифическая функционализация полиолефинов в расплаве". Варенье. Chem. Soc. 124 (7): 1164–5. Дои:10.1021 / ja016763j. PMID 11841273.
- ^ Iverson, Carl N .; Смит, Милтон Р. (1999-08-06). «Стехиометрическое и каталитическое образование связи B − C из неактивированных углеводородов и боранов». Журнал Американского химического общества. 121 (33): 7696–7697. Дои:10.1021 / ja991258w.
- ^ а б Хартвиг, Дж. Ф. (2012). «Борилирование и силилирование связей C-H: платформа для различных функционализаций связи C-H». Отчеты о химических исследованиях. 45 (6): 864–873. Дои:10.1021 / ar200206a. PMID 22075137.
- ^ Ishiyama, T .; Takagi, J .; Ishida, K .; Miyaura, N .; Анастаси, Н .; Хартвиг, Дж. Ф. (2002). «Мягкое катализируемое иридием борилирование аренов. Высокие числа оборота, реакции при комнатной температуре и выделение потенциального промежуточного продукта». Варенье. Chem. Soc. 124 (3): 390–391. Дои:10.1021 / ja0173019. PMID 11792205.
- ^ Лиски, К. Катализируемое иридием борилирование ароматических и алифатических связей C – H: методология и механизм. Диссертация, Университет Иллинойса. Урбанан-Шампейн. 2013.
- ^ Фишер, Д.Ф .; Сарпонг, Р. (2010). «Полный синтез (+) - компланадина A с использованием катализируемой иридием пиридиновой C-H-функционализации». Варенье. Chem. Soc. 132 (17): 5926–5927. Дои:10.1021 / ja101893b. ЧВК 2867450. PMID 20387895.
- ^ Boebel, T. A .; Хартвиг, Дж. Ф. (2008). "Силил-направленное, иридий-катализируемое орто-борилирование аренов. Однопоторто-борилирование фенолов, ариламинов и алкиларенов". Варенье. Chem. Soc. 130 (24): 7534–5. Дои:10.1021 / ja8015878. PMID 18494474.
- ^ Ishiyama, T .; Miyaura, N .; Isou, H .; Кикучи, Т. (2010). «Орто-C – H-борилирование бензоатных эфиров бис (пинаколато) дибороном, катализируемое иридий-фосфиновыми комплексами». Chem. Сообщество. 46 (1): 159–61. Дои:10.1039 / b910298a. HDL:2115/44631. PMID 20024326.
- ^ Kawamorita, S .; Ohmiya, H .; Hara, K .; Фукуока, А .; Савамура, М. (2009). «Направленное орто-борилирование функционализированных аренов, катализируемое компактной фосфин-иридиевой системой на кремнеземной основе». Варенье. Chem. Soc. 131 (14): 5058–9. Дои:10.1021 / ja9008419. PMID 19351202.
- ^ Ros, A .; Эстепа, Б .; Lopez-Rodriquez, R .; Alvarez, E .; Fernandez, R .; Лассалетта, Дж. Энгью. Chem. Int. Эд. 2011; 50, 1.
- ^ Boller, T.M .; Мерфи, Дж. М .; Hapke, M .; Ishiyama, T .; Miyaura, N .; Хартвиг, Дж. Ф. Варенье. Chem. Soc. 2005;, 127, 14263.
- ^ Boebel, T.A .; Хартвиг, Дж. Ф. (2008). "Силил-направленное, иридий-катализируемое орто-борилирование аренов. Однопоторто-борилирование фенолов, ариламинов и алкиларенов". Варенье. Chem. Soc. 130 (24): 7534. Дои:10.1021 / ja8015878. PMID 18494474.
- ^ Bisht, R .; Чаттопадхай, Б. (2016). "Формальное Ir-катализированное лиганд-активируемое орто- и мета-борилирование ароматических альдегидов посредством in situ-генерируемых иминов". Варенье. Chem. Soc. 138 (1): 84–7. Дои:10.1021 / jacs.5b11683. PMID 26692251.
- ^ Канаи; и другие. (2015). «Мета-селективное борилирование C – H, направленное вторичным взаимодействием между лигандом и субстратом». Nat. Chem. 7 (9): 712–7. Bibcode:2015НатЧ ... 7..712 тыс.. Дои:10.1038 / nchem.2322. PMID 26291942.
- ^ Хирао, Акира; Ицуно, Шиничи; Накахама, Сейичи; Ямазаки, Нобору (1981). «Асимметричное восстановление ароматических кетонов с хиральными алкокси-аминоборановыми комплексами». Журнал химического общества, химические коммуникации (7): 315. Дои:10.1039 / c39810000315.
- ^ Кори, Э. Дж .; Бакши, Раман К .; Шибата, Сайзо (сентябрь 1987 г.). «Высокоэнантиоселективное борановое восстановление кетонов, катализируемое хиральными оксазаборолидинами. Механизм и синтетические последствия». Журнал Американского химического общества. 109 (18): 5551–5553. Дои:10.1021 / ja00252a056.
- ^ Кори, Э. Дж .; Бакши, Раман К .; Шибата, Сайзо; Чен, Чунг Пин; Сингх, Винод К. (декабрь 1987 г.). «Стабильный и легко приготовленный катализатор энантиоселективного восстановления кетонов. Применение в многостадийных синтезах». Журнал Американского химического общества. 109 (25): 7925–7926. Дои:10.1021 / ja00259a075.
- ^ Мидленд, М. Марк; Трамонтано, Альфонсо; Здерич, Стивен А. (июль 1977 г.). «Простая реакция B-алкил-9-борабицикло [3.3.1] нонанов с бензальдегидом». Журнал металлоорганической химии. 134 (1): C17 – C19. Дои:10.1016 / S0022-328X (00) 93625-8.
- ^ Мидленд, М. Марк; Трамонтано, Альфонсо; Здерич, Стивен А. (июнь 1977 г.). «Получение оптически активного бензил-альфа-d спирта восстановлением B-3альфа-пинанил-9-борабицикло [3.3.1] нонаном. Новый высокоэффективный хиральный восстановитель». Журнал Американского химического общества. 99 (15): 5211–5213. Дои:10.1021 / ja00457a068.
- ^ Рамеш, Д .; Шехар, В .; Chantibabu, D .; Rajaram, S .; Ramulu, U .; Венкатешварлу Ю. (март 2012 г.). «Первый стереоселективный тотальный синтез пектинолида H». Буквы Тетраэдра. 53 (10): 1258–1260. Дои:10.1016 / j.tetlet.2011.12.122.
- ^ Petasis, Nicos A .; Акритопулу, Ирини (январь 1993 г.). «Реакция Манниха бороновой кислоты: новый метод синтеза геометрически чистых аллиламинов». Буквы Тетраэдра. 34 (4): 583–586. Дои:10.1016 / S0040-4039 (00) 61625-8.
- ^ Ю, Тао; Ли, Хуэй; У, Синьянь; Ян, июнь (2012). "Прогресс петазисной реакции". Китайский журнал органической химии. 32 (10): 1836. Дои:10.6023 / cjoc1202092.
- ^ Герольд, Томас; Хоффманн, Райнхард В. (октябрь 1978 г.). «Энантиоселективный синтез гомоаллиловых спиртов через хиральные аллилбороновые эфиры». Angewandte Chemie International Edition на английском языке. 17 (10): 768–769. Дои:10.1002 / anie.197807682.
- ^ Roush, William R .; Уолтс, Алан Э .; Хунг, Ли К. (декабрь 1985 г.). «Реакции диастерео- и энантиоселективного альдегидного присоединения сложных эфиров 2-аллил-1,3,2-диоксаборолан-4,5-дикарбоновой кислоты, полезного класса аллилборонатов, модифицированных сложным эфиром винной кислоты». Журнал Американского химического общества. 107 (26): 8186–8190. Дои:10.1021 / ja00312a062.
- ^ Roush, William R .; Андо, Каори; Пауэрс, Дэниел Б.; Halterman, Ronald L .; Палковиц, Алан Д. (январь 1988 г.). «Энантиоселективный синтез с использованием диизопропилтартрата, модифицированного (E) - и (Z) -кротилборонатами: реакции с ахиральными альдегидами». Буквы Тетраэдра. 29 (44): 5579–5582. Дои:10.1016 / S0040-4039 (00) 80816-3.
- ^ Roush, William R .; Гровер, Пол Т. (январь 1990 г.). «Диизопропилтартрат (E) -γ- (диметилфенилсилил) аллилборонат, эквивалент β-карбаниона хирального аллилового спирта для энантиоселективного синтеза 2-бутен-1,4-диолов из альдегидов». Буквы Тетраэдра. 31 (52): 7567–7570. Дои:10.1016 / S0040-4039 (00) 97300-3.
- ^ Roush, William R .; Говер, Пол Т .; Линь, Сяофа (январь 1990 г.). «Модифицированный диизопропилтартратом (E) -γ - [(циклогексилокси) диметилсилил-аллилборонат, хиральный реагент для стереоселективного синтеза анти-1,2-диолов посредством формального α-гидроксиаллилирования альдегидов». Буквы Тетраэдра. 31 (52): 7563–7566. Дои:10.1016 / S0040-4039 (00) 97299-X.
- ^ Fernandes, Rodney A .; Каттангуру, Пуллайя (ноябрь 2011 г.). «Полный синтез диастереомеров (8S, 11R, 12R) - и (8R, 11R, 12R) -топцентолид B2 и определение абсолютной конфигурации». Тетраэдр: асимметрия. 22 (20–22): 1930–1935. Дои:10.1016 / j.tetasy.2011.10.020.
- ^ Мияура, Норио; Судзуки, Акира (1979). «Стереоселективный синтез арилированных (E) -алкенов по реакции алк-1-енилборанов с арилгалогенидами в присутствии палладиевого катализатора». Журнал химического общества, химические коммуникации (19): 866. Дои:10.1039 / C39790000866.
- ^ Мияура, Норио; Ямада, Кинджи; Сузуки, Акира (январь 1979 г.). «Новое стереоспецифическое кросс-сочетание катализируемой палладием реакции 1-алкенилборанов с 1-алкенил- или 1-алкинилгалогенидами» (PDF). Буквы Тетраэдра. 20 (36): 3437–3440. Дои:10.1016 / S0040-4039 (01) 95429-2. HDL:2115/44006.
- ^ Немечек, Грегор; Томас, Роберт; Гесманн, Гельмут; Фельдманн, Клаус; Подлех, Иоахим (октябрь 2013 г.). «Выявление структуры и полный синтез альтеновой кислоты III и исследования в направлении полного синтеза альтеновой кислоты II». Европейский журнал органической химии. 2013 (28): 6420–6432. Дои:10.1002 / ejoc.201300879.
- ^ Курти, Ласло; Чако, Барбара (2007). Стратегические применения названных реакций в органическом синтезе: предпосылки и подробные механизмы; 250 названных реакций (Pbk. Ed., [Nachdr.]. Ed.). Амстердам [u.a.]: Elsevier Academic Press. стр.464 –465. ISBN 978-0-12-429785-2.
- ^ Quach, Tan D .; Бэйти, Роберт А. (апрель 2003 г.). "Синтез катализированного медью (II) эфира из алифатических спиртов и калийорганических солей трифторбората". Органические буквы. 5 (8): 1381–1384. Дои:10.1021 / ol034454n. PMID 12688764.
- ^ Quach, Tan D .; Бэйти, Роберт А. (1 ноября 2003 г.). «Образование связи C-N, катализируемое катализированной медью (II) лигандом и основанием: реакции перекрестного связывания борорганических соединений с алифатическими аминами и анилинами». Органические буквы. 5 (23): 4397–4400. Дои:10.1021 / ol035681s. PMID 14602009.
