Производство хлора - Chlorine production
Хлор газ может быть получен путем извлечения из природных материалов, в том числе электролиз из хлорид натрия решение (рассол ) и другими способами.
Добыча газа
Хлор может производиться электролиз из хлорид натрия решение (рассол ), который известен как Хлорно-щелочной процесс. Производство хлора приводит к побочным продуктам каустическая сода (едкий натр, NaOH) и водород газ (H2). Эти два продукта, как и сам хлор, обладают высокой реакционной способностью. Хлор можно также получить электролизом раствора хлорид калия, в этом случае побочными продуктами являются водород и едкий калий (гидроксид калия ). Существует три промышленных метода экстракции хлора электролизом хлоридных растворов, все они осуществляются в соответствии со следующими уравнениями:
- Катод: 2 H+ (водн.) + 2 е− → H2 (грамм)
- Анод: 2 Cl− (водный) → Cl2 (г) + 2 е−
Общий процесс: 2 NaCl (или KCl) + 2 H2O → Cl2 + H2 + 2 NaOH (или КОН)
Электролиз ртутных элементов
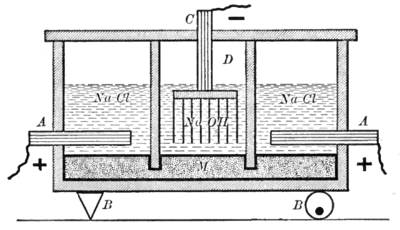
Меркурий электролиз клеток, также известный как Кастнер – Келлнер процесс, был первым методом, использованным в конце девятнадцатого века для производства хлора в промышленных масштабах.[1][2] Используемые "качающиеся" ячейки с годами совершенствовались.[3] Сегодня в «первичной камере» титан аноды, плакированные платина[4] или же проводящие оксиды металлов (ранее графит аноды) помещают в раствор хлорида натрия (или калия), протекающий над жидкой ртутью. катод. Когда прикладывается разность потенциалов и течет ток, хлор выделяется в титан анод и натрий (или же калий ) растворяется в ртутном катоде, образуя амальгама. Он непрерывно поступает в отдельный реактор ("обнажать "или" вторичный элемент "), где он обычно превращается обратно в ртуть в результате реакции с воды, производя водород и натрий (или калий) гидроксид в коммерчески полезной концентрации (50% по весу). Затем ртуть возвращается в первичный элемент с помощью насоса, расположенного внизу.
Ртутный процесс наименее энергоэффективен из трех основных технологий (ртуть, диафрагма и мембрана ) и есть также опасения по поводу ртути выбросы.
По оценкам, во всем мире все еще работает около 100 заводов по производству ртутных элементов. В Япония производство хлористо-щелочного металла на основе ртути было практически прекращено к 1987 г. (за исключением двух последних установок хлорида калия, остановленных в 2003 г.). в Соединенные Штаты, к концу 2008 года останется в эксплуатации всего пять ртутных заводов. Европа, на ртутные элементы приходилось 43% мощности в 2006 году, и западноевропейские производители обязались закрыть или преобразовать все оставшиеся хлорно-щелочные ртутные заводы к 2020 году.[5]
Электролиз диафрагменной ячейки (биполярный)
При электролизе диафрагменной ячейки асбест (или полимерно-волокнистая) диафрагма разделяет катод и анод, предотвращая повторное смешение хлора, образующегося на аноде, с гидроксидом натрия и водородом, образующимся на катоде.[6] Эта технология также была разработана в конце девятнадцатого века. Существует несколько вариантов этого процесса: ячейка Ле Суэра (1893 г.), ячейка Харгривса-Берда (1901 г.), ячейка Гиббса (1908 г.) и ячейка Таунсенда (1904 г.).[7][8] Ячейки различаются по конструкции и размещению диафрагмы, в некоторых из них диафрагма находится в прямом контакте с катодом.
В соль раствор непрерывно подается в анодное отделение и через диафрагму поступает в катодное отделение, где едкий щелочь производится, и рассол частично исчерпывается. В результате диафрагменные методы производят щелочь, которая довольно разбавлена (около 12%) и имеет более низкую чистоту, чем методы с использованием ртутных элементов.
Мембранные элементы не обременены проблемой предотвращения попадания ртути в окружающую среду; они также работают на более низких Напряжение, что приводит к экономии энергии по сравнению с методом ртутных элементов,[8] но большое количество пар требуются, если каустик должен быть испарился до промышленной концентрации 50%.
Электролиз мембранных элементов
Разработка этой технологии началась в 1970-х годах. Ячейка электролиза разделена на две «секции» катион проницаемый мембрана, действующая как катионит. Насыщенный раствор хлорида натрия (или калия) пропускается через анодное отделение, выходя при более низкой температуре. концентрация.[9] Раствор гидроксида натрия (или калия) циркулирует через катодное отделение с более высокой концентрацией на выходе. Часть концентрированного раствора гидроксида натрия, покидающая ячейку, отводится как продукт, а остальная часть разбавляется деионизированная вода и снова прошли через аппарат для электролиза.
Этот метод более эффективен, чем мембранная ячейка, и дает очень чистый гидроксид натрия (или калия) с концентрацией около 32%, но требует очень чистого рассола.

Другие электролитические процессы
Хотя речь идет о гораздо меньших масштабах производства, электролитические диафрагмы и мембранные технологии также используются в промышленности для извлечения хлора из соляная кислота растворы, производящие водород (но не едкую щелочь) в качестве побочного продукта.
Кроме того, электролиз плавленых хлоридных солей (Процесс спада ) также позволяет производить хлор, в данном случае как побочный продукт производства металлический натрий или магний.
Другие методы
До того, как электролитические методы стали использоваться для производства хлора, прямой окисление из хлористый водород с кислород (часто на воздухе) выполнялись в Дьяконский процесс:
- 4 HCl + O2 → 2 Cl2 + 2 часа2О
Эта реакция осуществляется с использованием хлорид меди (II) (CuCl2) как катализатор и выполняется при высокой температуре (около 400 ° C). Количество извлеченного хлора составляет примерно 80%. Из-за чрезвычайно агрессивной реакционной смеси промышленное использование этого метода затруднено, и несколько пилотных испытаний в прошлом потерпели неудачу. Тем не менее, недавние события обнадеживают. Недавно Сумитомо запатентовал катализатор процесса Дикона, используя оксид рутения (IV) (RuO2).[10]
Еще один более ранний процесс производства хлора заключался в нагревании рассола с кислота и диоксид марганца.
- 2 NaCl + 2H2ТАК4 + MnO2 → Na2ТАК4 + MnSO4 + 2 часа2O + Cl2
Используя этот процесс, химик Карл Вильгельм Шееле был первым, кто выделил хлор в лаборатории. В марганец может быть восстановлен Процесс Велдона.[11]
Небольшие количества газообразного хлора можно получить в лаборатории, поместив концентрированную соляную кислоту в колбу с боковым рычагом и присоединенной резиновой трубкой. Затем добавляют диоксид марганца и колбу закрывают пробкой. Реакция не является сильно экзотермической. Поскольку хлор плотнее воздуха, его можно легко собрать, поместив трубку внутрь колбы, где он вытеснит воздух. После заполнения колбу для сбора можно закрыть пробкой.
Другой метод получения небольших количеств газообразного хлора в лаборатории - добавление концентрированной соляной кислоты (обычно около 5M) в гипохлорит натрия или же хлорат натрия решение.
Перманганат калия может использоваться для образования газообразного хлора при добавлении к соляной кислоте.
Промышленное производство мембран
Крупномасштабное производство хлора включает несколько этапов и множество единиц оборудования. Приведенное ниже описание типично для мембранной установки. Завод также одновременно производит гидроксид натрия (каустическую соду) и газообразный водород. Типичная установка состоит из производства / обработки рассола, операций с ячейками, охлаждения и сушки хлора, сжатия и сжижения хлора, хранения и загрузки жидкого хлора, обработки щелочи, испарения, хранения и загрузки и обработки водорода.
Рассол
Ключом к производству хлора является работа системы насыщения / очистки рассола. Поддержание правильно насыщенного раствора с правильной чистотой жизненно важно, особенно для мембранных клеток. На многих заводах есть соляная куча, которую опрыскивают переработанным рассолом. В других есть цистерны для жидкого навоза, в которые подают сырую соль и переработанный рассол. Сырой рассол обрабатывают карбонат натрия и гидроксид натрия до осадок кальций и магний. Реакции часто проводят в серии реакторов перед тем, как обработанный рассол будет отправлен в большой осветлитель где осаждаются карбонат кальция и гидроксид магния. Флокулирующий агент может быть добавлен непосредственно перед осветлителем для улучшения осаждения. Декантированный рассол затем механически фильтруется с использованием песочные фильтры или же листовые фильтры перед входом в серию ионообменники для дальнейшего удаления примеси. На нескольких этапах этого процесса рассол проверяется на твердость и сила.
После ионообменников рассол считается чистым и переносится в резервуары для хранения для перекачки в камеру хранения. Чистый рассол нагревается до нужной температуры для контроля температуры рассола на выходе в соответствии с заданными параметрами. электрическая нагрузка. Рассол, выходящий из камеры, необходимо обработать для удаления остаточного хлора и контроля. pH уровней перед возвратом в насыщенность сцена. Это может быть выполнено с помощью колонн дехлорирования кислотой и бисульфит натрия добавление. Отсутствие удаления хлора может привести к повреждению ионообменных устройств. В рассоле необходимо следить за накоплением обоих хлорат анионы и сульфат-анионы, и либо иметь систему обработки, либо продувку контура солевого раствора для поддержания безопасных уровней, поскольку хлорат-анионы могут диффундировать через мембраны и загрязнять щелочь, а сульфат-анионы могут повредить покрытие поверхности анода.
Комната камеры
Здание, в котором находится множество электролитических ячеек, обычно называют ячейкой или ячейкой, хотя некоторые заводы строятся на открытом воздухе. Это здание содержит опорные конструкции для ячеек, соединения для подачи электричество к ячейкам и трубопроводам для жидкостей. Мониторинг и управление температурами каустической соды и рассола осуществляется для контроля температуры на выходе. Также отслеживаются напряжения каждой ячейки, которые меняются в зависимости от электрической нагрузки на камеру ячейки, которая используется для управления скоростью производства. Мониторинг и контроль давления в коллекторах хлора и водорода также осуществляется через клапаны регулирования давления.
Постоянный ток поставляется через исправленный источник питания. Нагрузка на установку контролируется изменением Текущий в клетки. При увеличении силы тока расход рассола, щелочи и деионизированная вода увеличиваются при понижении температуры подачи.
Охлаждение и сушка
Газообразный хлор, выходящий из линии ячеек, необходимо охладить и осушить, поскольку выходной газ может иметь температуру более 80 ° C и содержит влагу, которая делает газообразный хлор агрессивным для утюг трубопровод. Охлаждение газа позволяет пропускать большое количество влаги из рассола в конденсировать из газового потока. Охлаждение также улучшает эффективность как сжатие и разжижение следующий этап. Выход хлора в идеале составляет от 18 ° C до 25 ° C. После охлаждения поток газа проходит через ряд колонн с противотоком. серная кислота. Эти башни постепенно удаляют все оставшиеся влага от газообразного хлора. После выхода из сушильных колонн хлор фильтруют, чтобы удалить оставшуюся серную кислоту.
Сжатие и разжижение
Можно использовать несколько методов сжатия: жидкое кольцо, возвратно-поступательный, или же центробежный. На этой стадии газообразный хлор сжимается и может дополнительно охлаждаться с помощью промежуточных и дополнительных охладителей. После сжатия он поступает в ожижители, где охлаждается до степени разжижения. Неконденсирующиеся газы и остающийся газообразный хлор удаляются как часть контроля давления в системах сжижения. Эти газы направляются в газоочиститель, производя гипохлорит натрия, или используется в производстве соляной кислоты (сжиганием с водородом) или этилендихлорид (по реакции с этилен ).
Хранение и загрузка
Жидкий хлор обычно самотеком подается в резервуары для хранения. Его можно загружать в железнодорожные или автомобильные цистерны с помощью насосов или заполнять сжатым сухим газом.
Обработка, испарение, хранение и загрузка каустика
Каустик, подаваемый в камеру, течет по петле, которая одновременно отводится в хранилище с частью, разбавленной деионизированной водой, и возвращается в линию клеток для усиления внутри клеток. Щелочь, покидающую клеточную линию, необходимо контролировать на предмет прочности, чтобы поддерживать безопасные концентрации. Слишком сильный или слишком слабый раствор может повредить мембраны. Мембранные элементы обычно производят щелочь в диапазоне от 30% до 33% по весу. Поток исходной щелочи нагревается при низких электрических нагрузках для регулирования его температуры на выходе. Более высокие нагрузки требуют охлаждения каустика для поддержания правильной температуры на выходе. Каустик, поступающий в хранилище, отбирается из резервуара для хранения и может быть разбавлен для продажи клиентам, которым требуется слабый каустик, или для использования на месте. Другой поток может быть закачан в многоэффектный испаритель установка для производства товарного 50% каустика. Погрузка железнодорожных вагонов и автоцистерн осуществляется на станциях погрузки с помощью насосов.
Обработка водорода
Водород, образующийся в качестве побочного продукта, может выпускаться в необработанном виде непосредственно в атмосферу или охлаждаться, сжиматься и сушиться для использования в других процессах на месте или продаваться покупателю через трубопровод, баллоны или грузовики. Некоторые возможные применения включают производство соляной кислоты или пероксид водорода, а также обессеривание из нефть, или использовать как топливо в котлы или же топливные элементы.
Потребление энергии
Производство хлора чрезвычайно энергоемко.[12] Энергозатраты на единицу веса продукции не намного ниже, чем при производстве чугуна и стали.[13] и больше, чем для производства стекла[14] или цемент.[15]
С электричество является незаменимым сырьем для производства хлора, потребление энергии которого соответствует электрохимический реакция не может быть уменьшена. Экономия энергии достигается в первую очередь за счет применения более эффективных технологий и сокращения использования дополнительной энергии.
Рекомендации
- ^ Полинг, Линус, Общая химия, Изд. 1970 г., Дуврские публикации
- ^ «Электролитические процессы для хлора и каустической соды». Lenntech Водоподготовка и очистка воздуха Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, Нидерланды. Получено 2007-03-17.
- ^ «Ртутная ячейка». Евро Хлор. Архивировано из оригинал на 2011-09-18. Получено 2007-08-15.
- ^ Landolt, D .; Ибл Н. (1972). «Анодно-хлоратное образование на платинированном титане». Журнал прикладной электрохимии. Chapman and Hall Ltd. 2 (3): 201–210. Дои:10.1007 / BF02354977.
- ^ "Региональный семинар по повышению осведомленности о загрязнении ртутью" (PDF). ЮНЕП. Архивировано из оригинал (PDF) на 2007-10-29. Получено 2007-10-28.
- ^ «Мембранная ячейка». Евро Хлор. Архивировано из оригинал на 2007-09-27. Получено 2007-08-15.
- ^ «Электролиз рассола». Ассоциация производителей соли. Архивировано из оригинал на 2007-05-14. Получено 2007-03-17.
- ^ а б Кифер, Дэвид М. «Когда промышленность впереди». Хроники химии. Получено 2007-03-17.
- ^ «Мембранная ячейка». Евро Хлор. Архивировано из оригинал на 2007-08-14. Получено 2007-08-15.
- ^ J. Catal. 255, 29 (2008)
- ^ "Хлорная промышленность". Lenntech Водоподготовка и очистка воздуха Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, Нидерланды. Получено 2007-03-17.
- ^ «Комплексное предотвращение и контроль загрязнения (IPPC) - Справочный документ по наилучшим доступным технологиям в хлорно-щелочной промышленности». Европейская комиссия. Получено 2007-09-02.
- ^ «Комплексное предотвращение и контроль загрязнения (IPPC) - Справочный документ по наилучшим доступным методам производства чугуна и стали». Европейская комиссия. Получено 2007-09-02.
- ^ «Комплексное предотвращение и контроль загрязнения (IPPC) - Справочный документ по наилучшим доступным технологиям в стекольной промышленности». Европейская комиссия. Получено 2007-09-02.
- ^ «Комплексное предотвращение и контроль загрязнения (IPPC) - справочный документ по наилучшим доступным технологиям в промышленности по производству цемента и извести». Европейская комиссия. Получено 2007-09-02.
