Конканавалин А - Concanavalin A
| Конканавалин А | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Идентификаторы | |||||||
| Организм | |||||||
| Символ | ConA | ||||||
| PDB | 3CNA | ||||||
| UniProt | P81461 | ||||||
| |||||||
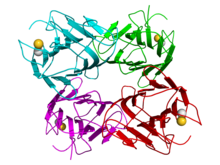
Конканавалин А (ConA) это лектин (углевод переплет белок ) первоначально извлечен из Джек-бин, Canavalia ensiformis. Он является членом лектин бобовых семья. Он специфически связывается с определенными структурами, обнаруженными в различных сахара, гликопротеины, и гликолипиды, в основном внутренний и невосстанавливающий концевой α-D-маннозил и α-D-глюкозильные группы.[2][3] ConA - это растение митоген, и известен своей способностью стимулировать субпопуляции Т-клеток мыши, приводя к возникновению четырех функционально различных популяций Т-клеток, включая предшественников регуляторные Т-клетки;[4] Подмножество супрессорных Т-клеток человека также чувствительно к ConA.[4] ConA был первым лектином, доступным на коммерческой основе, и широко используется в биология и биохимия охарактеризовать гликопротеины и другие сахаросодержащие вещества на поверхности различных клеток.[5] Он также используется для очистки гликозилированных макромолекул в лектиновая аффинная хроматография,[6] а также для изучения иммунной регуляции различными иммунными клетками.[4]
Структура и свойства
Как и большинство лектинов, ConA представляет собой гомотетрамер: каждое подразделение (26,5кДа, 235 аминокислоты, сильно гликозилированный) связывает атом металла (обычно Mn2+ и Ca2+). Он имеет D2 симметрия.[1] Его третичная структура была выяснена,[7] а также молекулярная основа его взаимодействия с металлами, а также его сродство к сахарам. манноза и глюкоза[8] хорошо известны.
ConA специфически связывает α-D-маннозил и α-D-глюкозильные остатки (две гексозы, различающиеся только спиртом на углероде 2) в концевых положениях разветвленных структур из B-гликанов (достигаются в α-маннозе или гибридных и двухантенных гликановые комплексы). Он имеет 4 сайта связывания, соответствующих 4 субъединицам.[3] В молекулярный вес это 104-112кДа и изоэлектрическая точка (pI) находится в диапазоне 4,5-5,5.
Конканавалин А имеет Низкая частота волновое число 20 см−1 в его Рамановские спектры.[9] Этот выброс был отнесен к дыхательное движение из бета-баррель состоящий из 14 бета-цепей в молекуле конканавалина А.[10]
ConA также может инициировать деление клеток (митогенез), в первую очередь воздействуя на Т-лимфоциты, стимулируя их энергетический метаболизм в течение нескольких секунд после воздействия.[11]
Биологическая активность
Конканавалин А взаимодействует с различными рецепторами, содержащими углеводы маннозы, особенно с родопсином, группа крови маркеры, рецептор инсулина[12] то Иммуноглобулины и карцино-эмбриональный антиген (CEA). Он также взаимодействует с липопротеины.[13]
ConA сильно агглютинирует эритроциты независимо от группы крови и различных раковых клеток.[14][15][16] Было продемонстрировано, что трансформированные клетки и трипсин -обработанные нормальные клетки не агглютинируют при 4 ° C, что позволяет предположить, что в ConA-опосредованной агглютинации участвует термочувствительный этап.[17][18]
Сообщалось о ConA-опосредованной агглютинации других типов клеток, включая мышечные клетки ,[19] B-лимфоциты (через поверхность Иммуноглобулины ),[20] фибробласты,[21] крыса тимоциты,[22] человеческий плод (но не взрослый) кишечные эпителиальные клетки,[23] и адипоциты.[24]
ConA - это лимфоцит митоген. Похожий на фитогемагглютинин (PHA), это селективный митоген Т-клеток по сравнению с его действием на В-клетки. PHA и ConA связывают и сшивают компоненты Рецептор Т-клеток, и их способность активировать Т-клетки зависит от экспрессии рецептора Т-клеток.[25][26]
ConA взаимодействует с поверхностью манноза остатки многих микробов, в том числе бактерий Кишечная палочка,[27] и Bacillus subtilis[28] и протист Dictyostelium discoideum.[29]
Он также был показан как стимулятор нескольких матричные металлопротеиназы (ММП).[30]
ConA оказался полезным в приложениях, требующих твердофазной иммобилизации гликоферментов, особенно тех, которые оказалось трудно иммобилизовать традиционным ковалентным связыванием. Используя матрицы ConA-пар, такие ферменты можно иммобилизовать в больших количествах без одновременной потери активности и / или стабильности. Такие нековалентные сочетания ConA-гликофермент можно относительно легко отменить путем конкуренции с сахарами или при кислом pH. Если необходимо для определенных приложений, эти связи можно преобразовать в ковалентные связи с помощью химических манипуляций.[31]
Отчет из Тайваня (2009 г.) продемонстрировал мощный терапевтический эффект ConA против экспериментальной гепатомы (рака печени); в исследовании Лэй и Чанг,[32] Было обнаружено, что ConA в большей степени секвестрируется опухолевыми клетками печени, чем окружающими нормальными гепатоцитами. Интернализация ConA происходит преимущественно в митохондриях после связывания с гликопротеинами клеточной мембраны, что вызывает аутофагическую гибель клеток. Было обнаружено, что ConA частично ингибирует рост опухолевых узлов независимо от активации его лимфоцитов; искоренение опухоли у мышей на месте Модель гепатомы в этом исследовании была дополнительно связана с митогенным / лимфопролиферативным действием ConA, которое могло активировать опосредованный CD8 + T-клетками, а также опосредованный NK- и NK-T-клетками иммунный ответ в печени.[32]
Интравитреальная инъекция ConA может использоваться при моделировании пролиферативная витреоретинопатия у крыс.[33][34]
использованная литература
- ^ а б PDB: 3CNA; Хардман К.Д., Эйнсворт К.Ф. (декабрь 1972 г.). «Структура конканавалина А при разрешении 2,4-А». Биохимия. 11 (26): 4910–9. Дои:10.1021 / bi00776a006. PMID 4638345.
- ^ Гольдштейн, Ирвин Дж .; Порец, Рональд Д. (2012). «Выделение, физико-химическая характеристика и специфичность связывания углеводов лектинов». В Liener, Irvin E .; Шарон, Натан; Гольдштейн, Ирвин Дж. (Ред.). Свойства, функции и применение лектинов в биологии и медицине. Эльзевир. С. 33–247. ISBN 978-0-323-14444-5.
- ^ а б Самнер Дж. Б., Грален Н., Эрикссон-Квенсель И. Б. (апрель 1938 г.). «Молекулярные массы уреазы, канавалина, конканавалина а и конканавалина B». Наука. 87 (2261): 395–6. Bibcode:1938Научный .... 87..395С. Дои:10.1126 / science.87.2261.395. PMID 17746464.
- ^ а б c Дуайер Дж. М., Джонсон С. (ноябрь 1981 г.). «Использование конканавалина А для изучения иммунорегуляции Т-клеток человека». Клиническая и экспериментальная иммунология. 46 (2): 237–49. ЧВК 1536405. PMID 6461456.
- ^ Шифер Х.Г., Краусс Х., Бруннер Х., Герхардт У. (декабрь 1975 г.). «Ультраструктурная визуализация поверхностных структур углеводов на мембранах микоплазм с помощью конканавалина А». Журнал бактериологии. 124 (3): 1598–600. Дои:10.1128 / JB.124.3.1598-1600.1975. ЧВК 236075. PMID 1104592.
- ^ GE Healthcare Life Sciences, Иммобилизованный лектин В архиве 2012-03-03 в Wayback Machine[требуется полная цитата ]
- ^ Мин В., Данн А.Дж., Джонс Д.Х. (апрель 1992 г.). «Негликозилированный рекомбинантный проконканавалин А активен без расщепления полипептида». Журнал EMBO. 11 (4): 1303–7. Дои:10.1002 / j.1460-2075.1992.tb05174.x. ЧВК 556578. PMID 1563347.
- ^ Лорис Р., Хамелрик Т., Букерт Дж., Винс Л. (март 1998 г.). «Лектиновый состав бобовых культур». Biochimica et Biophysica Acta (BBA) - Структура белка и молекулярная энзимология. 1383 (1): 9–36. Дои:10.1016 / S0167-4838 (97) 00182-9. PMID 9546043.
- ^ Painter PC, Mosher LE, Rhoads C (июль 1982 г.). «Низкочастотные моды в рамановских спектрах белков». Биополимеры. 21 (7): 1469–72. Дои:10.1002 / bip.360210715. PMID 7115900.
- ^ Chou KC (август 1985 г.). «Низкочастотные движения в белковых молекулах. Бета-лист и бета-баррель». Биофизический журнал. 48 (2): 289–97. Bibcode:1985BpJ .... 48..289C. Дои:10.1016 / S0006-3495 (85) 83782-6. ЧВК 1329320. PMID 4052563.
- ^ Krauss S, Buttgereit F, Brand MD (июнь 1999 г.). «Влияние митогена конканавалина А на пути энергетического метаболизма тимоцитов». Biochimica et Biophysica Acta (BBA) - Биоэнергетика. 1412 (2): 129–38. Дои:10.1016 / S0005-2728 (99) 00058-4. PMID 10393256.
- ^ Куатрекасас П., Телль Г. П. (февраль 1973 г.). «Инсулиноподобная активность конканавалина А и агглютинина зародышей пшеницы - прямое взаимодействие с рецепторами инсулина». Труды Национальной академии наук Соединенных Штатов Америки. 70 (2): 485–9. Bibcode:1973PNAS ... 70..485C. Дои:10.1073 / пнас.70.2.485. JSTOR 62526. ЧВК 433288. PMID 4510292.
- ^ Harmony JA, Cordes EH (ноябрь 1975 г.). «Взаимодействие липопротеидов низкой плотности плазмы человека с конканавалином А и рицином». Журнал биологической химии. 250 (22): 8614–7. PMID 171260.
- ^ Беттон Г.Р. (ноябрь 1976 г.). «Реакции агглютинации спонтанных опухолевых клеток собак, индуцированные конканавалином А, продемонстрированные с помощью изотопного анализа». Международный журнал рака. 18 (5): 687–96. Дои:10.1002 / ijc.2910180518. PMID 992901.
- ^ Какидзоэ Т., Комацу Х., Нидзима Т., Кавачи Т., Сугимура Т. (июнь 1980 г.). «Повышенная агглютинируемость клеток мочевого пузыря конканавалином А после введения канцерогенов». Исследования рака. 40 (6): 2006–9. PMID 7371036.
- ^ Беккер Ф. Ф., Шургин А. (октябрь 1975 г.). «Агглютинация конканавалином А клеток из первичных гепатоцеллюлярных карцином и узелков печени, индуцированная N-2-флуоренилацетамидом». Исследования рака. 35 (10): 2879–83. PMID 168971.
- ^ Инбар М., Бен-Бассат Н., Сакс Л. (ноябрь 1971 г.). «Специфическая метаболическая активность на поверхности мембраны при трансформации злокачественных клеток». Труды Национальной академии наук Соединенных Штатов Америки. 68 (11): 2748–51. Bibcode:1971PNAS ... 68.2748I. Дои:10.1073 / pnas.68.11.2748. JSTOR 61219. ЧВК 389516. PMID 4330939.
- ^ Села Б.А., Лис Х., Шарон Н., Сакс Л. (декабрь 1971 г.). «Количественное определение N-ацетил-D-галактозамин-подобных сайтов на поверхности мембраны нормальных и трансформированных клеток млекопитающих». Biochimica et Biophysica Acta (BBA) - Биомембраны. 249 (2): 564–8. Дои:10.1016/0005-2736(71)90132-5. PMID 4332414.
- ^ Gartner TK, Podleski TR (декабрь 1975 г.). «Доказательства того, что связанный с мембраной лектин опосредует слияние миобластов L6». Сообщения о биохимических и биофизических исследованиях. 67 (3): 972–8. Дои:10.1016 / 0006-291X (75) 90770-6. PMID 1201086.
- ^ де Петрис S (апрель 1975 г.). «Рецепторы конканавалина А, иммуноглобулины и тета-антиген поверхности лимфоцитов. Взаимодействие с конканавалином А и с цитоплазматическими структурами». Журнал клеточной биологии. 65 (1): 123–46. Дои:10.1083 / jcb.65.1.123. ЧВК 2111157. PMID 1092699.
- ^ Нунан К.Д., Бургер М.М. (октябрь 1973 г.). «Связь связывания конканавалина А с агглютинацией клеток, инициированной лектином». Журнал клеточной биологии. 59 (1): 134–42. Дои:10.1083 / jcb.59.1.134. ЧВК 2110924. PMID 4201706.
- ^ Capo C, Garrouste F, Benoliel AM, Bongrand P, Ryter A, Bell GI (август 1982 г.). «Конканавалин-А-опосредованная агглютинация тимоцитов: модель для количественного исследования клеточной адгезии». Журнал клеточной науки. 56: 21–48. PMID 7166565.
- ^ Вайзер М.М. (август 1972 г.). «Конканавалин А-агглютинация кишечных клеток плода человека». Наука. 177 (4048): 525–6. Bibcode:1972 г., наука ... 177..525 Вт. Дои:10.1126 / science.177.4048.525. PMID 5050484. S2CID 23661797.
- ^ Cuatrecasas P (март 1973 г.). «Взаимодействие агглютинина зародышей пшеницы и конканавалина А с изолированными жировыми клетками». Биохимия. 12 (7): 1312–23. Дои:10.1021 / bi00731a011. PMID 4696755.
- ^ Вайс А., Шилдс Р., Ньютон М., Янгер Б., Имбоден Дж. (Апрель 1987 г.). «Взаимодействия лиганд-рецептор, необходимые для активации гена интерлейкина 2». Журнал иммунологии. 138 (7): 2169–76. PMID 3104454.
- ^ Канеллопулос Дж. М., Де Петрис С., Лека Дж., Крамптон М. Дж. (Май 1985 г.). «Митогенный лектин Phaseolus vulgaris не распознает антиген Т3 человеческих Т-лимфоцитов». Европейский журнал иммунологии. 15 (5): 479–86. Дои:10.1002 / eji.1830150512. PMID 3873340.
- ^ Офек И., Мирельман Д., Шарон Н. (февраль 1977 г.). «Присоединение Escherichia coli к клеткам слизистой оболочки человека, опосредованное рецепторами маннозы». Природа. 265 (5595): 623–5. Bibcode:1977Натура.265..623O. Дои:10.1038 / 265623a0. PMID 323718. S2CID 4223466.
- ^ Дойл Р.Дж., Бердселл, округ Колумбия (февраль 1972 г.). «Взаимодействие конканавалина А с клеточной стенкой Bacillus subtilis». Журнал бактериологии. 109 (2): 652–8. Дои:10.1128 / JB.109.2.652-658.1972. ЧВК 285189. PMID 4621684.
- ^ West CM, McMahon D (июль 1977 г.). «Идентификация рецепторов конканавалина А и галактозосвязывающих белков в очищенных плазматических мембранах Dictyostelium discoideum». Журнал клеточной биологии. 74 (1): 264–73. Дои:10.1083 / jcb.74.1.264. ЧВК 2109878. PMID 559679.
- ^ Ю М., Сато Х., Сейки М., Томпсон Э. У. (август 1995 г.). «Комплексная регуляция экспрессии матричной металлопротеиназы мембранного типа и активация матричной металлопротеиназы-2 конканавалином А в клетках рака молочной железы человека MDA-MB-231». Исследования рака. 55 (15): 3272–7. PMID 7614461.
- ^ Салимуддин М., Хусейн К. (апрель 1991 г.). «Конканавалин А: полезный лиганд для иммобилизации гликофермента - обзор». Ферментные и микробные технологии. 13 (4): 290–5. Дои:10.1016/0141-0229(91)90146-2. PMID 1367163.
- ^ а б Лей Х.Й., Чанг С.П. (январь 2009 г.). «Лектин Конканавалина А как терапевтическое средство против гепатомы». Журнал биомедицинских наук. 16: 10. Дои:10.1186/1423-0127-16-10. ЧВК 2644972. PMID 19272170.
- ^ Ердяков А.К., Тихонович М.В., Ржавина Е.М., Гаврилова С.А. (май 2015 г.). «[Особенности сетчатки при развитии пролиферативной витреоретинопатии у крыс после внутриглазной инъекции конканавалина А и диспазы]». Российский Физиологический Журнал Имени И.М. Сеченова. 101 (5): 572–85. PMID 26263683.
- ^ Тихонович М.В., Ердяков А.К., Гаврилова С.А. (август 2018 г.). «Нестероидная противовоспалительная терапия более эффективно подавляет развитие пролиферативной витреоретинопатии, чем стероидная». Международная офтальмология. 38 (4): 1365–1378. Дои:10.1007 / s10792-017-0594-3. PMID 28639085. S2CID 4017540.
внешние ссылки
- Конканавалин + А в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Конканавалин + А + рецепторы в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Конканавалин А структура
- Мир лектина, путь к лектинам
- Протеопедия 1bxh con A в комплексе с метил-альфа1-2 маннобиозидом
