Сборка макромолекул - Macromolecular assembly
Эта статья включает список литературы, связанное чтение или внешние ссылки, но его источники остаются неясными, потому что в нем отсутствует встроенные цитаты. (Октябрь 2019) (Узнайте, как и когда удалить этот шаблон сообщения) |
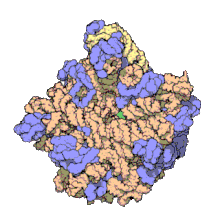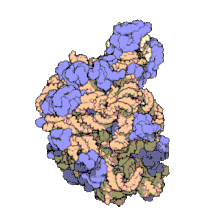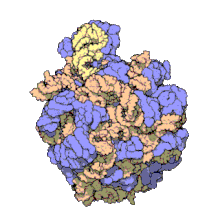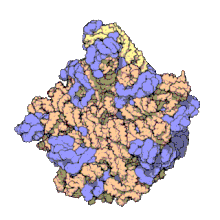
Период, термин сборка макромолекул (MA) относится к массивным химическим структурам, таким как вирусы и небиологический наночастицы, Сотовая связь органеллы и мембраны и рибосомы и т. д., которые представляют собой сложные смеси полипептид, полинуклеотид, полисахарид или другой полимерный макромолекулы. Как правило, они относятся к более чем одному из этих типов, и смеси определяются пространственно (то есть в отношении их химической формы), а также в отношении их основного химического состава и структура. Макромолекулы находятся в живых и неживых вещах и состоят из многих сотен или тысяч атомы держится вместе ковалентные связи; они часто характеризуются повторяющимися единицами (т. е. полимеры ). Их совокупности также могут быть биологическими или небиологическими, хотя термин MA чаще применяется в биологии, а термин супрамолекулярная сборка чаще применяется в небиологических контекстах (например, в супрамолекулярная химия и нанотехнологии ). МА макромолекул в определенных формах удерживаются нековалентный межмолекулярные взаимодействия (а не ковалентные связи), и могут быть в любой неповторяющейся структуре (например, как в рибосома (изображение) и клеточная мембрана архитектур), или в повторяющихся линейных, круговых, спиральных или других образцах (например, как в актиновые нити и жгутиковый мотор, изображение). Процесс формирования МА получил название молекулярная самосборка, термин, особенно применяемый в небиологическом контексте. Для изучения МА существует большое разнообразие физических / биофизических, химических / биохимических и вычислительных методов; Учитывая масштаб (молекулярные размеры) МА, попытки разработать их состав и структуру, а также выявить механизмы, лежащие в основе их функций, находятся на переднем крае современной структурной науки.

Биомолекулярный комплекс

А биомолекулярный комплекс, также называемый биомакромолекулярный комплекс, состоит ли любой биологический комплекс из более чем одного биополимер (белок, РНК, ДНК,[5]углевод ) или крупные неполимерные биомолекулы (липид ). Взаимодействия между этими биомолекулами нековалентны.[6]Примеры:
- Белковые комплексы, некоторые из которых мультиферментные комплексы: протеасома, Холофермент ДНК-полимераза III, Холофермент РНК-полимеразы II, симметричный вирусный капсиды, шаперониновый комплекс GroEL -GroES, фотосистема I, АТФ-синтаза, ферритин.
- РНК-белковые комплексы: рибосома, сплайсосома, свод, SnRNP. Такие комплексы в ядре клетки называют рибонуклеопротеины (РНП).
- ДНК-белковые комплексы: нуклеосома.
- Белково-липидные комплексы: липопротеин.[7][8]
Биомакромолекулярные комплексы изучаются структурно. Рентгеновская кристаллография, ЯМР-спектроскопия белков, криоэлектронная микроскопия и последующие анализ отдельных частиц, и электронная томография.[9]Модели атомной структуры, полученные методами рентгеновской кристаллографии и биомолекулярной ЯМР-спектроскопии, могут быть состыкованный в гораздо более крупные структуры биомолекулярных комплексов, полученные методами более низкого разрешения, такими как электронная микроскопия, электронная томография и малоугловое рассеяние рентгеновских лучей.[10]
Комплексы макромолекул повсеместно встречаются в природе, где они участвуют в создании вирусов и всех живых клеток. Кроме того, они играют фундаментальную роль во всех основных жизненных процессах (трансляция белков, деление клеток, торговля пузырьками, внутри- и межклеточный обмен материалом между компартментами и т. д.). В каждой из этих ролей сложные смеси организуются определенным структурным и пространственным образом. В то время как отдельные макромолекулы удерживаются вместе комбинацией ковалентных связей и внутримолекулярные нековалентные силы (то есть ассоциации между частями внутри каждой молекулы через заряд-зарядовые взаимодействия, силы Ван дер Ваальса, и диполь-дипольные взаимодействия такие как водородные связи ), по определению сами МА удерживаются вместе исключительно через нековалентный силы, за исключением прилагаемых сейчас между молекулы (т.е. межмолекулярные взаимодействия ).[нужна цитата ]
Шкалы MA и примеры
Изображения выше дают представление о составе и масштабе (размерах), связанных с МА, хотя они только начинают касаться сложности структур; в принципе, каждая живая клетка состоит из МА, но сама также является МА. В примерах и других подобных комплексах и сборках МА часто составляют миллионы дальтон по молекулярной массе (мегадальтон, т. е. в миллионы раз больше веса отдельного простого атома), но все же имея измеримые соотношения компонентов (стехиометрия ) с некоторым уровнем точности. Как указано в условных обозначениях изображений, при надлежащей подготовке МА или составляющие субкомплексы МА часто могут быть кристаллизованы для изучения с помощью кристаллография белков и родственные методы, или изучены другими физическими методами (например, спектроскопия, микроскопия ).[нужна цитата ]
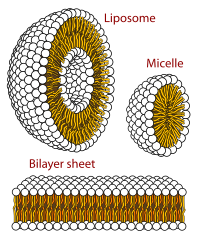

Вирусные структуры были одними из первых изученных магистров; другие биологические примеры включают рибосомы (частичное изображение выше), протеасомы и комплексы трансляции (с белок и нуклеиновая кислота компоненты), прокариотические и эукариотические транскрипционные комплексы, и ядерный и другие биологические поры которые позволяют материалу проходить между ячейками и клеточными компартментами. Биомембраны также обычно считаются МА, хотя требования к структурному и пространственному определению изменяются с учетом присущих молекулярная динамика мембраны липиды, и белков внутри липидные бислои.[нужна цитата ]
Исследования магистров
Изучение структуры и функции МА является сложной задачей, в частности, из-за их мегадальтонных размеров, но также из-за их сложного состава и различной динамической природы. Большинство из них применяли стандартные химические и биохимические методы (методы очистка белка и центрифугирование, химические и электрохимический характеристика и др.). Кроме того, их методы обучения включают современные протеомный подходы, вычислительные методы и структурные методы атомарного разрешения (например, Рентгеновская кристаллография ), малоугловое рассеяние рентгеновских лучей (SAXS) и малоугловое рассеяние нейтронов (SANS), силовая спектроскопия и просвечивающая электронная микроскопия и криоэлектронная микроскопия. Аарон Клуг был признан с 1982 г. Нобелевская премия в области химии за его работу по выяснению структуры с помощью электронной микроскопии, в частности, для МА белок-нуклеиновая кислота, включая вирус табачной мозаики (структура, содержащая 6400 базовых оцРНК молекулы и> 2000 молекул белка оболочки). Решение по кристаллизации и структуре рибосомы с молекулярной массой ~ 2,5 МДа, являющейся частью белкового синтетического «механизма» живых клеток, было предметом исследования 2009 г. Нобелевская премия по химии награжден Венкатраман Рамакришнан, Томас А. Стейтц, и Ада Э. Йонат.[нужна цитата ]
Небиологические аналоги
Наконец, биология - не единственная сфера магистерских программ. Поля супрамолекулярная химия и нанотехнологии у каждого есть области, которые были разработаны для разработки и расширения принципов, впервые продемонстрированных в биологических МА. Особый интерес в этих областях вызывает разработка фундаментальных процессов молекулярные машины, и расширение известных конструкций машин на новые типы и процессы.[нужна цитата ]
Смотрите также
- Многоступенчатое моделирование биомолекул
- Четвертичная структура
- Мультибелковый комплекс
- Органелла: самое широкое определение «органеллы» включает не только связанные с мембраной клеточные структуры, но и очень большие биомолекулярные комплексы.
- Многоступенчатое моделирование биомолекул
использованная литература
- ^ Бан Н., Ниссен П., Хансен Дж., Мур П., Стейтц Т. (2000). «Полная атомная структура большой рибосомальной субъединицы при разрешении 2,4 Ангстрема». Наука. 289 (5481): 905–20. Bibcode:2000Sci ... 289..905B. CiteSeerX 10.1.1.58.2271. Дои:10.1126 / science.289.5481.905. PMID 10937989.
- ^ Уильям МакКлюр. "50S субъединица рибосомы". Архивировано из оригинал на 2005-11-24. Получено 2019-10-09.
- ^ Осборн А.Р., Рапопорт Т.А., ван ден Берг Б. (2005). «Транслокация белка по каналу Sec61 / SecY». Ежегодный обзор клеточной биологии и биологии развития. 21: 529–50. Дои:10.1146 / annurev.cellbio.21.012704.133214. PMID 16212506.
- ^ Легенда, обложка, J. Bacteriol., Октябрь 2006 г.[требуется полная цитата ]
- ^ Кляйнджунг, Йенс; Franca Fraternali (1 июля 2005 г.). «ПОПСКОМП: автоматизированный анализ взаимодействия биомолекулярных комплексов». Исследования нуклеиновых кислот. 33 (приложение 2): W342 – W346. Дои:10.1093 / нар / gki369. ISSN 0305-1048. ЧВК 1160130. PMID 15980485. Получено 2013-11-14.
- ^ Мур, Питер Б. (2012). «Как мы должны думать о рибосомах?». Ежегодный обзор биофизики. 41 (1): 1–19. Дои:10.1146 / annurev-biophys-050511-102314. PMID 22577819.
- ^ Нойман, Николь (январь 2016). «Сложный высокомолекулярный комплекс: тенденции в биохимических науках». Тенденции в биохимических науках. 41 (1): 1–3. Дои:10.1016 / j.tibs.2015.11.006. PMID 26699226. Получено 2018-07-11.
- ^ Дутта, Шучисмита; Берман, Хелен М. (2005-03-01). «Крупные макромолекулярные комплексы в банке данных о белках: отчет о состоянии». Структура. 13 (3): 381–388. Дои:10.1016 / j.str.2005.01.008. ISSN 0969-2126. PMID 15766539.
- ^ Рассел, Роберт Б; Фрэнк Альбер; Патрик Элой; Фред П. Дэвис; Дмитрий Коркин; Матье Пишо; Майя Топф; Андрей Сали (июнь 2004 г.). «Структурная перспектива белок-белковых взаимодействий». Текущее мнение в структурной биологии. 14 (3): 313–324. Дои:10.1016 / j.sbi.2004.04.006. ISSN 0959-440X. PMID 15193311.
- ^ van Dijk, Aalt D. J .; Рольф Боленс; Александр М. Дж. Дж. Бонвин (2005). «Докинг на основе данных для исследования биомолекулярных комплексов». Журнал FEBS. 272 (2): 293–312. Дои:10.1111 / j.1742-4658.2004.04473.x. HDL:1874/336958. ISSN 1742-4658. PMID 15654870.
- ^ «Структура жидких липидных бислоев». Blanco.biomol.uci.edu. 2009-11-10. Получено 2019-10-09.
- ^ Экспериментальная система, диолеоилфосфатидилхолин бислои. Гидрофобная углеводородная область липида составляет ~ 30 Å (3,0 нм), как определено комбинацией методов рассеяния нейтронов и рентгеновских лучей; аналогично, полярная / интерфейсная область (глицерил, фосфат и фрагменты головной группы с их объединенной гидратацией) составляет ~ 15 Å (1,5 нм). с каждой стороны, для общей толщины, примерно равной углеводородной области. См. S.H. Белые ссылки, предшествующие и последующие.
- ^ Винер MC и Белый SH (1992). «Структура жидкого бислоя диолеоилфосфатидилхолина, определенная совместным уточнением данных рентгеновской дифракции и нейтронографии. III. Полная структура». Биофиз. J. 61 (2): 434–447. Bibcode:1992BpJ .... 61..434Вт. Дои:10.1016 / S0006-3495 (92) 81849-0. ЧВК 1260259. PMID 1547331.[неосновной источник необходим ]
- ^ Размеры углеводородов меняются в зависимости от температуры, механического напряжения, структуры PL, соформуляторов и т. Д. В процентах от однозначных до низких двузначных цифр от этих значений.[нужна цитата ]
дальнейшее чтение
Общие обзоры
- Уильямсон, Дж. Р. (2008). «Кооперативность в сборке макромолекул». Природа Химическая Биология. 4 (8): 458–465. Дои:10.1038 / nchembio.102. PMID 18641626.
- Перракис А., Мусаккио А., Кьюсак С., Петоса С. Исследование макромолекулярного комплекса: инструментарий методов. J Struct Biol. 2011 Август; 175 (2): 106-12. DOI: 10.1016 / j.jsb.2011.05.014. Epub 2011 18 мая. Обзор. PubMed PMID: 21620973.
- Dafforn TR. Так как же узнать, что у вас есть макромолекулярный комплекс? Acta Crystallogr D Biol Crystallogr. 2007 Янв; 63 (Pt 1): 17-25. Epub 2006 13 декабря. Обзор. PubMed PMID: 17164522; PubMed Central PMCID: PMC2483502.
- Вольгемут I, Ленц С., Урлауб Х. Изучение стехиометрии макромолекулярных комплексов с помощью масс-спектрометрии на основе пептидов. Протеомика. 2015 Март; 15 (5-6): 862-79. DOI: 10.1002 / pmic.201400466. Epub 2015 6 февраля. Обзор. PubMed PMID: 25546807; PubMed Central PMCID: PMC5024058.
- Синха К., Арора К., Мун С.С., Ярлагадда С., Вудроффе К., Нарен А.П. Фёрстеровский резонансный перенос энергии - подход к визуализации пространственно-временной регуляции образования макромолекулярных комплексов и компартментализированной клеточной передачи сигналов. Biochim Biophys Acta. 2014 Октябрь; 1840 (10): 3067-72. DOI: 10.1016 / j.bbagen.2014.07.015. Epub 2014 30 июля. Обзор. PubMed PMID: 25086255; PubMed Central PMCID: PMC4151567.
- Берг, Дж. Тимочко, Я. и Страйер, Л., Биохимия. (W. H. Freeman and Company, 2002), ISBN 0-7167-4955-6
- Кокс, М. и Нельсон, Д.Л., Принципы биохимии Ленингера. (Palgrave Macmillan, 2004), ISBN 0-7167-4339-6
Обзоры на конкретные МА
- Валле М. Почти потеряна в переводе. Крио-ЭМ динамического макромолекулярного комплекса: рибосома. Eur Biophys J. 2011 May; 40 (5): 589-97. DOI: 10.1007 / s00249-011-0683-6. Epub 2011 19 февраля. Обзор. PubMed PMID: 21336521.
- Мони Т.П. Каноническая инфламмасома: высокомолекулярный комплекс, вызывающий воспаление. Subcell Biochem. 2017; 83: 43-73. DOI: 10.1007 / 978-3-319-46503-6_2. Обзор. PubMed PMID: 28271472.
- Perino A, Ghigo A, Damilano F, Hirsch E. Идентификация макромолекулярного комплекса, ответственного за PI3Kgamma-зависимую регуляцию уровней цАМФ. Biochem Soc Trans. 2006 август; 34 (Pt 4): 502-3. Обзор. PubMed PMID: 16856844.
Основные источники
- Lasker, K .; Förster, F .; Walzthoeni, T .; Вилла, E .; Unverdorben, P .; Бек, Ф .; Aebersold, R .; Сали, А .; Баумейстер, В. (2012). «Молекулярная архитектура голокомплекса 26S протеасомы, определенная интегративным подходом». Proc Natl Acad Sci USA. 109 (5): 1380–7. Bibcode:2012ПНАС..109.1380Л. Дои:10.1073 / pnas.1120559109. ЧВК 3277140. PMID 22307589.
- Russel, D .; Lasker, K .; Webb, B .; Velázquez-Muriel, J .; Tjioe, E .; Шнейдман-Духовный, Д .; Петерсон, Б .; Сали, А. (2012). «Собираем части вместе: программное обеспечение платформы интегративного моделирования для определения структуры макромолекулярных сборок». ПЛОС Биол. 10 (1): e1001244. Дои:10.1371 / journal.pbio.1001244. ЧВК 3260315. PMID 22272186.
- Бархум С., Палит С., Йетирадж А. Исследования диффузионного ЯМР образования макромолекулярных комплексов, скученности и удержания в мягких материалах. Prog Nucl Magn Reson Spectrosc. 2016 Май; 94-95: 1-10. DOI: 10.1016 / j.pnmrs.2016.01.004. Epub 2016 4 февраля. Обзор. PubMed PMID: 27247282.
Другие источники
- Нобелевские премии по химии (2012 г.), Нобелевские премии по химии 2009 г., Венкатраман Рамакришнан, Томас А. Стейтц, Ада Э. Йонат, Нобелевская премия по химии 2009 г., по состоянию на 13 июня 2011 г.
- Нобелевские премии по химии (2012 г.), Нобелевские премии по химии 1982 г., Аарон Клуг, Нобелевская премия по химии 1982 г., по состоянию на 13 июня 2011 г.
внешние ссылки
- Beck Group (2019), Структура и функции крупных макромолекулярных ансамблей (домашняя страница группы Beck), Beck Group - Структура и функции больших молекулярных ансамблей - EMBL, по состоянию на 13 июня 2011 г.
- DMA Group (2019), Динамика сборки макромолекул (домашняя страница DMA Group), Динамика участка сборки макромолекул | Национальный институт биомедицинской визуализации и биоинженерии, по состоянию на 13 июня 2011 г.
