Нейростимуляция - Neurostimulation
| Нейростимуляция | |
|---|---|
| Код ОПС-301 | 8-631 |
Нейростимуляция целенаправленная модуляция нервная система активность с использованием инвазивных (например, микроэлектроды ) или неинвазивными средствами (например, транскраниальная магнитная стимуляция или же транскраниальная электростимуляция, tES, например tDCS или же транскраниальная стимуляция переменным током, tACS). Нейростимуляция обычно относится к электромагнитным подходам к нейромодуляция.
Технология нейростимуляции может улучшить качество жизни тех, кто серьезно парализован или страдает от глубоких поражений различных органов чувств, а также для постоянного уменьшения сильной хронической боли, которая в противном случае потребовала бы постоянной (круглосуточной) высокой дозы опиоидная терапия (например, невропатическая боль и повреждение спинного мозга). Он служит ключевой частью нервное протезирование за слуховые аппараты, искусственное зрение, Протезы, и мозг-машина интерфейсы. В случае нейронной стимуляция в основном используется электрическая стимуляция и используются зарядово-сбалансированные двухфазные сигналы постоянного тока или подходы к инжекции заряда с емкостной связью. В качестве альтернативы, транскраниальная магнитная стимуляция и транскраниальная электростимуляция были предложены как неинвазивные методы, в которых либо магнитное поле или транскраниально приложенные электрические токи вызывают нейростимуляцию.[1][2]
Стимуляция мозга
Стимуляция мозга имеет потенциал для лечения некоторых заболеваний, таких как: эпилепсия. В этом методе запланированная стимуляция применяется к конкретным кортикальным или подкорковым целям. Есть в наличии коммерческие устройства[3] который может доставлять электрический импульс через запланированные промежутки времени. Предполагается, что запланированная стимуляция изменяет внутренние нейрофизиологические свойства эпилептических сетей. Наиболее изученными целями для запланированной стимуляции являются переднее ядро таламус и гиппокамп. Было изучено переднее ядро таламуса, которое показало значительное уменьшение приступов при применении стимулятора. на против выключенный в течение нескольких месяцев после имплантации стимулятора.[4] Более того, приступообразная головная боль (CH) можно лечить с помощью временного стимулирующего электрода в клиновидно-небный ганглий (САУ). Облегчение боли достигается в течение нескольких минут после стимуляции при использовании этого метода.[5] Чтобы избежать использования имплантированных электродов, исследователи разработали способы вписать «окно» из диоксида циркония, которое было модифицировано, чтобы стать прозрачным, и имплантировано в черепа мышей, чтобы позволить оптическим волнам проникать более глубоко, как в оптогенетика, чтобы стимулировать или ингибировать отдельные нейроны.[6]
Глубокая стимуляция мозга
Глубокая стимуляция мозга (DBS) показал преимущества при двигательных расстройствах, таких как: болезнь Паркинсона, тремор и дистония и аффективные расстройства, такие как депрессия, обсессивно-компульсивное расстройство, синдром Туретта, хроническая боль и кластерная головная боль. Поскольку DBS может напрямую изменять активность мозга контролируемым образом, он используется для картирования фундаментальных механизмов функций мозга наряду с методами нейровизуализации.
Простая система DBS состоит из двух разных частей. Сначала в мозг имплантируются крошечные микроэлектроды, которые доставляют в ткани импульсы стимуляции. Во-вторых, электрическая генератор импульсов (PG) генерирует импульсы стимуляции, которые посылаются на электроды через микропровода.
Применение и влияние DBS как на нормальный, так и на больной мозг включает множество параметров. К ним относятся физиологические свойства ткани мозга, которые могут изменяться в зависимости от болезненного состояния. Также важны параметры стимуляции, такие как амплитудные и временные характеристики, а также геометрическая конфигурация электрода и ткани, которая его окружает.
Несмотря на огромное количество исследований DBS, механизм его действия до сих пор не изучен. Разработка микроэлектродов DBS по-прежнему остается сложной задачей.[7]
Неинвазивная стимуляция мозга

Транскраниальная магнитная стимуляция
По сравнению с электростимуляцией, которая использует кратковременный электрический разряд высокого напряжения для активации нейронов, которые потенциально могут активировать болевые волокна, транскраниальная магнитная стимуляция (ТМС) был разработан Baker в 1985 году. TMS использует магнитный провод над скальп, который несет резкий и сильный импульс тока. Изменяющееся во времени магнитное поле индуцируется перпендикулярно катушке из-за приложенного импульса, который, следовательно, создает электрическое поле на основе Максвелл закон. Электрическое поле обеспечивает необходимый ток для неинвазивной и гораздо менее болезненной стимуляции. Существуют два устройства TMS, которые называются TMS с одиночным импульсом и TMS с повторяющимися импульсами (rTMS), в то время как последнее имеет больший эффект, но может вызвать приступ. ТМС может использоваться для терапии, особенно при психиатрия, как инструмент для измерения центральной моторной проводимости и инструмент исследования для изучения различных аспектов физиологии человеческого мозга, таких как моторная функция, зрение и язык. Метод rTMS использовался для лечения эпилепсии с частотой 8–25 Гц в течение 10 секунд. Другие терапевтические применения rTMS включают болезни паркинсона, дистонию и расстройства настроения. Кроме того, ТМС можно использовать для определения вклада корковых сетей в определенные когнитивные функции путем нарушения активности в фокальной области мозга.[1] Были получены ранние, неубедительные результаты по выздоровлению из комы (стойкое вегетативное состояние ) Папе и др. (2009).[8]

Транскраниальная электростимуляция
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Апрель 2017 г.) |
- Транскраниальная стимуляция постоянным током (tDCS)
- Транскраниальная стимуляция переменным током (tACS)
- Транскраниальная стимуляция импульсным током (tPCS)
- Транскраниальная стимуляция случайным шумом (tRNS)
Стимуляция спинного мозга
Стимуляция спинного мозга (SCS) - эффективная терапия для лечения хронической и трудноизлечимой боли, включая диабетическая невропатия, синдром неудачной операции на спине, рефлекторная симпатическая дистрофия, фантомная конечность боль, ишемическая конечность боль, синдром рефрактерной односторонней боли в конечностях, постгерпетическая невралгия и острый опоясывающий герпес боль. Еще одно болевое состояние, которое является потенциальным кандидатом на лечение СКС, - это Шарко-Мари-Зуб (ШМТ) заболевание, которое связано с умеренной и сильной хронической болью в конечностях.[9] СКС-терапия заключается в электростимуляции спинного мозга для «маскировки» боли. В теория ворот предложен в 1965 г. Мельзак и стена[10] предоставил теоретическую конструкцию для попытки использования СКС в качестве клинического лечения хронической боли. Эта теория постулирует, что активация миелинизированных первичных клеток большого диаметра афферентные волокна подавляет реакцию спинной рог нейроны поступают от небольших немиелинизированных первичных афферентов. Простая система SCS состоит из трех различных частей. Сначала в эпидуральное пространство имплантируют микроэлектроды для доставки импульсов стимуляции к ткани. Во-вторых, генератор электрических импульсов, имплантированный в нижнюю часть живота или ягодичная область в то время как подключается к электродам с помощью проводов, а в-третьих, пульт дистанционного управления для регулировки параметров стимула, таких как ширина импульса и частота импульсов в PG. Были достигнуты улучшения как в клинических аспектах SCS, таких как переход от субдурального размещения контактов к эпидуральному размещению, что снижает риск и заболеваемость имплантации SCS, так и в технических аспектах SCS, таких как улучшение чрескожных отведений и полностью имплантируемые мульти- стимуляторы каналов. Однако существует множество параметров, которые необходимо оптимизировать, включая количество имплантированных контактов, размер и расстояние контактов, а также источники электрического тока для стимуляции. Ширина импульса стимула и частота импульсов являются важными параметрами, которые необходимо настроить в SCS, которые обычно составляют 400 мкс и 8–200 Гц соответственно.[11]
Чрескожная стимуляция супраорбитального нерва
Предварительные данные подтверждают чрескожную стимуляцию супраорбитального нерва.[12] Побочных эффектов немного.[13]
Кохлеарные имплантаты

Кохлеарные имплантаты обеспечили частичный слух более чем 120 000 человек во всем мире по состоянию на 2008 год. Электрическая стимуляция используется в кохлеарном имплантате для обеспечения функционального слуха у полностью глухих людей. Кохлеарные имплантаты включают несколько компонентов подсистемы от внешнего речевого процессора и радиочастота (RF) канал передачи к внутреннему приемнику, стимулятору и массивам электродов. Современные исследования кохлеарных имплантатов начались в 1960-х и 1970-х годах. В 1961 году грубое одноэлектродное устройство было имплантировано двум глухим пациентам, и было сообщено о полезном слухе с помощью электрической стимуляции. Первое полное одноканальное устройство, одобренное FDA, было выпущено в 1984 году.[14]В кохлеарных имплантатах звук улавливается микрофоном и передается на заушный внешний процессор для преобразования в цифровые данные. Оцифрованные данные затем модулируются радиочастотным сигналом и передаются на антенна внутри головного убора. Носитель данных и мощности передаются через пару связанных катушек в герметичный внутренний блок. За счет извлечения мощности и демодуляции данных команды электрического тока отправляются на улитка для стимуляции слухового нерва с помощью микроэлектродов.[15] Ключевым моментом является то, что во внутреннем блоке нет батареи, и он должен быть в состоянии извлекать необходимую энергию. Также для уменьшения заражения данные передаются по беспроводной сети вместе с питанием. Катушки с индуктивной связью являются хорошими кандидатами для телеметрии мощности и данных, хотя радиочастотная передача может обеспечить лучшую эффективность и скорость передачи данных.[16] Параметры, необходимые внутреннему блоку, включают амплитуду импульса, длительность импульса, интервал между импульсами, активный электрод и обратный электрод, которые используются для определения двухфазного импульса и режима стимуляции. Примером коммерческих устройств является устройство Nucleus 22, в котором использовалась несущая частота 2,5 МГц, а в более поздней версии, названной устройством Nucleus 24, несущая частота была увеличена до 5 МГц.[17] Внутренний блок кохлеарных имплантатов - это ASIC (специализированная интегральная схема ) чип, отвечающий за безопасную и надежную электростимуляцию. Внутри микросхемы ASIC есть прямой путь, обратный путь и блоки управления. Прямой канал восстанавливает цифровую информацию из радиочастотного сигнала, которая включает параметры стимуляции и некоторые биты подтверждения связи, чтобы уменьшить ошибку связи. Обратный путь обычно включает в себя устройство выборки напряжения обратной телеметрии, которое считывает напряжение в течение определенного периода времени на регистрирующем электроде. Блок стимулятора отвечает за подачу заданного тока от внешнего блока к микроэлектродам. Этот блок включает эталонный ток и цифро-аналоговый преобразователь преобразовывать цифровые команды в аналоговый ток.[18]
Визуальный протез

Теоретические и экспериментальные клинические данные свидетельствуют о том, что прямая электрическая стимуляция сетчатки могла бы обеспечить некоторое зрение субъектам, утратившим светочувствительные элементы своего тела. сетчатка.[19] Следовательно, визуальные протезы разработаны для восстановления зрения слепых с помощью стимуляции. В зависимости от того, какой зрительный путь локация предназначена для нервной стимуляции, рассмотрены разные подходы. Зрительный путь состоит в основном из глаз, Зрительный нерв, латеральное коленчатое ядро (LGN) и зрительная кора. Следовательно, стимуляция сетчатки, зрительного нерва и зрительной коры - это три различных метода, используемых в визуальных протезах.[20]Дегенеративные заболевания сетчатки, такие как пигментный ретинит (RP) и возрастная дегенерация желтого пятна (AMD) - это два вероятных заболевания-кандидата, при которых может быть полезна стимуляция сетчатки. Три подхода, называемые внутриглазной эпиретинальной, субретинальной и экстраокулярной трансретинальной стимуляцией, используются в устройствах для сетчатки, которые стимулируют оставшиеся нервные клетки сетчатки для обхода потерянных фоторецепторов и позволяют зрительному сигналу достигать мозга через нормальный зрительный путь. При эпиретинальном доступе электроды располагаются на верхней стороне сетчатки рядом с ганглиозные клетки,[21] тогда как электроды помещаются под сетчатку при субретинальных доступах.[22] Наконец, задняя склеральная поверхность глаза - это место, в котором расположены электроды экстраокулярного доступа. Second Sight и группа Humayun в USC являются наиболее активными группами в разработке внутриглазных протезов сетчатки. Имплант сетчатки ArgusTM 16 представляет собой внутриглазный протез сетчатки с использованием технологий обработки видео. Что касается стимуляции зрительной коры, Бриндли и Добелле были первыми, кто провел эксперименты и продемонстрировал это, стимулировав верхнюю сторону зрительной коры большинства электродов. может производить визуальное восприятие.[11] Совсем недавно Саван построил полный имплант для внутрикортикальной стимуляции и проверил операцию на крысах.[23]

LGN, который расположен в среднем мозге и передает сигналы от сетчатки в зрительную кору, является еще одной потенциальной областью, которая может быть использована для стимуляции. Но доступ к этой области ограничен из-за сложности хирургического вмешательства. Недавний успех методов глубокой стимуляции мозга, нацеленных на средний мозг поощряет исследования по применению метода стимуляции LGN для визуального протеза.[24]
Аппараты электростимуляции сердца
Имплантируемые кардиостимуляторы были предложены впервые в 1959 году и с тех пор стали более совершенными. Терапевтическое применение кардиостимуляторов состоит из множества нарушения ритма включая некоторые формы тахикардия (слишком быстрое сердцебиение), сердечная недостаточность, и даже Инсульт. Первые имплантируемые кардиостимуляторы работали недолго и нуждались в периодической подзарядке с помощью индуктивной связи. Этим имплантируемым кардиостимуляторам необходим генератор импульсов для стимуляции сердца. мышцы с определенной скоростью помимо электродов.[25] Сегодня современные генераторы импульсов программируются неинвазивным способом с помощью сложных компьютеризированных машин, использующих радиочастоты, которые получают информацию о состоянии пациента и устройства с помощью телеметрии. Также они используют одиночный герметичный иодид лития (LiI) элемент в качестве аккумулятора. Схема кардиостимулятора включает в себя усилители чувствительности для обнаружения внутренних электрических сигналов сердца, которые используются для отслеживания сердечной активности, схемы адаптации частоты, которые определяют необходимость увеличения или уменьшения частоты кардиостимуляции, микропроцессор, память для хранения параметров, управление телеметрией для связи протокол и источники питания для обеспечения регулируемого напряжения.[26]
Микроэлектродные технологии стимуляции
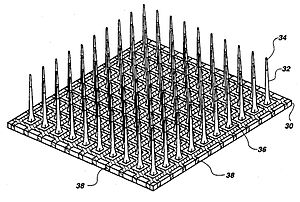
Микроэлектроды - один из ключевых компонентов нейростимуляции, которые доставляют ток к нейронам. Типичные микроэлектроды состоят из трех основных компонентов: подложки ( перевозчик), проводящий металлический слой и изоляционный материал. В кохлеарных имплантатах микроэлектроды состоят из платино-иридиевый сплав. Современные электроды имеют более глубокий ввод, чтобы лучше соответствовать тонотопный место стимуляции в полосе частот, назначенной каждому каналу электрода, что повышает эффективность стимуляции и уменьшает травмы, связанные с введением. Эти электроды кохлеарного имплантата бывают прямыми или спиральными, например, микроэлектроды Med El Combi 40+ и Advanced Bionics Helix соответственно. В визуальных имплантатах существует два типа электродных решеток, называемых плоскими или трехмерными игольчатыми или столбчатыми, где массив игольчатых типов, например поскольку матрица Utah в основном используется для стимуляции кортикального и зрительного нервов и редко используется в имплантатах сетчатки из-за возможного повреждения сетчатки. Однако массив золотых электродов в форме столбика на тонкой пленке полиимид был использован в экстраокулярном имплантате. С другой стороны, плоские электродные решетки сформированы из гибких полимеров, таких как силикон, полиимид и Парилен в качестве кандидатов для имплантатов сетчатки. Что касается микроэлектродов DBS, массив, которым можно управлять независимо, распределенный по ядру-мишени, позволит точно контролировать пространственное распределение стимуляции и, таким образом, позволит лучше персонализировать DBS. К микроэлектродам DBS предъявляется несколько требований, которые включают длительный срок службы без повреждения тканей или разрушения электродов, адаптированный для различных участков мозга, длительный срок службы. биосовместимость материала, механически прочный, чтобы достичь цели без повреждения во время манипуляции хирургом-имплантологом, и, наконец, равномерность работы микроэлектродов в определенной матрице. Вольфрам микропровода, микропровода иридия, напыленные или электроосажденные[27] Платино-иридиевый сплав микроэлектроды являются примерами микроэлектродов, используемых в DBS.[11] Карбид кремния представляет собой потенциально интересный материал для создания биосовместимых полупроводниковых устройств.[28]
История
Основные выводы о нейростимуляции возникли из идеи стимуляции нервов в терапевтических целях. Первое зарегистрированное использование электростимуляции для снятия боли относится к 46 году нашей эры, когда Скрибоний Ларг использовали рыбу-торпеду (электрический скат) для снятия головной боли.[29] В конце 18 века Луиджи Гальвани обнаружили, что мышцы мертвых лягушачьих лапок подергиваются при попадании постоянного тока в нервную систему.[30] Модуляция мозг активность путем электростимуляции моторной коры у собак была показана в 1870 году, что привело к движению конечностей.[31] С конца 18 века до сегодняшнего дня было разработано много вех. В настоящее время сенсорные протезы, такие как визуальные имплантаты, кохлеарные имплантаты, слуховые имплантаты среднего мозга и стимуляторы спинного мозга, а также моторные протезы, такие как глубокие стимуляторы головного мозга, микростимуляторы Bion, интерфейс управления и восприятия мозга и устройства электростимуляции сердца широко используются.[11]
В 2013 году британская фармацевтическая компания GlaxoSmithKline (GSK) придумала термин «электроокевтика» для широкого охвата медицинское оборудование которые используют электрическую, механическую или световую стимуляцию для воздействия электрическая сигнализация в соответствующих типах тканей.[32][33] Клинические нейронные имплантаты, такие как кохлеарные имплантаты восстановить слух, имплантаты сетчатки восстановить зрение, стимуляторы спинного мозга для снятия боли или кардиостимуляторы и имплантируемый дефибрилляторы Предлагаются образцы электрокосовтиков.[32] GSK сформировала венчурный фонд и сообщила, что в 2013 году проведет конференцию, чтобы изложить программу исследований в этой области.[34] Обзор исследований взаимодействия нервной и иммунной систем в 2016 г. аутоиммунные расстройства вскользь и в кавычках упомянули «электрохимические препараты», имея в виду разрабатываемые устройства нейростимуляции для лечения таких состояний, как артрит.[35]
Исследование
Помимо того, что нейростимуляция широко используется в клинических целях, она также широко используется в лабораториях, основанных еще в 1920-х годах такими людьми, как Дельгадо, которые использовали стимуляцию в качестве экспериментальной манипуляции для изучения основ работы мозга. Основные работы были над центром вознаграждения мозга, в котором стимуляция этих структур приводила к удовольствию, которое требовало большей стимуляции. Другой недавний пример - электрическая стимуляция МТ-области первичной зрительной коры для искажения восприятия. В частности, направленность движения регулярно отображается в области МТ. Они представили обезьян с движущимися изображениями на экране, а пропускная способность обезьян должна была определить направление. Они обнаружили, что, систематически вводя некоторые ошибки в реакции обезьяны, стимулируя МТ-область, отвечающую за восприятие движения в другом направлении, обезьяна реагировала где-то посередине между фактическим движением и стимулированным. Это было изящное использование стимуляции, чтобы показать, что область МП играет важную роль в реальном восприятии движения. В рамках объем памяти поле, стимуляция очень часто используется для проверки прочности связи между одним пучком клеток с другим путем приложения небольшого тока в одной клетке, что приводит к высвобождению нейротрансмиттеров и измерению постсинаптический потенциал.
Как правило, короткий, но высокочастотный ток в диапазоне 100 Гц помогает укрепить соединение, известное как долгосрочное потенцирование. Однако более длинный, но низкочастотный ток имеет тенденцию ослаблять соединения, известные как длительная депрессия.[36]
Смотрите также
Рекомендации
- ^ а б Халлетт М (июль 2000 г.). «Транскраниальная магнитная стимуляция и мозг человека». Природа. 406 (6792): 147–50. Bibcode:2000Натурал.406..147H. Дои:10.1038/35018000. PMID 10910346.
- ^ Ниче, Майкл А .; Коэн, Леонардо Г.; Вассерманн, Эрик М .; Приори, Альберто; Ланг, Николас; Антал, Андреа; Паулюс, Уолтер; Хуммель, Фридхельм; Boggio, Paulo S .; Фрегни, Фелипе; Паскуаль-Леоне, Альваро (2008). «Транскраниальная стимуляция постоянным током: современное состояние 2008». Стимуляция мозга 1 (3): 206–23.
- ^ Medtronic, Миннеаполис, Миннесота, США.
- ^ Джобст BC, Дарси TM, Тадани В.М., Робертс Д.В. (июль 2010 г.). «Стимуляция мозга для лечения эпилепсии». Эпилепсия. 51 (Дополнение 3): 88–92. Дои:10.1111 / j.1528-1167.2010.02618.x. PMID 20618409.
- ^ Ансариния М., Резаи А., Теппер С.Дж. и др. (Июль 2010 г.). «Электростимуляция клиновидно-небного ганглия для лечения острых кластерных головных болей». Головная боль. 50 (7): 1164–74. Дои:10.1111 / j.1526-4610.2010.01661.x. PMID 20438584.
- ^ Даместани, Ясаман (2013). «Прозрачный нанокристаллический протез свода черепа из стабилизированного оксидом иттрия диоксида циркония». Наномедицина. 9 (8): 1135–8. Дои:10.1016 / j.nano.2013.08.002. PMID 23969102. • Объяснил Мохан, Джеффри (4 сентября 2013 г.). «Окно в мозг? Оно здесь, - говорит команда UC Riverside». Лос-Анджелес Таймс.
- ^ Крингельбах М.Л., Дженкинсон Н., Оуэн С.Л., Азиз Т.З. (август 2007 г.). «Трансляционные принципы глубокой стимуляции мозга». Nat. Преподобный Neurosci. 8 (8): 623–35. Дои:10.1038 / nrn2196. PMID 17637800.
- ^ Папе Т., Розенов Дж., Льюис Дж., Ахмед Дж., Уокер М., Гернон А., Рот Х., Патил В. (2009). Повторяющиеся нейроповеденческие достижения, связанные с транскраниальной магнитной стимуляцией, во время выхода из комы, Brain Stimul, 2 (1): 22–35. Epub 2008 23 октября.
- ^ Скарибас И.М .; Вашберн С.Н. (Январь 2010 г.). «Успешное лечение хронической боли Шарко-Мари-Зуб с помощью стимуляции спинного мозга: тематическое исследование». Нейромодуляция. 13 (3): 224–8. Дои:10.1111 / j.1525-1403.2009.00272.x. PMID 21992836.
- ^ Melzack R, Wall PD (ноябрь 1965 г.). «Механизмы боли: новая теория». Наука. 150 (3699): 971–9. Bibcode:1965Научный ... 150..971М. Дои:10.1126 / science.150.3699.971. PMID 5320816.
- ^ а б c d Greenbaum, Elias S .; Дэвид Чжоу (2009). Имплантируемые нейронные протезы 1: устройства и применение. Биологическая и медицинская физика, биомедицинская инженерия. Берлин: Springer. ISBN 978-0-387-77260-8.
- ^ Jürgens, TP; Леоне, М. (июнь 2013 г.). «Жемчуг и подводные камни: нейростимуляция при головной боли». Цефалгия: международный журнал головной боли. 33 (8): 512–25. Дои:10.1177/0333102413483933. PMID 23671249.
- ^ Schoenen, J; Роберта, B; Magis, D; Коппола, Г. (29 марта 2016 г.). «Неинвазивные методы нейростимуляции для терапии мигрени: имеющиеся данные». Цефалгия: международный журнал головной боли. 36 (12): 1170–1180. Дои:10.1177/0333102416636022. PMID 27026674.
- ^ Дом WF, Urban J (1973). «Отдаленные результаты имплантации электродов и электронной стимуляции улитки у человека». Анна. Отол. Ринол. Ларингол. 82 (4): 504–17. Дои:10.1177/000348947308200408. PMID 4721186.
- ^ СК, Парк С.И., Джун С.Б. и др. (Июнь 2007 г.). «Дизайн упрощенной системы кохлеарного имплантата». IEEE Trans Biomed Eng. 54 (6 Pt 1): 973–82. Дои:10.1109 / TBME.2007.895372. HDL:10371/7911. PMID 17554817.
- ^ Николаев, Денис; Джозеф, Wout; Жадобов, Максим; Сауло, Ронан; Мартенс, Люк (13 марта 2019 г.). «Оптимальное излучение капсул, имплантированных в тело». Письма с физическими проверками. 122 (10): 108101. Bibcode:2019PhRvL.122j8101N. Дои:10.1103 / PhysRevLett.122.108101. HDL:1854 / LU-8611129. PMID 30932680.
- ^ П. Кросби, К. Дейли, Д. Мани и др., Август 1985 г., "Система кохлеарных имплантатов для слухового протеза". Патент США 4532930.
- ^ Ghovanloo M .; Наджафи К. (декабрь 2004 г.). «Модульная 32-позиционная микросистема беспроводной нейростимуляции». IEEE J. Твердотельные схемы. 39 (12): 2457–66. Bibcode:2004IJSSC..39.2457G. CiteSeerX 10.1.1.681.6677. Дои:10.1109 / jssc.2004.837026.
- ^ Клаузен Дж (1955). «Визуальные ощущения (фосфены), вызванные стимуляцией синусоидальной волны переменного тока». Acta Psychiatr Neurol Scand Suppl. 94: 1–101. PMID 13258326.
- ^ Weiland J.D .; Хумаюн М.С. (Июль 2008 г.). «Визуальный протез». Труды IEEE. 96 (7): 1076–84. Дои:10.1109 / JPROC.2008.922589.
- ^ Хумаюн М.С., де Хуан Э., Дагнели Г., Гринберг Р.Дж., Пропст Р.Х., Филлипс Д.Х. (январь 1996 г.). «Визуальное восприятие, вызванное электрической стимуляцией сетчатки у слепых людей». Arch. Офтальмол. 114 (1): 40–6. Дои:10.1001 / archopht.1996.01100130038006. PMID 8540849.[постоянная мертвая ссылка ]
- ^ Чау А.Ю., Чау В.Ю. (март 1997 г.). «Субретинальная электростимуляция сетчатки глаза кролика». Neurosci. Латыш. 225 (1): 13–6. Дои:10.1016 / S0304-3940 (97) 00185-7. PMID 9143006.
- ^ Саван, Мохамад. "Биография Резюме".
- ^ Pezaris JS, Reid RC (май 2007 г.). «Демонстрация искусственного зрительного восприятия, созданного посредством микростимуляции таламуса». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 104 (18): 7670–5. Bibcode:2007ПНАС..104.7670П. Дои:10.1073 / pnas.0608563104. ЧВК 1863473. PMID 17452646.
- ^ Elmvquist R .; Сеннинг А. (1960). «Имплантируемый кардиостимулятор для сердца». В Smyth CN (ред.). Медицинская электроника. Париж: Iliffe & Sons.
- ^ Уоррен Дж., Нельсон Дж. (2000). «Электрокардиостимуляторы и схемы импульсного генератора ICD». В Ellenbogen KA, Kay GN, Wilkoff BL (ред.). Клиническая кардиостимуляция и дефибрилляция (2-е изд.). Филадельфия: У. Б. Сондерс. С. 194–216.
- ^ «Микроэлектроды».
- ^ Saddow SE (2011). Биотехнология карбида кремния: биосовместимый полупроводник для современных биомедицинских устройств и приложений. Elsevier LTD. ISBN 978-0-12385-906-8.
- ^ Дженсен Дж. Э., Конн Р. Р., Хейзелригг Г., Хьюетт Дж. Э. (1985). «Использование чрескожной нервной стимуляции и изокинетического тестирования в артроскопической хирургии коленного сустава». Am J Sports Med. 13 (1): 27–33. Дои:10.1177/036354658501300105. PMID 3872082.
- ^ Вайсштейн, Эрик В. (2002). "Гальвани, Луиджи (1737–1798)". Мир научной биографии Эрика Вайсштейна. Wolfram Research.
- ^ Fritsch G .; Хитциг Э. (1870). «Uber die elektrische Erregbarkeit des Grosshirns». Arch. Анат. Физиол. 37: 300–332.
- ^ а б Мур, Сэмюэл (29 мая 2015 г.). "Блуждающий нерв: черный ход для взлома мозга". IEEE Spectrum. Получено 4 июн 2015.
- ^ Фамм, Кристоффер; Литт, Брайан; Трейси, Кевин Дж .; Бойден, Эдвард С .; Слауи, Монсеф (10 апреля 2013 г.). «Открытие лекарств: толчок для электрокцевтики». Природа. 496 (7444): 159–161. Bibcode:2013Натура.496..159F. Дои:10.1038 / 496159a. ЧВК 4179459. PMID 23579662.
- ^ Солон, Оливия (28 мая 2013 г.). «Электроокерамика: замена лекарств на приборы». Проводная Великобритания.
- ^ Рирдон, Колин (октябрь 2016 г.). «Нейроиммунные взаимодействия при холинергическом противовоспалительном рефлексе». Письма иммунологии. 178: 92–96. Дои:10.1016 / j.imlet.2016.08.006. PMID 27542331.
- ^ Интервью с доктором Дж. Маннсом, Университет Эмори, октябрь 2010 г.
