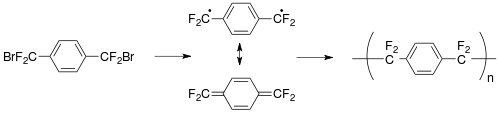
Парилен - Parylene

Парилен это общее название полимер чей костяк состоит из параграф -бензолдиил кольца -C
6ЧАС
4- связаны 1,2-этандиил мосты -CH
2–CH
2-. Его можно получить полимеризацией параграф-ксилилен ЧАС
2C=C
6ЧАС
4=CH
2.
Это название также используется для нескольких полимеров с одной и той же основной цепью, где некоторые водород атомы заменяются другими функциональные группы. Некоторые из этих вариантов обозначаются в продаже буквенно-цифровыми кодами, такими как «парилен C» и «парилен AF-4». Некоторые из этих имен зарегистрированы товарные знаки в некоторых странах.
Покрытия из парилена часто наносят на электронные схемы и другое оборудование как электрическая изоляция, влагозащитные барьеры или защита от коррозия и химическая атака. Они также используются для уменьшения трение и в медицине для предотвращения побочных реакций на имплантированные устройства. Эти покрытия обычно наносятся химическое осаждение из паровой фазы в атмосфере мономер параграф-ксилилен.
Парилен считается «зеленый» полимер потому что его полимеризация не требует инициатор или другие химические вещества для прерывания цепи; и покрытия могут наноситься при комнатной температуре или около нее, без каких-либо растворитель.
История
Парилен был открыт в 1947 г. Майкл Шварц как один из продуктов термического разложения параграф-ксилол ЧАС
3C–C
6ЧАС
4–CH
3 выше 1000 ° C. Шварц идентифицировал параграф-ксилилен в качестве предшественника, наблюдая, что реакция с йодом дает параграф-ксилилен ди-иодид как единственный продукт. Выход реакции составлял всего несколько процентов.[1][2]
Более эффективный маршрут был найден в 1965 году Уильямом Ф. Горхэмом в Union Carbide. Он наносил париленовые пленки термическим разложением [2.2] парациклофана при температурах выше 550 ° C и в вакууме ниже 1 торр. Для этого процесса не требовался растворитель, и в результате были получены химически стойкие пленки без отверстий. Union Carbide выпустила на рынок систему покрытия из парилена в 1965 году.[1][2]
Union Carbide продолжила исследования по синтезу многочисленных прекурсоров парилена, включая парилен AF-4, с 1960-х по начало 1970-х годов. Union Carbide приобрела NovaTran (установку для нанесения покрытий из парилена) в 1984 году и объединила ее с другими предприятиями по производству химических покрытий для электроники, чтобы сформировать подразделение Specialty Coating Systems. Подразделение было продано Cookson Electronics в 1994 году.[3]
В мире есть компании, предоставляющие услуги по нанесению покрытий из парилена, но коммерческая доступность парилена ограничена. Предшественники [2.2] парациклофана можно приобрести для париленов N, C, D, AF-4 и VT-4. Услуги по парилену предоставляются для N, C, AF-4, VT-4 и E (сополимер N и E).
Разновидности
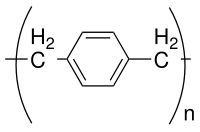
Парилен Н
Парилен N представляет собой незамещенный полимер, полученный полимеризацией параграф-ксилилен промежуточный.
Хлорированные парилены

Производные парилена могут быть получены заменой атомов водорода на фенил кольцо или алифатический мост другими функциональными группами. Наиболее распространенным из этих вариантов является парилен C, в котором один атом водорода в арильном кольце заменен на хлор. Другой распространенный вариант - парилен D с двумя такими заменами в кольце.
Парилен С является наиболее часто используемой разновидностью из-за низкой стоимости его предшественника и баланса его свойств, таких как диэлектрические и влагонепроницаемые свойства, а также простоты осаждения. Основным недостатком для многих применений является его нерастворимость в каком-либо растворителе при комнатной температуре, что препятствует удалению покрытия при повторной обработке детали.
Парилен С также является наиболее часто используемым из-за его относительно низкой стоимости.[4] Его можно наносить при комнатной температуре, сохраняя при этом высокую степень конформности и однородности, а также умеренную скорость нанесения в периодическом процессе.
Кроме того, хлор на фенильном кольце париленовой повторяющейся единицы C проблематичен для RoHS соблюдение, особенно для печатная плата производство. Кроме того, часть предшественника димера разлагается за счет разрыва связи арил-хлор во время пиролиза, образуя углеродистый материал, который загрязняет покрытие, и хлористый водород HCl это может повредить вакуумные насосы и другое оборудование. Атом хлора покидает фенильное кольцо в пиролизной трубке при всех температурах; однако оптимизация температуры пиролиза минимизирует эту проблему. Свободный радикал (фенильный радикал), образующийся в этом процессе, не стабилизируется резонансом и смягчает отложение париленоподобного материала на нижней стороне трубки для пиролиза. Этот материал обугливается и на месте образует частицы, загрязняющие чистые помещения и вызывающие дефекты на печатных платах, которые часто называют «стрингерами и узелками». Парилен N и E не имеют этой проблемы и предпочтительны для производства и использования в чистых помещениях.
Фторированные парилены
Другой распространенный галогенированный вариант - парилен AF-4, в котором четыре атома водорода в алифатической цепи заменены на фтор атомы. Этот вариант также продается под торговыми марками парилен SF (Киско ) и НТ парилен (SCS ). -CF
2- звено, которое включает этиленовую цепь, такое же, как повторяющееся звено PTFE (Тефлон), обладающий превосходной стойкостью к окислению и УФ-излучению. Парилен AF-4 использовался для защиты наружных ВЕЛ успешно отображает и освещает воду, соль и загрязняющие вещества.
Другой фторированный вариант - это парилен VT-4 (также называемый париленом F), в котором четыре атома водорода арильного кольца замещены фтором. Этот вариант продается компанией Kisco под торговой маркой Parylene CF. Из-за алифатического -CH2- единиц, он имеет плохую стойкость к окислению и УФ-излучению, но все же лучше, чем N, C или D.
Алкилзамещенные парилены
Атомы водорода можно заменить также на алкильные группы. Замещение может происходить либо в фенильном кольце, либо в этиленовом мостике, либо в обоих.
В частности, замена одного водорода в фенильном кольце на метильная группа или этильная группа группа дает парилен M и парилен E соответственно.

Парилен М

Парилен E

Парилен АМ-2
Эти замещения увеличивают межмолекулярное расстояние (от цепи к цепи), что делает полимер более растворимым и проницаемым. Например, было показано, что по сравнению с париленом C, парилен M имеет более низкую диэлектрическую проницаемость (2,48 против 3,2 при 1 кГц ). Парилен E имел более низкий модуль упругости (175 кПи против 460 кПи / кв. Дюйм), более низкую диэлектрическую проницаемость (2,34 против 3,05 при 10 кГц), несколько худшие влагонепроницаемые свойства (4,1 против 0,6 г-мил / атом-100 дюйм2-24ч). и эквивалентный пробой диэлектрика 5-6 кВоль / мил для покрытия толщиной 1 мил), но с лучшей растворимостью.[5][6]. Однако сополимер парилена N и E имеет такие же барьерные характеристики, как и парилен C.
Замена одного водорода на метил на каждом атоме углерода этильного мостика дает парилен АМ-2, [- (CH
3) CH– (C
6ЧАС
4) - (CH
3) CH–]
п (не путать с амин -замещенный вариант торговой марки Kisco). Растворимость парилена АМ-2 не так хороша, как у парилена Е.
Реактивные парилены
Хотя париленовые покрытия в основном используются для защиты объекта от воды и других химикатов, для некоторых применений требуется покрытие, которое может связываться с клеями или другими покрытыми деталями или иммобилизовать различные молекулы, такие как красители, катализаторы или ферменты.
Эти «реактивные» париленовые покрытия могут быть получены с химически активными заместителями. Два имеющихся в продаже продукта - парилен А, один из которых амин заместитель -NH
2 в каждом блоке, и парилен AM, с одним метилен аминовая группа -CH
2NH
2 на единицу. (Оба являются товарными знаками Kisco.)
Парилен AM более реактивен, чем вариант A. Амин последнего, находящийся рядом с фенильным кольцом, находится в состоянии резонансной стабилизации и поэтому менее щелочной. Однако парилен А синтезировать гораздо проще, и, следовательно, он стоит дешевле.
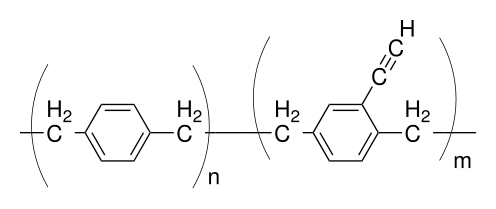
Другой реактивный вариант - парилен X, который имеет этинильная группа –C≡CH присоединен к фенильному кольцу в некоторых звеньях. Этот вариант, не содержащий элементов, кроме водорода и углерода, может быть сшитый под действием тепла или УФ-излучения и может реагировать с медь или же серебро соли для образования соответствующих металлоорганических комплексов Cu-ацетилид или же Ag-ацетилид. Он также может пройти 'щелкните по химии ', и может использоваться как клей, позволяя связывать парилен с париленом без каких-либо побочных продуктов во время обработки. В отличие от большинства других вариантов, парилен X аморфный (некристаллический).
Цветные парилены
Есть возможность прикрепить хромофор непосредственно к молекуле основания [2.2] парациклофана для придания цвета парилену.[нужна цитата ]
Париленоподобные сополимеры
Сополимеры[7] и нанокомпозиты (SiO2/ парилен C)[8] парилена осаждались ранее при температуре, близкой к комнатной; а с сильно электроноакцепторными сомономерами парилен можно использовать в качестве инициатора для инициирования полимеризации, например, с N-фенилом. малеимид. Использование парилена C / SiO2 В нанокомпозитах парилен С может быть использован в качестве жертвенного слоя для изготовления тонких нанопористых пленок диоксида кремния с пористостью> 90%.[9]
Характеристики
Прозрачность и кристалличность
Тонкие пленки и покрытия из парилена прозрачны; однако они не являются аморфными, за исключением алкилированных париленов. т.е. парилен E. В результате того, что покрытия являются полукристаллическими, они рассеивают свет. Парилен N и C имеют низкую степень кристалличности; однако парилен VT-4 и AF-4 являются высококристаллическими ~ 60% в их состоянии после осаждения (гексагональная кристаллическая структура) и поэтому обычно не подходят в качестве оптических материалов.
Парилен C станет более кристаллическим при нагревании при повышенных температурах до температуры плавления 270 ° C.
Парилен N имеет моноклинная кристаллическая структура в своем состоянии после осаждения, и он не становится заметно более кристаллическим, пока не подвергнется кристаллографическому фазовому превращению при ~ 220 ° C в гексагональный, при котором он становится высококристаллическим, как фторированные парилены. Он может достигать 80% кристалличности при температуре отжига до 400 ° C, после чего он разрушается.
Механический и химический
Парилены относительно гибкие (парилен N 0,5 ГПа).[10] кроме сшитого парилена X (1,0 ГПа)[11] и они обладают плохой стойкостью к окислению (~ 60-100 ° C в зависимости от критериев отказа) и устойчивостью к УФ-излучению,[12] кроме парилена АФ-4. Однако парилен AF-4 более дорогой из-за трехстадийного синтеза его предшественника с низким выходом и низкой эффективностью осаждения. Их устойчивость к ультрафиолетовому излучению настолько низка, что парилен нельзя подвергать воздействию обычного солнечного света без пожелтения.
Почти все парилены нерастворимы при комнатной температуре, за исключением алкилированных париленов, одним из которых является парилен E [6] и алкилированные этинилпаралены.[13] Отсутствие растворимости затрудняет переработку печатных плат, покрытых париленом.
Проницаемость
В качестве барьера для диффузии влаги эффективность галогенированных париленовых покрытий нелинейно зависит от их плотности. Атомы галогена, такие как F, Cl и Br, добавляют покрытию большую плотность и, следовательно, позволяют покрытию быть лучшим диффузионным барьером; однако, если парилены используются в качестве диффузионного барьера против воды, то неполярные химические соединения, такие как парилен E, намного более эффективны. Три основных параметра материала, которые должны быть оптимизированы для мебельных барьеров, это: плотность покрытия, полярность покрытия (лучше всего химический состав олефинов) и температура стеклования выше комнатной температуры, а в идеале выше предела службы печатной платы, устройства или детали. В этом отношении лучшим выбором является парилен E, хотя он имеет более низкую плотность по сравнению, например, с париленом C.
Процесс нанесения покрытия
Покрытия из парилена обычно наносятся путем химического осаждения из паровой фазы в атмосфере мономера. параграф-ксилилен или его производное. Этот метод имеет одно очень сильное преимущество, а именно, что он не производит никаких побочных продуктов, кроме полимера парилена, которые необходимо удалить из реакционной камеры и которые могут помешать полимеризации.
Покрываемые детали должны быть чистыми, чтобы обеспечить хорошее прилегание пленки. Поскольку мономер диффундирует, участки, на которые не следует наносить покрытие, должны быть герметично закрыты, без зазоров, щелей или других отверстий. Деталь необходимо поддерживать в относительно узком диапазоне давления и температуры.[14]
Процесс состоит из трех этапов: образование газообразного мономера, адсорбция на поверхности детали и полимеризация адсорбированной пленки.
Полимеризация
Полимеризация адсорбированного п-ксилиленовый мономер требует минимальной пороговой температуры. Для парилена N его пороговая температура составляет 40 ° C.
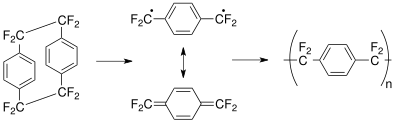
В п-ксилиленовый промежуточный продукт имеет два квантово-механических состояния, бензоидное состояние (триплетное состояние) и хиноидное состояние (синглетное состояние). Триплетное состояние эффективно является инициатором, а синглетное состояние - мономером. Триплетное состояние может быть деактивировано при контакте с переходными металлами или оксидами металлов, включая Cu / CuO.Икс.[15][16] Многие парилены демонстрируют эту селективность, основанную на квантово-механической дезактивации триплетного состояния, включая парилен X.
Полимеризация может протекать разными путями, которые различаются временным окончанием растущих цепей, например радикальной группой -CH•
2 или отрицательная анионная группа CH−
2:

Физисорбция
Полимеризация мономера происходит только после его физической адсорбции (физисорбированный ) на поверхности детали. Этот процесс имеет обратный Кинетика Аррениуса, что означает, что он сильнее при более низких температурах, чем при более высоких температурах. Существует критическая пороговая температура, выше которой физическая адсорбция практически отсутствует, а значит, и осаждения. Чем ближе температура осаждения к пороговой температуре, тем слабее физадсорбция. Парилен C имеет более высокую пороговую температуру, 90 ° C, и, следовательно, имеет гораздо более высокую скорость осаждения, более 1 нм / с, при этом получаются достаточно однородные покрытия.[4] Напротив, пороговая температура парилена AF-4 очень близка к комнатной температуре (30–35 ° C), в результате его эффективность осаждения низкая.[17]
Важным свойством мономера является так называемый «коэффициент прилипания», который выражает степень его адсорбции на полимере. Более низкий коэффициент приводит к более равномерной толщине осаждения и более плотному покрытию.
Другое важное свойство процесса осаждения - поляризуемость, которая определяет, насколько сильно мономер взаимодействует с поверхностью. Осаждение галогенированных париленов сильно коррелирует с молекулярной массой мономера. Исключением являются фторированные варианты: поляризуемость парилена AF-4 низкая, что приводит к неэффективному осаждению.
Генерация мономера
Из циклического димера
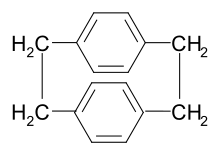
В п-ксилиленовый мономер обычно образуется в процессе нанесения покрытия путем испарения циклический димер [2.2]параграф-циклофан при относительно низкой температуре, затем разлагается пар при 450–700 ° C и давлении 0,01–1,0 торр. Этот метод (процесс Горхэма) дает 100% мономер без побочных продуктов или разложения мономера. [18],[19][20]
Димер можно синтезировать из п-ксилол, включающий несколько стадий, включающих бромирование, аминирование и Устранение Хофмана.[21]
Тот же метод можно использовать для нанесения замещенных париленов. Например, парилен C может быть получен из димерного предшественника дихлор [2.2]параграф-циклофан, за исключением того, что температуру необходимо тщательно контролировать, так как хлор -арил связь разрывается при 680 ° C.
Стандартный процесс Горэма[5] приведено выше для парилена AF-4. Октафтор [2.2]параграфДимер предшественника -циклофана может быть сублимирован при температуре ниже <100 ° C и подвергнут крекингу при 700-750 ° C, что выше, чем температура (680 ° C), используемая для крекинга незамещенного циклофана, поскольку -CF2-CF2- связь прочнее, чем -CH2-CH2- связь. Этот стабилизированный резонансом промежуточный продукт транспортируется в камеру для осаждения при комнатной температуре, где полимеризация происходит в условиях низкого давления (1–100 мТорр).[17]
Из замещенного п-ксилолы
Другой путь к получению мономера - использование параграфпредшественник -ксилола с подходящим заместителем на каждом метильные группы, устранение которых порождает параграф-ксилилен.
При выборе уходящей группы можно учитывать ее токсичность (которая исключает реакции на основе серы и амина), то, насколько легко она покидает предшественник, и возможное вмешательство в полимеризацию. Уходящая группа может либо улавливаться перед камерой осаждения, либо она может быть очень летучей, так что она не конденсируется в последней.[22]
Например, предшественник α, α'-дибром-α, α, α ', α'-тетрафтор-параграф-ксилол (CF
2Br)
2(C
6ЧАС
4) дает парилен АФ-4 с удалением бром.[23]
Преимущество этого процесса - низкая стоимость синтеза прекурсора. Прекурсор также является жидкостью и может быть доставлен стандартными методами, разработанными в полупроводниковой промышленности, такими как испаритель, испаритель с барботер, или регулятор массового расхода. Первоначально прекурсор был просто термически растрескавшимся.[24], но подходит катализаторы понизьте температуру пиролиза, что приведет к меньшему количеству остатков полукокса и лучшему покрытию.[25][26] В любом случае атомарный бром свободный радикал испускается с каждого метильного конца, который может быть преобразован в бромистый водород HBr и удален из потока мономеров. Необходимы особые меры предосторожности, поскольку бром и HBr токсичны и вызывают коррозию по отношению к большинству металлов и металлических сплавов, а бром может повредить витон Уплотнительные кольца.

В аналогичном синтезе для парилена N используется прекурсор α, α'-диметокси-п-ксилол.[27] В метокси группа ЧАС
3CO- уходящая группа; хотя он конденсируется в камере для осаждения, он не мешает осаждению полимера.[22] Этот прекурсор намного дешевле, чем [2.2]параграф-циклофан. Более того, поскольку температура жидкости чуть выше комнатной, этот прекурсор можно надежно доставить с помощью регулятор массового расхода; в то время как образование и доставка газообразного мономера в процессе Горхэма трудно измерить и контролировать.[28]

Тот же химический состав может генерировать парилен. AM-2 может быть получен из прекурсора α, α'-диметил-α, α'-диметокси-п-ксилол.
Другой пример этого подхода - синтез парилена AF-4 из α, α'-дифенокси-α, α, α ', α'-тетрафтор-параграф-ксилол. В этом случае уходящая группа фенокси CH
5О-, который может конденсироваться перед камерой осаждения.[29]
Характеристики и преимущества
Парилены могут придавать деталям с покрытием несколько желаемых качеств. Среди других свойств они
- Гидрофобный, химически стойкие и в основном непроницаемые для газов (включая водяной пар) и неорганических и органических жидкостей (включая сильные кислоты и базы ).
- Хороший электрический изолятор с низким диэлектрическая постоянная (в среднем в плоскости и вне плоскости: 2,67 парилена N и 2,5 парилена AF-4, SF, HT)[30]
- Стабильно и приемлемо в биологических тканях, одобрено США FDA для различных медицинских приложений.
- Плотный и без отверстий для толщины более 1,4 нм[31]
- Однородный и равномерно толстый, даже внутри полостей.
- Устойчив к окислению до 350 ° C (AF-4, SF, HT)
- Низкий коэффициент трения (AF-4, HT, SF)
Поскольку процесс нанесения покрытия происходит при температуре окружающей среды в умеренном вакууме, его можно наносить даже на чувствительные к температуре объекты, такие как сухие биологические образцы. Низкая температура также приводит к низкому внутреннее напряжение в тонкой пленке. Более того, единственный газ в камере осаждения - это мономер, без каких-либо растворителей, катализаторов или побочных продуктов, которые могут повредить объект.
Парилен AF-4 и VT-4 оба фторированы и, как следствие, очень дороги по сравнению с париленами N и C, что серьезно ограничивает их коммерческое использование, за исключением нишевых приложений.
Приложения
Для покрытия применяют парилен С и в меньшей степени АФ-4, СФ, НТ (все тот же полимер). печатные платы (Печатные платы) и медицинское оборудование. Существует множество других применений, поскольку парилен является отличным барьером для влаги. Это наиболее биологически приемлемое покрытие для стентов, дефибрилляторов, кардиостимуляторов и других устройств, постоянно имплантируемых в тело.[32]
Молекулярные слои
Классический химический состав молекулярного слоя: самособирающиеся монослои (ЗУР). SAM представляют собой длинноцепочечные алкильные цепи, которые взаимодействуют с поверхностями на основе взаимодействия серы и металла (алкилтиолаты).[33] или реакция золь-гель типа с гидроксилированной оксидной поверхностью (трихлорсилилалкилы или триалкоксиалкилы).[34] Однако, если поверхность золота или оксида не подвергается тщательной обработке и алкильная цепь не является длинной, эти SAM образуют неупорядоченные монослои, которые плохо упаковываются.[35][36] Отсутствие упаковки вызывает проблемы, например, в прикол в МЭМС устройств.[37]
Наблюдение за тем, что парилены могут образовывать упорядоченные молекулярные слои (МС), пришло с угол контакта измерения, где ML толщиной более 10 Å имели равновесный контактный угол 80 градусов (такой же, как объемный парилен N), но более тонкие имели уменьшенный контактный угол.[31] Это также было подтверждено электрическими измерениями (измерения напряжения смещения и температуры) с использованием конденсаторов металл-диэлектрик-полупроводник (MISCAP).[38] Короче говоря, парилен N и AF-4 (эти парилены без функциональных групп) не имеют точечных отверстий при ~ 14 Å. Это происходит из-за того, что повторяющиеся звенья парилена обладают фенильным кольцом и из-за высокой электронной поляризуемости соседних повторяющихся звеньев фенильного кольца упорядочиваются в плоскости XY. В результате этого взаимодействия МС париленов не зависят от поверхности, за исключением переходных металлов, которые деактивируют триплетное (бензоидное) состояние, и поэтому парилены не могут быть инициированы. Открытие париленов в виде молекулярных слоев очень важно для промышленного применения из-за надежности процесса и того, что ML осаждаются при комнатной температуре. Таким образом, парилены могут использоваться в качестве диффузионных барьеров и для снижения поляризуемости поверхности (дезактивации оксидных поверхностей). Сочетая свойства реакционноспособных париленов с наблюдением, что они могут образовывать плотные молекулярные слои, свободные от точечных отверстий, парилен X был использован в качестве интерфейсного слоя секвенирования генома.
Одно предостережение в отношении париленов молекулярного слоя, а именно, они откладываются в виде олигомеров, а не с высоким содержанием полимера.[31] В результате требуется вакуумный отжиг для превращения олигомеров в высокополимер. Для парилена N эта температура составляет 250 ° C, а для пайрлена AF-4 - 300 ° C.
Типичные области применения
Пленки из парилена используются в различных областях, в том числе[1]
- Гидрофобное покрытие (гидроизоляция, например, для биомедицинских шлангов)
- Барьерные слои (например, для фильтров, диафрагм, клапанов)
- СВЧ-электроника (например, защита диэлектрических подложек из ПТФЭ от загрязнения маслом)
- Имплантируемые медицинские устройства
- Датчики в неблагоприятных условиях (например, автомобильные датчики топлива / воздуха)
- Электроника для космических путешествий и обороны
- Защита от коррозии металлических поверхностей
- Армирование микроструктур
- Защита пластика, резины и др. От вредных условий окружающей среды
- Сокращение трение, например, для направления катетеров, игл для акупунктуры и микроэлектромеханические системы.
Смотрите также
Рекомендации
- ^ а б c Джеффри Б. Фортин; То-Мин Лу (2003). Химическая полимеризация методом осаждения из паровой фазы: рост и свойства тонких пленок парилена. Springer. С. 4–7. ISBN 978-1-4020-7688-6.
- ^ а б Маттокс, Д. М. Основы технологии нанесения покрытий в вакууме В архиве 2009-10-07 на Wayback Machine, Springer, 2003 г. ISBN 978-3-540-20410-7 Книги Google
- ^ История SCS Coatings В архиве 2012-01-12 в Wayback Machine. Scscoatings.com. Проверено 4 июня 2012.
- ^ а б «Парилен: истинно конформное тонкопленочное покрытие» (PDF). Плазменные решения повышенной прочности. Сбн.
- ^ а б У. Ф. Горхэм (1966). «Новый общий синтетический метод получения линейных поли-пара-ксилиленов». Journal of Polymer Science Part A-1: Polymer Chemistry. 4 (12): 3027–3039. Bibcode:1966JPoSA ... 4,3027G. Дои:10.1002 / pol.1966.150041209.
- ^ а б Ю. Дж. Сенкевич; К. Дж. Митчелл; А. Виджаярагаван; Э. В. Барнат; Дж. Ф. Макдональд; Т.-М. Лу (2002). «Уникальная структура / свойства химического осажденного парилена E». Журнал вакуумной науки и техники A. 20 (4): 1445–9. Bibcode:2002JVSTA..20.1445S. Дои:10.1116/1.1487870.
- ^ Дж. Ф. Гейнор; Ю. Дж. Сенкевич; С. Б. Десу (1996). «Новый метод изготовления тонких полимерных пленок с высокими эксплуатационными характеристиками путем химической паровой полимеризации». J. Mater. Res. 11 (7): 1842–50. Bibcode:1996JMatR..11.1842G. Дои:10.1557 / JMR.1996.0233.
- ^ J.J. Сенкевич; С. Б. Десу (1999). «Термическое химическое осаждение из паровой фазы поли (хлор-п-ксилилен) / SiO2 Нанокомпозиты ». Химия материалов. 11 (7): 1814–21. Дои:10,1021 / см 990042q.
- ^ Ю. Дж. Сенкевич (1999). «CVD нанопористого кремнезема». Химическое осаждение из паровой фазы. 5 (6): 257–60. Дои:10.1002 / (SICI) 1521-3862 (199912) 5: 6 <257 :: AID-CVDE257> 3.0.CO; 2-J.
- ^ К. Чан, А. С. Мак, К. Пан, Ю.-Л. Линг, Д. Б. Фрейзер Мат. Res. Soc. Symp. Proc. т. 381, 123 (1995).
- ^ Ю. Дж. Сенкевич; Б. В. Вудс; Дж. Дж. МакМахон; П.-И Ван (2007). "Термомеханические свойства парилена X, химического осажденного сшиваемого полимера при комнатной температуре". Химическое осаждение из паровой фазы. 13 (1): 55–59. Дои:10.1002 / cvde.200606541.
- ^ J.B. Fortin и T.-M. Лу (2001). «Деградация тонких пленок из поли-пара-ксилилена (парилена), вызванная ультрафиолетовым излучением». Тонкие твердые пленки. 397 (1–2): 223–228. Bibcode:2001TSF ... 397..223F. Дои:10.1016 / S0040-6090 (01) 01355-4.
- ^ Сенкевич, Джей Дж. (2014). «Трет-бутилэтинилпарилен и фенилэтинилпарилен». Химическое осаждение из паровой фазы. 20 (1–2–3): 39–43. Дои:10.1002 / cvde.201307071.
- ^ Хорн, Шон "Процесс осаждения парилена: предварительное осаждение" https://www.paryleneconformalcoating.com/#TheParyleneDepositionProcess
- ^ К. М. Ваэт и К. Ф. Йенсен (1999). «Селективный рост поли (п-фениленвинилена), полученного методом химического осаждения из паровой фазы». Современные материалы. 11 (10): 814–820. Дои:10.1002 / (SICI) 1521-4095 (199907) 11:10 <814 :: AID-ADMA814> 3.0.CO; 2-Z.
- ^ J.J. Сенкевич; C.J. Wiegand; Г.-Р. Ян; Т.-М. Лу (2004). «Селективное осаждение ультратонких пленок поли (пара-ксилилен) на диэлектриках по сравнению с медными поверхностями». Химическое осаждение из паровой фазы. 10 (5): 247–9. Дои:10.1002 / cvde.200304179.
- ^ а б "GlobalTop Technology | Тайвань | Порошок нитрида алюминия".
- ^ Дж. Б. Фортин и Т.-М. Лу (2000). «Масс-спектрометрические исследования при осаждении из паровой фазы тонких пленок поли-пара-ксилилена». Журнал вакуумной науки и техники A. 18 (5): 2459. Bibcode:2000JVSTA..18.2459F. Дои:10.1116/1.1289773.
- ^ Х. Дж. Райх; Д. Дж. Крам (1969). «Макро-кольца. XXXVI. Расширение кольца, рацемизация и взаимные превращения изомеров в [2.2] парациклофановой системе через бирадикальный промежуточный продукт». Журнал Американского химического общества. 91 (13): 3517–3526. Дои:10.1021 / ja01041a016.
- ^ П. Крамер; А. К. Шарма; Э. Э. Хеннеке; Х. Ясуда (2003). «Полимеризация производных пара-ксилилена (полимеризация парилена). I. Кинетика осаждения парилена N и парилена C». Журнал науки о полимерах: издание по химии полимеров. 22 (2): 475–491. Bibcode:1984JPoSA..22..475K. Дои:10.1002 / pol.1984.170220218.
- ^ Х. Э. Винберг и Ф. С. Фосетт (1973). «Трицикло [8.2.2.24,7] гексадека-4,6,10,12,13,15-гексаен». Органический синтез.
- ^ а б J.J. Сенкевич (2011): «CVD поли (α, α'-диметил-п-ксилилен и поли (α, α, α ', α'-тетраметил-п-ксилилен) -со-поли (п-ксилилен) из предшественников алкоксидов I: оптические свойства и термическая стабильность ». Химическое осаждение из паровой фазы, том 17, страницы 235-240.
- ^ П. К. Ву; Г. -Р. Ян; L. Вы; Д. Матур; А. Кокозиелло; C. -I. Lang; Дж. А. Мур; Т. -М. Лу; Х. Бакру (1997). «Осаждение высокочистого парилена-F с использованием химического осаждения из паровой фазы при низком давлении и низкой температуре». Журнал электронных материалов. 26 (8): 949–953. Bibcode:1997JEMat..26..949W. Дои:10.1007 / s11664-997-0280-8. S2CID 94987047.
- ^ Pebalk, A. V .; Кардаш, И. Э .; Козлова, Н. В .; Зайцева, Э. Л .; Козлов, Ю. А .; Праведников, А. Н. (1980). Высокомолекулярные соединения, Серия А. 22 (5): 972–6. Отсутствует или пусто
| название =(помощь) - ^ Ли, Чанг Дж .; Ван, Хуэй; Фоджиато, Джованни Антонио, Патент США 6,140,456 , Дата выдачи: 31 октября 2000 г.
- ^ Ли, Чанг Дж., Патент США 6,703,462 , Дата выдачи: 9 марта 2004 г.
- ^ Сенкевич, Джей Дж. (2011). "Путь к получению парилена из негалогенных жидких прекурсоров". Химическое осаждение из паровой фазы. 17 (4–6): 76–79. Дои:10.1002 / cvde.201104304.
- ^ D.M. Добкин, С. Мохтари, М. Шмидт, А. Пант, Л. Робинсон, Механизмы осаждения SiO2 из ТЭОС и родственных кремнийорганических соединений и озона »J. Electrochem. Soc. 142 (7), 2332-40 (1995).
- ^ Сенкевич, Джей Дж. (2013). «Парилен AF-4 через улавливание уходящей фенокси-группы». Химическое осаждение из паровой фазы. 19 (10–11–12): 327–331. Дои:10.1002 / cvde.201304321.
- ^ Ю. Дж. Сенкевич; С. Б. Десу (1999). «Композиционные исследования термического химического осаждения из паровой фазы поли (хлор-п-ксилилен) / SiO при температуре, близкой к комнатной.2 нанокомпозиты ». Химия материалов. 11 (5): 1814. Bibcode:2000АпФА..70..541С. Дои:10.1007 / s003390051076. S2CID 96072554.
- ^ а б c J. J. Senkevich & P.-I. Ван (2009). «Химия молекулярного слоя через парилены». Химическое осаждение из паровой фазы. 15 (4–6): 91–94. Дои:10.1002 / cvde.200804266.
- ^ Джеймс А. Шварц; Кристиан И. Контеску; Кароль Путьера (2004). Энциклопедия Деккера нанонауки и нанотехнологий, Том 1. CRC Press. п. 263. ISBN 978-0-8247-5047-3.
- ^ Laibinis, Paul E .; Whitesides, Джордж М .; Аллара, Дэвид Л .; Тао, Юй Тай; Парих, Атул Н .; Нуццо, Ральф Г. (1991). «Сравнение структур и смачивающих свойств самоорганизующихся монослоев н-алкантиолов на металлических поверхностях чеканки, меди, серебра и золота». Журнал Американского химического общества. 113 (19): 7152. Дои:10.1021 / ja00019a011.
- ^ Вассерман, Стивен Р .; Тао, Юй Тай; Whitesides, Джордж М. (1989). «Структура и реакционная способность монослоев алкилсилоксанов, образованных реакцией алкилтрихлорсиланов на кремниевых подложках». Langmuir. 5 (4): 1074. Дои:10.1021 / la00088a035.
- ^ Фадеев, Александр Юрьевич .; Маккарти, Томас Дж. (2000). «Самосборка - не единственная возможная реакция между алкилтрихлорсиланами и поверхностями: мономолекулярные и олигомерные ковалентно связанные слои дихлор- и трихлоралкилсиланов на кремнии». Langmuir. 16 (18): 7268. Дои:10.1021 / la000471z.
- ^ Сенкевич, Джей Дж .; Митчелл, Кристофер Дж .; Yang, G.-R .; Лу, Т.-М. (2002). "Химия поверхности меркаптана и рост молекулярных слоев алкоксисилана пиридина с короткой цепью". Langmuir. 18 (5): 1587. Дои:10.1021 / la010970f.
- ^ З. Япу (2003). «Сдержанность и антистик в МЭМС и НЭМС». Acta Mechanica Sinica. 19 (1): 1. Bibcode:2003AcMSn..19 .... 1Z. Дои:10.1007 / BF02487448. S2CID 110540114.
- ^ Сенкевич, Джей Дж .; Wang, Pei-I .; Виганд, Крис Дж .; Лу, Т.-М. (2004). "Стабильность температуры смещения ультратонких диэлектриков PETEOS, покрытых париленом: влияние поверхностного кислорода на диффузию ионов меди". Письма по прикладной физике. 84 (14): 2617. Bibcode:2004АпФЛ..84.2617С. Дои:10.1063/1.1691488.