Осмотерапия - Osmotherapy
| Осмотерапия | |
|---|---|
 На этой диаграмме показан основной процесс осмотерапии. | |
| Специальность | сосудистая неврология |
Осмотерапия это использование осмотически активные вещества для уменьшения объема внутричерепной содержание. Осмотерапия служит основным методом лечения отек мозга. Основная цель осмотерапии - улучшить эластичность и уменьшить внутричерепной объем путем удаления свободной воды, накопленной в результате отека мозга, из внеклеточного и внутриклеточного пространства мозга в сосудистый отсек путем создания осмотический градиент между кровью и мозгом. Нормальная сыворотка осмоляльность колеблется от 280 до 290 мОсм / кг, а осмолярность сыворотки, вызывающая удаление воды из мозга без особых побочных эффектов, колеблется от 300 до 320 мОсм / кг. Обычно 90 мл пространства создается в внутричерепной свод на 1,6% снижение содержания воды в мозге.[1] Осмотерапия обладает церебральным обезвоживающим действием.[2] Основная цель осмотерапии - уменьшить внутричерепное давление (ВЧД) путем отвода лишней жидкости из мозга. Это достигается внутривенный введение осмотических агентов, которые увеличивают осмоляльность сыворотки, чтобы переместить избыток жидкости из внутриклеточного или внеклеточного пространства мозга во внутрисосудистое пространство. Возникающее в результате сокращение мозга эффективно снижает внутричерепной объем и снижает ВЧД.[3][4]
История
В 1919 году Вид и МакКиббен, биомедицинские исследователи из Медицинской школы Джонса Хопкинса, первыми задокументировали использование и влияние осмотически активных веществ на массу мозга. При изучении переноса солевых растворов из крови в Спинномозговая жидкость (CSF), они сначала отметили, что внутривенная (IV) инъекция концентрированного хлорида натрия привела к коллапсу текальный мешок что помешало им вывести CSF из поясничная цистерна. Для дальнейшего изучения эффекта они провели лабораторные эксперименты на анестезированных кошках, которые подверглись краниотомия. Они наблюдали изменения выпуклости мозга кошки при внутривенной инъекции, в частности, они отметили, что внутривенная инъекция гипертонического раствора приводила к максимальному усыханию мозга через 15-30 минут, а введение гипотонических растворов приводило к выпячиванию и разрыву ткани мозга. К 1927 году использование осмотических агентов при внутривенном введении стало официальным.[1]
Отек мозга

Повышение содержания воды в головном мозге называется отеком мозга и обычно возникает в результате: травматическое повреждение мозга (TBI), субарахноидальное кровоизлияние (SAH), внутримозговое кровоизлияние (ICH), субдуральная гематома, ишемический приступ, опухоли головного мозга, инфекционные заболевания и внутричерепная хирургия. Отек мозга может привести к нарушению регионального церебрального кровотока (CBF) и внутричерепное давление (ICP) градиенты, которые могут привести к смерти пострадавшего.[1] Повышенное ВЧД приводит к увеличению внутричерепного объема. Неконтролируемый ВЧД приводит к повреждению мозга глобальными гипоксический ишемическое повреждение из-за снижения церебральное перфузионное давление (CPP), который находится путем вычитания ICP из среднее артериальное давление (MAP), церебральный кровоток и механическое сжатие ткани мозга из-за разделенных градиентов ICP.[2]Отек головного мозга в основном подразделяется на цитотоксический отек, вазогенный отек и интерстициальный отек. Цитотоксический отек поражает как белое, так и серое вещество и возникает в результате набухания клеточных элементов, таких как нейроны, глия и эндотелиальные клетки Вазогенный отек влияет на белое вещество и результаты из гематоэнцефалический барьер Межклеточный отек возникает из-за недостаточного всасывания спинномозговой жидкости (ЦСЖ).[1]
Осмотические агенты
Осмотические агенты работают, прежде всего, воздействуя на гематоэнцефалический барьер.[1] Очень важно, чтобы осмотические агенты не могли преодолевать гематоэнцефалический барьер, потому что основная идея заключается в использовании осмотических агентов для увеличения осмолярности плазмы и создания осмотического градиента, заставляющего воду из клеток мозга течь в плазму. По достижении равновесия как ВЧД, так и внутриклеточный объем возвращаются к исходным нормальным условиям.[3] Идеальный осмотический агент будет характеризоваться своей инертностью, относительной нетоксичностью и полным исключением для проникновения в мозг. Таким образом, осмотические агенты с коэффициент отражения (σ) ближе к 1 (0 = свободно проницаемый, 1 = полностью непроницаемый) является предпочтительным, поскольку маловероятно проявление каких-либо обратных эффектов, таких как отек мозга и повышение ВЧД при отмене. Обычно используемые осмотические агенты: мочевина, глицерин, маннитол и Гипертонический раствор.[1] Дозировка введения осмотического агента выражается в граммах на массу тела человека (г / кг).[3]
Мочевина
Мочевина с σ = 0,59 была введена в 1956 г. из-за низкого молекулярного веса и медленного проникновения ГЭБ. Однако это может вызвать эффекты отскока и побочные эффекты, такие как внутрисосудистый гемолиз и флебит.[1] При введении мочевины доза составляет 1,5 г / кг или 0,5 г / кг (для пожилых людей).[3]
Глицерин

Глицерин с σ = 0,48 был введен в производство в 1964 году, но у него есть вероятность проявления эффектов отскока и побочных эффектов, таких как гемолиз, гемоглобинурия, почечная недостаточность, гиперосмолярная кома и тошнота.[1] При использовании глицерина доза составляет 1,2 г / кг, а затем 0,5-1 г / кг в течение 3-4 часов.[3]
Маннитол
Маннитол представляет собой спиртовое производное простой сахарной маннозы, и его использование исследуется с 1962 года. С σ = 0,9, молекулярной массой 182 дальтон, периодом полураспада 2–4 часа, простотой приготовления, химической стабильностью и улавливанием свободных радикалов. свойств, он считается основным осмотическим агентом для клинического использования. Однако это могло вызвать диурез, почечная недостаточность, гиперкалиемия и гемолиз.[1] При введении маннита используется 20% раствор маннита 1-1,5 г / кг с последующими дозами 0,25-1 г / кг по мере необходимости каждые 1-6 часов в зависимости от ВЧД.[2]
Гипертонический раствор
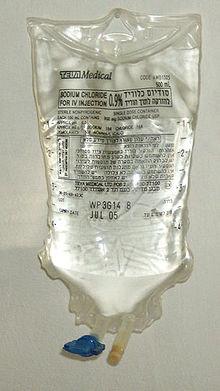
Гипертонический физиологический раствор с σ = 1 представляет интерес с начала 1980-х годов. Гипертонический раствор, содержащий хлорид натрия, регулирует ВЧД, внутрисосудистый объем и сердечный выброс без значительного диуреза, но теоретические побочные эффекты варьируются от неврологических осложнений до субдуральная гематома. Гипертонический солевой раствор в последние несколько лет является выбором для нервно-реанимации.[1] Используемый гипертонический солевой раствор может быть 3%, 7,5%, 10% или 24,3% солевым раствором.[5] При введении гипертонического раствора дозировка составляет 2 г / кг.[6]
Текущее состояние
В настоящее время осмотерапия - единственный способ уменьшить отек мозга, а гипертонический раствор лучше, чем другие осмотические агенты. По мнению некоторых исследователей, глицерин лучше всего вводить в качестве базального лечения, тогда как маннитол можно вводить для контроля внезапного повышения ВЧД.[7] По сравнению с маннитом, есть доказательства того, что улучшение ВЧД, церебрального кровотока и ЦПД из-за введения гипертонического раствора длится дольше. Кроме того, гипертонический раствор также показывает значительный эффект в улучшении реологии крови, такой как гематокрит и скорость сдвига на уровне внутренняя сонная артерия (МКА).[6]
Будущее
Исследования продолжаются, чтобы найти более эффективные механизмы лечения отека мозга. Сочетание осмотерапии с другими механизмами лечения имеет больший потенциал для более эффективного лечения отека мозга и его серьезных патологических эффектов.
RVOT
Восстановительная желудочковая омотерапия (RVOT) может быть новым методом лечения отека мозга без использования осмотических агентов. RVOT использует катетеры проницаемость для водяного пара для увеличения осмолярности спинномозговой жидкости. Ex vivo Были проведены эксперименты по проверке эффективности RVOT. RVOT проводится локально, поэтому он более эффективен в тяжелых случаях отека мозга. Продувочный газ, любой газ, используемый для протекания через полое волокно, проходит через катетер RVOT, состоящий из полого волокна с полупроницаемый стены для удаления свободной несвязанной воды из желудочки в виде водяного пара.[8]
Терапия второго уровня
Если осмотическая терапия с использованием осмотических агентов не помогает при лечении отека мозга, другие методы лечения с использованием барбитураты и кортикостероиды могут быть разработаны. пентобарбитал может действовать как поглотители свободных радикалов а также уменьшить объем внутричерепной крови за счет снижения метаболических потребностей головного мозга. Однако введение барбитуратов сопряжено с такими рисками, как: гипотония, вызывали кому и инфекцию, что ограничивало их возможное клиническое применение. Хотя кортикостероиды не очень эффективны при лечении отека головного мозга в результате ишемического инсульта и внутримозгового кровоизлияния, они очень эффективны при лечении вазогенного отека, вызванного опухолями головного мозга. Идея применения как барбитуратов, так и кортикостероидов состоит в том, чтобы обеспечить пространство для отека мозга, возникающего в результате отека, поэтому это очень неспецифические методы лечения.[9]
Новые цели
Некоторые исследования направлены на выявление новых мишеней, предотвращающих образование отека головного мозга. Чтобы разработать стратегии предотвращения отека мозга, важно понимать отек мозга на молекулярном уровне. Выявленные цели включают: NKCC1, SUR1 / TRPM4 канал, Антагонист рецепторов вазопрессина.[9]
NKCCl
Во время раннего и реперфузия этап ишемия, существует усиление регулирования вторично активных котранспортер NKCCl. NKCCl играют важную роль в модулировании нагрузки натрия и хлорида в нейронах, глии, эндотелиальных клетках и сосудистое сплетение. Повышающая регуляция NKCCl сопровождается повышенным отложением натрия (Na) и хлорида в эндотелиальных клетках и Na + K + АТФаза активность играет роль в вытеснении Na, а затем хлорида и воды из эндотелиальных клеток во внеклеточное пространство, что приводит к вазогенному отеку. Таким образом, предотвращение активации NKCCl может предотвратить формирование отека мозга. Буметанид, который может доставляться через гематоэнцефалический барьер, является ингибитором NKCCl.[9] Буметанид значительно снижает воспаление, вызванное ЧМТ.[10] Определение правильной дозы буметанида, который действует как ингибитор NKCC1, может в некоторой степени предотвратить отек мозга. Это представляет собой АТФ-зависимую стадию формирования отека церебральной области.[9]
SUR1 / TRPM4
Существует повышенная регуляция этого неселективного катионного канала SUR1 / TRPM4, за которой следует опухоль головного мозга, ишемическое повреждение и черепно-мозговое повреждение. Этот канал, который активируется истощением АТФ, находится на нейронах, нейроглии и эндотелий. Этот канал обеспечивает пассивный транспорт воды и растворенных веществ и представляет собой АТФ-независимую стадию церебрального образования. Открытие этих каналов приводит к сотовому деполяризация и пузыри, вызывающие цитотоксический отек. Этого можно избежать, используя глибурид (глибенкламид ), который блокирует эти каналы.[9]
Антагонист рецепторов вазопрессина
Рецепторы вазопрессина активируются вазопрессин находятся на базолатеральная мембрана клеток, выстилающих собирательные протоки почек. Аневризматическое субарахноидальное кровоизлияние (aSAH) приводит к гипонатриемии, которая приводит к задержке воды и высвобождению антидиуретического гормона, вызывая повышение внутричерепного давления и образование отека мозга. Этого можно избежать, введя Conivaptan, безопасный одобренный FDA препарат, который лечит эуволемическая гипонатриемия. В процессе акварель, кониваптен, который является антагонистом рецепторов вазопрессина, улучшает концентрацию натрия в сыворотке, устраняя при этом свободную воду без какого-либо отрицательного воздействия на систолическое артериальное давление и частота пульса. Поскольку он может уменьшить объем головного мозга и ВЧД, он может лечить многие формы отека мозга.[9][11]
Рекомендации
- ^ а б c d е ж грамм час я j Бхардвадж, А (2007). «Осмотерапия в нейрокритической помощи». Текущие отчеты по неврологии и неврологии. 7 (6): 513–521. Дои:10.1007 / s11910-007-0079-2. PMID 17999898.
- ^ а б c Майер, Стефан; Чонг Дж (2002). «Управление интенсивной терапии повышенного внутричерепного давления». J Intensive Care Med. 17 (2): 55–67. Дои:10.1046 / j.1525-1489.2002.17201.x.
- ^ а б c d е Калита, Дж; Ranjan P; Мисра У (март 2003 г.). «Текущее состояние осмотерапии при внутримозговом кровоизлиянии». Неврология Индия. 51 (1): 104–109. PMID 12865537.
- ^ Хейс, Анджела; Lazaridis C; Neyens R; Николас Дж; Гей S; Чалела Дж (2011). «Осмотерапия: использование среди нейроинтенсивистов». Neuro Critical Care. 14 (2): 222–228. Дои:10.1007 / s12028-010-9477-4. PMID 21153930.
- ^ Куреши, Ал; Суарес Джи (2012). «Использование гипертонических солевых растворов при лечении отека мозга и внутричерепной гипертензии». Реанимационная медицина. 28 (9): 3303–3313. Дои:10.1097/00003246-200009000-00032. PMID 11008996.
- ^ а б Котансо, Винсент; Masson F; Махамид Э; Petit L; Шик В; Sztark F; Zaaroor M; Soustiel J (октябрь 2011 г.). «Сравнение эффектов эквиосмолярных доз маннита и гипертонического солевого раствора на церебральный кровоток и метаболизм при травматическом повреждении головного мозга». Журнал нейротравмы. 28 (10): 2003–2012. Дои:10.1089 / neu.2011.1929. PMID 21787184.
- ^ Биестро, А; Р. Альберти; Р. Галли; М. Канчела; А. Сока; Х. Панзардо; Б. Борович (1997). «Осмотерапия повышенного внутричерепного давления: сравнение маннита и глицерина». Acta Neurochir. 139 (8): 725–733. Дои:10.1007 / bf01420045. PMID 9309287.
- ^ Odland, R.M .; Panter, S. S .; Роксволд, Г. Л. (2011). «Влияние восстановительной желудочковой осмотерапии на осмолярность искусственной цереброспинальной жидкости и содержание воды в тканях мозга Ex vivo». Журнал нейротравмы. 28 (1): 135–42. Дои:10.1089 / neu.2010.1282. ЧВК 3019589. PMID 21121814.
- ^ а б c d е ж Уолкотт, Брайан; К. Кале; Дж. Симард (январь 2012 г.). «Новые цели лечения отека мозга». Нейротерапия. 9 (1): 65–72. Дои:10.1007 / s13311-011-0087-4. ЧВК 3271162. PMID 22125096.
- ^ Лу, К; Wu C; Yen H; Peng JF; Ван С; Ян И (июнь 2007 г.). «Введение буметанида ослабило черепно-мозговые травмы за счет сверхэкспрессии IL-1». Neurol Res. 29 (4): 404–409. Дои:10.1179 / 016164107X204738. PMID 17626737.
- ^ Райт, Венди; Asbury WH; Гилмор JL; Сэмюэлс О.Б. (август 2009 г.). «Кониваптан при гипонатриемии в отделении нейрокритической помощи». Нейрокритическая помощь. 11 (1): 6–13. Дои:10.1007 / s12028-008-9152-1. PMID 19003543.
