Уравнение Гаммета - Hammett equation
| Заместитель | пара- эффект | мета- эффект |
|---|---|---|
| Диметиламино | -0.83 | -0.211 |
| Амино | -0.66 | -0.161 |
| Бутиламино | -0.51 | -0.34 |
| Гидрокси | -0.37 | +0.12 |
| Метокси | -0.268 | +0.115 |
| Этокси | -0.25 | +0.015 |
| Метил | -0.170 | -0.069 |
| Триметилсилил | -0.07 | -0.04 |
| Никто | 0.000 | 0.000 |
| Фторо | +0.062 | +0.337 |
| Хлор | +0.227 | +0.373 |
| Бромо | +0.232 | +0.393 |
| Йодо | +0.276 | +0.353 |
| Этоксикарбонил | +0.45 | +0.37 |
| Трифторметил | +0.54 | +0.43 |
| Циано | +0.66 | +0.56 |
| Нитро | +0.778 | +0.710 |
В Уравнение Гаммета в органическая химия описывает линейный отношения свободной энергии относящийся скорость реакции и константы равновесия для многих реакций с участием бензойная кислота производные с мета- и пара-заместители друг к другу с помощью всего двух параметров: константы заместителя и константы реакции.[3][4] Этот уравнение был разработан и опубликован Луи Плак Хэммет в 1937 г.[1] как продолжение качественных наблюдений в публикации 1935 г.[5]
Основная идея состоит в том, что для любых двух реакций с двумя ароматическими реагентами, различающимися только типом заместителя, изменение свободная энергия активации пропорционально изменению Свободная энергия Гиббса.[6] Это понятие не следует из стихийного термохимия или же химическая кинетика и был введен Хамметом интуитивно.[7]
Основное уравнение:
относящийся к константа равновесия, K, для данной равновесной реакции с заместителем R и эталоном K0 константа, когда R - атом водорода константа заместителя σ который зависит только от конкретного заместителя R и константа реакции ρ который зависит только от типа реакции, но не от используемого заместителя.
Уравнение справедливо и для скорость реакции k серии реакций с замещенными производными бензола:
В этом уравнении k0 - эталонная скорость реакции незамещенного реагента, а k - скорость реакции замещенного реагента.
Участок журнала (К / К0) для данного равновесия по сравнению с log (k / k0) для данной скорости реакции со многими по-разному замещенными реагентами будет давать прямую линию.
Константы заместителей
Отправной точкой для сбора констант заместителей является химическое равновесие для которого и константа заместителя, и константа реакции произвольно установлены равными 1: ионизация из бензойная кислота или же бензолкарбоновая кислота (R и R 'оба H) в воде при 25 ° C.

Получив значение K0, ряд констант равновесия (K) теперь определяется на основе того же процесса, но теперь с изменением пара-заместителя - например, п-гидроксибензойная кислота (R = OH, R '= H) или p-аминобензойная кислота (R = NH2, R '= H). Эти значения в сочетании в уравнении Гаммета с K0 и помня, что ρ = 1, зададим константы пара-заместителей составлено в таблице 1 для амин, метокси, этокси, диметиламино, метил, фтор, бром, хлор, йод, нитро и циано заместители. Повторение процесса с мета-заместителями дает константы мета-заместителей. Это лечение не включает орто-заместители, который представит стерические эффекты.
Значения σ, представленные в таблице выше, показывают определенные эффекты заместителей. При ρ = 1 группа заместителей с возрастающими положительными значениями, особенно циано и нитро - вызвать увеличение константы равновесия по сравнению с водород ссылка, что означает, что кислотность карбоновой кислоты (изображенной слева от уравнения) увеличилось. Эти заместители стабилизируют отрицательный заряд карбоксилатного атома кислорода за счет электроноакцепторного индуктивный эффект (-I) а также отрицательным мезомерный эффект (-М).
Следующий набор заместителей - это галогены, для которого эффект заместителя остается положительным, но гораздо более скромным. Причина в том, что пока индуктивный эффект все еще отрицательный, мезомерный эффект положительный, вызывая частичную отмену. Данные также показывают, что для этих заместителей мета-эффект намного больше, чем пара-эффект из-за того, что мезомерный эффект значительно снижается в мета-заместителе. С мета-заместителями атом углерода, несущий отрицательный заряд, находится дальше от группы карбоновой кислоты (структура 2b).
Этот эффект изображен на схема 3, где в пара-замещенном арене 1а, один резонансная структура 1b это хиноид с положительным зарядом на заместителе X, высвобождая электроны и таким образом дестабилизируя заместитель Y. Этот дестабилизирующий эффект невозможен, когда X имеет мета-ориентацию.

Другие заместители, такие как метокси и этокси, может даже иметь противоположные знаки для константы заместителя в результате противоположного индуктивного и мезомерного эффекта. Только алкильные и арильные заместители, такие как метил высвобождают электроны в обоих отношениях.
Конечно, когда знак константы реакции отрицательный (следующий раздел), только заместители с такой же отрицательной константой заместителя будут увеличивать константы равновесия.
Σп– и σп+ константы
Поскольку карбонильная группа не может служить источником электронов для групп -M (в отличие от доноров неподеленной пары, таких как OH), для реакций с участием исходных материалов фенола и анилина величина σп значения для электроноакцепторных групп окажутся слишком маленькими. Для реакций, где ожидается, что резонансные эффекты будут иметь большое влияние, модифицированный параметр и модифицированный набор σп– константы могут подойти лучше. Этот параметр определяется с помощью констант ионизации параграф замещенные фенолы, используя коэффициент масштабирования, чтобы согласовать значения σп– с таковыми из σп для «неаномальных» заместителей, чтобы поддерживать сопоставимые значения ρ: для ArOH ⇄ ArO– + H+, мы определяем .
Точно так же карбонильный углерод бензойной кислоты находится в узловом положении и не может служить стоком для + M групп (в отличие от карбокатиона в бензильном положении). Таким образом, для реакций с участием карбокатионов в α-положении величина σп значения для электронодонорных групп окажутся недостаточно отрицательными. Исходя из аналогичных соображений, набор σп+ константы лучше подходят для реакций с участием электронодонорных групп на параграф положение и образование карбокатиона в бензильном сайте. Σп+ основаны на ставка константы SN1 реакция кумилхлоридов в 90% ацетоне / воде: для ArCMe2Cl + H2O → ArCMe2OH + HCl, определим . Обратите внимание, что коэффициент масштабирования отрицательный, поскольку электронодонорная группа ускоряет реакцию. Для реакции, график Хаммета которой строится, эти альтернативные константы Гаммета, возможно, потребуется протестировать, чтобы увидеть, можно ли получить лучшую линейность.
Значение Rho
Зная константы заместителей, теперь можно получить константы реакции для широкого диапазона органические реакции. Архетипическая реакция - это щелочной гидролиз из этилбензоат (R = R '= H) в смеси вода / этанол при 30 ° C. Измерение скорость реакции k0 в сочетании со многими замещенными этилбензоатами в конечном итоге дает константу реакции +2,498.[1][нуждается в обновлении ][неосновной источник необходим ]

Константы реакций известны для многих других реакций и равновесий. Вот некоторые из них, предоставленные самим Хэмметом (их значения указаны в скобках):
- гидролиз замещенного коричная кислота сложный эфир в этаноле / воде (+1,267)
- ионизация замещенных фенолы в воде (+2.008)
- кислотный катализатор этерификация замещенных эфиров бензойной кислоты в этиловый спирт (-0.085)
- катализируемое кислотой бромирование замещенных ацетофеноны (Галогенирование кетонов ) в уксусная кислота / вода / соляная кислота (+0,417)
- гидролиз замещенного бензилхлориды в ацетон -воды при 69,8 ° C (-1,875).
Константа реакции или константа чувствительности, ρ, описывает восприимчивость реакции к заместителям по сравнению с ионизацией бензойной кислоты. Это эквивалентно наклону графика Хэммета. Информацию о реакции и связанном с ней механизме можно получить на основании значения, полученного для ρ. Если значение:
- р> 1, реакция более чувствительна к заместителям, чем бензойная кислота, и во время реакции создается отрицательный заряд (или теряется положительный заряд).
- 0 <р <1, реакция менее чувствительна к заместителям, чем бензойная кислота, и возникает отрицательный заряд (или теряется положительный заряд).
- ρ = 0, нет чувствительности к заместителям, и нет накопления или потери заряда.
- р <0, реакция создает положительный заряд (или теряет отрицательный заряд).
Эти отношения могут быть использованы для выяснения механизма реакции. В качестве значения ρ связана с зарядом на этапе определения тарифа, на основе этой информации можно разработать механизмы. Если предполагается, что механизм реакции ароматического соединения происходит через один из двух механизмов, соединение может быть модифицировано заместителями с разными σ значения и кинетические измерения. После того, как эти измерения будут сделаны, можно построить график Хаммета для определения значения ρ. Если один из этих механизмов связан с образованием заряда, это можно проверить на основании значения ρ. И наоборот, если график Хэммета показывает, что заряд не образуется, то есть с нулевым наклоном, механизм, связанный с накоплением заряда, можно отбросить.
Сюжеты Хаммета не всегда могут быть идеально линейными. Например, кривая может показывать внезапное изменение наклона или ρ ценить. В таком случае вполне вероятно, что механизм реакции изменяется при добавлении другого заместителя. Другие отклонения от линейности могут быть связаны с изменением положения переходного состояния. В такой ситуации определенные заместители могут вызвать переходное состояние раньше (или позже) в механизме реакции.[8][страница нужна ]
Доминирующие электронные эффекты
3 вида основного состояния или статический Преобладают электрические воздействия:
- Резонанс (мезомерный) эффект
- Индуктивный эффект: электрическое влияние группы, которое передается в основном за счет поляризации связывающих электронов от одного атома к другому.
- Прямой электростатический (полевой) эффект: электрическое воздействие полярный или диполярный заместитель который передается в первую очередь реактивной группе через пространство (включая растворитель, если есть) по законам классической электростатика
Последние два влияния часто рассматриваются вместе как составной эффект, но здесь рассматриваются отдельно. Вестхаймер продемонстрировал, что электрические эффекты π-замещенных диполярных групп на кислотность бензойный и фенилуксусные кислоты может быть количественно коррелирован, если предположить только прямое электростатическое действие заместителя на ионизируемый протон карбоксильная группа. Обработка Вестхаймера сработала хорошо, за исключением тех кислот с заместителями, у которых есть неподеленные электронные пары, такие как –OH и –OCH3, поскольку эти заместители сильно взаимодействуют с бензольным кольцом.[9][неосновной источник необходим ][10][нуждается в обновлении ][неосновной источник необходим ]
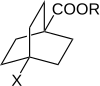
Робертс и Морленд изучили реакционную способность 4-замещенных бицикло [2.2.2] октан-1-карбоновых кислот и сложных эфиров. В такой молекуле передача электрических эффектов заместителей через кольцо за счет резонанса невозможна. Следовательно, это намекает на роль π-электронов в передаче эффектов заместителя через ароматические системы.[11][неосновной источник необходим ]
Реакционную способность 4-замещенных бицикло [2.2.2] октан-1-карбоновых кислот и сложных эфиров измеряли в 3 различных процессах, каждый из которых ранее использовался с производными бензойной кислоты. График зависимости log (k) от log (KА) показала линейную зависимость. Такие линейные зависимости соответствуют линейным зависимостям свободной энергии, которые строго подразумевают, что влияние заместителей проявляется через изменения потенциальная энергия и что стерический и энтропийные термины остаются почти постоянными на протяжении всей серии. Линейная зависимость хорошо вписывается в уравнение Хэммета. Для производных 4-замещенной бицикло [2.2.2.] Октан-1-карбоновой кислоты заместитель и константы реакции обозначены как σ ’и ρ’.
Сравнение ρ и ρ ’
| Реакция[нужна цитата ] | ρ ' | ρ | Dе |
|---|---|---|---|
| Ионизация кислот | 1.464 | 1.464 | 54 |
| Щелочной гидролиз этиловых эфиров | 2.24 | 2.494 | 28 |
| Кислоты с дифенилдиазометаном | 0.698 | 0.937 | 24 |
Данные о реакционной способности показывают, что влияние групп заместителей на определение реакционной способности замещенных бензойных и бицикло [2.2.2.] Октан-1-карбоновых кислот сопоставимо. Это означает, что ароматические π-электроны не играют доминирующей роли в передаче электрических эффектов диполярных групп ионизируемой карбоксильной группе. Разница между ρ и ρ 'для реакций кислот с дифенилазометаном, вероятно, связана с обратной зависимостью растворитель диэлектрическая постоянная Dе
Сравнение σ и σ ’
В этом разделе цитируется источники но это ссылки на страницы диапазоны слишком широки. (Июнь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Заместитель | σ ’[нужна цитата ] | σпараграфc | σметаc | σпараграф - σ ’[нужна цитата ] | σмета - σ ’[нужна цитата ] |
|---|---|---|---|---|---|
| ЧАС | 0 | 0 | 0 | 0 | 0 |
| ОЙ | 0.283 | −0.341 | 0.014 | −0.624 | −0.269 |
| CO2C2ЧАС5 | 0.297 | 0.402 | 0.334 | 0.105 | 0.037 |
| Br | 0.454 | 0.232 | 0.391 | −0.222 | −0.063 |
| CN | 0.579 | 0.656 | 0.608 | 0.077 | 0.029 |
Для мета-направляющих групп (электроноакцепторная группа или EWG ), σмета и σпараграф более положительны, чем σ ’. (Верхний индекс c в таблице обозначает данные из Hammett, 1940.[12][страница нужна ]) Для орто-пара направляющих групп (электронодонорная группа или EDG ), σ ’более положительно, чем σмета и σпараграф. Разница между σпараграф и σ ’(σпараграф - σ ’) больше, чем между σмета и σ ’(σмета - σ ’). Это ожидается, поскольку эффекты электронного резонанса сильнее ощущаются в p-положениях. Значения (σ - σ ’) можно принять как разумное измерение резонансных эффектов.
Нелинейность
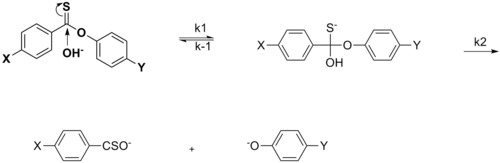
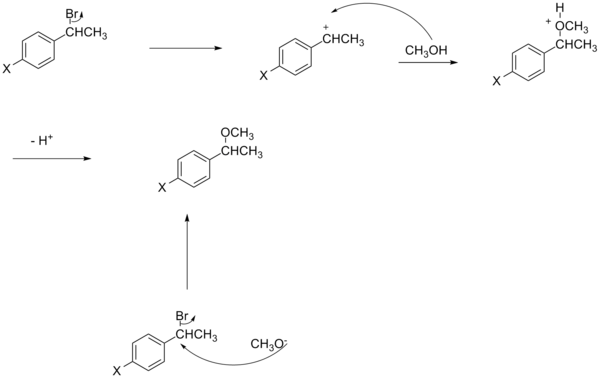
Этот раздел может требовать уборка встретиться с Википедией стандарты качества. Конкретная проблема: изображения в разделе слишком слабо привязаны к тексту, например, нет упоминания о сульфинатном эфире или гидролизе имина, хотя это и присутствует в схемах, и нет источников, указанных для схем, нарушающих либо РГ: ИЛИ или же WP: ПРОВЕРИТЬ (Июнь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
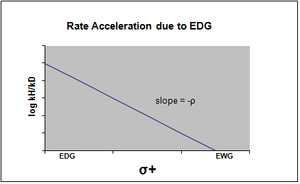
График уравнения Хаммета обычно рассматривается как линейный, с положительным или отрицательным наклоном, коррелирующим со значением rho. Однако нелинейность на графике Хаммета проявляется, когда заместитель влияет на скорость реакции или изменяет этап определения ставки или же механизм реакции реакции. По причине первого случая были введены новые сигма-константы, чтобы компенсировать отклонение от линейности, которое иначе наблюдается в результате воздействия заместителя. σ + учитывает накопление положительного заряда, происходящее в переходном состоянии реакции. Следовательно, электронодонорная группа (EDG) ускорит скорость реакции за счет стабилизации резонанса и даст следующий сигма-график с отрицательным значением rho.[13][неосновной источник необходим ]
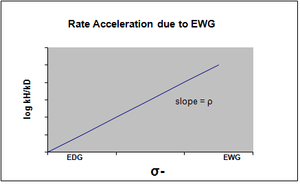
σ- обозначают в том случае, когда происходит накопление отрицательного заряда в переходном состоянии, и, следовательно, скорость реакции увеличивается за счет электроноакцепторных групп (EWG). EWG снимает электронную плотность за счет резонанса и эффективно стабилизирует генерируемый отрицательный заряд. Соответствующий график покажет положительное значение rho.
В случае нуклеофильное ацильное замещение эффект заместителя X не уходящей группы может фактически ускорить скорость реакции нуклеофильного присоединения, когда X представляет собой EWG. Это объясняется резонансным вкладом EWG в отвод электронной плотности, тем самым увеличивая восприимчивость к нуклеофильной атаке на карбонильный углерод. Изменение скорости происходит, когда X является EDG, что подтверждается при сравнении скоростей между X = Me и X = OMe, а на графике Хаммета наблюдается нелинейность.[14][неосновной источник необходим ]
Влияние заместителя может изменить стадию, определяющую скорость (rds) в механизме реакции. Определенный электронный эффект может ускорить определенный шаг так, что он больше не будет стрельбой.[15][неосновной источник необходим ]

Изменение механизма реакции также приводит к нелинейности графика Хаммета. Как правило, в этом случае для измерения изменений скорости используется модель реакции SN2.[16][неосновной источник необходим ] Однако было замечено, что в некоторых случаях SN2 реакция что EWG не ускоряет реакцию, как можно было бы ожидать[17][неосновной источник необходим ] и что скорость зависит от заместителя. Фактически, в случае бензильной системы на знак заряда и степень его развития будет влиять заместитель.[16][неосновной источник необходим ]

Например, заместитель может определять механизм как SN1 типа реакция на SN2 Тип реакции, и в этом случае полученный график Хаммета будет указывать на ускорение скорости из-за EDG, таким образом выясняя механизм реакции.
Другое отклонение от обычного уравнения Гаммета объясняется зарядом нуклеофила.[16][неосновной источник необходим ] Несмотря на нелинейность реакций бензильного SN2, электроноакцепторные группы могут либо ускорять, либо замедлять реакцию. Если нуклеофил заряжен отрицательно (например, цианид), электроноакцепторная группа увеличит скорость из-за стабилизации дополнительного заряда, который наносится на углерод в переходном состоянии. С другой стороны, если нуклеофил не заряжен (например, трифенилфосфин), электроноакцепторная группа замедлит реакцию за счет уменьшения электронной плотности на антисвязывающей орбитали уходящей группы в переходном состоянии.
Модификации Hammett
Теперь существуют другие уравнения, уточняющие исходное уравнение Гаммета: Уравнение Суэйна – Луптона,[нужна цитата ] то Уравнение Тафта,[нужна цитата ] то Уравнение Грюнвальда – Винштейна.,[нужна цитата ] и Уравнение Юкавы – Цуно.[нужна цитата ] Также было разработано уравнение, которое касается стереохимии в алифатических системах.[нечеткий ][18][неосновной источник необходим ]
Оценка констант сигмы Хаммета
Эта статья может содержать чрезмерное количество сложных деталей, которые могут заинтересовать только определенную аудиторию. (Июнь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

Сдвиги энергии связи остовных электронов (CEBE) линейно коррелируют с константами заместителей Гаммета (σ) в замененном бензол производные.[19][неосновной источник необходим ]
- ΔCEBE ≈ κσп
(1)
Рассмотрим пара-дизамещенный бензол p-F-C6ЧАС4-Z, где Z - заместитель такие как NH2, НЕТ2и т. д. Атом фтора является пара-пара по отношению к заместителю Z в бензольном кольце. На изображении справа показаны четыре выделенных кольцевых атома углерода C1 (ipso ), C2 (орто ), C3 (мета ), C4 (параграф ) в п-F-C6ЧАС4-Z молекула. Углерод с Z определяется как C1 (ipso), а фторированный углерод как C4 (пара). Этому определению следуют даже при Z = H. Левая часть (1) называется сдвигом CEBE или ΔCEBE и определяется как разница между CEBE атома фторированного углерода в p-F-C6ЧАС4-Z и фторированного углерода в эталонной молекуле FC6ЧАС5.
- ΔCEBE ≡ CEBE (C4 в p-F-C6ЧАС4-Z) - CEBE (C4 в p-F-C6ЧАС5)
(2)
Правая часть уравнения. 1 является продуктом параметра κ и константа заместителя Гаммета в пара-положении, σp. Параметр κ определяется уравнением. 3:
- κ = 2.3kT(ρ - ρ*)
(3)
куда ρ и ρ* - константы реакции Гаммета для реакции нейтральной молекулы и остовной ионизированной молекулы соответственно. ΔCEBE кольцевых атомов углерода в p-F-C6H4-Z рассчитывали с помощью теория функционала плотности чтобы увидеть, как они соотносятся с σ-константами Хаммета. Линейные графики были получены, когда рассчитанные сдвиги CEBE для орто-, мета- и пара-углерода были построены против Хаммета σо, σм и σп константы соответственно.
- κ расчетное значение ≈ 1.
Отсюда и приблизительное согласие по числовому значению и знаку между сдвигами CEBE и их соответствующей константой Хаммета σ.[20][неосновной источник необходим ]

График рассчитанного сдвига CEBE (эВ) от сигма-пара

Таблица сдвигов CEBE (эВ) и сигма-пара

График рассчитанного сдвига CEBE (эВ) от сигма-мета
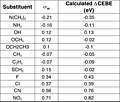
Таблица сдвигов CEBE (эВ) и сигма-мета

График рассчитанного сдвига CEBE (эВ) от сигма-о

Таблица сдвигов CEBE (эВ) и сигма-орто
Смотрите также
- Принцип Белла – Эванса – Поланьи.
- Крейг сюжет
- Отношения свободной энергии
- пKа
- Количественная структура - взаимосвязь деятельности
Рекомендации
- ^ а б c Хэммет, Луи П. (1937). «Влияние структуры на реакции органических соединений. Производные бензола». Варенье. Chem. Soc. 59 (1): 96–103. Дои:10.1021 / ja01280a022.
- ^ Табличные значения являются оригинальной публикацией 1937 года и отличаются от значений, приведенных в последующих публикациях. Дополнительные стандартные значения см .: C. Hansch; А. Лео; Р. В. Тафт (1991). «Обзор констант заместителей Гаммета, резонансных и полевых параметров». Chem. Ред. 91 (2): 165–195. Дои:10.1021 / cr00002a004.
- ^ ИЮПАК, Сборник химической терминологии 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "Уравнение Гаммета (соотношение Гаммета) ". Дои:10.1351 / goldbook.H02732
- ^ Keenan, Sheue L .; Петерсон, Карл П .; Петерсон, Келли; Джейкобсон, Кайл (2008). "Определение константы Ро уравнения Хаммета для гидролиза п-нитрофенилбензоатных эфиров". J. Chem. Educ. 85 (4): 558. Bibcode:2008JChEd..85..558K. Дои:10.1021 / ed085p558.
- ^ Луи П. Хэмметт (1935). «Некоторые соотношения между скоростями реакций и константами равновесия». Chem. Ред. 17 (1): 125–136. Дои:10.1021 / cr60056a010.
- ^ Расширенная органическая химия, часть A Второе издание F.A. Carey, R.J. Сундберг Пленум Пресс ISBN 0-306-41198-9
- ^ Первая строка его публикации 1935 года гласит: Идея о том, что существует какая-то связь между скоростью реакции и константой равновесия, является одной из наиболее стойких и в то же время наиболее решительно отрицаемых концепций химической теории.
- ^ Е.В. Анслин и Д.А. Догерти, Современная физико-органическая химия, стр. TBD, Саусалито, Калифорния, США: University Science Books, ISBN 1891389319.[страница нужна ]
- ^ Вестхаймер Ф.Х. (1939). «Электростатическое действие заместителей на константы диссоциации органических кислот. IV. Ароматические кислоты». Варенье. Chem. Soc. 61 (8): 1977–1980. Дои:10.1021 / ja01877a012.[неосновной источник необходим ]
- ^ Kirkwood J.G .; Вестхаймер Ф. Х. (1938). «Электростатическое влияние заместителей на константы диссоциации органических кислот. I [Missing Subtitle]». J. Chem. Phys. 6 (9): 506. Bibcode:1938ЖЧФ ... 6..506К. Дои:10.1063/1.1750302.[нуждается в обновлении ][неосновной источник необходим ]
- ^ Робертс Дж.Д .; Морленд младший W.T. (1953). «Электрические эффекты групп заместителей в насыщенных системах. Реакционная способность 4-замещенных бицикло [2.2.2] октан-1-карбоновых кислот». Варенье. Chem. Soc. 75 (9): 2167–2173. Дои:10.1021 / ja01105a045.[неосновной источник необходим ]
- ^ L.P.Hammett, 1940, «Глава III», «Глава IV» и «Глава VII» в Физико-органическая химия, Нью-Йорк, Нью-Йорк, США: McGraw-Hill.[страница нужна ]
- ^ Ю. Юкава и Ю. Цуно, 1959, "Резонансный эффект в отношениях Хаммета. II. Сигма-константы в электрофильных реакциях и их взаимосвязь", Бык. Chem. Soc. Jpn. 32: 965-971, см. [1], по состоянию на 22 июня 2015 г.[неосновной источник необходим ]
- ^ Гм, Ик-Хван; Ли, Джи-Юн; Ким, Хан-Тэ; Бэ, Сун-Кун (2004). "Изогнутый график Хаммета при щелочном гидролизе О-арилтионобензоаты: изменение стадии, определяющей скорость, по сравнению со стабилизацией в основном состоянии ». J. Org. Chem. 69 (7): 2436–2441. Дои:10.1021 / jo035854r. PMID 15049643.[неосновной источник необходим ]
- ^ Hart, H .; Седор, Эдвард А. (1967). «Механизм циклодегидратации 2-фенилтриарилкарбинолов». Варенье. Chem. Soc. 89 (10): 2342. Дои:10.1021 / ja00986a018.[неосновной источник необходим ]
- ^ а б c Stein, Allan R .; Тенсер, Михал; Moffatt, Elizabeth A .; Доу, Роберт; Милый, Джеймс (1980). "Нелинейность корреляций Hammett .sigma..rho. Для бензильных систем: параметры активации и их механистические последствия". J. Org. Chem. 45 (17): 3539–3540. Дои:10.1021 / jo01305a045.[неосновной источник необходим ]
- ^ Янг, П. Р .; Дженкс, У. П. (1979). «Разделение полярных и резонансных эффектов заместителей в реакциях ацетофенонов с бисульфитом и бензилгалогенидов с нуклеофилами». Варенье. Chem. Soc. 101 (12): 3288. Дои:10.1021 / ja00506a025.[неосновной источник необходим ]
- ^ Болс, Микаэль; Лян, Сифу; Дженсен, Хенрик Х. (2002). «Экваториальные противоаксиальные полярные заместители. Связь химической реакции со стереохимическими константами заместителей». J. Org. Chem. 67 (25): 8970. Дои:10.1021 / jo0205356.[неосновной источник необходим ]
- ^ Linderberg, B .; Svensson, S .; Malmquist, P.A .; Basilier, E .; Гелиус, У .; Зигбан, К. (1976). «Корреляция сдвигов ESCA и констант заместителя Гаммета в замещенных производных бензола». Chem. Phys. Lett. 40 (2): 175. Bibcode:1976CPL .... 40..175L. Дои:10.1016/0009-2614(76)85053-1.[неосновной источник необходим ]
- ^ Takahata Y .; Чонг Д.П. (2005). «Оценка сигма-констант Гаммета замещенных бензолов посредством точного функционального расчета плотности сдвигов энергии связи остовных электронов». Международный журнал квантовой химии. 103 (5): 509–515. Bibcode:2005IJQC..103..509T. Дои:10.1002 / qua.20533.[неосновной источник необходим ]
дальнейшее чтение
Общий
- Томас Х. Лоури и Кэтлин Шуэллер Ричардсон, 1987 г., Механизм и теория в органической химии, 3-е изд., Нью-Йорк, Нью-Йорк, США: Harper & Row, ISBN 0060440848, видеть [2], по состоянию на 20 июня 2015 г.
- Фрэнсис А. Кэри и Ричард Дж. Сандберг, 2006, "Заголовок" Продвинутая органическая химия: Часть A: Структура и механизмы ", 4-е изд., Нью-Йорк, Нью-Йорк, США: Springer Science & Business Media, ISBN 0306468565, видеть [3], по состоянию на 19 июня 2015 г.
- Майкл Б. Смит и Джерри, март, 2007 г., «Марш продвинутая органическая химия: реакции, механизмы и структура», 6-е изд., Нью-Йорк, Нью-Йорк, США: Wiley & Sons, ISBN 0470084944, видеть [4], по состоянию на 19 июня 2015 г.
Теория
- Л.П. Хэммет, 1970 г., Физико-органическая химия, 2-е изд., Нью-Йорк, Нью-Йорк, США: McGraw-Hill.
- Джон Шортер, 1982, Корреляционный анализ органической реакционной способности, Чичестер 1982.
- Отто Экснер, 1988 год, Корреляционный анализ химических данных, Нью-Йорк, Нью-Йорк, США: Пленум.
Обзоры дескрипторов
- Роберто Тодескини, Вивиана Консонни, Раймунд Маннхолд, Хьюго Кубиньи и Хендрик Тиммерман, 2008, «Запись: электронные константы заместителя (константы заместителя Хаммета, электронные константы σ)», в Справочник молекулярных дескрипторов, Vol. 11 из Методы и принципы медицинской химии (серия книг), стр. 144–157, Нью-Йорк, Нью-Йорк, США: John Wiley & Sons, ISBN 3527613110, видеть [5], по состоянию на 22 июня 2015 г.
- Н. Чепмен, 2012 г., Корреляционный анализ в химии: последние достижения, Нью-Йорк, Нью-Йорк, США: Springer Science & Business, ISBN 1461588316, видеть [6], по состоянию на 22 июня 2015 г.
История
- Робертс, Джон Д. (1996). «Истоки физической органической химии в США» (PDF). Бык. Hist. Chem. 19: 48–56.
- Джон Шортер, 2000, «Предыстория уравнения Хаммета», Chem. Листи, 94:210-214.
- Фрэнк Вестхаймер, 1997, «Луи Плак Хэммет, 1894–1987: биографические воспоминания», стр. 136–149, в Биографические воспоминания, Вашингтон, округ Колумбия, США: National Academies Press, см. [7], по состоянию на 22 июня 2015 г.