Фенилаланин — тРНК лигаза - Phenylalanine—tRNA ligase
| фенилаланин-тРНК лигаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 6.1.1.20 | ||||||||
| Количество CAS | 9055-66-7 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
| Ферредоксиновый антикодон-связывающий домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
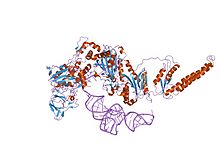 кристаллическая структура фенилаланил-тРНК синтетазы из Термус термофильный в комплексе с родственной тРНКPhe | |||||||||
| Идентификаторы | |||||||||
| Символ | FDX-ACB | ||||||||
| Pfam | PF03147 | ||||||||
| ИнтерПро | IPR005121 | ||||||||
| SCOP2 | 1pys / Объем / СУПФАМ | ||||||||
| |||||||||
В энзимология, а фенилаланин-тРНК лигаза (EC 6.1.1.20 ) является фермент который катализирует то химическая реакция
- АТФ + L-фенилаланин + тРНКPhe АМФ + дифосфат + L-фенилаланил-тРНКPhe
3 субстраты этого фермента АТФ, L-фенилаланин, и тРНКPhe, а его 3 товары находятся AMP, дифосфат и L-фенилаланил-тРНКPhe.
Этот фермент принадлежит к семейству лигазы, а именно те, которые образуют углерод-кислородные связи в аминоацил-тРНК и родственных соединениях. В систематическое название этого класса ферментов L-фенилаланин: tRNAPhe-лигаза (AMP-образующая). Другие широко используемые имена включают фенилаланил-тРНК синтетаза, рибонуклеатсинтетаза с переносом фенилаланила, фенилаланин-тРНК синтетаза, фенилаланил-переносящая РНК синтетаза, фенилаланил-тРНК лигаза, фенилаланил-переносящая РНК-лигаза, L-фенилаланил-тРНК синтетаза, и фенилаланин транслаза. Этот фермент участвует в биосинтезе фенилаланина, тирозина и триптофана, а также в биосинтезе аминоацил-тРНК.
Фенилаланин-тРНК синтетаза (PheRS), как известно, является одной из самых сложных ферменты АРС (Аминоацил-тРНК синтетаза ) семья. Бактериальный и митохондриальный PheRS разделяют ферредоксин -складывать антикодон привязка (FDX-ACB) домен, который представляет собой каноническое двойное разделение альфа + бета мотив без прошивок. Домен FDX-ACB отображает типичный Кратность распознавания РНК (RRM), образованный четырехцепочечным антипараллельный бета-лист, с двумя спирали упакованы против этого.[1][2][3][4][5]
Структурные исследования
На конец 2007 г. 10 структуры были решены для этого класса ферментов, с PDB коды доступа 1B70, 1B7Y, 1EIY, 1JJC, 1PYS, 2AKW, 2АЛИ, 2AMC, 2CXI, и 2IY5.
Рекомендации
- ^ Мосяк Л., Решетникова Л., Гольдгур Ю., Деларю М., Сафро М.Г. (июль 1995 г.). «Структура фенилаланил-тРНК синтетазы из Thermus thermophilus». Nat. Struct. Биол. 2 (7): 537–47. Дои:10.1038 / nsb0795-537. PMID 7664121. S2CID 13042127.
- ^ Гольдгур Ю., Мосяк Л., Решетникова Л., Анкилова В., Лаврик О., Ходырева С., Сафро М. (январь 1997 г.). «Кристаллическая структура фенилаланил-тРНК синтетазы из Thermus thermophilus в комплексе с родственным тРНКФе». Структура. 5 (1): 59–68. Дои:10.1016 / s0969-2126 (97) 00166-4. PMID 9016717.
- ^ Родова М., Анкилова В., Сафро М.Г. (февраль 1999 г.). «Человеческая фенилаланил-тРНК синтетаза: клонирование, характеристика выведенных аминокислотных последовательностей с точки зрения структурных доменов и скоординированно регулируемая экспрессия альфа- и бета-субъединиц в клетках хронического миелоидного лейкоза». Biochem. Биофиз. Res. Сообщество. 255 (3): 765–73. Дои:10.1006 / bbrc.1999.0141. PMID 10049785.
- ^ Моор Н., Лаврик О., Фавр А., Сафро М. (сентябрь 2003 г.). «Прокариотические и эукариотические тетрамерные фенилаланил-тРНК синтетазы демонстрируют сохранение режима связывания конца тРНК (Phe) CCA». Биохимия. 42 (36): 10697–708. Дои:10.1021 / bi034732q. PMID 12962494.
- ^ Клипкан Л., Левин И., Кесслер Н., Мур Н., Финаров И., Сафро М. (июль 2008 г.). «ТРНК-индуцированная конформационная активация митохондриальной фенилаланил-тРНК синтетазы человека». Структура. 16 (7): 1095–104. Дои:10.1016 / j.str.2008.03.020. PMID 18611382.
дальнейшее чтение
- Стульберг М.П. (1967). «Выделение и свойства синтетазы фенилаланил рибонуклеиновой кислоты из Escherichia coli B». J. Biol. Chem. 242 (5): 1060–4. PMID 5335910.
| Этот лигаза статья - это заглушка. Вы можете помочь Википедии расширяя это. |

