Субъединица II цитохром с оксидазы - Cytochrome c oxidase subunit II

| Субъединица II цитохром с оксидазы, трансмембранный домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
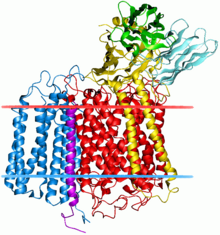 Бактериальный цитохром с оксидаза сложный. Подразделение II обозначается синим. | |||||||||
| Идентификаторы | |||||||||
| Символ | COX2_TM | ||||||||
| Pfam | PF02790 | ||||||||
| ИнтерПро | IPR011759 | ||||||||
| PROSITE | PDOC00075 | ||||||||
| SCOP2 | 1occ / Объем / СУПФАМ | ||||||||
| TCDB | 3.D.4 | ||||||||
| OPM суперсемейство | 4 | ||||||||
| Белок OPM | 1v55 | ||||||||
| |||||||||
| Субъединица II цитохром С оксидазы, периплазматический домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | COX2 | ||||||||
| Pfam | PF00116 | ||||||||
| ИнтерПро | IPR002429 | ||||||||
| CDD | cd13912 | ||||||||
| |||||||||
Субъединица 2 цитохром с оксидазы, также известен как полипептид цитохром с оксидазы II, это белок что у человека кодируется MT-CO2 ген.[4] Субъединица II цитохром с оксидазы, сокращенно COXII, COX2, COII, или MT-CO2, является второй субъединицей цитохром с оксидаза. Это также один из трех митохондриальная ДНК (мтДНК) субъединицы (MT-CO1, MT-CO2, MT-CO3 ) из респираторный комплекс IV.
Структура
В MT-CO2 ген находится на p рука из митохондриальная ДНК в положении 12 и охватывает 683 пары оснований.[4] В MT-CO2 ген продуцирует белок 25,6 кДа, состоящий из 227 аминокислоты.[5][6] MT-CO2 - субъединица фермента Цитохром с оксидаза (EC 1.9.3.1 )[7][8] (Комплекс IV), олигомерный ферментативный сложный из митохондриальная дыхательная цепь участвует в передаче электроны от цитохром с к кислород. У эукариот это фермент сложный расположен в митохондриальная внутренняя мембрана; в аэробный прокариоты он находится в плазматическая мембрана. Ферментный комплекс состоит из 3-4 субъединиц (прокариоты ) до 13 полипептиды (млекопитающие). N-концевой домен цитохром С оксидазы содержит две трансмембранные альфа-спирали.[8][7] Известно, что структура МТ-СО2 содержит один окислительно-восстановительный центр и биядерный медный А-центр (CuA). В CuA находится в консервированном цистеин петля на 196 и 200 аминокислота позиции и сохранены гистидин at 204. Некоторые бактериальные MT-CO2 имеют С-концевое удлинение, которое содержит ковалентно связанный гем c.[9][10]
Функция
В MT-CO2 ген кодирует вторую субъединицу цитохром с оксидаза (комплекс IV), компонент митохондриальная дыхательная цепь что катализирует сокращение из кислород к воды. MT-CO2 - одна из трех субъединиц, которые отвечают за формирование функционального ядра цитохром с оксидаза. MT-CO2 играет важную роль в переносе электронов из цитохром с к биметаллическому центру каталитическая субъединица 1 используя свои биядерный медный центр. Он содержит две смежные трансмембранные области в своем N-конец и большая часть белка подвергается периплазматическому или митохондриальному межмембранное пространство соответственно. MT-CO2 обеспечивает сайт связывания субстрата и содержит биядерный медный центр, вероятно, первичный акцептор цитохром с оксидазы.[11][12][4]
Клиническое значение
Дефицит митохондриального комплекса IV
Варианты MT-CO2 были связаны с митохондриальный Комплекс IV дефицит, дефицит ферментного комплекса митохондриальная дыхательная цепь который катализирует окисление цитохром с использование молекулярный кислород.[13] Дефицит характеризуется неоднородный фенотипы начиная от изолированных миопатия к суровому мультисистемное заболевание поражая несколько тканей и органов. Другие клинические проявления включают: гипертрофическая кардиомиопатия, гепатомегалия и нарушение функции печени, гипотония, мышечная слабость, непереносимость упражнений, отставание в развитии, с задержкой моторное развитие и умственная отсталость.[14] Мутации MT-CO2 также известно, что вызывает Болезнь Ли, что может быть вызвано аномалией или недостатком цитохромоксидаза.[8][7]
У пациентов с патогенными мутациями в MT-CO2 ген с митохонрдиальный Комплекс IV дефицит. А делеционная мутация одного нуклеотида (7630delT) в гене вызывает симптомы обратимого афазия, правильно гемипарез, гемианопсия, непереносимость упражнений, прогрессивный умственная отсталость, и коротко рост.[15] Кроме того, пациент с бессмысленная мутация (7896G> A) гена приводили к таким фенотипам, как невысокий рост, низкий вес, микроцефалия, кожные аномалии, серьезный гипотония, и нормальный рефлексы.[16] Роман гетероплазматический мутации (7587T> C), которая изменила кодон инициации MT-CO2 гена у пациентов проявились клинические проявления, такие как прогрессирующая походка атаксия, когнитивные нарушения двусторонний атрофия зрительного нерва, пигментная ретинопатия, уменьшение цветовое зрение, и умеренно дистально-атрофия мышц.[17]
Другие
Несовершеннолетний миопатия, энцефалопатия, лактоацидоз, и Инсульт также были связаны с мутациями в MT-CO2 ген.[4]
Взаимодействия
Известно, что MT-CO2 взаимодействует с цитохром с за счет использования лизинового кольца вокруг карбоксил содержащий край гема из цитохром с в MT-CO2, включая глутамат 129, аспартат 132 и глутамат 19.
использованная литература
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000064354 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d «Ген Entrez: субъединица II цитохром с оксидазы COX2».
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ Zong NC, Li H, Li H, Lam MP, Jimenez RC, Kim CS, Deng N, Kim AK, Choi JH, Zelaya I, Liem D, Meyer D, Odeberg J, Fang C, Lu HJ, Xu T, Weiss J , Дуан Х., Улен М., Йетс Дж. Р., Апвейлер Р., Ге Дж., Хермякоб Х., Пинг П. (октябрь 2013 г.). «Интеграция биологии кардиального протеома и медицины посредством специализированной базы знаний». Циркуляционные исследования. 113 (9): 1043–53. Дои:10.1161 / CIRCRESAHA.113.301151. ЧВК 4076475. PMID 23965338.
- ^ «Субъединица 2 цитохром с оксидазы». Атлас кардиоорганических белков (COPaKB).[постоянная мертвая ссылка ]
- ^ а б c Капальди Р.А., Малатеста Ф., Дарли-Усмар В.М. (июль 1983 г.). «Структура цитохром с оксидазы». Biochimica et Biophysica Acta (BBA) - Обзоры по биоэнергетике. 726 (2): 135–48. Дои:10.1016/0304-4173(83)90003-4. PMID 6307356.
- ^ а б c Гарсия-Хорсман Дж. А., Баркера Б., Рамбли Дж., Ма Дж., Геннис Р. Б. (сентябрь 1994 г.). «Надсемейство респираторных оксидаз гем-медь». Журнал бактериологии. 176 (18): 5587–600. Дои:10.1128 / jb.176.18.5587-5600.1994. ЧВК 196760. PMID 8083153.
- ^ Капальди Р.А. (1990). «Структура и функции цитохром с оксидазы». Ежегодный обзор биохимии. 59: 569–96. Дои:10.1146 / annurev.bi.59.070190.003033. PMID 2165384.
- ^ Hill BC (апрель 1993 г.). «Последовательность переносчиков электронов в реакции цитохром с оксидазы с кислородом». Журнал биоэнергетики и биомембран. 25 (2): 115–20. Дои:10.1007 / bf00762853. PMID 8389744. S2CID 45975377.
- ^ «MT-CO2 - субъединица 2 цитохром с оксидазы - Homo sapiens (человек) - ген и белок MT-CO2». Получено 2018-08-07.
 Эта статья включает текст доступно под CC BY 4.0 лицензия.
Эта статья включает текст доступно под CC BY 4.0 лицензия. - ^ «UniProt: универсальная база знаний о белках». Исследования нуклеиновых кислот. 45 (D1): D158 – D169. Январь 2017 г. Дои:10.1093 / нар / gkw1099. ЧВК 5210571. PMID 27899622.
- ^ Остергаард Э., Вераарпачай В., Равн К., Борн А. П., Йонсон Л., Дуно М., Вибранд Ф., Шубридж Е. А., Виссинг Дж. (Март 2015 г.). «Мутации в COA3 вызывают изолированный дефицит комплекса IV, связанный с невропатией, непереносимостью физических упражнений, ожирением и низким ростом». Журнал медицинской генетики. 52 (3): 203–7. Дои:10.1136 / jmedgenet-2014-102914. PMID 25604084. S2CID 43018915.
- ^ «Дефицит митохондриального комплекса IV». www.uniprot.org.
- ^ Россманиф В., Фрайлингер М., Рока Дж., Раффельсбергер Т., Мозер-Тьер К., Молитва D, Бернерт Дж., Биттнер Р. Э. (февраль 2008 г.). «Изолированная недостаточность цитохром с оксидазы как причина MELAS». Журнал медицинской генетики. 45 (2): 117–21. Дои:10.1136 / jmg.2007.052076. ЧВК 3027970. PMID 18245391.
- ^ Кампос И., Гарсия-Редондо А., Фернандес-Морено М.А., Мартинес-Пардо М., Года Дж., Рубио Дж. К., Мартин М.А., дель Ойо П., Кабельо А., Борнштейн Б., Гарес Р., Аренас Дж. (Сентябрь 2001 г.). «Раннее начало мультисистемного митохондриального расстройства, вызванного бессмысленной мутацией в гене цитохром С оксидазы II митохондриальной ДНК». Анналы неврологии. 50 (3): 409–13. Дои:10.1002 / ana.1141. PMID 11558799. S2CID 23891106.
- ^ Кларк К.М., Тейлор Р.В., Джонсон М.А., Чиннери П.Ф., Хшановска-Лайтаулерс З.М., Эндрюс Р.М., Нельсон И.П., Вуд Н.В., Ламонт П.Дж., Ханна М.Г., Лайтаулерс Р.Н., Тернбулл Д. «Мутация мтДНК в инициирующем кодоне гена субъединицы II цитохром С-оксидазы приводит к более низким уровням белка и митохондриальной энцефаломиопатии». Американский журнал генетики человека. 64 (5): 1330–9. Дои:10.1086/302361. ЧВК 1377869. PMID 10205264.
дальнейшее чтение
- Торрони А., Ахилли А., Маколей В., Ричардс М., Бандельт Х. Дж. (Июнь 2006 г.). «Сбор плодов дерева мтДНК человека». Тенденции в генетике. 22 (6): 339–45. Дои:10.1016 / j.tig.2006.04.001. PMID 16678300.
- Баррелл Б.Г., Банкир А.Т., Друин Дж. (Ноябрь 1979 г.). «Другой генетический код в митохондриях человека». Природа. 282 (5735): 189–94. Bibcode:1979Натура.282..189Б. Дои:10.1038 / 282189a0. PMID 226894. S2CID 4335828.
- Bodenteich A, Mitchell LG, Polymeropoulos MH, Merril CR (май 1992 г.). «Динуклеотидный повтор в митохондриальной D-петле человека». Молекулярная генетика человека. 1 (2): 140. Дои:10.1093 / hmg / 1.2.140-а. PMID 1301157.
- Лу X, Уокер Т., Макманус Дж. П., Селиги В. Л. (июль 1992 г.). «Дифференциация клеток аденокарциномы толстой кишки человека HT-29 коррелирует с повышенной экспрессией митохондриальной РНК: эффекты трегалозы на рост и созревание клеток». Исследования рака. 52 (13): 3718–25. PMID 1377597.
- Марзуки С., Ноер А.С., Лертрит П., Тьягараджан Д., Капса Р., Уттанапхол П., Бирн Э. (декабрь 1991 г.). «Нормальные варианты митохондриальной ДНК человека и продукты трансляции: создание справочной базы данных». Генетика человека. 88 (2): 139–45. Дои:10.1007 / bf00206061. PMID 1757091. S2CID 28048453.
- Мораес С.Т., Андреетта Ф., Бонилла Э., Шанске С., ДиМауро С., Шон Э.А. (март 1991 г.). «Компетентная к репликации митохондриальная ДНК человека без промоторной области тяжелой цепи». Молекулярная и клеточная биология. 11 (3): 1631–7. Дои:10.1128 / MCB.11.3.1631. ЧВК 369459. PMID 1996112.
- Power MD, Kiefer MC, Barr PJ, Reeves R (август 1989). «Нуклеотидная последовательность кДНК человеческой митохондриальной цитохром с оксидазы II». Исследования нуклеиновых кислот. 17 (16): 6734. Дои:10.1093 / nar / 17.16.6734. ЧВК 318375. PMID 2550900.
- Attardi G, Chomyn A, Doolittle RF, Mariottini P, Ragan CI (1987). «Семь неопознанных рамок считывания митохондриальной ДНК человека кодируют субъединицы НАДН-дегидрогеназы дыхательной цепи». Симпозиумы Колд-Спринг-Харбор по количественной биологии. 51 (1): 103–14. Дои:10.1101 / sqb.1986.051.01.013. PMID 3472707.
- Чомин А., Клитер М.В., Раган К.И., Райли М., Дулиттл Р.Ф., Аттарди Дж. (Октябрь 1986 г.). «URF6, последняя неопознанная рамка считывания мтДНК человека, кодирует субъединицу НАДН-дегидрогеназы». Наука. 234 (4776): 614–8. Bibcode:1986Наука ... 234..614C. Дои:10.1126 / science.3764430. PMID 3764430.
- Чомин А., Мариоттини П., Клитер М.В., Раган К.И., Мацуно-Яги А., Хатефи Ю., Дулиттл Р.Ф., Аттарди Г. (1985). «Шесть неопознанных рамок считывания митохондриальной ДНК человека кодируют компоненты НАДН-дегидрогеназы дыхательной цепи». Природа. 314 (6012): 592–7. Bibcode:1985Натура.314..592С. Дои:10.1038 / 314592a0. PMID 3921850. S2CID 32964006.
- Андерсон С., Банкир А.Т., Баррелл Б.Г., де Брейн М.Х., Коулсон А.Р., Друин Дж., Эперон И.К., Нирлих Д.П., Роу Б.А., Сэнгер Ф., Шрайер П.Х., Смит А.Дж., Стаден Р., Янг И.Г. (апрель 1981 г.). «Последовательность и организация митохондриального генома человека». Природа. 290 (5806): 457–65. Bibcode:1981Натура.290..457A. Дои:10.1038 / 290457a0. PMID 7219534. S2CID 4355527.
- Монтойя Дж., Охала Д., Аттарди Дж. (Апрель 1981 г.). «Отличительные особенности 5'-концевых последовательностей митохондриальных мРНК человека». Природа. 290 (5806): 465–70. Bibcode:1981Натура.290..465М. Дои:10.1038 / 290465a0. PMID 7219535. S2CID 4358928.
- Хораи С., Хаясака К., Кондо Р., Цугане К., Такахата Н. (январь 1995 г.). «Недавнее африканское происхождение современных людей выявлено с помощью полных последовательностей гоминоидных митохондриальных ДНК». Труды Национальной академии наук Соединенных Штатов Америки. 92 (2): 532–6. Bibcode:1995PNAS ... 92..532H. Дои:10.1073 / пнас.92.2.532. ЧВК 42775. PMID 7530363.
- Руволо М., Зер С., фон Дорнум М., Пан Д., Чанг Б., Лин Дж. (Ноябрь 1993 г.). «Митохондриальные последовательности COII и современное происхождение человека». Молекулярная биология и эволюция. 10 (6): 1115–35. Дои:10.1093 / oxfordjournals.molbev.a040068. PMID 8277847.
- Поляк К., Ли И, Чжу Х., Ленгауэр С., Уилсон Дж. К., Марковиц С.Д., Труш М.А., Кинзлер К.В., Фогельштейн Б. (ноябрь 1998 г.). «Соматические мутации митохондриального генома при колоректальных опухолях человека». Природа Генетика. 20 (3): 291–3. Дои:10.1038/3108. PMID 9806551. S2CID 19786796.
- Като М.В. (март 1999 г.). «Механизмы гибели линии эритролейкозных клеток от р53: участие микротрубочек и митохондрий». Лейкемия и лимфома. 33 (1–2): 181–6. Дои:10.3109/10428199909093740. PMID 10194136.
- Эндрюс Р.М., Кубака И., Чиннери П.Ф., Лайтаулерс Р.Н., Тернбулл Д.М., Хауэлл Н. (октябрь 1999 г.). «Повторный анализ и пересмотр кембриджской эталонной последовательности митохондриальной ДНК человека». Природа Генетика. 23 (2): 147. Дои:10.1038/13779. PMID 10508508. S2CID 32212178.
- Ingman M, Kaessmann H, Pääbo S, Gyllensten U (декабрь 2000 г.). «Вариации митохондриального генома и происхождение современного человека». Природа. 408 (6813): 708–13. Bibcode:2000Натура 408..708И. Дои:10.1038/35047064. PMID 11130070. S2CID 52850476.
- Finnilä S, Lehtonen MS, Majamaa K (июнь 2001 г.). «Филогенетическая сеть европейской мтДНК». Американский журнал генетики человека. 68 (6): 1475–84. Дои:10.1086/320591. ЧВК 1226134. PMID 11349229.
- Мака-Мейер Н., Гонсалес А. М., Ларруга Дж. М., Флорес С., Кабрера В. М. (2003). «Основные геномные митохондриальные линии определяют раннюю экспансию человека». BMC Genetics. 2: 13. Дои:10.1186/1471-2156-2-13. ЧВК 55343. PMID 11553319.
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.

