Иммуноглобулин E - Immunoglobulin E
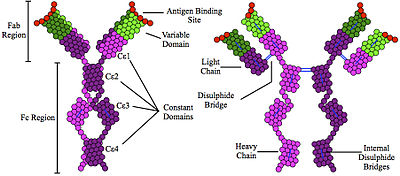


Иммуноглобулин E (IgE) является разновидностью антитело (или же иммуноглобулин (Ig) "изотип "), который был найден только в млекопитающие. IgE синтезируется плазматические клетки. Мономеры IgE состоят из двух тяжелых цепей (ε-цепь) и двух легких цепей, при этом ε-цепь содержит 4 Ig-подобных константных домена (Cε1-Cε4).[1] Основная функция IgE - иммунитет паразитам, таким как гельминты[2] подобно Schistosoma mansoni, Трихинелла спиральная, и Фасциола гепатика.[3][4][5] IgE используется во время иммунной защиты от некоторых простейшие паразиты Такие как Плазмодий falciparum.[6] IgE мог развиться как последняя линия защиты от ядов.[7][8][9]
IgE также играет важную роль в гиперчувствительность I типа,[10] что проявляется при различных аллергических заболеваниях, например, аллергических астма, большинство типов синусит, аллергический ринит, пищевая аллергия и определенные типы хроническая крапивница и атопический дерматит. IgE также играет ключевую роль в ответах на аллергены, такие как: анафилактический реакции на лекарства, укусы пчел и антигенные препараты, используемые для десенсибилизации иммунотерапия.
Хотя IgE обычно является наименее распространенным изотипом -сыворотка крови Уровни IgE в норме («не-атопический ") индивидуальные составляют всего 0,05% от концентрации Ig,[11] по сравнению с 75% для IgGs при 10 мг / мл, которые являются изотипами, ответственными за большинство классических адаптивный иммунный ответ - он способен вызывать сильнейшие воспалительные реакции.[нужна цитата ]
Открытие
IgE был одновременно открыт в 1966 и 1967 годах двумя независимыми группами:[12] Кимишиге Ишизака и его жена Теруко Ишизака в Детском научно-исследовательском институте астмы и больнице в г. Денвер, Колорадо,[13] и С. Г. О. Йоханссоном и Хансом Беннихом в Упсала, Швеция.[14] Их совместная статья была опубликована в апреле 1969 г.[15]
Рецепторы
IgE запускает опосредованный IgE аллергический ответ путем связывания с Fc рецепторы найдено на поверхности тучные клетки и базофилы. Рецепторы Fc также находятся на эозинофилы, моноциты, макрофаги и тромбоциты в людях. Существует два типа рецепторов Fcε:
- FcεRI (рецептор Fcε типа I), высокоаффинный рецептор IgE
- FcεRII (рецептор Fcε типа II), также известный как CD23, рецептор IgE с низким сродством
IgE может повышать экспрессию обоих типов рецепторов Fcε. FcεRI экспрессируется на тучные клетки, базофилы, а антигенпредставляющий дендритные клетки как у мышей, так и у людей. Связывание антигены с IgE, уже связанным FcεRI на тучных клетках, вызывает перекрестное связывание связанного IgE и агрегацию нижележащего FcεRI, что приводит к дегрануляция (высвобождение медиаторов из клеток) и секреция нескольких типов цитокинов типа 2, таких как IL-3 и фактор стволовых клеток (SCF), которые помогают тучным клеткам выжить и накапливаться в ткани, IL-4, IL-5 и IL-13, а также IL-33, которые, в свою очередь, активируют врожденные лимфоидные клетки группы 2 (ILC2 или естественные вспомогательные клетки). Базофилы, имеющие общий гемопоэтический предшественник с тучными клетками, при перекрестном связывании их поверхностно-связанных IgE антигенами также выделяют тип 2. цитокины подобно интерлейкин-4 (Ил-4) и интерлейкин-13 (IL-13) и другие медиаторы воспаления. Рецептор низкой аффинности (FcεRII) всегда экспрессируется на В-клетки; но IL-4 может вызывать его экспрессию на поверхности макрофаги, эозинофилы, тромбоциты, и немного Т-клетки.[16][17]
Функция
Гипотеза паразита
За последнее десятилетие накопилось много данных о физиологической роли IgE: этот изотип эволюционировал совместно с базофилами и тучными клетками в защите от паразитов, таких как гельминты (например, шистосома), но также может быть эффективным при бактериальных инфекциях. Эпидемиологические исследования показывают, что уровень IgE повышается при заражении Schistosoma mansoni,[18] Некатор американский,[19] и нематоды[20] в людях. Скорее всего, он полезен при удалении анкилостомы из легких.[нужна цитата ]
Токсиновая гипотеза аллергического заболевания
В 1981 г. Марджи Профет предположили, что аллергические реакции превратились в последнюю линию защиты от яды.[7] Хотя в то время это было противоречиво, новая работа поддерживает некоторые мысли Профета об адаптивной роли аллергии как защите от вредных токсинов.[8]
В 2013 году выяснилось, что IgE-антитела играют важную роль в приобретенной устойчивости к пчела[9] и Гадюка рассела яды.[9][21] Авторы приходят к выводу, что «небольшая доза пчелиного яда обеспечила иммунитет к гораздо большей, смертельной дозе» и «этот вид специфического для яда, IgE-ассоциированного адаптивного иммунного ответа развился, по крайней мере, в эволюционном плане, для защиты хозяина от потенциально токсичное количество яда, такое как могло бы произойти, если бы животное наткнулось на целое гнездо пчел или в случае укуса змеи ».[9][22][23] Основной аллерген пчелиного яда (фосфолипаза А2) индуцирует иммунные ответы Th2, связанные с выработкой антител IgE, которые могут «повышать устойчивость мышей к заражению потенциально летальными дозами».[24]
Рак
Хотя это еще не совсем понятно, IgE могут играть важную роль в распознавании иммунной системой рак,[25] в котором будет полезна стимуляция сильного цитотоксического ответа против клеток, отображающих только небольшое количество ранних маркеров рака. Если бы это было так, лечение анти-IgE, такое как омализумаб (при аллергии) могут иметь некоторые нежелательные побочные эффекты. Однако недавнее исследование, которое было проведено на основе объединенного анализа с использованием всеобъемлющих данных 67 клинических испытаний фазы I-IV омализумаба при различных показаниях, пришло к выводу, что причинная связь между терапией омализумабом и злокачественными новообразованиями маловероятна.[26]
Роль в болезни
Атопический у людей может быть в десять раз выше нормальный уровень IgE в крови (как и у людей, страдающих синдром гипер-IgE ). Однако это может не быть требованием для появления симптомов, как это наблюдалось у астматиков с нормальным уровнем IgE в крови - недавние исследования показали, что производство IgE может происходить локально в слизистой оболочке носа.[27]
IgE, который может специфически распознавать аллерген (обычно это белок, например пылевой клещ Der p 1, Кот Fel d 1, трава или амброзия пыльца и т. д.) обладает уникальным долгоживущим взаимодействием благодаря высокому сродству рецептор FcεRI так, чтобы базофилы и тучные клетки, способные опосредовать воспалительные реакции, становятся «заряженными», готовыми выделять химические вещества, такие как гистамин, лейкотриены, и некоторые интерлейкины. Эти химические вещества вызывают многие из симптомов, которые мы связываем с аллергией, например сужение дыхательных путей в астма, местное воспаление в экзема, повысился слизь секреция в аллергический ринит Предполагается, что повышенная проницаемость сосудов позволяет другим иммунным клеткам получить доступ к тканям, но это может привести к потенциально фатальному падению артериального давления, как в анафилаксия.[нужна цитата ]
Уровень IgE повышен при различных аутоиммунных заболеваниях, таких как SLE, ревматоидный артрит (RA), и псориаз, и теоретически имеет патогенетическое значение при СКВ и РА, вызывая реакцию гиперчувствительности.[28][29]
Регулирование уровней IgE посредством контроля дифференцировки В-клеток в секретирующие антитела плазматические клетки считается, что он связан с рецептором "низкого сродства" FcεRII, или CD23.[30] CD23 может также способствовать облегченной презентации антигена, IgE-зависимому механизму, посредством которого В-клетки выражая CD23 способны представлять аллерген (и стимулировать) специфические Т-хелперные клетки, вызывая сохранение ответа Th2, одним из отличительных признаков которого является выработка большего количества антител.[31]
Роль в диагностике
Диагностика аллергии чаще всего проводится путем изучения истории болезни человека и определения положительного результата на наличие аллергенспецифических IgE при проведении анализа кожи или крови.[32] Специфический тест на IgE - проверенный тест для выявления аллергии; данные не показывают, что неизбирательное тестирование на IgE или на иммуноглобулин G (IgG) может подтвердить диагноз аллергии.[33]
Лекарства, нацеленные на путь IgE
В настоящее время аллергические заболевания и астму обычно лечат одним или несколькими из следующих препаратов: (1) антигистаминные препараты и антилейкотриены, которые противодействуют медиаторам воспаления гистамину и лейкотриенам, (2) местные или системные (пероральные или инъекционные) кортикостероиды, которые подавляют широкий спектр воспалительных механизмов, (3) короткого или длительного действия бронходилататоры, которые расслабляют гладкие мышцы суженных дыхательных путей при астме, или (4) стабилизаторы тучных клеток, которые подавляют дегрануляция тучных клеток, что обычно запускается связыванием IgE в FcεRI. Известно, что длительное использование системных кортикостероидов вызывает множество серьезных побочных эффектов, и их рекомендуется избегать, если доступны альтернативные методы лечения.[нужна цитата ]
IgE, путь синтеза IgE и опосредованный IgE путь аллергии / воспаления - все они являются важными мишенями для вмешательства в патологические процессы аллергии, астмы и других заболеваний, опосредованных IgE. Путь дифференцировки и созревания B-лимфоцитов, который в конечном итоге генерирует плазматические клетки, секретирующие IgE, проходит через промежуточные стадии B-лимфобластов, экспрессирующих IgE, и включает взаимодействие с B-клетками памяти, экспрессирующими IgE. Танокс, биотехнологическая компания, базирующаяся в Хьюстоне, штат Техас, в 1987 году предложила, что, воздействуя на мембраносвязанный IgE (mIgE) на В-лимфобласты и В-клетки памяти, эти клетки можно лизировать или подавлять, таким образом достигая ингибирования продукции антигена. -специфический IgE и, следовательно, сдвиг иммунного баланса в сторону механизмов, не связанных с IgE.[34] Были разработаны два подхода, нацеленных на путь IgE, и оба они активно развиваются. В первом подходе анти-IgE лекарство с антителами омализумаб (торговое наименование Xolair ) распознает IgE, не связанный с его рецепторами, и используется для нейтрализации или поглощения существующего IgE и предотвращения его связывания с рецепторами тучных клеток и базофилов. Xolair был одобрен во многих странах для лечения тяжелой стойкой аллергической астмы. Он также был одобрен в марте 2014 года в Европейском Союзе.[35] и США.[36] для лечения хроническая спонтанная крапивница, которые нельзя адекватно лечить с помощью H1-антигистаминные препараты. Во втором подходе были получены антитела, специфичные к домену из 52 аминокислотных остатков, называемому CεmX или M1 '(первичный M1), присутствующим только на человеческом mIgE на В-клетках, а не на свободном растворимом IgE, и их количество ниже клиническая разработка для лечения аллергии и астмы.[37][38] Гуманизированное антитело против M1 ’, квилизумаб, находится в фазе клинических испытаний IIb.[39][40]
В 2002 году исследователи из The Рэндалл Отдел клеточной и молекулярной биофизики определили структуру IgE.[41] Понимание этой структуры (которая нетипична для других изотипов в том смысле, что она сильно изогнута и асимметрична) и взаимодействия IgE с рецептором FcεRI позволит разработать новое поколение лекарств от аллергии, которые стремятся вмешиваться во взаимодействие IgE-рецептора. Возможно, удастся разработать лечение дешевле, чем моноклональные антитела (например, низкомолекулярные препараты), которые используют аналогичный подход для ингибирования связывания IgE с его рецептором.[нужна цитата ]
Рекомендации
- ^ «Структура антитела». Архивировано из оригинал 6 сентября 2008 г.
- ^ Эрб К.Дж. (май 2007 г.). «Гельминты, аллергические расстройства и IgE-опосредованные иммунные реакции: где мы находимся?». Европейский журнал иммунологии. 37 (5): 1170–3. Дои:10.1002 / eji.200737314. PMID 17447233. S2CID 24519249.
- ^ Фитцсиммонс С.М., Макбит Р., Джозеф С., Джонс Ф.М., Уолтер К., Хоффманн К.Ф. и др. (2007). «Факторы, влияющие на ответы человеческого IgE и IgG на аллергеноподобные антигены Schistosoma mansoni: молекулярная структура и образцы воздействия in vivo». Международный архив аллергии и иммунологии. 142 (1): 40–50. Дои:10.1159/000095997. PMID 17019080. S2CID 16676316.
- ^ Ватанабэ Н., Бруски Ф., Коренага М. (апрель 2005 г.). «IgE: вопрос защитного иммунитета при инфекции Trichinella spiralis». Тенденции в паразитологии. 21 (4): 175–8. Дои:10.1016 / j.pt.2005.02.010. PMID 15780839.
- ^ Пфистер К., Тернер К., Карри А., Холл Е, Джарретт Э. (ноябрь 1983 г.). «Продукция IgE при фасциолезе крыс». Иммунология паразитов. 5 (6): 587–93. Дои:10.1111 / j.1365-3024.1983.tb00775.x. PMID 6657297. S2CID 1530964.
- ^ Дуарте Дж., Дешпанде П., Гуйеди В., Мешери С., Фесель С., Казенав П.А. и др. (Январь 2007 г.). «Общие и функциональные паразитоспецифические IgE-ответы у пациентов, инфицированных Plasmodium falciparum, с различным клиническим статусом». Журнал Малярии. 6: 1. Дои:10.1186/1475-2875-6-1. ЧВК 1781948. PMID 17204149.
- ^ а б Профет М (март 1991 г.). «Функция аллергии: иммунологическая защита от токсинов». Ежеквартальный обзор биологии. 66 (1): 23–62. Дои:10.1086/417049. PMID 2052671. S2CID 5648170.
- ^ а б Palm NW, Розенштейн Р.К., Меджитов Р. (апрель 2012 г.). «Аллергическая защита хозяина». Природа. 484 (7395): 465–72. Bibcode:2012Натура.484..465П. Дои:10.1038 / природа11047. ЧВК 3596087. PMID 22538607.
- ^ а б c d Маричал Т., Старкл П., Ребер Л.Л., Калесникофф Дж., Этген Х.С., Цай М. и др. (Ноябрь 2013). «Благоприятная роль иммуноглобулина Е в защите хозяина от яда медоносной пчелы». Иммунитет. 39 (5): 963–75. Дои:10.1016 / j.immuni.2013.10.005. ЧВК 4164235. PMID 24210352.
- ^ Гулд Х.Дж., Саттон Б.Дж., Бивил А.Дж., Бивил Р.Л., Макклоски Н., Кокер Х.А. и др. (2003). «Биология ИГЭ и основы аллергических заболеваний». Ежегодный обзор иммунологии. 21: 579–628. Дои:10.1146 / annurev.immunol.21.120601.141103. PMID 12500981.
- ^ Winter WE, Hardt NS, Fuhrman S (сентябрь 2000 г.). «Иммуноглобулин E: важность при паразитарных инфекциях и реакциях гиперчувствительности». Архив патологии и лабораторной медицины. 124 (9): 1382–5. Дои:10.1043 / 0003-9985 (2000) 124 <1382: IE> 2.0.CO; 2 (неактивно 13.11.2020). PMID 10975945.CS1 maint: DOI неактивен по состоянию на ноябрь 2020 г. (ссылка на сайт)
- ^ Стэнворт Д.Р. (февраль 1993 г.). «Открытие IgE». Аллергия. 48 (2): 67–71. Дои:10.1111 / j.1398-9995.1993.tb00687.x. PMID 8457034. S2CID 36262710.
- ^ Ишизака К., Ишизака Т., Хорнбрук М.М. (июль 1966 г.). «Физико-химические свойства реагинового антитела человека. IV. Наличие уникального иммуноглобулина как носителя реагиновой активности». Журнал иммунологии. 97 (1): 75–85. PMID 4162440.
- ^ Йоханссон С.Г., Беннич Х. (октябрь 1967 г.). «Иммунологические исследования атипичного (миеломного) иммуноглобулина». Иммунология. 13 (4): 381–94. ЧВК 1409218. PMID 4168094.
- ^ Ишизака Т., Ишизака К., Йоханссон С.Г., Беннич Х. (апрель 1969 г.). «Высвобождение гистамина из лейкоцитов человека анти-гамма-антителами Е». Журнал иммунологии. 102 (4): 884–92. PMID 4181251. Получено 2016-02-29.
- ^ Юарт М.А., Озанн Б.В., Кушли В. (май 2002 г.). «Проксимальные промоторы CD23a и CD23b проявляют разную чувствительность к экзогенным стимулам в B-лимфоцитах». Гены и иммунитет. 3 (3): 158–64. Дои:10.1038 / sj.gene.6363848. PMID 12070780.
- ^ Новак Н., Крафт С., Бибер Т. (декабрь 2001 г.). «Рецепторы IgE». Текущее мнение в иммунологии. 13 (6): 721–6. Дои:10.1016 / s0952-7915 (01) 00285-0. PMID 11677096.
- ^ Риет П., Демер С.Е., Бургуа А., Прата А., Дессейн А.Дж. (ноябрь 1991 г.). «Доказательства связи между устойчивостью человека к Schistosoma mansoni и высокими уровнями антител к личинкам IgE». Европейский журнал иммунологии. 21 (11): 2679–86. Дои:10.1002 / eji.1830211106. PMID 1936116. S2CID 1103861.
- ^ Причард Д.И., Куиннелл Р.Дж., Уолш Е.А. (февраль 1995 г.). «Иммунитет человека к Necator americanus: IgE, масса паразита и плодовитость». Иммунология паразитов. 17 (2): 71–5. Дои:10.1111 / j.1365-3024.1995.tb00968.x. PMID 7761110. S2CID 41222700.
- ^ Тернер Дж. Д. и др. (Июнь 2005 г.). «Аллерген-специфические IgE и IgG4 являются маркерами устойчивости и восприимчивости при кишечной нематодной инфекции человека». Микробы и инфекции. 7 (7–8): 990–6. Дои:10.1016 / j.micinf.2005.03.036. PMID 15961339.
- ^ Старкл П., Маричал Т., Гауденцио Н., Ребер Л.Л., Сибилано Р., Цай М., Галли С.Дж. (январь 2016 г.). «Антитела IgE, FcεRIα и IgE-опосредованная местная анафилаксия могут ограничивать токсичность змеиного яда». Журнал аллергии и клинической иммунологии. 137 (1): 246–257.e11. Дои:10.1016 / j.jaci.2015.08.005. ЧВК 4715494. PMID 26410782.
- ^ Шарлах, Молли (24 октября 2013 г.). «Аллергия на пчелиный укус может быть неадекватной защитной реакцией, - говорят ученые». Стэнфордский центр медицинских новостей. Получено 20 ноября 2019.
- ^ Фоли, Джеймс А. (25 октября 2013 г.). «Тяжелая аллергия на пчелиные укусы может быть нарушением эволюционной реакции». Новости мира природы.
- ^ Цай М., Старкл П., Маричал Т., Галли С.Дж. (октябрь 2015 г.). «Проверка« токсинной гипотезы аллергии »: тучные клетки, IgE, а также врожденные и приобретенные иммунные ответы на яды». Текущее мнение в иммунологии. 36: 80–7. Дои:10.1016 / j.coi.2015.07.001. ЧВК 4593748. PMID 26210895.
- ^ Карагианнис С.Н., Ван К., Восточный Н., Берк Ф., Риффард С., Бракер М.Г. и др. (Апрель 2003 г.). «Активность человеческих моноцитов в IgE-антителозависимом наблюдении и уничтожении опухолевых клеток яичников». Европейский журнал иммунологии. 33 (4): 1030–40. Дои:10.1002 / eji.200323185. PMID 12672069. S2CID 29495137.
- ^ Бусс В., Буль Р., Фернандес Видаурре С., Блог М., Чжу Дж., Эйснер М.Д., Канвин Дж. (Апрель 2012 г.). «Омализумаб и риск злокачественных новообразований: результаты объединенного анализа». Журнал аллергии и клинической иммунологии. 129 (4): 983–9.e6. Дои:10.1016 / j.jaci.2012.01.033. PMID 22365654.
- ^ Тахар П., Смуртуэйт Л., Кокер Х.А., Страх DJ, Банфилд Г.К., Карр В.А. и др. (Апрель 2005 г.). «Аллерген вызывает переключение класса на IgE в слизистой оболочке носа при аллергическом рините». Журнал иммунологии. 174 (8): 5024–32. Дои:10.4049 / jimmunol.174.8.5024. PMID 15814733.
- ^ Permin H, Wiik A (октябрь 1978 г.). «Распространенность антинуклеарных антител IgE при ревматоидном артрите и системной красной волчанке». Acta Pathologica et Microbiologica Scandinavica, Раздел C. 86C (5): 245–9. Дои:10.1111 / j.1699-0463.1978.tb02587.x. PMID 309705.
- ^ Элькаям О., Тамир Р., Пик А.И., Вайзенбек А. (январь 1995 г.). «Концентрации IgE в сыворотке, активность заболевания и атопические расстройства при системной красной волчанке». Аллергия. 50 (1): 94–6. PMID 7741196.
- ^ Конрад Д.Х., Форд Дж. В., Стерджилл Дж. Л., Гибб Д. Р. (сентябрь 2007 г.). «CD23: недооцененный регулятор аллергических заболеваний». Текущие отчеты об аллергии и астме. 7 (5): 331–7. Дои:10.1007 / s11882-007-0050-у. PMID 17697638. S2CID 24816595.
- ^ Холм Дж., Виллумсен Н., Вюртцен П.А., Кристенсен Л.Х., Лунд К. (апрель 2011 г.). «Облегченная презентация антигена и его ингибирование путем блокирования антител IgG зависит от сложности репертуара IgE». Журнал аллергии и клинической иммунологии. 127 (4): 1029–37. Дои:10.1016 / j.jaci.2011.01.062. PMID 21377718.
- ^ Кокс Л., Уильямс Б., Шичерер С., Оппенгеймер Дж., Шер Л., Гамильтон Р., Голден Д. (декабрь 2008 г.). «Жемчужины и подводные камни диагностического тестирования аллергии: отчет Американского колледжа аллергии, астмы и иммунологии / Американской академии аллергии, астмы и иммунологической целевой группы тестирования IgE». Анналы аллергии, астмы и иммунологии. 101 (6): 580–92. Дои:10.1016 / S1081-1206 (10) 60220-7. PMID 19119701.
- ^ Американская академия аллергии, астмы и иммунологии. «Пять вещей, которые должны задать вопросы врачам и пациентам» (PDF). Мудрый выбор: инициатива ABIM Foundation. Архивировано из оригинал (PDF) 3 ноября 2012 г.. Получено 14 августа, 2012.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Чанг Т.В., Ву ПК, Сюй Ц.Л., Хунг А.Ф. (2007). Антитела против IgE для лечения аллергических заболеваний, опосредованных IgE. Adv. Иммунол. Успехи иммунологии. 93. С. 63–119. Дои:10.1016 / S0065-2776 (06) 93002-8. ISBN 9780123737076. PMID 17383539.
- ^ «Novartis объявляет, что Xolair® одобрен в ЕС как первая и единственная лицензированная терапия для пациентов с хронической спонтанной крапивницей (CSU), не реагирующих на антигистаминные препараты». Новартис. 2014-03-06. Архивировано из оригинал на 2014-12-18. Получено 2014-12-04.
- ^ «Novartis объявляет об одобрении FDA США препарата Xolair® для лечения хронической идиопатической крапивницы (CIU)». Новартис. 2014-03-21. Архивировано из оригинал на 2014-12-03. Получено 2014-12-04.
- ^ Chen JB, Wu PC, Hung AF, Chu CY, Tsai TF, Yu HM и др. (Февраль 2010 г.). «Уникальные эпитопы на C-эпсилон mX в рецепторах клеток IgE-B потенциально применимы для нацеливания на IgE-коммитированные B-клетки». Журнал иммунологии. 184 (4): 1748–56. Дои:10.4049 / jimmunol.0902437. PMID 20083663.
- ^ Brightbill HD, Jeet S, Lin Z, Yan D, Zhou M, Tan M и др. (Июнь 2010 г.). «Антитела, специфичные к сегменту человеческого мембранного IgE, истощают IgE-продуцирующие В-клетки у гуманизированных мышей». Журнал клинических исследований. 120 (6): 2218–29. Дои:10.1172 / JCI40141. ЧВК 2877936. PMID 20458139.
- ^ "MEMP1972A". ClinicalTrials.gov. НАС. Национальные институты здоровья. Получено 2014-12-04.
- ^ Говро Дж. М., Харрис Дж. М., Буле Л. П., Шеренс Х., Фицджеральд Дж. М., Патнам В.С. и др. (Июль 2014 г.). «Нацеливание на мембранно-экспрессируемый B-клеточный рецептор IgE с помощью антитела к первичному эпитопу M1 снижает продукцию IgE». Научная трансляционная медицина. 6 (243): 243ra85. Дои:10.1126 / scitranslmed.3008961. PMID 24990880. S2CID 41593528.
- ^ Ван Т., Бивил Р.Л., Фабиан С.М., Бивил А.Дж., Сохи М.К., Кеун М. и др. (Июль 2002 г.). «Кристаллическая структура IgE Fc обнаруживает асимметрично изогнутую конформацию». Иммунология природы. 3 (7): 681–6. Дои:10.1038 / ni811. PMID 12068291. S2CID 32347451.
