Ароматичность Мёбиуса - Möbius aromaticity


В органическая химия, Ароматичность Мёбиуса это особый вид ароматичность считается, что существует в ряде Органические молекулы.[1][2] С точки зрения теория молекулярных орбиталей эти соединения имеют общий моноциклический массив молекулярные орбитали в котором наблюдается нечетное количество перекрытий в противофазе, картина противоположная по сравнению с ароматическим характером для Системы Hückel. Узловая плоскость орбиталей, рассматриваемая как лента, представляет собой Лента Мебиуса, а не цилиндр, отсюда и название. Картина орбитальных энергий дана повернутым Морозный круг (с краем многоугольника внизу вместо вершины), поэтому системы с 4п электроны ароматические, а с 4п + 2 электрона являются антиароматическими / неароматическими. Из-за постепенно закрученной природы орбиталей ароматической системы Мебиуса, стабильные ароматические молекулы Мебиуса должны содержать по крайней мере 8 электронов, хотя 4-хэлектронные ароматические переходные состояния Мебиуса хорошо известны в контексте концепции Дьюара-Циммермана для перициклические реакции. Молекулярные системы Мебиуса считались в 1964 г. Эдгар Хайльброннер путем применения Метод Хюккеля,[3] но первое такое выделяемое соединение не было синтезировано до 2003 г. Райнер Хергес.[4] Однако мимолетное транс-C9ЧАС9+ катион, одна из конформаций которого показана справа, был предложен в качестве промежуточного соединения ароматического ряда Мебиуса в 1998 году на основании расчетных и экспериментальных данных.
Ароматичность Хюккеля-Мебиуса
Комплекс Хергеса (6 на изображении ниже) был синтезирован в нескольких фотохимический циклоприсоединение реакция от тетрадегидродиантрацен 1 и Ladderane син-трициклооктадиен 2 в качестве замены циклооктатетраен.[5]
Средний 5 была смесью 2 изомеры и конечный продукт 6 смесь 5 изомеров с разными цис- и транс-конфигурации. У одного из них была обнаружена буква C2 молекулярная симметрия соответствующий ароматическому веществу Мебиуса, а другой изомер Хюккеля был обнаружен с Cs симметрия. Несмотря на то, что в его пи-системе 16 электронов (что делает его 4n антиароматический соединение) Предсказание Хейльброннера Это подтвердилось, потому что, согласно Хергесу, соединение Мебиуса обладает ароматическими свойствами. С длина облигаций выведено из Рентгеновская кристаллография а HOMA было получено значение 0,50 (для полиен только часть) и 0,35 для всего соединения, что квалифицирует его как умеренный аромат.
На это указал Генри Рзепа что преобразование промежуточных 5 к 6 может пройти либо по Хюккелю, либо по Мёбиусу. переходное состояние.[6]
Разница была продемонстрирована на гипотетическом перициклический реакция раскрытия кольца на циклододекагексаен. TS Hückel (слева) включает 6 электронов (стрелка нажата красным) с Cs молекулярная симметрия сохраняется на протяжении всей реакции. Открытие кольца отвратительный и надфасциальный и оба длина облигации чередование и НИКС значения указывают на то, что 6-членное кольцо является ароматическим. С другой стороны, ТС Мёбиуса с 8 электронами имеет более низкую расчетную энергия активации и характеризуется C2 симметрия, а соперничающий и антарафациальный раскрытие кольца и ароматичность 8-членного кольца.
Другой интересной системой является циклононатетраенильный катион, исследованный более 30 лет специалистами Пол против Р. Шлейера и другие. Этот реактивный промежуточный продукт подразумевается в сольволиз из бициклический хлористый 9-дейтеро-9'-хлорбицикло [6.1.0] -нонатриен 1 к инден дигидроинденол 4.[7][8] Исходный хлорид дейтерированный только в одной позиции, но в конечном продукте дейтерий распределяется в каждой доступной позиции. Это наблюдение объясняется использованием закрученного 8-электронного циклононатетраенильного катиона 2 для чего НИКС значение -13,4 (перехитрить бензол ) рассчитывается.[9]
 Расчетная структура транс-C9ЧАС9+, 2, иллюстрирующий закрученную природу кольца, позволяющую постепенно вращать ориентацию p-атомных орбиталей вокруг кольца: отслеживание p-орбиталей по всему кольцу приводит к инверсии фазы относительно начальной p-орбитали. Плоскость углеродного скелета (то есть узловая плоскость p-орбиталей) образует ленту Мёбиуса.
Расчетная структура транс-C9ЧАС9+, 2, иллюстрирующий закрученную природу кольца, позволяющую постепенно вращать ориентацию p-атомных орбиталей вокруг кольца: отслеживание p-орбиталей по всему кольцу приводит к инверсии фазы относительно начальной p-орбитали. Плоскость углеродного скелета (то есть узловая плоскость p-орбиталей) образует ленту Мёбиуса.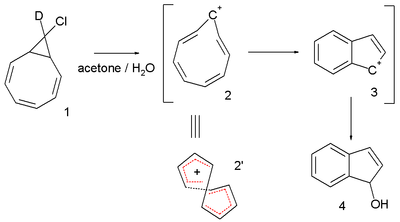
В 2005 году тот же П. против Р. Шлейера [10] поставил под сомнение утверждение Хергеса 2003 года: он проанализировал те же кристаллографические данные и пришел к выводу, что действительно существует большая степень чередования длин связей, приводящая к значению HOMA -0,02, вычисленное значение NICS -3,4 ppm также не указывает на ароматичность и ( также выведено из компьютерной модели) стерическое напряжение предотвратит эффективное перекрытие пи-орбиталей.
А Ароматичность Хюккеля-Мебиуса switch (2007) был описан на основе 28 пи-электронов порфирин система:[11][12]
В фенилен кольца в этой молекуле могут свободно вращаться, образуя набор конформеры: один с полувручением Мёбиуса и другой с двойным закруткой Хюккеля (конфигурация в виде восьмерки) примерно равной энергии.
В 2014 году Чжу и Ся (с помощью Шлейера) синтезировали планарную систему Мебиуса, состоящую из двух пентеновых колец, связанных с атомом осмия.[13] Они сформировали производные, в которых осмий имел 16 и 18 электронов, и определили, что ароматичность Крейга-Мебиуса более важна для стабилизации молекулы, чем количество электронов в металле.
Переходные состояния
В отличие от редких ароматов Мебиуса основное состояние молекулярных систем, есть много примеров перициклический переходные состояния которые демонстрируют ароматичность Мебиуса. Классификация перициклического переходного состояния как топологии Мёбиуса или Хюккеля определяет, будет ли 4N или 4N + 2 электрона необходимы, чтобы сделать переходное состояние ароматическим или антиароматическим и, следовательно, разрешенным или запрещенным соответственно. На основе диаграмм уровней энергии, полученных из Теория Хюккеля, (4N + 2) -электрон Хюккеля и (4N) -электронные переходные состояния Мебиуса являются ароматическими и разрешенными, а (4N + 2) -электрон Мебиуса и (4N) -электронные переходные состояния Хюккеля являются антиароматическими и запрещенными. Это основная предпосылка Концепция Мебиуса-Хюккеля.[14][15]
Вывод уровней энергии теории МО Хюккеля для топологии Мебиуса
Из рисунка выше также видно, что взаимодействие между двумя последовательными АО ослабляется постепенным скручиванием орбиталей на , куда - угол скручивания между последовательными орбиталями по сравнению с обычной системой Хюккеля. По этой причине резонансный интеграл дан кем-то
- ,
куда является стандартным значением резонансного интеграла Хюккеля (с полностью параллельными орбиталями). Тем не менее, после полного обхода N-я и 1-я орбитали почти полностью не в фазе. (Если бы скручивание продолжалось после -й орбиталь 1-я орбиталь будет точно инвертирована по фазе по сравнению с 1-й орбиталью). По этой причине в матрице Хюккеля резонансный интеграл между углеродными и является .
Для общего углеродная система Мёбиуса, матрица гамильтониана является:
- .
Теперь можно найти собственные значения для этой матрицы, которые соответствуют энергетическим уровням системы Мебиуса. С это матрица, у нас будет собственные значения и МО. Определение переменной
- ,
у нас есть:
- .
Чтобы найти нетривиальные решения этого уравнения, мы устанавливаем определитель этой матрицы равным нулю, чтобы получить
- .
Следовательно, мы находим уровни энергии для циклической системы с топологией Мёбиуса:
- .
Напротив, вспомним уровни энергии для циклической системы с топологией Хюккеля:
- .
Смотрите также
Рекомендации
- ^ Рзепа, Генри С. (2005). «Ароматичность Мёбиуса и делокализация». Chem. Rev. 105 (10): 3697–3715. Дои:10.1021 / cr030092l.
- ^ Сок Юн, Зин; Осука, Атсухиро; Ким, Донхо (2009). «Ароматичность Мёбиуса и антиароматичность расширенных порфиринов». Химия природы. 1: 113–122. Дои:10.1038 / nchem.172.
- ^ Хайльброннер, Э. (1964). "Молекулярные орбитали Хюккеля конформаций аннуленов типа Мебиуса". Буквы Тетраэдра. 5 (29): 1923–1928. Дои:10.1016 / S0040-4039 (01) 89474-0.
- ^ Ajami, D .; Oeckler, O .; Саймон, А .; Хергес, Р. (декабрь 2003 г.). «Синтез ароматического углеводорода Мебиуса». Природа. 426: 819–821. Дои:10.1038 / природа02224. PMID 14685233.
- ^ Отметим, что кольцо Мебиуса формируется формально. реакция метатезиса между 1 и СОТ
- ^ Ароматичность переходных состояний перициклических реакций. Генри С. Рзепа J. Chem. Educ. 2007, 84, 1535. Абстрактный
- ^ Павел; Шлейер Р. (1971). «Термическая перегруппировка бицикло [6.1.0] нонатриенилхлорид-дигидроинденилхлорид». Журнал Американского химического общества. 93: 279–281. Дои:10.1021 / ja00730a063.
- ^ Хергес, Райнер (2006). «Топология в химии: проектирование молекул Мёбиуса †». Химические обзоры. 106: 4820–4842. Дои:10.1021 / cr0505425.
- ^ Моноциклический (CH) 9+ - раскрыта ароматическая система Heilbronner Möbius Angewandte Chemie International Edition Том 37, выпуск 17, дата: 18 сентября, г. 1998, Страницы: 2395-2397 Майкл Маукш, Валентин Гогонеа, Хайджун Цзяо, Пол фон Раге Шлейер
- ^ Кастро, Клэр (2005). "Исследование предполагаемого ароматического углеводорода Мебиуса. Влияние бензаннелирования на ароматичность мебиуса [4 n] аннулена". Журнал Американского химического общества. 127: 2425–2432. Дои:10.1021 / ja0458165.
- ^ Стемпень, Марцин (2007). «Расширенный порфирин с расщепленной личностью: переключатель ароматичности Хюккеля – Мебиуса». Angewandte Chemie International Edition. 46: 7869–7873. Дои:10.1002 / anie.200700555.
- ^ Реагенты: пиррол, бензальдегид, трифторид бора, последующее окисление DDQ, Ph = фенил Mes = мезитил
- ^ Чжу, Цунцин; Мин Ло; Цинь Чжу; Цзюнь Чжу; Пол против Р. Шлейера; Джуди И-Чиа Ву; Синь Лу; Хайпин Ся (25 февраля 2014 г.). «Планарные ароматические пенталены Мебиуса, содержащие осмий с валентными электронами 16 и 18». Nature Communications. 5: 3265. Bibcode:2014 НатКо ... 5E3265Z. Дои:10.1038 / ncomms4265. PMID 24567039.
- ^ Циммерман, Х. Э (1966). "О диаграммах молекулярной орбитальной корреляции, появлении систем Мебиуса в реакциях циклизации и факторах, управляющих реакциями основного и возбужденного состояния. I". Варенье. Chem. Soc. 88: 1564–1565. Дои:10.1021 / ja00959a052.
- ^ Циммерман, Х. Э (1966). "О диаграммах молекулярной орбитальной корреляции, системах Мебиуса и факторах, управляющих реакциями основного и возбужденного состояний. II". Варенье. Chem. Soc. 88: 1566–1567. Дои:10.1021 / ja00959a053.
























