Перицит - Википедия - Pericyte
| Перицит | |
|---|---|
 Передача инфекции электронная микрофотография из микрососуд показывая перициты, выстилающие внешнюю поверхность эндотелиальные клетки которые окружают эритроцит (E). | |
| Подробности | |
| Идентификаторы | |
| латинский | перицит |
| MeSH | D020286 |
| TH | H3.09.02.0.02006 |
| FMA | 63174 |
| Анатомические термины микроанатомии | |
Перициты (ранее известный как Клетки Руже)[1] многофункциональны настенные клетки из микроциркуляция которые обертывают эндотелиальные клетки эта линия капилляры и венулы по всему телу.[2] Перициты встроены в базальная мембрана, где они общаются с эндотелиальными клетками мельчайших кровеносный сосуд посредством как прямого физического контакта, так и паракринная передача сигналов.[3] Перициты помогают поддерживать гомеостатический и кровоостанавливающий функции в мозг а также поддерживать гематоэнцефалический барьер.[4] Эти клетки также являются ключевым компонентом сосудисто-нервное устройство, в состав которого входят эндотелиальные клетки, астроциты, и нейроны.[5][6] Перициты регулируют капиллярный кровоток, клиренс и фагоцитоз клеточного дебриса и проницаемости гематоэнцефалического барьера. Перициты стабилизируют и контролируют созревание эндотелиальных клеток посредством прямого взаимодействия между клеточной мембраной, а также посредством паракринной передачи сигналов.[7] Дефицит перицитов в Центральная нервная система может привести к разрушению гематоэнцефалического барьера.[4]
Структура
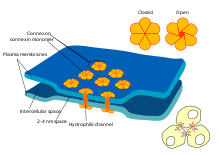
В центральной нервной системе перициты окружают эндотелиальные клетки, выстилающие внутреннюю часть капилляра. Эти два типа ячеек можно легко отличить друг от друга по наличию выступающего круглого ядро перицита по сравнению с плоским удлиненным ядром эндотелиальных клеток.[5] Перициты также выступают в виде пальцев, которые охватывают стенку капилляра, позволяя клеткам регулировать капиллярный кровоток.[4]
И перициты, и эндотелиальные клетки имеют общую базальную мембрану, в которой образуются различные межклеточные связи. Многие виды интегрин молекулы облегчают связь между перицитами и эндотелиальными клетками, разделенными базальной мембраной.[4] Перициты также могут образовывать прямые связи с соседними ячейками, образуя штифты и гнезда, в которых части ячеек сцепляются друг с другом, как шестерни часов. На этих взаимосвязанных сайтах щелевые соединения могут образовываться, что позволяет перицитам и соседним клеткам обмениваться ионами и другими небольшими молекулами.[4] Важные молекулы в этих межклеточных связях включают: N-кадгерин, фибронектин, коннексин и различные интегрины.[5]
В некоторых областях базальной мембраны адгезионные бляшки состоит из фибронектина. Эти бляшки облегчают соединение базальной мембраны с цитоскелет структура состоит из актин и плазматическая мембрана перицитов и эндотелиальных клеток.[4]
Функция
Регенерация скелетных мышц и образование жира
Перициты в скелетно-поперечно-полосатая мышца принадлежат к двум разным популяциям, каждая из которых играет свою роль. Первый подтип перицита (Тип-1) может различаться на толстый клетки, а другой (Тип 2) - в мышечные клетки. Тип 1 характеризуется отрицательным выражением для нестин (PDGFRβ + CD146 + Nes-) и тип 2, характеризующиеся положительной экспрессией нестина (PDGFRβ + CD146 + Nes +). Хотя оба типа способны размножаться в ответ на глицерин или повреждение, вызванное BaCl2, перициты типа 1 дают рост адипогенных клеток только в ответ на инъекцию глицерина, а тип 2 становится миогенным в ответ на оба типа травма, повреждение. Степень участия перицитов 1-го типа в накоплении жира неизвестна.
Ангиогенез и выживание эндотелиальных клеток
Перициты также связаны с дифференцировкой и размножением эндотелиальных клеток, ангиогенез, выживание апоптотический сигналы и путешествия. Определенные перициты, известные как перициты микрососудов, развиваются вокруг стенок капилляров и помогают выполнять эту функцию. Перициты микрососудов могут не быть сократительными клетками, поскольку в них отсутствуют альфа-актин изоформы, структуры, которые распространены среди других сократительных клеток. Эти клетки связываются с эндотелиальными клетками через щелевые соединения, и, в свою очередь, вызывают пролиферацию эндотелиальных клеток или их избирательное ингибирование. Если этого не произошло, гиперплазия и аномальные сосуды морфогенез может привести. Эти типы перицитов также могут фагоцитоз экзогенные белки. Это говорит о том, что тип клеток мог быть получен из микроглия.[8]
Была предложена родственная связь с другими типами клеток, включая гладкомышечные клетки,[9] нервные клетки,[9] NG2 глия,[10] мышечные волокна, адипоциты, а также фибробласты[11] и другие мезенхимальные стволовые клетки. Однако, дифференцируются ли эти клетки друг в друга, остается нерешенным в данной области. На регенерационную способность перицитов влияет старение.[11] Такая универсальность полезна, поскольку они активно реконструируют кровеносные сосуды по всему телу и, таким образом, могут однородно смешиваться с местными. ткань среда.[12]
Было обнаружено, что помимо создания и ремоделирования кровеносных сосудов перициты защищают эндотелиальные клетки от гибели через апоптоз или цитотоксический элементы. Было показано in vivo что перициты выпускают гормон известен как перицитический аминопептидаза N / pAPN, который может способствовать ангиогенезу. Когда этот гормон смешивали с мозговой эндотелиальные клетки, а также астроциты, перициты сгруппированы в структуры, напоминающие капилляры. Кроме того, когда экспериментальная группа содержала все перечисленное, за исключением перицитов, эндотелиальные клетки подвергались апоптозу.[требуется дальнейшее объяснение ] Таким образом, был сделан вывод, что перициты должны присутствовать для обеспечения правильного функционирования эндотелиальных клеток, а астроциты должны присутствовать, чтобы гарантировать, что оба остаются в контакте. В противном случае не может произойти правильный ангиогенез.[13] Также было обнаружено, что перициты способствуют выживанию эндотелиальных клеток, поскольку они секретируют белок. Bcl-w во время сотовых перекрестных помех. Bcl-w - это инструментальный белок в пути, обеспечивающем VEGF-A экспрессия и препятствует апоптозу.[14] Хотя есть некоторые предположения, почему VEGF непосредственно отвечает за предотвращение апоптоза, считается, что он отвечает за модуляцию апоптоза пути передачи сигналов и ингибирует активацию индуцирующего апоптоз ферменты. Для этого VEGF использует два биохимических механизма: фосфорилирование из внеклеточная регуляторная киназа 1 (ERK-1, также известный как MAPK3), который поддерживает выживание клеток с течением времени, и ингибирует стресс-активированную протеинкиназу / c-jun-NH2 киназу, которая также способствует апоптозу.[15]
Гематоэнцефалический барьер
Перициты играют решающую роль в формировании и функционировании гематоэнцефалический барьер. Этот барьер состоит из эндотелиальных клеток и обеспечивает защиту и функциональность мозга и центральной нервной системы. Было обнаружено, что перициты имеют решающее значение для постнатального формирования этого барьера. Перициты отвечают за плотные контакты формирование и торговля пузырьками среди эндотелиальных клеток. Кроме того, они позволяют формировать гематоэнцефалический барьер, подавляя эффекты ЦНС. иммунные клетки (что может повредить формирование барьера) и за счет снижения экспрессии молекул, которые увеличивают проницаемость сосудов.[16]
Помимо образования гематоэнцефалического барьера, перициты также играют активную роль в его функциональности, контролируя поток внутри кровеносных сосудов и между кровеносными сосудами и мозгом. В моделях на животных с более низким покрытием перицитов перемещение молекул через эндотелиальные клетки происходит с более высокой частотой, позволяя проникать в мозг белками, которые обычно исключаются.[17] Утрата или дисфункция перицитов также теоретически способствует развитию нейродегенеративных заболеваний, таких как Болезнь Альцгеймера, Болезнь Паркинсона и ALS через нарушение гематоэнцефалического барьера.
Кровоток
Все больше данных свидетельствует о том, что перициты могут регулировать кровоток на капиллярном уровне. По сетчатке опубликованы фильмы[18] показывая, что перициты сужают капилляры, когда их мембранный потенциал изменяется, вызывая приток кальция, а в головном мозге сообщалось, что активность нейронов увеличивает местный кровоток, заставляя перициты расширять капилляры до того, как происходит расширение артериол вверх по течению.[19] Этот район является спорным, с недавним исследованием, утверждая, что перициты не выражают сократительные белки и не способны сжатия в естественных условиях,[20] хотя последняя статья была подвергнута критике за использование весьма нетрадиционного определения перицита, которое явно исключает сократительные перициты.[21] По-видимому, разные сигнальные пути регулируют сужение капилляров перицитами и артериол гладкомышечными клетками.[22]
Перициты важны для поддержания кровообращения. В исследовании с участием взрослых мышей с дефицитом перицитов церебральный кровоток снижался с одновременной регрессией сосудов из-за потери как эндотелия, так и перицитов. Сообщалось о значительно большей гипоксии в гиппокампе мышей с дефицитом перицитов, а также о воспалении и учусь и объем памяти обесценение.[23]
Клиническое значение
Из-за их решающей роли в поддержании и регулировании структуры эндотелиальных клеток и кровотока, нарушения функции перицитов наблюдаются при многих патологиях. Они могут либо присутствовать в избытке, что приводит к таким заболеваниям, как гипертония и образование опухолей, либо в дефиците, что приводит к нейродегенеративным заболеваниям.
Гемангиома
Клинические фазы гемангиома имеют физиологические различия, коррелированные с иммунофенотипическими профилями Takahashi et al. Во время ранней пролиферативной фазы (0–12 месяцев) опухоли экспрессируют ядерный антиген пролиферирующих клеток (перицитесна), фактор роста эндотелия сосудов (VEGF) и коллагеназу типа IV, причем первые два локализуются как в эндотелии, так и в перицитах, а последние - в эндотелии. . Сосудистые маркеры CD31, фактор фон Виллебранда (vWF) и актин гладких мышц (маркер перицита) присутствуют во время фазы пролиферации и инволюции, но теряются после того, как поражение полностью инволюционировано.[24]
Гемангиоперицитома
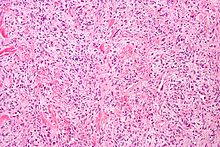
Гемангиоперицитома представляет собой редкое сосудистое новообразование или аномальный рост, которое может быть доброкачественным или злокачественным. При злокачественной форме могут возникать метастазы в легкие, печень, мозг и конечности. Чаще всего он проявляется в бедренной кости и проксимальном отделе большеберцовой кости в виде саркомы кости и обычно обнаруживается у пожилых людей, хотя случаи были обнаружены и у детей. Гемангиоперицитома возникает из-за чрезмерного наслоения листов перицитов вокруг неправильно сформированных кровеносных сосудов. Диагностика этой опухоли затруднена из-за невозможности отличить перициты от других типов клеток с помощью световой микроскопии. Лечение может включать хирургическое удаление и лучевую терапию, в зависимости от уровня проникновения в кости и стадии развития опухоли.[25]
Диабетическая ретинопатия
В сетчатке диабетиков часто наблюдается потеря перицитов, и эта потеря является характерным фактором ранних стадий заболевания. диабетическая ретинопатия. Исследования показали, что перициты необходимы диабетикам для защиты эндотелиальных клеток капилляров сетчатки. При потере перицитов в капиллярах образуются микроаневризмы. В ответ сетчатка увеличивает проницаемость сосудов, что приводит к отеку глаза через макулярный отек, или образует новые сосуды, проникающие в стекловидная оболочка глаза. Конечный результат - снижение или потеря зрения.[26] Хотя неясно, почему перициты теряются у пациентов с диабетом, одна из гипотез состоит в том, что токсичность сорбитол и конечные продукты с улучшенным гликированием (AGE) накапливаются в перицитах. Из-за накопления глюкозы путь полиола увеличивает его приток, а внутриклеточные сорбит и фруктоза накапливаются. Это приводит к осмотическому дисбалансу, что приводит к повреждению клеток. Наличие высокого уровня глюкозы также приводит к накоплению AGE, которые также повреждают клетки.[27]
Нейродегенеративные заболевания
Исследования показали, что потеря перицитов во взрослом и стареющем мозге ведет к нарушению надлежащей церебральной перфузии и поддержанию гематоэнцефалического барьера, что вызывает нейродегенерацию и нейровоспаление.[28] Апоптоз перицитов в стареющем мозге может быть результатом нарушения связи между факторами роста и рецепторами перицитов. Фактор роста тромбоцитов B (PDGFB ) высвобождается из эндотелиальных клеток в сосудистой сети головного мозга и связывается с рецептором PDGFRB на перицитах, инициируя их пролиферацию и вложение в сосудистую сеть.
Иммуногистохимические исследования тканей человека от болезни Альцгеймера и бокового амиотрофического склероза показывают потерю перицитов и нарушение гематоэнцефалического барьера. Модели мышей с дефицитом перицитов (в которых отсутствуют этапы кодирования генов в сигнальном каскаде PDGFB: PDGFRB) и имеют мутацию, вызывающую болезнь Альцгеймера, усугубили патологию, подобную болезни Альцгеймера, по сравнению с мышами с нормальным покрытием перицитов и мутацией, вызывающей болезнь Альцгеймера.
Гладить
В условиях Инсульт перициты сужают капилляры головного мозга, а затем умирают, что может привести к длительному снижению кровотока и потере функции гематоэнцефалического барьера, что увеличивает гибель нервных клеток.[19]
Исследование
Эндотелиальные и перицитные взаимодействия
Эндотелиальные клетки и перициты взаимозависимы, и нарушение надлежащего взаимодействия между двумя типами клеток может привести к многочисленным патологиям человека.[29]
Между эндотелиальными клетками и перицитами существует несколько путей сообщения. Первый трансформирующий фактор роста (TGF) передача сигналов, которая опосредуется эндотелиальными клетками. Это важно для дифференциации перицитов.[30][31] Ангиопоэтин 1 и Галстук-2 передача сигналов важна для созревания и стабилизации эндотелиальных клеток.[32] Фактор роста тромбоцитов (PDGF) путь передачи сигналов от эндотелиальных клеток рекрутирует перициты, так что перициты могут мигрировать в развивающиеся кровеносные сосуды. Если этот путь заблокирован, это приводит к дефициту перицитов.[33] Сфингозин-1-фосфат (S1P) сигнализация также помогает в рекрутировании перицитов посредством коммуникации через G-белковые рецепторы. S1P отправляет сигналы через GTPases которые способствуют доставке N-кадгерина к эндотелиальным мембранам. Этот трафик усиливает контакты эндотелия с перицитами.[34]
Связь между эндотелиальными клетками и перицитами жизненно важна. Ингибирование пути PDGF приводит к дефициту перицитов. Это вызывает гиперплазию эндотелия, аномальные соединения и диабетическую ретинопатию.[26] Недостаток перицитов также вызывает повышенную регуляцию фактор роста эндотелия сосудов (VEGF), что приводит к утечке сосудов и кровоизлияние.[35] Ангиопоэтин 2 может действовать как антагонист Tie-2,[36] дестабилизирует эндотелиальные клетки, что приводит к меньшему взаимодействию эндотелиальных клеток и перицитов. Иногда это приводит к образованию опухолей.[37] Подобно ингибированию пути PDGF, ангиопоэтин 2 снижает уровни перицитов, что приводит к диабетической ретинопатии.[38]
Рубцевание
Обычно астроциты связаны с процессом рубцевания в Центральная нервная система, формируя глиальные рубцы. Было высказано предположение, что подтип перицитов участвует в этом рубцевании независимо от глии. Посредством исследований по отслеживанию происхождения этих подтипов перицитов наблюдали после инсульта, обнаружив, что они вносят вклад в глиальный рубец, дифференцируясь в миофибробласты и откладывая внеклеточный матрикс.[39] Однако это остается спорным, поскольку более поздние исследования показывают, что типом клеток, использованных в этих исследованиях рубцов, скорее всего, будут не перициты, а фибробласты.[40][41]
Вклад в нейрогенез у взрослых
Новые данные (по состоянию на 2019 год) предполагают, что перициты нервных микрососудов под руководством резидентных глиальных клеток перепрограммируются в интернейроны и обогащают местные нейронные микросхемы.[42] Этот ответ усиливается сопутствующим ангиогенезом.
Смотрите также
- Гемангиоперицитома
- Мезоангиобласт
- Диабетическая ретинопатия вызвано гибелью перицитов
- Список типов клеток человека, полученных из зародышевых листков
Рекомендации
- ^ Дор-Даффи, П. (2008). «Перициты: плюрипотентные клетки гематоэнцефалического барьера». Текущий фармацевтический дизайн. 14 (16): 1581–93. Дои:10.2174/138161208784705469. PMID 18673199.
- ^ Бирбрайр А., Чжан Т., Ван З.М., Месси М.Л., Минц А., Дельбоно О. (январь 2015 г.). «Перициты на стыке регенерации тканей и патологии». Клиническая наука. 128 (2): 81–93. Дои:10.1042 / CS20140278. ЧВК 4200531. PMID 25236972.
- ^ Бергерс Г., Песня С. (октябрь 2005 г.). «Роль перицитов в формировании и поддержании кровеносных сосудов». Нейроонкология. 7 (4): 452–64. Дои:10.1215 / S1152851705000232. ЧВК 1871727. PMID 16212810.
- ^ а б c d е ж Винклер Э.А., Белл Р.Д., Злокович Б.В. (октябрь 2011 г.). «Перициты центральной нервной системы в здоровье и болезни». Природа Неврология. 14 (11): 1398–1405. Дои:10.1038 / № 2946. ЧВК 4020628. PMID 22030551.
- ^ а б c Дор-Даффи П., Клири К. (2011). «Морфология и свойства перицитов». Кровь-мозг и другие нейронные барьеры. Методы молекулярной биологии. 686. С. 49–68. Дои:10.1007/978-1-60761-938-3_2. ISBN 978-1-60761-937-6. PMID 21082366.
- ^ Либнер S, Czupalla CJ, Wolburg H (2011). «Современные концепции развития гематоэнцефалического барьера». Международный журнал биологии развития. 55 (4–5): 467–76. Дои:10.1387 / ijdb.103224sl. PMID 21769778.
- ^ Фахреджахани Э., Той М (2012). «Ангиогенез опухоли: перициты и созревание нельзя игнорировать». Журнал онкологии. 2012: 1–10. Дои:10.1155/2012/261750. ЧВК 3191787. PMID 22007214.
- ^ «Ассоциация перицитов, астроцитов и базальной пластинки с гематоэнцефалическим барьером (BBB)». Университет медицинских наук Аризоны. Архивировано из оригинал 16 февраля 2017 г.
- ^ а б Бирбрайр А., Чжан Т., Ван З.М., Месси М.Л., Эниколопов Г.Н., Минц А., Дельбоно О. (январь 2013 г.). «Подтипы перицитов скелетных мышц различаются по потенциалу дифференцировки». Исследования стволовых клеток. 10 (1): 67–84. Дои:10.1016 / j.scr.2012.09.003. ЧВК 3781014. PMID 23128780.
- ^ Бирбрайр А., Чжан Т., Ван З.М., Месси М.Л., Эниколопов Г.Н., Минц А., Дельбоно О. (январь 2013 г.). «Клетки-предшественники нейронов скелетных мышц проявляют свойства NG2-глии». Экспериментальные исследования клеток. 319 (1): 45–63. Дои:10.1016 / j.yexcr.2012.09.008. ЧВК 3597239. PMID 22999866.
- ^ а б Бирбрайр А., Чжан Т., Ван З.М., Месси М.Л., Минц А., Дельбоно О. (декабрь 2013 г.). «Перициты типа 1 участвуют в отложении фиброзной ткани в старых скелетных мышцах». Американский журнал физиологии. Клеточная физиология. 305 (11): C1098–113. Дои:10.1152 / ajpcell.00171.2013. ЧВК 3882385. PMID 24067916.
- ^ Герхардт Х., Бетсгольц С. (октябрь 2003 г.). «Эндотелиально-перицитные взаимодействия в ангиогенезе». Исследования клеток и тканей. 314 (1): 15–23. Дои:10.1007 / s00441-003-0745-х. PMID 12883993. S2CID 24258796.
- ^ Рамзауэр М., Краузе Д., Дермицель Р. (август 2002 г.). «Ангиогенез гематоэнцефалического барьера in vitro и функция церебральных перицитов». Журнал FASEB. 16 (10): 1274–6. Дои:10.1096 / fj.01-0814fje. PMID 12153997. S2CID 37606009.
- ^ Франко М., Розвалл П., Кортез Э., Ханахан Д., Пьетрас К. (сентябрь 2011 г.). «Перициты способствуют выживанию эндотелиальных клеток за счет индукции аутокринной передачи сигналов VEGF-A и экспрессии Bcl-w». Кровь. 118 (10): 2906–17. Дои:10.1182 / кровь-2011-01-331694. ЧВК 3172806. PMID 21778339.
- ^ Гупта К., Кширсагар С., Ли В., Гуй Л., Рамакришнан С., Гупта П., Ло П. Я., Хеббель Р. П. (март 1999 г.). «VEGF предотвращает апоптоз эндотелиальных клеток микрососудов человека за счет противоположных эффектов на передачу сигналов MAPK / ERK и SAPK / JNK». Экспериментальные исследования клеток. 247 (2): 495–504. Дои:10.1006 / excr.1998.4359. PMID 10066377.
- ^ Данеман Р., Чжоу Л., Кебеде А.А., Баррес Б.А. (ноябрь 2010 г.). «Перициты необходимы для целостности гематоэнцефалического барьера во время эмбриогенеза». Природа. 468 (7323): 562–6. Bibcode:2010Натура.468..562D. Дои:10.1038 / природа09513. ЧВК 3241506. PMID 20944625.
- ^ Armulik A, Genové G, Mäe M, Nisancioglu MH, Wallgard E, Niaudet C, He L, Norlin J, Lindblom P, Strittmatter K, Johansson BR, Betsholtz C (ноябрь 2010 г.). «Перициты регулируют гематоэнцефалический барьер». Природа. 468 (7323): 557–61. Bibcode:2010Натура.468..557A. Дои:10.1038 / природа09522. HDL:10616/40288. PMID 20944627. S2CID 4429989. Сложить резюме – Каролинский институт (14 октября 2010 г.).
- ^ Peppiatt CM, Howarth C, Mobbs P, Attwell D (октябрь 2006 г.). «Двунаправленный контроль диаметра капилляров ЦНС перицитами». Природа. 443 (7112): 700–4. Bibcode:2006Натура.443..700П. Дои:10.1038 / природа05193. ЧВК 1761848. PMID 17036005.
- ^ а б Холл С.Н., Рейнелл С., Гесслейн Б., Гамильтон Н.Б., Мишра А., Сазерленд Б.А., О'Фаррелл FM, Бьюкен А.М., Лауритцен М., Аттвелл Д. (апрель 2014 г.). «Капиллярные перициты регулируют церебральный кровоток при здоровье и болезни». Природа. 508 (7494): 55–60. Bibcode:2014Натура508 ... 55ч. Дои:10.1038 / природа13165. ЧВК 3976267. PMID 24670647.
- ^ Hill RA, Tong L, Yuan P, Murikinati S, Gupta S, Grutzendler J (июль 2015 г.). «Региональный кровоток в нормальном и ишемическом мозге контролируется сократимостью гладкомышечных клеток артериол, а не капиллярными перицитами». Нейрон. 87 (1): 95–110. Дои:10.1016 / j.neuron.2015.06.001. ЧВК 4487786. PMID 26119027.
- ^ Аттвелл Д., Мишра А., Холл CN, О'Фаррелл FM, Далкара Т. (февраль 2016 г.). "Что такое перицит?". Журнал церебрального кровотока и метаболизма. 36 (2): 451–5. Дои:10.1177 / 0271678x15610340. ЧВК 4759679. PMID 26661200.
- ^ Мишра А., Рейнольдс Дж. П., Чен Ю., Гурин А. В., Русаков Д. А., Атвелл Д. (декабрь 2016 г.). «Астроциты опосредуют нервно-сосудистую передачу сигналов перицитам капилляров, но не артериолам». Природа Неврология. 19 (12): 1619–1627. Дои:10.1038 / № 4428. ЧВК 5131849. PMID 27775719.
- ^ Белл Р.Д., Винклер Е.А., Сагаре А.П., Сингх И., ЛаРю Б., Дин Р., Злокович Б.В. (ноябрь 2010 г.). «Перициты контролируют ключевые нервно-сосудистые функции и нейрональный фенотип в мозге взрослого человека и во время старения мозга». Нейрон. 68 (3): 409–27. Дои:10.1016 / j.neuron.2010.09.043. ЧВК 3056408. PMID 21040844.
- ^ Мюнде П. «Перициты в здоровье и болезнях». Celesta Software Pvt Ltd. Получено 22 ноября 2014.
- ^ Геллман Х. «Солитарная фиброзная опухоль». Medscape. Получено 2 ноября 2011.
- ^ а б Hammes HP, Лин Дж., Реннер О., Шани М., Лундквист А., Бетсхольц С., Браунли М., Deutsch U (октябрь 2002 г.). «Перициты и патогенез диабетической ретинопатии». Сахарный диабет. 51 (10): 3107–12. Дои:10.2337 / диабет.51.10.3107. PMID 12351455.
- ^ Чиулла Т.А., Амадор А.Г., Зинман Б. (сентябрь 2003 г.). «Диабетическая ретинопатия и диабетический макулярный отек: патофизиология, скрининг и новые методы лечения». Уход за диабетом. 26 (9): 2653–64. Дои:10.2337 / diacare.26.9.2653. PMID 12941734.
- ^ Сагаре, Абхай; Белл, Роберт; Чжао, Чжэнь; Ма, Цинъи; Винклер, Итан; Раманатан, Анита; Злокович, Берислав (13 декабря 2013 г.). «Потеря перицитов влияет на нейродегенерацию, подобную болезни Альцгеймера, у мышей». Nature Communications. 4: 2932. Bibcode:2013НатКо ... 4.2932S. Дои:10.1038 / ncomms3932. ЧВК 3945879. PMID 24336108.
- ^ Армулик А., Абрамссон А., Бетсгольц С. (сентябрь 2005 г.). «Эндотелиальные / перицитные взаимодействия». Циркуляционные исследования. 97 (6): 512–23. Дои:10.1161 / 01.RES.0000182903.16652.d7. PMID 16166562.
- ^ Карвалью Р.Л., Йонкер Л., Гуманс М.Дж., Ларссон Дж., Бауман П., Карлссон С., Дейк П.Т., Артур Х.М., Mummery CL (декабрь 2004 г.). «Нарушение паракринной передачи сигналов с помощью TGFbeta в сосудистой сети желточного мешка мышей с мутантным эндоглином: парадигма наследственной геморрагической телеангиэктазии». Разработка. 131 (24): 6237–47. Дои:10.1242 / dev.01529. PMID 15548578.
- ^ Хирши К.К., Роховский С.А., Д'Амор П.А. (май 1998 г.). «PDGF, TGF-бета и гетеротипические межклеточные взаимодействия опосредуют индуцированное эндотелиальными клетками рекрутирование клеток 10T1 / 2 и их дифференцировку в судьбу гладких мышц». Журнал клеточной биологии. 141 (3): 805–14. Дои:10.1083 / jcb.141.3.805. ЧВК 2132737. PMID 9566978.
- ^ Терстон Дж., Сури К., Смит К., Макклейн Дж., Сато Т. Н., Янкопулос Г. Д., Макдональд Д. М. (декабрь 1999 г.). «Устойчивые к утечке кровеносные сосуды у мышей, трансгенно сверхэкспрессирующих ангиопоэтин-1». Наука. 286 (5449): 2511–4. Дои:10.1126 / science.286.5449.2511. PMID 10617467.
- ^ Бьярнегард М., Энге М., Норлин Дж., Густафсдоттир С., Фредрикссон С., Абрамссон А., Такемото М., Густафссон Е., Фесслер Р., Бетсхольц С. (апрель 2004 г.). «Эндотелий-специфическое удаление PDGFB приводит к потере перицитов и аномалиям клубочков, сердца и плаценты». Разработка. 131 (8): 1847–57. Дои:10.1242 / dev.01080. PMID 15084468.
- ^ Пайк Дж. Х., Скура А., Чае СС, Коуэн А. Э., Хан Д. К., Пройа Р. Л., Хла Т. (октябрь 2004 г.). «Регулирование сфингозин-1-фосфатным рецептором N-кадгерина опосредует стабилизацию сосудов». Гены и развитие. 18 (19): 2392–403. Дои:10.1101 / gad.1227804. ЧВК 522989. PMID 15371328.
- ^ Hellström M, Gerhardt H, Kalén M, Li X, Eriksson U, Wolburg H, Betsholtz C (апрель 2001 г.). «Недостаток перицитов приводит к гиперплазии эндотелия и аномальному морфогенезу сосудов». Журнал клеточной биологии. 153 (3): 543–53. Дои:10.1083 / jcb.153.3.543. ЧВК 2190573. PMID 11331305.
- ^ Maisonpierre PC, Suri C, Jones PF, Bartunkova S, Wiegand SJ, Radziejewski C, Compton D, McClain J, Aldrich TH, Papadopoulos N, Daly TJ, Davis S, Sato TN, Yancopoulos GD (июль 1997 г.). «Ангиопоэтин-2, естественный антагонист Tie2, который нарушает ангиогенез in vivo». Наука. 277 (5322): 55–60. Дои:10.1126 / science.277.5322.55. PMID 9204896.
- ^ Чжан Л., Ян Н., Пак Дж. В., Катсарос Д., Фраккиоли С., Цао Дж., О'Брайен-Дженкинс А., Рэндалл Т.С., Рубин СК, Кукос Дж. (Июнь 2003 г.). «Произведенный из опухоли фактор роста эндотелия сосудов активирует ангиопоэтин-2 в эндотелии хозяина и дестабилизирует сосудистую сеть хозяина, поддерживая ангиогенез при раке яичников». Исследования рака. 63 (12): 3403–12. PMID 12810677.
- ^ Hammes HP, Lin J, Wagner P, Feng Y, Vom Hagen F, Krzizok T., Renner O, Breier G, Brownlee M, Deutsch U (апрель 2004 г.). «Ангиопоэтин-2 вызывает выпадение перицитов в нормальной сетчатке: доказательства участия в диабетической ретинопатии». Сахарный диабет. 53 (4): 1104–10. Дои:10.2337 / диабет.53.4.1104. PMID 15047628.
- ^ Гериц К., Диас Д.О., Томилин Н., Барбакид М., Шупляков О., Фризен Дж. (Июль 2011 г.). «Перицитное происхождение рубцовой ткани спинного мозга». Наука. 333 (6039): 238–42. Bibcode:2011Sci ... 333..238G. Дои:10.1126 / science.1203165. PMID 21737741. S2CID 206532774.
- ^ Содерблом С., Ло Х, Блюменталь Е., Брей Е., Ляпичев К., Рамос Дж., Кришнан В., Лай-Сюй С., Парк К. К., Цулфас П., Ли Дж. К. (август 2013 г.). «Периваскулярные фибробласты образуют фиброзный рубец после контузионного повреждения спинного мозга». Журнал неврологии. 33 (34): 13882–7. Дои:10.1523 / JNEUROSCI.2524-13.2013. ЧВК 3755723. PMID 23966707.
- ^ Vanlandewijck M, He L, Mäe MA, Andrae J, Ando K, Del Gaudio F, Nahar K, Lebouvier T., Laviña B, Gouveia L, Sun Y, Raschperger E, Räsänen M, Zarb Y, Mochizuki N, Keller A, Lendahl U, Betsholtz C (февраль 2018 г.). «Молекулярный атлас типов клеток и зональности в сосудистой сети мозга». Природа. 554 (7693): 475–480. Bibcode:2018Натура.554..475V. Дои:10.1038 / природа25739. HDL:10138/301079. PMID 29443965. S2CID 205264161.
- ^ Farahani, Ramin M .; Резаи ‐ Лотфи, Саба; Симонян, Мэри; Шаймардан, Мунира; Хантер, Нил (2019). «Нервные микрососудистые перициты вносят вклад в нейрогенез взрослого человека». Журнал сравнительной неврологии. 527 (4): 780–796. Дои:10.1002 / cne.24565. ISSN 1096-9861. PMID 30471080. S2CID 53711787.
внешняя ссылка
- www.stemcellsfreak.com - Перициты можно использовать для регенерации мышц
- Схема на udel.edu
