CDH2 - CDH2
N-кадгерин, также известный как Кадгерин-2 (CDH2) или же нейронный кадгерин (NCAD) представляет собой белок, который у человека кодируется CDH2 ген.[5][6] CDH2 также был обозначен как CD325 (кластер дифференциации 325). N-кадгерин представляет собой трансмембранный белок экспрессируется во многих тканях и выполняет функции, обеспечивающие межклеточную адгезию. В сердечная мышца, N-кадгерин является неотъемлемым компонентом прилипает к стыкам проживающий в вставные диски, которые служат для механического и электрического соединения соседних кардиомиоциты. Пока мутации в CDH2 до сих пор не были связаны с заболеваниями человека, изменениями экспрессии и целостности N-кадгерина белок наблюдался при различных формах болезней, в том числе у человека дилатационная кардиомиопатия.
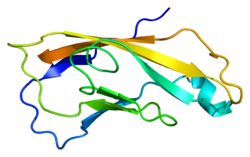
Структура
N-кадгерин представляет собой белок с молекулярной массой 99,7 кДа и 906 аминокислоты в длину.[7] N-кадгерин, классический кадгерин из суперсемейства кадгеринов, состоит из пяти внеклеточных кадгерин повторяет, а трансмембранная область и очень консервативный цитоплазматический хвост. N-кадгерин, как и другие кадгерины, взаимодействовать с N-кадгерином в соседней клетке в антипараллельное строение, таким образом создавая линейную липкую «молнию» между ячейками.[8]
Функция
N-кадгерин, первоначально названный в честь его роли в нервная ткань, играет роль в нейроны и позже было обнаружено, что он также играет роль в сердечная мышца и в раке метастаз. N-кадгерин представляет собой трансмембранный, гомофильный гликопротеин принадлежащий к семейство молекул кальций-зависимой адгезии клеток. Эти белки имеют внеклеточные домены которые опосредуют гомофильные взаимодействия между соседними клетками, и C-терминал, цитоплазматический хвосты, которые опосредуют привязку к катенины, которые, в свою очередь, взаимодействуют с актин цитоскелет.[9][10][11]
Роль в развитии
N-кадгерин играет роль в развитии как кальций-зависимая межклеточная адгезия. гликопротеин который функционирует во время гаструляция и требуется для создания лево-правая асимметрия.[12]
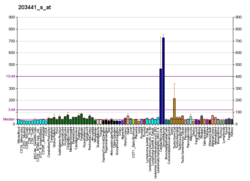
N-кадгерин широко экспрессируется в эмбрион после имплантации, показывая высокие уровни в мезодерма с устойчивым выражением в зрелом возрасте.[13] Мутация N-кадгерина во время развития оказывает наиболее значительное влияние на адгезию клеток в примитивном сердце; диссоциированный миоциты и происходит ненормальное развитие сердечной трубки.[14] N-кадгерин играет роль в развитии сердца позвоночных при переходе эпителиальные клетки к трабекулярный и компактный миокард формирование клеточного слоя.[15] Дополнительное исследование показало, что миоциты экспрессия доминантно-отрицательного мутанта N-кадгерина показала значительные отклонения в миоцит распространение и миграция в сторону эндокард, что приводит к дефектам трабекулярного образования внутри миокард.[16][17]
Роль в сердечной мышце
В сердечная мышца, N-кадгерин находится в вставной диск структуры, которые обеспечивают соединения между ячейками, что облегчает механическое и электрическое соединение между соседними кардиомиоциты. В вставные диски бывают три типа стыков: прилипает к стыкам, десмосомы и щелевые соединения;[18] N-кадгерин является важным компонентом в прилипает к стыкам, который обеспечивает межклеточную адгезию и передачу силы через сарколемма.[19] N-кадгерин в комплексе с катенины был описан как главный регулятор вставной диск функция.[20] N-кадгерин появляется на межклеточных соединениях до щелевой переход формирование[21][22] и имеет решающее значение для нормального миофибриллогенез.[23] Экспрессия мутантной формы N-кадгерина, несущей большую делецию в внеклеточный домен подавляет функцию эндогенного N-кадгерина у взрослых желудочковый кардиомиоциты, и соседние кардиомиоциты потеря межклеточного контакта и щелевой переход бляшки.[24]
Мышиные модели, использующие трансгенез, подчеркнули функцию N-кадгерина в сердечная мышца. Мыши с измененной экспрессией N-кадгерина и / или E-кадгерина показали дилатационная кардиомиопатия фенотип, вероятно, из-за неисправности вставные диски.[25] В соответствии с этим, мыши с удалением N-кадгерина во взрослых сердцах с помощью кардиоспецифического индуцируемого тамоксифеном трансгена Cre N-кадгерина показали нарушенную сборку вставные диски, дилатационная кардиомиопатия, нарушение сердечной функции, снижение саркомер длина, увеличенная Z-линия толщина, уменьшается в коннексин 43, и потеря мышечного напряжения. Мыши умерли в течение двух месяцев после экспрессии трансгена, в основном из-за спонтанного Вентрикулярная тахикардия.[26] Дальнейший анализ мышей с нокаутом N-кадгерина показал, что аритмии вероятно из-за ионный канал ремоделирование и аберрантная функция канала Kv1.5. Эти животные показали длительную потенциал действия продолжительность, уменьшенная плотность входной выпрямительный калиевый канал и снижение выраженности Kv1.5, KCNE2 и кортактин в сочетании с нарушенной актин цитоскелет на сарколемма.[27]
Роль в нейронах
В нервных клетках, в определенной центральной нервной системе синапсы от пресинаптического к постсинаптическому адгезия по крайней мере частично опосредуется N-кадгерином.[28] N-кадгерины взаимодействуют с катенинами, чтобы играть важную роль в обучении и памяти (Полный текст статьи см. Кадгерин-катениновый комплекс в обучении и памяти ).
Роль в метастазировании рака
N-кадгерин обычно обнаруживается в раковых клетках и обеспечивает механизм трансэндотелиальной миграции. Когда раковая клетка прикрепляется к эндотелиальным клеткам кровеносного сосуда, она активирует src киназа путь, который фосфорилирует бета-катенины прикреплен как к N-кадгерину (этот белок), так и к E-кадгерины. Это приводит к нарушению межклеточной связи между двумя соседними эндотелиальными клетками и позволяет раковой клетке проскользнуть внутрь.[29]
Клиническое значение
Мутации в CDH2 не были окончательно связаны с какими-либо заболеваниями человека. Одно исследование, изучающее генетические основы обсессивно-компульсивное расстройство и Расстройство Туретта обнаружил, что пока CDH2 варианты, скорее всего, не вызывают болезни как отдельные сущности, они могут создавать риск, когда исследуются как часть панели родственных генов межклеточной адгезии.[30] Для однозначного определения этого потребуются дальнейшие исследования на более крупных когортах.
В человеческом дилатационная кардиомиопатия, было показано, что экспрессия N-кадгерина была усилена и организована беспорядочно, что позволяет предположить, что дезорганизация белка N-кадгерина в сердечное заболевание может быть компонентом ремоделирования.[31]
Взаимодействия
CDH2 показал взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000170558 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск ансамбля 89: ENSMUSG00000024304 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Уолш Ф.С., Бартон С.Х., Путт В., Мур С.Е., Келселл Д., Сперр Н., Гудфеллоу П.Н. (сентябрь 1990 г.). «Ген N-кадгерина отображается на хромосоме 18 человека и не связан с геном E-кадгерина». J. Neurochem. 55 (3): 805–12. Дои:10.1111 / j.1471-4159.1990.tb04563.x. PMID 2384753. S2CID 29840435.
- ^ Рид Р.А., Хемперли Дж. Дж. (Октябрь 1990 г.). «Человеческий N-кадгерин: нуклеотидная и расчетная аминокислотная последовательность». Нуклеиновые кислоты Res. 18 (19): 5896. Дои:10.1093 / nar / 18.19.5896. ЧВК 332345. PMID 2216790.
- ^ «Белковая последовательность человеческого CDH2 (Uniprot ID: P19022)». Атлас кардиоорганических белков (COPaKB). Архивировано из оригинал 24 сентября 2015 г.. Получено 20 июля 2015.
- ^ Шапиро Л., Фаннон А.М., Квонг П.Д., Томпсон А., Леманн М.С., Грюбель Г., Легран Дж. Ф., Альс-Нильсен Дж., Колман Д. Р., Хендриксон В. А. (март 1995 г.). «Структурные основы межклеточной адгезии кадгеринами». Природа. 374 (6520): 327–37. Дои:10.1038 / 374327a0. PMID 7885471. S2CID 4314442.
- ^ Бакстон Р.С., Маги А.И. (июнь 1992 г.). «Структура и взаимодействие десмосомных и других кадгеринов». Семинары по клеточной биологии. 3 (3): 157–67. Дои:10.1016 / с 1043-4682 (10) 80012-1. PMID 1623205.
- ^ Takeichi M (1990). «Кадгерины: молекулярное семейство, важное в селективной межклеточной адгезии». Ежегодный обзор биохимии. 59: 237–52. Дои:10.1146 / annurev.bi.59.070190.001321. PMID 2197976.
- ^ Одзава М., Барибо Х, Кемлер Р. (июнь 1989 г.). «Цитоплазматический домен молекулы клеточной адгезии увоморулин ассоциируется с тремя независимыми белками, структурно связанными у разных видов». Журнал EMBO. 8 (6): 1711–7. Дои:10.1002 / j.1460-2075.1989.tb03563.x. ЧВК 401013. PMID 2788574.
- ^ Гарсия-Кастро М.И., Вильметтер Э., Броннер-Фрейзер М. (май 2000 г.). «N-кадгерин, молекула клеточной адгезии, участвующая в установлении эмбриональной лево-правой асимметрии». Наука. 288 (5468): 1047–51. Дои:10.1126 / science.288.5468.1047. PMID 10807574.
- ^ Angst BD, Хан Л.Ю., Северс Нью-Джерси, Уайтли К., Ротери С., Томпсон Р.П., Маги А.И., Гурди Р.Г. (январь 1997 г.). «Диссоциированное пространственное формирование паттерна щелевых контактов и стыков клеточной адгезии во время постнатальной дифференцировки желудочкового миокарда». Циркуляционные исследования. 80 (1): 88–94. Дои:10.1161 / 01.res.80.1.88. PMID 8978327.
- ^ Radice GL, Rayburn H, Matsunami H, Knudsen KA, Takeichi M, Hynes RO (январь 1997 г.). «Дефекты развития эмбрионов мышей, лишенные N-кадгерина». Биология развития. 181 (1): 64–78. Дои:10.1006 / dbio.1996.8443. PMID 9015265.
- ^ Костецкий И., Мур Р., Кемлер Р., Радис Г.Л. (июнь 2001 г.). «Дифференциальная адгезия приводит к сегрегации и исключению N-кадгерин-дефицитных клеток в химерных эмбрионах». Биология развития. 234 (1): 72–9. Дои:10.1006 / dbio.2001.0250. PMID 11356020.
- ^ Линаск К.К., Кнудсен К.А., Гуй Ю.Х. (май 1997 г.). «Взаимодействие N-кадгерин-катенин: необходимый компонент компартментализации сердечных клеток во время раннего развития сердца позвоночных». Биология развития. 185 (2): 148–64. Дои:10.1006 / dbio.1997.8570. PMID 9187080.
- ^ Онг Л.Л., Ким Н., Мима Т., Коэн-Гулд Л., Микава Т. (январь 1998 г.). «Трабекулярным миоцитам эмбрионального сердца требуется N-кадгерин для идентификации мигрирующих единиц». Биология развития. 193 (1): 1–9. Дои:10.1006 / dbio.1997.8775. PMID 9466883.
- ^ Питерс Н.С., Северс Нью-Джерси, Ротери С.М., Линкольн С., Якуб М.Х., Грин CR (август 1994 г.). «Пространственно-временная связь между щелевыми соединениями и соединениями фасций во время постнатального развития миокарда желудочков человека». Тираж. 90 (2): 713–25. Дои:10.1161 / 01.cir.90.2.713. PMID 8044940.
- ^ Форбс М.С., Сперелакис Н. (1985). «Вставные диски сердца млекопитающих: обзор структуры и функций». Ткани и клетки. 17 (5): 605–48. Дои:10.1016/0040-8166(85)90001-1. PMID 3904080.
- ^ Vite, A; Радис, Г.Л. (июнь 2014 г.). «Комплекс N-кадгерин / катенин как главный регулятор функции интеркалированного диска». Связь и адгезия клеток. 21 (3): 169–79. Дои:10.3109/15419061.2014.908853. ЧВК 6054126. PMID 24766605.
- ^ Zuppinger C, Schaub MC, Eppenberger HM (апрель 2000 г.). «Динамика образования ранних контактов в культивируемых кардиомиоцитах взрослых крыс, изученная с помощью N-кадгерина, слитого с зеленым флуоресцентным белком». Журнал молекулярной и клеточной кардиологии. 32 (4): 539–55. Дои:10.1006 / jmcc.1999.1086. PMID 10756112.
- ^ Dou, JP; Цзяо, B; Sheng, JJ; Ю, З.Б. (25 октября 2014 г.). «[Динамическая сборка вставочного диска во время постнатального развития в миокарде крысы]». Шэн Ли сюэ бао: [Acta Physiologica Sinica]. 66 (5): 569–74. PMID 25332002.
- ^ Гончарова Е.Ю., Кам З., Гейгер Б. (январь 1992 г.). «Участие компонентов соединения адгезивов в миофибриллогенезе в культивируемых сердечных миоцитах». Разработка. 114 (1): 173–83. PMID 1576958.
- ^ Hertig CM, Eppenberger-Eberhardt M, Koch S, Eppenberger HM (январь 1996 г.). «N-кадгерин в кардиомиоцитах взрослых крыс в культуре. I. Функциональная роль N-кадгерина и нарушение межклеточного контакта усеченным мутантом N-кадгерина». Журнал клеточной науки. 109 (1): 1–10. PMID 8834785.
- ^ Феррейра-Корнуэлл М.С., Луо Ю., Нарула Н., Ленокс Дж.М., Либерман М., Радис Г.Л. (апрель 2002 г.). «Ремоделирование интеркалированного диска приводит к кардиомиопатии у мышей, неправильно экспрессирующих кадгерины в сердце». Журнал клеточной науки. 115 (Pt 8): 1623–34. PMID 11950881.
- ^ Костецкий И., Ли Дж., Сюн Й., Чжоу Р., Феррари В.А., Патель В.В., Молькентин Д.Д., Радис Г.Л. (февраль 2005 г.). «Индуцированная делеция гена N-кадгерина в сердце приводит к растворению структуры интеркалированного диска». Циркуляционные исследования. 96 (3): 346–54. Дои:10.1161 / 01.RES.0000156274.72390.2c. PMID 15662031.
- ^ Cheng, L; Юнг, А; Covarrubias, M; Radice, GL (10 июня 2011 г.). «Кортактин необходим для регуляции N-кадгерином функции канала Kv1.5». Журнал биологической химии. 286 (23): 20478–89. Дои:10.1074 / jbc.m111.218560. ЧВК 3121477. PMID 21507952.
- ^ «Ген Энтреза: CDH2 кадгерин 2, тип 1, N-кадгерин (нейрональный)».
- ^ Рамис-Конде I, капеллан М.А., Андерсон А.Р., Драсдо Д. (2009). «Многомасштабное моделирование интравазации раковых клеток: роль кадгеринов в метастазировании». Phys Biol.. 6 (1): 016008. Дои:10.1088/1478-3975/6/1/016008. PMID 19321920.
- ^ Моя, PR; Додман, Нью-Хэмпшир; Timpano, KR; Рубинштейн, Л. М.; Рана, Z; Жареный, RL; Райхардт, LF; Heiman, GA; Tischfield, JA; Кинг, РА; Галджичка, М; Ginns, EI; Вендланд-младший (август 2013 г.). «Редкие варианты миссенс-гена кадгерина нейронов (CDH2) при определенных фенотипах обсессивно-компульсивного расстройства и расстройства Туретта». Европейский журнал генетики человека. 21 (8): 850–4. Дои:10.1038 / ejhg.2012.245. ЧВК 3722668. PMID 23321619.
- ^ Ципис, А; Athanassiadou, AM; Athanassiadou, P; Каванцас, Н; Agrogiannis, G; Пацурис, Э (15 сентября 2010 г.). «Связанные с апоптозом факторы p53, bcl-2 и дефекты передачи силы при дилатационной кардиомиопатии». Патология, исследования и практика. 206 (9): 625–30. Дои:10.1016 / j.prp.2010.05.007. PMID 20591580.
- ^ а б c d е Straub BK, Boda J, Kuhn C, Schnoelzer M, Korf U, Kempf T, Spring H, Hatzfeld M, Franke WW (декабрь 2003 г.). «Новая система межклеточного соединения: мозаика коры adhaerens клеток хрусталика». J. Cell Sci. 116 (Pt 24): 4985–95. Дои:10.1242 / jcs.00815. PMID 14625392.
- ^ а б c Wahl JK, Kim YJ, Cullen JM, Johnson KR, Wheelock MJ (май 2003 г.). «Комплексы N-кадгерин-катенин образуются до расщепления прорегиона и транспорта на плазматическую мембрану». J. Biol. Chem. 278 (19): 17269–76. Дои:10.1074 / jbc.M211452200. PMID 12604612.
- ^ Идзава I, Нисидзава М., Отакара К., Инагаки М. (февраль 2002 г.). «Денсин-180 взаимодействует с белком, связанным с дельта-катенином / нейральным плакофилином, повторяющимся белком броненосца в синапсах». J. Biol. Chem. 277 (7): 5345–50. Дои:10.1074 / jbc.M110052200. PMID 11729199.
- ^ Брэди-Калнай С.М., Римм Д.Л., Тонкс Н.К. (1995). «Рецепторный белок тирозинфосфатазы PTPmu ассоциирует с кадгеринами и катенинами in vivo». J. Cell Biol. 130 (4): 977–86. Дои:10.1083 / jcb.130.4.977. ЧВК 2199947. PMID 7642713.
- ^ Брэди-Калнай С.М., Мортон Т., Никсон Дж.П., Пиц Г.Е., Кинч М., Чен Х., Бракенбери Р., Римм Д.Л., Дель Веккио Р.Л., Тонкс Н.К. (1998). «Динамическое взаимодействие PTPmu с множеством кадгеринов in vivo». J. Cell Biol. 141 (1): 287–96. Дои:10.1083 / jcb.141.1.287. ЧВК 2132733. PMID 9531566.
- ^ Беско Дж. А., Хофт ван Хейсдуйнен Р., Фростхольм А., Роттер А. (октябрь 2006 г.). «Внутриклеточные субстраты мозга, обогащенные рецептором протеина тирозинфосфатазы rho (RPTPrho / PTPRT)». Brain Res. 1116 (1): 50–7. Дои:10.1016 / j.brainres.2006.07.122. PMID 16973135. S2CID 23343123.
- ^ Sacco PA, McGranahan TM, Wheelock MJ, Johnson KR (август 1995 г.). «Идентификация доменов плакоглобина, необходимых для ассоциации с N-кадгерином и альфа-катенином». J. Biol. Chem. 270 (34): 20201–6. Дои:10.1074 / jbc.270.34.20201. PMID 7650039.
- ^ Sinn HW, Balsamo J, Lilien J, Lin JJ (сентябрь 2002 г.). «Локализация нового белка Xin в комплексе адгезивных соединений в сердечной и скелетной мышцах во время развития». Динамика развития. 225 (1): 1–13. Дои:10.1002 / dvdy.10131. PMID 12203715. S2CID 23393425.
- ^ Schroen B, Leenders JJ, van Erk A, Bertrand AT, van Loon M, van Leeuwen RE, Kubben N, Duisters RF, Schellings MW, Janssen BJ, Debets JJ, Schwake M, Høydal MA, Heymans S, Saftig P, Pinto YM (Май 2007 г.). «Интегральный лизосомный мембранный белок 2 является новым компонентом интеркалированного диска сердца и жизненно важен для индуцированной нагрузкой гипертрофии сердечных миоцитов». Журнал экспериментальной медицины. 204 (5): 1227–35. Дои:10.1084 / jem.20070145. ЧВК 2118572. PMID 17485520.
дальнейшее чтение
- Доэрти П., Смит П., Уолш Ф. С. (1997). «Общие домены гомологии молекулы клеточной адгезии (CAM) указывают на передачу сигналов CAM через рецепторы FGF». Перспективы нейробиологии развития. 4 (2–3): 157–68. PMID 9168198.
- Макригианнакис A, Coukos G, Blaschuk O, Coutifaris C (2000). «Фолликулярная атрезия и лютеолиз. Доказательства роли N-кадгерина». Анна. Акад. Наука. 900: 46–55. Дои:10.1111 / j.1749-6632.2000.tb06215.x. PMID 10818391. S2CID 30583247.
- Хазан РБ, Цяо Р., Керен Р., Бадано И., Суяма К. (2004). «Кадгериновый переключатель в прогрессии опухоли». Анна. Акад. Наука. 1014: 155–63. Дои:10.1196 / летопись.1294.016. PMID 15153430. S2CID 37486403.
- Кавалларо У (2005). «N-кадгерин как промотор инвазии: новая мишень для противоопухолевой терапии?». Текущее мнение об исследуемых лекарствах. 5 (12): 1274–8. PMID 15648948.
- Саломон Д., Аялон О., Патель-Кинг Р., Хайнс Р.О., Гейгер Б. (1992). «Внефункциональное распределение N-кадгерина в культивируемых эндотелиальных клетках человека». J. Cell Sci. 102 (1): 7–17. PMID 1500442.
- Кнудсен К.А., Уилок М.Дж. (1992). «Плакоглобин или гомолог массой 83 кДа, отличный от бета-катенина, взаимодействует с E-кадгерином и N-кадгерином». J. Cell Biol. 118 (3): 671–9. Дои:10.1083 / jcb.118.3.671. ЧВК 2289540. PMID 1639850.
- Рид Р. А., Хемперли Дж. Дж. (1990). «Человеческий N-кадгерин: нуклеотидная и расчетная аминокислотная последовательность». Нуклеиновые кислоты Res. 18 (19): 5896. Дои:10.1093 / nar / 18.19.5896. ЧВК 332345. PMID 2216790.
- Уолш Ф.С., Бартон С.Х., Путт В., Мур С.Е., Келселл Д., Сперр Н., Гудфеллоу П.Н. (1990). «Ген N-кадгерина отображается на хромосоме 18 человека и не связан с геном E-кадгерина». J. Neurochem. 55 (3): 805–12. Дои:10.1111 / j.1471-4159.1990.tb04563.x. PMID 2384753. S2CID 29840435.
- Селиг С., Бруно С., Шарф Дж.М., Ван С.Х., Витале Э, Гиллиам Т.С., Кункель Л.М. (1995). «Экспрессированные псевдогены кадгерина локализованы в критической области гена спинальной мышечной атрофии». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 92 (9): 3702–6. Дои:10.1073 / пнас.92.9.3702. ЧВК 42029. PMID 7731968.
- Уоллис Дж, Фокс М.Ф., Уолш Ф.С. (1994). «Структура гена N-кадгерина человека: анализ YAC и точное картирование хромосом на 18q11.2». Геномика. 22 (1): 172–9. Дои:10.1006 / geno.1994.1358. PMID 7959764.
- Андерссон AM, Эдвардсен K, Skakkebaek NE (1995). «Экспрессия и локализация N- и E-кадгерина в яичках и придатках яичка человека». Int. Дж. Андрол. 17 (4): 174–80. Дои:10.1111 / j.1365-2605.1994.tb01239.x. PMID 7995652.
- Мацуёси Н., Имамура С. (1997). «Множественные кадгерины экспрессируются в человеческих фибробластах». Biochem. Биофиз. Res. Сообщество. 235 (2): 355–8. Дои:10.1006 / bbrc.1997.6707. PMID 9199196.
- Наварро П., Руко Л., Дежана Е. (1998). «Дифференциальная локализация VE- и N-кадгеринов в эндотелиальных клетках человека: VE-кадгерин конкурирует с N-кадгерином за локализацию в соединении». J. Cell Biol. 140 (6): 1475–84. Дои:10.1083 / jcb.140.6.1475. ЧВК 2132661. PMID 9508779.
- Гайдар Ю.А., Лепехин Е.А., Шейчетова Г.А., Витт М. (1998). «Распределение N-кадгерина и NCAM в нейронах и эндокринных клетках эмбриональной и фетальной гастроэнтеропанкреатической системы». Acta Histochem. 100 (1): 83–97. Дои:10.1016 / s0065-1281 (98) 80008-1. PMID 9542583.
- Креммидиотис Дж., Бейкер Э., Кроуфорд Дж., Эйр Х. Дж., Нахмиас Дж., Каллен Д. Ф. (1998). «Локализация генов кадгерина человека в областях хромосом, демонстрирующих связанную с раком потерю гетерозиготности». Геномика. 49 (3): 467–71. Дои:10.1006 / geno.1998.5281. PMID 9615235.
- Лу К., Паредес М., Медина М., Чжоу Дж., Кавалло Р., Пайфер М., Ореккио Л., Косик К. С. (1999). «дельта-катенин, белок, связанный с адгезивным соединением, который способствует рассеянию клеток». J. Cell Biol. 144 (3): 519–32. Дои:10.1083 / jcb.144.3.519. ЧВК 2132907. PMID 9971746.
- Шан В.С., Танака Х., Филлипс Г.Р., Арндт К., Йошида М., Колман Д.Р., Шапиро Л. (2000). «Функциональные цис-гетеродимеры N- и R-кадгеринов». J. Cell Biol. 148 (3): 579–90. Дои:10.1083 / jcb.148.3.579. ЧВК 2174798. PMID 10662782.
- Хуси Х., Уорд М.А., Чоудхари Д.С., Блэксток В.П., Грант С.Г. (2000). «Протеомный анализ сигнальных комплексов рецептор NMDA-белок адгезии». Nat. Неврологи. 3 (7): 661–9. Дои:10.1038/76615. HDL:1842/742. PMID 10862698. S2CID 14392630.
внешняя ссылка
- CDH2 + белок, + человеческий в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- CDH2 расположение человеческого гена в Браузер генома UCSC.
- CDH2 детали человеческого гена в Браузер генома UCSC.
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.