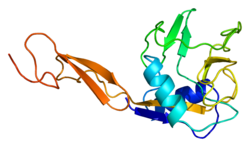E-selectin - E-selectin
E-selectin, также известный как CD62 антигеноподобный член семейства E (CD62E), молекула адгезии эндотелия-лейкоцитов 1 (ЕЛАМ-1), или молекула адгезии лейкоцитов и эндотелиальных клеток 2 (LECAM2), является селектин молекула клеточной адгезии выражено только на эндотелиальный клетки активированы цитокины. Как и другие селектины, это играет важную роль в воспаление. У человека E-селектин кодируется SELE ген.[5]
Структура
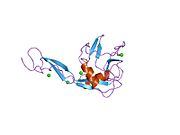
E selectin имеет кассетную структуру: N-концевой, Лектин С-типа домен, EGF (эпидермальный фактор роста) -подобный домен, 6 Суши-домен (Повтор SCR) единиц, a трансмембранный домен (TM) и внутриклеточный цитоплазматический хвост (цито). Трехмерная структура лиганд-связывающей области человеческого E-селектина была определена с разрешением 2,0 Å в 1994 году.[6] Структура показывает ограниченный контакт между двумя доменами и координацию Ca2+ не предсказывается от других лектинов С-типа. Анализ структуры / функции указывает на определенную область и определенные боковые цепи аминокислот, которые могут участвовать в связывании лиганда. E-селектин, связанный с сиалил-ЛьюисИкс (SLeИкс; NeuNAcα2,3Galβ1,4 [Fucα1,3] GlcNAc) тетрасахарид был решен в 2000 году.[7]
Ген и регуляция
У человека E-селектин кодируется SELE ген. Его лектиновый домен С-типа, EGF-подобные, SCR-повторы и трансмембранные домены каждый кодируются отдельными экзонами, тогда как цитозольный домен E-селектина происходит от двух экзонов. Локус E-selectin примыкает к L-селектин локус на хромосоме 1.[8]
Отличается от Р-селектин, который хранится в пузырьках, называемых Тела Weibel-Palade, E-селектин не сохраняется в клетке и должен транскрибироваться, транслироваться и транспортироваться на поверхность клетки. Производство E-селектина стимулируется экспрессией P-селектина, который, в свою очередь, стимулируется фактором некроза опухоли α (TNFα ), интерлейкин-1 (Ил-1 ) и липополисахарид (LPS ).[9][10] Проходит около двух часов, после цитокин распознавание для экспрессии Е-селектина на поверхности эндотелиальных клеток. Максимальная экспрессия E-селектина происходит примерно через 6–12 часов после стимуляции цитокинами, а уровни возвращаются к исходному уровню в течение 24 часов.[10]
Поперечные силы также обнаружено, что они влияют на экспрессию E-селектина. Высокий ламинарный сдвиг усиливает острую реакцию эндотелиальных клеток на интерлейкин-1β в наивных или обусловленных сдвигом эндотелиальных клетках, что может быть обнаружено в патологических условиях ишемии /реперфузионная травма одновременно обеспечивая быстрое подавление E-селектина для защиты от хронического воспаления.[11]
Фитоэстрогены, растительные соединения с эстрогеноподобной биологической активностью, такие как геништейн, формононетин, биоханин А и Daidzein, а также смесь этих фитоэстрогенов способны снижать уровень Е-селектина, а также VCAM-1 и ICAM-1 на поверхности клеток и в культуральном супернатанте.[12]
Лиганды
E-селектин распознает и связывается с сиалированными углеводами, присутствующими на поверхностных белках определенных лейкоциты. Лиганды E-селектина экспрессируются нейтрофилами, моноцитами, эозинофилами, эффекторными Т-подобными лимфоцитами памяти и естественные клетки-киллеры. Каждый из этих типов клеток обнаруживается в очагах острого и хронического воспаления в связи с экспрессией Е-селектина, таким образом вовлекая Е-селектин в рекрутирование этих клеток в такие участки воспаления.
Эти углеводы включают членов Льюис Икс и Льюис А семьи найдены на моноциты, гранулоциты, и Т-лимфоциты.[13]
Гликопротеин ESL-1, присутствующий на нейтрофилах и миелоидных клетках, был первым описанным контррецептором для E-селектина. Это вариант гликорецептора FGF тирозинкиназы, что повышает вероятность того, что его связывание с E-селектином участвует в инициации передачи сигналов в связанных клетках.
Р-селектин гликопротеиновый лиганд-1 (ПСГЛ-1 ), полученный из нейтрофилов человека, также является высокоэффективным лигандом для экспрессируемого эндотелием E-селектина в потоке.[14] Он опосредует перекатывание лейкоцитов на активированный эндотелий, окружающий воспаленную ткань.
И ESL-1, и PSGL-1 должны нести сиалил-Льюис a / x для связывания E / P-селектинов.[15]
Обнаружено, что E-селектин опосредует адгезию опухолевых клеток к эндотелиальным клеткам, связываясь с лигандами E-селектина на опухолевых клетках. Лиганды E-селектина также играют роль в метастазировании рака. Роль этих двух лигандов E-селектина в метастазировании in vivo плохо определена и еще предстоит четко продемонстрировать. PSGL-1 был обнаружен на поверхности костно-метастатических опухолевых клеток простаты, что позволяет предположить, что он может играть функциональную роль в костном тропизме опухолевых клеток простаты.[16]
В раковых клетках CD44, рецептор смерти-3 (DR3), ЛАМПА1, и ЛАМПА2 были идентифицированы как лиганды E-селектина, присутствующие на клетках рака толстой кишки.,[17] и CD44v, Mac2-BP, и ганглиозиды были идентифицированы как лиганды E-селектина, присутствующие на клетках рака груди.[18][19][20]
На нейтрофилах человека гликосфинголипид NeuAcα2-3Galβ1-4GlcNAcβ1-3 [Galβ1-4 (Fucα1-3) GlcNAcβ1-3] 2 [Galβ1-4GlcNAcβ1-3] 2Galβ1-4GlcβCer (и близкородственные структуры) являются функциональными рецепторами E-селектина.[21]
Функция
Роль в воспалении
В течение воспаление, E-селектин играет важную роль в набор лейкоцитов к месту травмы. Местный выброс цитокинов Ил-1 и TNF-α Макрофаги в воспаленной ткани индуцируют сверхэкспрессию Е-селектина на эндотелиальных клетках близлежащих кровеносных сосудов.[22] Лейкоциты в крови, экспрессирующие правильный лиганд, будут связываться с Е-селектином с низким сродством, также под воздействием сдвигового напряжения кровотока, заставляя лейкоциты «катиться» по внутренней поверхности кровеносного сосуда, поскольку временные взаимодействия происходят и нарушаются.
По мере прогрессирования воспалительной реакции хемокины высвобождаемые поврежденной тканью, попадают в кровеносные сосуды и активируют катящиеся лейкоциты, которые теперь могут плотно связываться с эндотелиальной поверхностью и начинают свой путь в ткань.[13]
Р-селектин имеет аналогичную функцию, но экспрессируется на поверхности эндотелиальных клеток в течение нескольких минут, поскольку сохраняется внутри клетки, а не производится по требованию.[13]
Роль в раке
Е-селектин был впервые обнаружен как трансмембранный рецептор, индуцируемый в эндотелиальных клетках при воспалительной стимуляции, которая опосредует адгезию моноцитарных или лейкозных клеток HL60.[23][24] Это привело к гипотезе, что раковые клетки секретируют воспалительные цитокины, такие как ИЛ-1β или же TNFα для индукции Е-селектина на расстоянии метастатический места. Эта индукция позволит циркулирующие опухолевые клетки задерживать на стимулируемых участках, катиться по активированному эндотелию, экстравазировать и формировать метастазы.[25] С тех пор исследования показали, что связывание Е-селектина с клетками рака толстой кишки коррелирует с увеличением метастатического потенциала,[26] и что раковые клетки нескольких типов опухолей связывают Е-селектин с использованием гликопротеина или гликолипидных лигандов, обычно экспрессируемых на иммунных клетках.[27][28] Исследования также описали механистический каскад, в котором раковые клетки сначала связывают E-селектин со скоростью сдвига: связывание E-селектина приводит к взаимодействию, подобному липучке, позволяя раковым клеткам взаимодействовать с более высокой аффинностью. интегрин связывание, которое в конечном итоге приводит к прочному связыванию между опухолевыми клетками и активированным эндотелием.[29][30]
Хотя многочисленные части in vitro и клинические данные продолжают поддерживать эту гипотезу метастазирования рака, опосредованного E-селектином, in vivo исследования метастаз рака показали, что нокаут E-селектина лишь минимально влияет на адгезию лейкемических клеток к кости сразу после инъекции.[31] в то время как на экспериментальные метастазы в легкие не влияет генетическая делеция E-селектина.[32][33] Кроме того, исследования также показали, что рост первичной опухоли увеличивается у мышей с нокаутом E-селектина.[34][35] Этот парадокс был недавно разрешен тремя исследованиями, показавшими, что Е-селектин только конститутивно экспрессируется в эндотелии костного мозга.[36] где считается, что он выполняет функции, жизненно важные для кроветворение.[37] которые захватываются именно метастазирующими клетками в кости, а не другими участками.[38] Эти данные подтверждают текущие клинические усилия по подавлению метастазов рака груди в кости с помощью агентов, блокирующих E-селектин.[39] Сложность биологии лиганда E-селектина также может играть роль в этих несоответствиях. in vitro и in vivo полученные результаты. По меньшей мере 15 различных гликопротеиновых и гликолипидных субстратов для E-селектина были описаны на различных раковых клетках, в то время как только n-гликан Glg1 (Esl1) опосредует метастазирование в кости.[40] Другие лиганды или их комбинации могут приводить к различным механизмам метастазирования рака.
Помимо прямого взаимодействия с опухолевыми клетками, индукция Е-селектина в ответ на цитокины, локально секретируемые раковыми клетками, позволяет специфично нацеливать на опухоль sLeX-конъюгированные наночастицы или тиоаптамеры, содержащие противоопухолевые полезные нагрузки.[41] Кроме того, E-селектин может также задействовать моноциты в первичных опухолях или метастазах в легких, способствуя развитию воспалительного проопухолевого микроокружения.[42] Блокирование этих взаимодействий или включение торговли CAR-T клетки на E-селектин-положительные сайты могут быть многообещающими для будущих терапевтических разработок.
Патологическая актуальность
Критические заболевания полиневромиопатия
В случаях повышенного уровня глюкозы в крови, например, при сепсисе, экспрессия E-селектина выше нормы, что приводит к большей проницаемости микрососудов. Большая проницаемость приводит к отек (опухоль) скелета эндотелий (облицовка кровеносных сосудов), в результате чего образуются скелетные мышцы ишемия (ограниченное кровоснабжение) и в конечном итоге некроз (смерть клетки). Эта основная патология является причиной симптоматического заболевания. критическое заболевание полинейромиопатия (CIPNM).[43] Традиционные китайские лечебные травы, такие как берберин подавлять E-селектин.[44]
Привязанность патогена
Исследование показывает приверженность Porphyromonas gingivalis к эндотелиальным клеткам пупочной вены человека увеличивается с индукцией экспрессии Е-селектина посредством TNF-α. Антитело к Е-селектину и сиалилу ЛьюисаИкс подавлен P. gingivalis соблюдение стимулированных HUVEC. P. gingivalis мутанты отсутствуют OmpA -подобные белки Pgm6 / 7 имели пониженную приверженность к стимулированным HUVEC, но фимбрии -дефицитные мутанты не пострадали. E-селецин-опосредованный P. gingivalis адгезия активирована эндотелиальным экзоцитоз. Эти результаты предполагают, что взаимодействие между Е-селектином хозяина и патогеном Pgm6 / 7 опосредует прикрепление P. gingivalis к эндотелиальным клеткам и может вызвать воспаление сосудов.[45]
Острый коронарный синдром
Иммуногистохимическое выражение E-селектина и ПЕКАМ-1 были значительно увеличены на интима в уязвимых бляшках острый коронарный синдром (ACS), особенно в неоваскулярных эндотелиальных клетках, и положительно коррелировали с плотностью воспалительных клеток, предполагая, что PECAM-1 и E-селектин могут играть важную роль в воспалительной реакции и развитии уязвимых бляшек. E-селектин Ser128Arg полиморфизм ассоциируется с ОКС, и это может быть фактором риска ОКС.[46]
Никотин-опосредованная индукция
Курение тесно связано с повышенной вероятностью атеросклероз вызывая эндотелиальную дисфункцию. Показано, что в эндотелиальных клетках различные молекулы клеточной адгезии, включая E-селектин, активируются при воздействии никотин, вызывающий привыкание компонент табачного дыма. Никотин-стимулированная адгезия моноцитов к эндотелиальным клеткам зависит от активации α7-нАХР, β-Arr1 и cSrc регулируемое увеличение E2F1 -опосредованная транскрипция гена E-селектина. Следовательно, такие агенты, как RRD-251, которые могут воздействовать на активность E2F1, могут иметь потенциальную терапевтическую пользу против атеросклероза, вызванного сигаретным дымом.[47]
Церебральная аневризма
Также обнаружено, что экспрессия E-селектина увеличивалась в разорванных церебральная аневризма ткани. Е-селектин может быть важным фактором, вовлеченным в процесс образования и разрыва церебральной аневризмы, способствуя воспалению и ослабляя стенки церебральных артерий.[48]
Как биомаркер
E-селектин также является новым биомаркер для метастатического потенциала некоторых видов рака, включая колоректальный рак и рецидивы.[49]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000007908 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000026582 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Коллинз Т., Уильямс А., Джонстон Г.И., Ким Дж., Эдди Р., Шоу-т., Джимброн, М.А., Бевилаква, член парламента (февраль 1991 г.). «Структура и хромосомное расположение гена эндотелиально-лейкоцитарной молекулы адгезии 1». Журнал биологической химии. 266 (4): 2466–73. PMID 1703529.
- ^ Грейвс Б.Дж., Кроутер Р.Л., Чандран С., Румбергер Дж.М., Ли С., Хуанг К.С., Прески Д.Х., Фамиллетти П.С., Волицки Б.А., Бернс Д.К. (февраль 1994 г.). «Понимание взаимодействия E-селектин / лиганд из кристаллической структуры и мутагенеза доменов lec / EGF». Природа. 367 (6463): 532–8. Bibcode:1994Натура.367..532Г. Дои:10.1038 / 367532a0. PMID 7509040.
- ^ Somers WS, Tang J, Shaw GD, Camphausen RT (октябрь 2000 г.). «Понимание молекулярных основ связывания и сворачивания лейкоцитов, выявленных структурами P- и E-селектина, связанными с SLe (X) и PSGL-1». Клетка. 103 (3): 467–79. Дои:10.1016 / S0092-8674 (00) 00138-0. PMID 11081633.
- ^ Каммингс Р.Д. (2008). "Селектины". В Варки А., Каммингс Р. Д., Эско Дж. Д., Фриз Х. Х., Стэнли П., Бертоцци С. Р., Харт Г. В., Эцлер М. Э. (ред.). Основы гликобиологии (2-е изд.). Плейнвью, Нью-Йорк: Лаборатория Колд-Спринг-Харбор. ISBN 978-0-87969-770-9.
- ^ Джейнвей C (2005). Иммунобиология: иммунная система в здоровье и болезни. Нью-Йорк: Наука Гарланд. ISBN 0-8153-4101-6.
- ^ а б Леувенберг JF, Смитс EF, Neefjes JJ, Shaffer MA, Cinek T, Jeunhomme TM, Ahern TJ, Buurman WA (декабрь 1992 г.). «Е-селектин и молекула-1 межклеточной адгезии высвобождаются активированными эндотелиальными клетками человека in vitro». Иммунология. 77 (4): 543–9. ЧВК 1421640. PMID 1283598.
- ^ Хуанг РБ, Эниола-Адефесо О. (2012). «Модуляция напряжения сдвига индуцированной IL-1β экспрессии Е-селектина в эндотелиальных клетках человека». PLOS One. 7 (2): e31874. Bibcode:2012PLoSO ... 731874H. Дои:10.1371 / journal.pone.0031874. ЧВК 3286450. PMID 22384091.
- ^ Андраде К.М., Саи М.Ф., Толой М.Р. (апрель 2012 г.). «Влияние фитоэстрогенов, полученных из соевых бобов, на экспрессию молекул адгезии на HUVEC». Климактерический. 15 (2): 186–94. Дои:10.3109/13697137.2011.582970. PMID 22066752.
- ^ а б c Роббинс С.Л., Котран Р.С., Кумар В., Коллинз Т. (1999). Патологическая основа болезни Роббинса. Филадельфия: У. Б. Сондерс. ISBN 0-7216-7335-X.
- ^ Зоу X, Шинде Патил В.Р., Дагия Н.М., Смит Л.А., Варго М.Дж., Интерлигги К.А., Ллойд К.М., Тис Д.Ф., Валчек Б., Лоуренс МБ, Гетц Д.Дж. (август 2005 г.). «PSGL-1, полученный из нейтрофилов человека, является высокоэффективным лигандом для экспрессируемого эндотелием E-селектина в потоке». Американский журнал физиологии. Клеточная физиология. 289 (2): C415-24. Дои:10.1152 / ajpcell.00289.2004. PMID 15814589.
- ^ Каннаги Р., Идзава М., Коике Т., Миядзаки К., Кимура Н. (май 2004 г.). «Опосредованная углеводами клеточная адгезия при метастазировании рака и ангиогенезе». Наука о раке. 95 (5): 377–84. Дои:10.1111 / j.1349-7006.2004.tb03219.x. PMID 15132763.
- ^ Димитрофф С.Дж., Дешени Л., Трухильо Н., Ким Р., Нгуен В., Хуанг В., Пиента К.Дж., Куток Д.Л., Рубин М.А. (июль 2005 г.). «Идентификация лигандов E-селектина лейкоцитов, лиганда-1 гликопротеина P-селектина и лиганда-1 E-селектина на клетках метастатической опухоли простаты человека». Исследования рака. 65 (13): 5750–60. Дои:10.1158 / 0008-5472.CAN-04-4653. ЧВК 1472661. PMID 15994950.
- ^ Подагра S, Tremblay PL, Huot J (2008). «Селектины и лиганды селектина в экстравазации раковых клеток и избирательность органов метастазирования». Клинические и экспериментальные метастазы. 25 (4): 335–44. Дои:10.1007 / s10585-007-9096-4. PMID 17891461.
- ^ Ширур В.С., Лю Т., Дельгадилло Л.Ф., Куклер С.М., Тис Д.Ф., Бененсия Ф., Гетц DJ, Бурдик М.М. (январь 2015 г.). «Варианты изоформы CD44, экспрессируемые клетками рака груди, являются функциональными лигандами E-селектина в условиях потока». Американский журнал физиологии. Клеточная физиология. 308 (1): C68-78. Дои:10.1152 / ajpcell.00094.2014. ЧВК 4281670. PMID 25339657.
- ^ Ширур В.С., Рейнольдс Н.М., Бурдик М.М. (2012). «Связывающий белок Mac-2 представляет собой новый лиганд Е-селектина, экспрессируемый клетками рака груди». PLOS One. 7 (9): e44529. Bibcode:2012PLoSO ... 744529S. Дои:10.1371 / journal.pone.0044529. ЧВК 3435295. PMID 22970241.
- ^ Ширур В.С., Хенсон К.А., Шнаар Р.Л., Нимрихтер Л., Бурдик М.М. (март 2011 г.). «Ганглиозиды, экспрессируемые на клетках рака груди, являются лигандами Е-селектина». Сообщения о биохимических и биофизических исследованиях. 406 (3): 423–9. Дои:10.1016 / j.bbrc.2011.02.061. PMID 21329670.
- ^ Нимрихтер Л., Бурдик М.М., Аоки К., Ларой В., Фиерро М.А., Хадсон С.А., фон Сеггерн К.Э., Коттер Р.Дж., Бохнер Б.С., Таймейер М., Константопулос К., Шнаар Р.Л. (ноябрь 2008 г.). «Рецепторы Е-селектина на лейкоцитах человека». Кровь. 112 (9): 3744–52. Дои:10.1182 / кровь-2008-04-149641. ЧВК 2572800. PMID 18579791.
- ^ Иммунобиология Джейнуэя, 8-е издание: «Распознавание образов клетками системы врожденного иммунитета», глава 3, стр. 83.
- ^ Bevilacqua MP, Pober JS, Mendrick DL, Cotran RS, Gimbrone MA (декабрь 1987 г.). «Идентификация индуцибельной молекулы адгезии эндотелия-лейкоцитов». Труды Национальной академии наук Соединенных Штатов Америки. 84 (24): 9238–42. Bibcode:1987PNAS ... 84.9238B. Дои:10.1073 / пнас.84.24.9238. ЧВК 299728. PMID 2827173.
- ^ Walz G, Aruffo A, Kolanus W., Bevilacqua M, Seed B (ноябрь 1990 г.). «Распознавание с помощью ELAM-1 детерминанты сиалил-Lex на миелоидных и опухолевых клетках». Наука. 250 (4984): 1132–5. Bibcode:1990Sci ... 250.1132W. Дои:10.1126 / science.1701275. PMID 1701275.
- ^ Хатиб А.М., Контогианнеа М., Фаллаволлита Л., Джемисон Б., Метериссиан С., Бродт П. (март 1999 г.). «Быстрая индукция экспрессии цитокинов и Е-селектина в печени в ответ на метастатические опухолевые клетки». Исследования рака. 59 (6): 1356–61. PMID 10096570.
- ^ Савада Р., Цубои С., Фукуда М. (январь 1994 г.). «Дифференциальная эффективность адгезии, зависящей от E-селектина, в сублинии рака толстой кишки человека, проявляющей различные метастатические потенциалы». Журнал биологической химии. 269 (2): 1425–31. PMID 7507108.
- ^ Димитрофф CJ, Lechpammer M, Long-Woodward D, Kutok JL (август 2004 г.). «Скатывание человеческих костно-метастатических опухолевых клеток простаты на эндотелий костного мозга человека под действием сдвигового потока опосредуется Е-селектином». Исследования рака. 64 (15): 5261–9. Дои:10.1158 / 0008-5472.CAN-04-0691. PMID 15289332.
- ^ Лаферриер Дж, Уль Ф, Хуот Дж (2004). «Адгезия клеток карциномы толстой кишки HT-29 к эндотелиальным клеткам требует последовательных событий с участием Е-селектина и интегрина бета4». Клинические и экспериментальные метастазы. 21 (3): 257–64. Дои:10.1023 / B: CLIN.0000037708.09420.9a. PMID 15387376.
- ^ Бартел С.Р., Хейс Д.Л., Ядзава Е.М., Опперман М., Уолли К.С., Нимрихтер Л. и др. (Январь 2013). «Определение молекулярных детерминант экстравазации костей клеток рака простаты». Исследования рака. 73 (2): 942–52. Дои:10.1158 / 0008-5472.CAN-12-3264. ЧВК 3548951. PMID 23149920.
- ^ Эспозито М., Кан И (февраль 2014 г.). «Ориентация на опухолево-стромальные взаимодействия при метастазах в кости». Фармакология и терапия. 141 (2): 222–33. Дои:10.1016 / j.pharmthera.2013.10.006. ЧВК 3947254. PMID 24140083.
- ^ Сипкинс Д.А., Вей Х, Ву Дж. У., Руннелс Дж. М., Коте Д., Средство ТЗ и др. (Июнь 2005 г.). «Визуализация in vivo специализированных эндотелиальных микродоменов костного мозга для приживления опухоли». Природа. 435 (7044): 969–73. Bibcode:2005Натура.435..969С. Дои:10.1038 / природа03703. ЧВК 2570168. PMID 15959517.
- ^ Läubli H, Borsig L (февраль 2010 г.). «Селектины как медиаторы метастазов в легкие». Микроокружение рака. 3 (1): 97–105. Дои:10.1007 / s12307-010-0043-6. ЧВК 2990482. PMID 21209777.
- ^ Эспозито М., Мондал Н., Греко ТМ, Вэй Ю., Спадацци С., Лин С.К. и др. (Май 2019). «Е-селектин в нише костных сосудов вызывает мезенхимно-эпителиальный переход и активацию Wnt в раковых клетках, способствуя метастазированию в кости». Природа клеточной биологии. 21 (5): 627–639. Дои:10.1038 / s41556-019-0309-2. ЧВК 6556210. PMID 30988423.
- ^ Эспозито М., Мондал Н., Греко ТМ, Вей Ю., Спадацци С., Лин С.К. и др. (Май 2019). «Е-селектин в нише костных сосудов вызывает мезенхимно-эпителиальный переход и активацию Wnt в раковых клетках, способствуя метастазированию в кости». Природа клеточной биологии. 21 (5): 627–639. Дои:10.1038 / s41556-019-0309-2. ЧВК 6556210. PMID 30988423.
- ^ Таверна Д., Мохер Х., Кроули Д., Борсиг Л., Варки А., Хайнс РО (январь 2004 г.). «Повышенный рост первичной опухоли у мышей, лишенных бета3- или бета3 / бета5-интегринов или селектинов». Труды Национальной академии наук Соединенных Штатов Америки. 101 (3): 763–8. Дои:10.1073 / pnas.0307289101. ЧВК 321755. PMID 14718670.
- ^ Прайс Т.Т., Бернесс М.Л., Сиван А., Уорнер М.Дж., Ченг Р., Ли Ч.и. (Май 2016). «Спящие микрометастазы рака молочной железы находятся в определенных нишах костного мозга, которые регулируют их прохождение к кости и обратно». Научная трансляционная медицина. 8 (340): 340ra73. Дои:10.1126 / scitranslmed.aad4059. PMID 27225183.
- ^ Винклер И.Г., Барбье В., Новлан Б., Якобсен Р.Н., Forristal CE, Паттон Дж. Т. и др. (Ноябрь 2012 г.). «Сосудистая ниша Е-селектин регулирует состояние покоя гемопоэтических стволовых клеток, самообновление и химиорезистентность». Природа Медицина. 18 (11): 1651–7. Дои:10,1038 / нм.2969. PMID 23086476.
- ^ Эспозито М., Мондал Н., Греко ТМ, Вэй Ю., Спадацци С., Лин С.К. и др. (Май 2019). «Е-селектин в нише костных сосудов вызывает мезенхимно-эпителиальный переход и активацию Wnt в раковых клетках, способствуя метастазированию в кости». Природа клеточной биологии. 21 (5): 627–639. Дои:10.1038 / s41556-019-0309-2. ЧВК 6556210. PMID 30988423.
- ^ «GlycoMimetics объявляет о планах начать исследование рака груди для оценки GMI-1359». www.businesswire.com. 2019-04-12. Получено 2019-06-10.
- ^ Эспозито М., Мондал Н., Греко ТМ, Вэй Ю., Спадацци С., Лин С.К. и др. (Май 2019). «Е-селектин в нише костных сосудов вызывает мезенхимно-эпителиальный переход и активацию Wnt в раковых клетках, способствуя метастазированию в кости». Природа клеточной биологии. 21 (5): 627–639. Дои:10.1038 / s41556-019-0309-2. ЧВК 6556210. PMID 30988423.
- ^ Май Дж, Хуанг И, Му Ц, Чжан Г, Сю Р, Го Х и др. (Август 2014 г.). «Терапевтические средства, нацеленные на эндотелий костного мозга при метастатическом раке молочной железы». Журнал контролируемого выпуска. 187: 22–9. Дои:10.1016 / j.jconrel.2014.04.057. ЧВК 4109393. PMID 24818768.
- ^ Любли Х., Спанаус К.С., Борсиг Л. (ноябрь 2009 г.). «Активация эндотелиальных клеток, опосредованная селектином, индуцирует экспрессию CCL5 и способствует метастазированию за счет привлечения моноцитов». Кровь. 114 (20): 4583–91. Дои:10.1182 / кровь-2008-10-186585. PMID 19779041.
- ^ Visser LH (ноябрь 2006 г.). «Критические заболевания, полинейропатия и миопатия: клиника, факторы риска и прогноз». Европейский журнал неврологии. 13 (11): 1203–12. Дои:10.1111 / j.1468-1331.2006.01498.x. PMID 17038033.
- ^ Ху И, Чен Х, Дуань Х, Ху И, Му Х (2009). «Китайские растительные лекарственные ингредиенты подавляют секрецию IL-6, IL-8, E-селектина и TXB2 в LPS-индуцированных эндотелиальных клетках микрососудов кишечника крыс». Иммунофармакология и иммунотоксикология. 31 (4): 550–5. Дои:10.3109/08923970902814129. PMID 19874221.
- ^ Komatsu T, Nagano K, Sugiura S, Hagiwara M, Tanigawa N, Abiko Y, Yoshimura F, Furuichi Y, Matsushita K (июль 2012 г.). «Е-селектин опосредует прилипание Porphyromonas gingivalis к эндотелиальным клеткам человека». Инфекция и иммунитет. 80 (7): 2570–6. Дои:10.1128 / IAI.06098-11. ЧВК 3416463. PMID 22508864.
- ^ Фанг Ф, Чжан В., Ян Л., Ван З., Лю Д. Г. (декабрь 2011 г.). «[Экспрессия PECAM-1 и E-селектина при уязвимой чуме и их связь с миокардиальным полиморфизмом Leu125Val PECAM-1 и полиморфизмом Ser128Arg E-селектина у пациентов с острым коронарным синдромом]». Чжунхуа Синь Сюэ Гуань Бин За Чжи (на китайском языке). 39 (12): 1110–6. PMID 22336504.
- ^ Аламанда В., Сингх С., Лоуренс Н.Дж., Челлаппан С.П. (февраль 2012 г.). «Никотин-опосредованная индукция E-селектина в эндотелиальных клетках аорты требует транскрипционной активности Src-киназы и E2F1». Сообщения о биохимических и биофизических исследованиях. 418 (1): 56–61. Дои:10.1016 / j.bbrc.2011.12.127. ЧВК 3273677. PMID 22240023.
- ^ Цзя В., Ван Р., Чжао Дж, Лю И.Ю., Чжан Д., Ван Х, Хань Х (ноябрь 2011 г.). «Экспрессия E-селектина увеличилась в тканях с разрывом церебральной аневризмы человека». Канадский журнал неврологических наук. 38 (6): 858–62. Дои:10,1017 / с0317167100012439. PMID 22030423.
- ^ Сато Х., Усуда Н., Курода М., Хашимото С., Марута М., Маэда К. (ноябрь 2010 г.). «Значение сывороточных концентраций E-селектина и CA19-9 в прогнозе колоректального рака». Японский журнал клинической онкологии. 40 (11): 1073–80. Дои:10.1093 / jjco / hyq095. PMID 20576794.
внешняя ссылка
- E-Selectin в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)