Йодат калия - Potassium iodate
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Йодат калия | |
| Другие имена Йодная кислота, калиевая соль | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.938 |
| Номер ЕС |
|
| Номер E | E917 (глазурь, ...) |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| КИО3 | |
| Молярная масса | 214,001 г / моль |
| Внешность | белый кристаллический порошок |
| Запах | без запаха |
| Плотность | 3,89 г / см3 |
| Температура плавления | 560 ° С (1040 ° F, 833 К) (разлагается) |
| 4,74 г / 100 мл (0 ° С) 9,16 г / 100 мл (25 ° С) 32,3 г / 100 мл (100 ° С) | |
| Растворимость | растворим в KI решение не растворим в алкоголь, жидкость аммиак, азотная кислота |
| −63.1·10−6 см3/ моль | |
| Опасности | |
| R-фразы (устарело) | R9, R22, R36, R37, R38 |
| S-фразы (устарело) | S35 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Родственные соединения | |
Другой анионы | Хлорат калия Бромат калия |
Другой катионы | Йодат натрия |
Родственные соединения | Йодистый калий Периодат калия |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
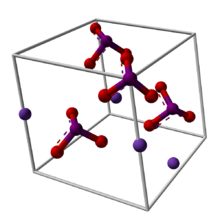
Йодат калия (KяО3 ) является ионный химическое соединение состоящий из K+ ионы и IO3− ионы в соотношении 1: 1.
Подготовка и свойства
Йодат калия - это окислитель и, как таковой, он может вызвать пожар при контакте с горючими материалами или восстановители. Его можно получить в результате реакции калийсодержащего основания, такого как гидроксид калия с йодная кислота, Например:
Его также можно приготовить, добавив йод в горячий концентрированный раствор гидроксида калия.
Или путем сплавления йодида калия с хлорат калия, бромат или же перхлорат, расплав экстрагируют водой и йодат калия выделяют из раствора кристаллизацией:[1]
- KI + KClO3 → КИО3 + KCl
Условия / вещества, которых следует избегать, включают: высокая температура, шок, трение, горючие материалы, восстановители, алюминий, органические соединения, углерод, пероксид водорода и сульфиды.
Приложения
Йодат калия иногда используется для йодирования поваренной соли, чтобы предотвратить дефицит йода. Поскольку йодид может окисляться до йода молекулярным кислородом во влажных условиях, американские компании добавляют: тиосульфаты или другой антиоксиданты к йодиду калия. В других странах йодат калия используется в качестве источника диетического йода. Он также входит в состав некоторых детское питание молоко.
Нравиться бромат калия, йодат калия иногда используется в качестве агент созревания в выпечке.
Радиационная защита
Йодат калия можно использовать для защиты от накопления радиоактивный йод в щитовидная железа путем насыщения организма стабильным источником йод до воздействия.[2] Утверждено Всемирная организация здоровья для радиационной защиты йодат калия (KIO3) является альтернативой йодид калия (KI), который имеет бедные срок годности в жарких и влажных климат.[3] В Великобритания, Сингапур, Объединенные Арабские Эмираты, а Штаты США Айдахо и Юта известны[кем? ] запасать йодат калия в планшет форма.[нужна цитата ] Правительство Ирландия также, следуя 11 сентября нападения выдал всем домохозяйствам таблетки йодата калия.[4][5] Не одобрено Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для использования в качестве блокатор щитовидной железы, и FDA приняло меры против веб-сайтов США, которые продвигают такое использование.[6][7]

| Возраст | KI в мг | КИО3 в мг |
|---|---|---|
| Старше 12 лет | 130 | 170 |
| 3 - 12 лет | 65 | 85 |
| 1 - 36 месяцев | 32 | 42 |
| <1 месяц | 16 | 21 |
Рекомендации
Эта статья нужны дополнительные цитаты для проверка. (Январь 2009 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
- ^ Прадёт Патнаик. Справочник неорганических химикатов. Макгроу-Хилл, 2002 г., ISBN 0-07-049439-8
- ^ Эстбери, Джон; Хорсли, Стивен; Гент, Ник (1999), «Оценка схемы предварительного распределения стабильного йода (йодата калия) среди гражданского населения, проживающего в зоне непосредственного противодействия объекта строительства атомной подводной лодки», Журнал общественного здравоохранения, 21 (4): 2008–10, Дои:10.1093 / pubmed / 21.4.412, PMID 11469363
- ^ Pahuja, D.N .; Rajan, M.G .; Боркарь, А.В .; Самуэль, А. (Ноябрь 2008 г.), «Йодат калия и его сравнение с йодидом калия в качестве блокатора захвата 131I щитовидной железой у крыс», Физика здоровья, 65 (5): 545–9, Дои:10.1097/00004032-199311000-00014, PMID 8225995
- ^ «Архивная копия». Архивировано из оригинал на 2013-10-17. Получено 2013-04-08.CS1 maint: заархивированная копия как заголовок (связь)
- ^ а б c «Архивная копия». Архивировано из оригинал на 2013-10-18. Получено 2013-05-22.CS1 maint: заархивированная копия как заголовок (связь)
- ^ http://www.nukepills.com/potassium-iodate-vs-potesium-iodide.html
- ^ http://www.nukepills.com/docs/Potassium%20Iodate%20warning%20letter.pdf
- ^ «Архивная копия». Архивировано из оригинал на 2013-10-17. Получено 2013-04-08.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Руководящие принципы йодной профилактики после ядерных аварий (PDF), Женева: Всемирная организация здоровья, 1999

