LIG1 - LIG1
ДНК-лигаза 1 является фермент что у людей кодируется LIG1 ген. ДНК-лигаза I является единственной известной эукариотической ДНК-лигазой, участвующей как в репликации, так и в репарации ДНК, что делает ее наиболее изученной из лигазы.
Открытие
Было известно, что репликация ДНК происходит за счет разрыва двойной цепи ДНК, но фермент, ответственный за обратное лигирование цепей, и механизм действия были неизвестны до тех пор, пока лаборатории Лемана, Геллерта, Ричардсона и Гурвица не внесли значительный вклад в исследование. открытие ДНК-лигазы в 1967 году.[5]

Набор и регулирование
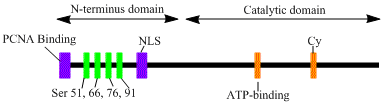
Ген LIG1 кодирует фермент 120 кДа, 919 остатки длинная, известная как ДНК-лигаза I. Полипептид ДНК-лигазы I содержит N-концевой последовательность, нацеленная на фабрику репликации (RFTS), за которой следует последовательность ядерной локализации (NLS) и три функциональных домена.[6] Три домена состоят из N-концевого ДНК-связывающий домен (DBD) и каталитический нуклеотидилтрансфераза (NTase) и C-терминал олигонуклеотид / олигосахарид связывающие (OB) домены. Хотя N-конец пептида не обладает каталитической активностью, он необходим для активности внутри клеток. N-конец белка содержит последовательность, нацеленную на фабрику репликации, которая используется для рекрутирования его в сайты репликации ДНК, известные как фабрики репликации.
Активация и рекрутирование ДНК-лигазы I, по-видимому, связаны с посттрансляционными модификациями. N-концевой домен завершается через фосфорилирование четырех серин остатки в этом домене, Ser51, Ser76 и Ser91 циклин-зависимая киназа (CDK) и Ser66 от казеинкиназа II (CKII). Было показано, что фосфорилирование этих остатков (в частности, Ser66), возможно, регулирует взаимодействие между RFTS и ядерный антиген пролиферирующих клеток (PCNA), когда лигаза I набирается на фабрики репликации во время S-фаза.[6][7] Росси и др. предположили, что когда Ser66 дефосфорилируется, RFTS лигазы I взаимодействует с PCNA, что было подтверждено in vitro Tom et al. Оба набора данных предоставляют убедительные доказательства того, что N-концевой участок лигазы I играет регулирующую роль в функционировании ферментов in vivo в ядре.[7][8] Более того, идентификация мотива связывания циклина (Cy) в каталитическом C-концевом домене, как было показано мутационным анализом, играет роль в фосфорилировании серинов 91 и 76. Вместе N-концевые серины являются субстратами CDK и CKII, которые, по-видимому, играют важную регуляторную роль в привлечении ДНК-лигазы I к фабрике репликации во время S-фазы клеточный цикл.[6][9]
Функция и механизм
LIG1 кодирует ДНК-лигазу I, которая функционирует в ДНК репликация и базовая эксцизионная пластика процесс.[10]
Эукариотическая ДНК-лигаза 1 катализирует реакцию, химически универсальную для всех лигаз. ДНК-лигаза 1 использует аденозинтрифосфат (АТФ), чтобы катализировать энергетически выгодные события лигирования в обоих Репликация ДНК и ремонт. Вовремя фаза синтеза (S-фаза) эукариотической клеточный цикл, Происходит репликация ДНК. ДНК-лигаза 1 отвечает за присоединение Фрагменты Окадзаки образуются во время прерывистого синтеза ДНК на отстающей цепи ДНК после ДНК-полимераза δ заменил нуклеотиды праймера РНК нуклеотидами ДНК. Если фрагменты Окадзаки не будут должным образом лигированы вместе, нелигированная ДНК (содержащая «ник») может легко распадаться на двойной разрыв цепи, явление, которое, как известно, вызывает генетические мутации. Чтобы связать эти фрагменты вместе, лигаза проходит через три этапа:
- Добавление аденозинмонофосфат (AMP) группа к ферменту, называемая аденилилированием,
- Перенос аденозинмонофосфата в ДНК и
- Никель-уплотнение или образование фосфодиэфирной связи.[8][11]

В течение аденилилирование, Существует нуклеофильная атака на альфа-фосфат АТФ от каталитического лизин приводя к производству неорганических пирофосфат (PPi) и ковалентно связанный промежуточный лизин-AMP в активном центре ДНК-лигазы 1.
Во время стадии переноса AMP ДНК-лигаза связывается с ДНК, определяет местонахождение разрыва и катализирует реакцию на 5’-фосфатном сайте разрыва ДНК. Анионный кислород на 5’-фосфате ника ДНК служит нуклеофилом, атакуя альфа-фосфат ковалентно связанного АМФ, заставляя АМФ быть ковалентно связанным промежуточным соединением (промежуточное соединение ДНК-АМФ).
Для образования фосфодиэфирной связи промежуточное соединение ДНК-АМФ должно быть отщеплено. Для выполнения этой задачи происходит нуклеофильная атака на 5’-фосфат со стороны расположенного выше 3’-гидроксила, что приводит к образованию фосфодиэфирной связи. Во время этой нуклеофильной атаки группа АМФ отталкивается от 5’-фосфата в качестве уходящей группы, позволяя запечатать разрыв и высвобождать АМФ, завершая один цикл лигирования ДНК.
В субоптимальных условиях лигаза может отделиться от ДНК до того, как закончится полная реакция. Было показано, что магний уровни могут замедлить процесс запечатывания зарубки, заставляя лигазу отделяться от ДНК, оставляя прерванный аденилилированный промежуточный продукт неспособным к фиксации без помощи фосфодиэстераза. Апратаксин (фосфодиэстераза), как было показано, действует на прерванные промежуточные соединения ДНК посредством гидролиза АМФ-фосфатной связи, восстанавливая ДНК в исходное состояние до того, как лигаза прореагировала.[12][13]
Роль в ремонте поврежденной базы
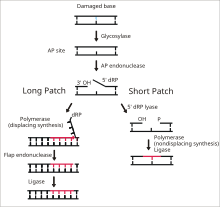
ДНК-лигаза I выполняет функцию лигирования разрывов одноцепочечной ДНК на последнем этапе базовая эксцизионная пластика (BER) путь.[14] Азотистые основания ДНК обычно повреждаются опасностями окружающей среды, такими как активные формы кислорода, токсины и ионизирующего излучения. BER - это основной путь восстановления, ответственный за удаление и замену поврежденных оснований. Лигаза I участвует в пути LP-BER, тогда как лигаза III участвует в основном пути SN-BER (2).[15] LP-BER проходит в 4 каталитических этапа. Первый ДНК гликозилаза раскалывает N-гликозидная связь, освобождая поврежденную базу и создавая AP-сайт - сайт, на котором отсутствует пурин или же пиримидин основание. На следующем этапе AP-эндонуклеаза создает «ник» на 5'-конце AP-сайта, создавая висящий дезоксирибоза фосфатный (dRP) остаток вместо AP-сайта. ДНК-полимераза затем синтезирует несколько новых оснований в направлении от 5 'до 3', создавая висячий участок ДНК с dRP на его 5 'конце. Именно на этом этапе механизмы SN-BER и LP-BER расходятся - в SNBER добавляется только один нуклеотид, а ДНК-полимераза действует как лиаза для вырезания AP-сайта. В LP-BER синтезируется несколько оснований, образуя висячий лоскут ДНК, который расщепляется эндонуклеаза лоскута. Это оставляет после себя разорванную цепь ДНК, которая воспринимается и лигируется ДНК-лигазой.[14][15][16] Действие лигазы I стимулируется другими ферментами LP-BER, особенно AP-эндонуклеазой и ДНК-полимеразой.[16]
Клиническое значение
Мутации в LIG1, которые приводят к дефициту ДНК-лигазы I, приводят к иммунодефицит и повышенная чувствительность к агентам, повреждающим ДНК.[10]
Есть только один подтвержденный случай, когда у пациента обнаруживается дефицит лигазы I, который возник в результате наследственного мутантного аллеля. Симптомы этого дефицита проявляются в задержке роста и развития и иммунодефиците. Модель мыши была создана на основе клеточных линий, полученных от пациента, что подтвердило, что мутантная лигаза вызывает ошибки репликации, приводящие к геномная нестабильность. Примечательно, что мутантные мыши также показали увеличение туморогенез.[8]
Было также обнаружено, что лигаза I активируется в пролиферирующих опухолевых клетках, в отличие от линий доброкачественных опухолевых клеток и нормальных клеток человека. Кроме того, было показано, что ингибирование экспрессии лигазы I в этих клетках может иметь цитотоксический эффект, предполагая, что ингибиторы лигазы I могут быть жизнеспособными химиотерапевтическими агентами.[17]
Недостатки в апратаксин, а фосфодиэстераза ответственный за восстановление ДНК (после того, как ДНК-лигаза I прерывает аденилилированный промежуточный продукт ДНК), был связан с нейродегенерация. Это говорит о том, что ДНК неспособна повторно войти в путь репарации без дополнительных резервных механизмов для исправления ошибок лигазы.[13]
Поскольку структура ДНК хорошо известна, а многие компоненты, необходимые для ее манипуляции, восстановления и использования, становятся идентифицированными и охарактеризованными, исследователи начинают изучать разработку наноскопических механизмов, которые будут включены в живой организм, который будет обладать способность лечить болезни, бороться с раком и выпускать лекарства на основе биологического стимула, предоставляемого организмом нанокопическому аппарату. Скорее всего, в такую машину придется встроить ДНК-лигазу.[18]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000105486 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000056394 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Кресдж Н., Симони Р.Д., Хилл Р.Л. (январь 2007 г.). "Взгляд на объединение ДНК: I. Работа Роберта Лемана по ДНК-лигазе". Журнал биологической химии. 282 (2): e1.
- ^ а б c Ferrari G, Росси R, Arosio D, Vindigni A, Biamonti G, Montecucco A (сентябрь 2003 г.). «Зависимое от клеточного цикла фосфорилирование ДНК-лигазы I человека по сайтам циклин-зависимых киназ». J. Biol. Chem. 278 (39): 37761–7. Дои:10.1074 / jbc.M304462200. PMID 12851383.
- ^ а б Росси Р., Вилла А, Негри С., Сковасси I, Чиаррокки Г., Биамонти Г., Монтекукко А. (октябрь 1999 г.). «Нацеливающая последовательность фабрики репликации / сайт связывания PCNA требуется в G (1) для контроля статуса фосфорилирования ДНК-лигазы I». EMBO J. 18 (20): 5745–54. Дои:10.1093 / emboj / 18.20.5745. ЧВК 1171641. PMID 10523317.
- ^ а б c Элленбергер Т., Томкинсон А.Е. (2008). «Эукариотические ДНК-лигазы: структурное и функциональное понимание». Анну. Преподобный Biochem. 77: 313–38. Дои:10.1146 / annurev.biochem.77.061306.123941. ЧВК 2933818. PMID 18518823.
- ^ Приджент С., Ласко Д.Д., Кодама К., Вудгетт Дж. Р., Линдал Т. (август 1992 г.). «Активация ДНК-лигазы I млекопитающих посредством фосфорилирования казеинкиназой II». EMBO J. 11 (8): 2925–33. Дои:10.1002 / j.1460-2075.1992.tb05362.x. ЧВК 556774. PMID 1639065.
- ^ а б «Ген Entrez: LIG1-лигаза I, ДНК, АТФ-зависимая».
- ^ Шрисканда В., Шуман С. (январь 1998 г.). «ДНК-лигаза вируса хлореллы: распознавание ников и мутационный анализ». Нуклеиновые кислоты Res. 26 (2): 525–31. Дои:10.1093 / nar / 26.2.525. ЧВК 147278. PMID 9421510.
- ^ Тейлор М.Р., Конрад Дж. А., Уол Д., О'Брайен П. Дж. (Июль 2011 г.). «Кинетический механизм ДНК-лигазы I человека обнаруживает магний-зависимые изменения на этапе ограничения скорости, которые ставят под угрозу эффективность лигирования». J. Biol. Chem. 286 (26): 23054–62. Дои:10.1074 / jbc.M111.248831. ЧВК 3123073. PMID 21561855.
- ^ а б Расс У, Ахель I, Западный СК (март 2007 г.). «Действия апратаксина в нескольких путях репарации ДНК». J. Biol. Chem. 282 (13): 9469–74. Дои:10.1074 / jbc.M611489200. PMID 17276982.
- ^ а б Sattler U, Frit P, Salles B, Calsou P (апрель 2003 г.). «Синтез репарации длинных участков ДНК во время эксцизионной репарации оснований в клетках млекопитающих». EMBO Rep. 4 (4): 363–7. Дои:10.1038 / sj.embor.embor796. ЧВК 1319152. PMID 12671676.
- ^ а б Хегде М.Л., Хазра Т.К., Митра С. (январь 2008 г.). «Ранние этапы пути удаления оснований ДНК / репарации однонитевых прерываний в клетках млекопитающих». Cell Res. 18 (1): 27–47. Дои:10.1038 / кр.2008.8. ЧВК 2692221. PMID 18166975.
- ^ а б Балакришнан Л., Брандт П.Д., Линдси-Больц Л.А., Санкар А., Бамбара Р.А. (май 2009 г.). «Эксцизионная репарация длинного патч-основания происходит посредством скоординированной стимуляции мультиферментного комплекса репарации ДНК». J. Biol. Chem. 284 (22): 15158–72. Дои:10.1074 / jbc.M109.000505. ЧВК 2685697. PMID 19329425.
- ^ Сан Д., Уррабаз Р., Нгуен М., Марти Дж., Стрингер С., Круз Э., Медина-Гундрам Л., Вайтман С. (декабрь 2001 г.). «Повышенная экспрессия ДНК-лигазы I при раке человека». Clin. Рак Res. 7 (12): 4143–8. PMID 11751514.
- ^ Макдональд, Джоанн. «Умная ДНК: программирование молекулы жизни для работы и развлечений [превью]». научный американский. Получено 2013-02-22.
дальнейшее чтение
- Леонхардт Х., Кардосо М.С. (1996). «Нацеливание и ассоциация белков с функциональными доменами в ядре: нерастворимый раствор». Int. Преподобный Цитол. Международный обзор цитологии. 162B: 303–35. Дои:10.1016 / S0074-7696 (08) 62620-0. ISBN 9780123645661. PMID 8557490.
- Томкинсон А.Е., Макки З.Б. (1998). «Структура и функция ДНК-лигаз млекопитающих». Мутат. Res. 407 (1): 1–9. Дои:10.1016 / s0921-8777 (97) 00050-5. PMID 9539976.
- Perrigot M, Pierrot-Deseilligny E, Bussel B, Held JP (1976). «[Паралич после радикулографии Dimer X]». La Nouvelle Presse Médicale. 5 (17): 1120–2. PMID 934827.
- Webster AD, Barnes DE, Arlett CF и др. (1992). «Задержка роста и иммунодефицит у пациента с мутациями в гене ДНК-лигазы I». Ланцет. 339 (8808): 1508–9. Дои:10.1016 / 0140-6736 (92) 91266-Б. PMID 1351188. S2CID 11874717.
- Барнс Д.Е., Томкинсон А.Е., Леманн А.Р. и др. (1992). «Мутации в гене ДНК-лигазы I человека с иммунодефицитами и клеточной гиперчувствительностью к агентам, повреждающим ДНК». Клетка. 69 (3): 495–503. Дои:10.1016 / 0092-8674 (92) 90450-Q. PMID 1581963. S2CID 11736507.
- Барнс Д.Е., Кодама К., Тайнан К. и др. (1992). «Отнесение гена, кодирующего ДНК-лигазу I, к хромосоме человека 19q13.2-13.3». Геномика. 12 (1): 164–6. Дои:10.1016 / 0888-7543 (92) 90422-О. PMID 1733856.
- Петрини Дж. Х., Хувилер К. Г., Уивер Д. Т. (1991). «Ген ДНК-лигазы I дикого типа экспрессируется в клетках синдрома Блума». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 88 (17): 7615–9. Дои:10.1073 / пнас.88.17.7615. ЧВК 52352. PMID 1881902.
- Ласко Д.Д., Томкинсон А.Е., Линдал Т. (1990). «ДНК-лигазы млекопитающих. Биосинтез и внутриклеточная локализация ДНК-лигазы I.». J. Biol. Chem. 265 (21): 12618–22. PMID 2197279.
- Barnes DE, Johnston LH, Kodama K и др. (1990). «КДНК ДНК-лигазы I человека: клонирование и функциональная экспрессия в Saccharomyces cerevisiae». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 87 (17): 6679–83. Дои:10.1073 / pnas.87.17.6679. ЧВК 54600. PMID 2204063.
- Монтекукко А., Савини Э., Вейгардт Ф. и др. (1996). «N-концевой домен ДНК-лигазы I человека содержит сигнал ядерной локализации и направляет фермент к сайтам репликации ДНК». EMBO J. 14 (21): 5379–86. Дои:10.1002 / j.1460-2075.1995.tb00222.x. ЧВК 394647. PMID 7489727.
- Маруяма К., Сугано С. (1994). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Траск Б., Фертитта А., Кристенсен М. и др. (1993). «Флуоресцентное гибридизационное картирование хромосомы 19 человека: расположение цитогенетических полос 540 космид и 70 генов или ДНК-маркеров». Геномика. 15 (1): 133–45. Дои:10.1006 / geno.1993.1021. PMID 8432525.
- Петрини Дж. Х., Уолш М. Е., ДиМаре С. и др. (1996). «Выделение и характеристика человеческого гомолога MRE11». Геномика. 29 (1): 80–6. Дои:10.1006 / geno.1995.1217. PMID 8530104.
- Бентли Д., Селфридж Дж., Миллар Дж. К. и др. (1996). «ДНК-лигаза I необходима для эритропоэза печени плода, но не важна для жизнеспособности клеток млекопитающих». Nat. Genet. 13 (4): 489–91. Дои:10.1038 / ng0896-489. PMID 8696349. S2CID 20264173.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К. и др. (1997). «Конструирование и характеристика полноразмерной библиотеки кДНК с обогащением по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
- Росси Р., Вилла А, Негри С. и др. (1999). «Нацеливающая последовательность фабрики репликации / сайт связывания PCNA требуется в G (1) для контроля статуса фосфорилирования ДНК-лигазы I.» EMBO J. 18 (20): 5745–54. Дои:10.1093 / emboj / 18.20.5745. ЧВК 1171641. PMID 10523317.
- Мацумото Ю., Ким К., Гурвиц Дж. И др. (1999). «Восстановление ядерной антиген-зависимой репарации апуриновых / апиримидиновых участков пролиферирующих клеток очищенными белками человека». J. Biol. Chem. 274 (47): 33703–8. Дои:10.1074 / jbc.274.47.33703. PMID 10559261.
- Vispé S, Satoh MS (2000). «Образование двухцепочечных разрывов ДНК, опосредованное патчем репарации ДНК в клетках человека». J. Biol. Chem. 275 (35): 27386–92. Дои:10.1074 / jbc.M003126200. PMID 10827190.







