Белок распознавания пептидогликана 1 - Peptidoglycan recognition protein 1

Белок распознавания пептидогликана 1, PGLYRP1, также известный как TAG7, является антибактериальным и провоспалительный врожденный иммунитет белок что у людей кодируется PGLYRP1 ген.[5][6][7][8]
Открытие
PGLYRP1 был открыт независимо двумя лабораториями в 1998 году.[5][7] Хокан Штайнер и его коллеги с помощью дифференциального дисплея идентифицировали и клонировали Белок распознавания пептидогликанов (ПГРП) в моли (Trichoplusia ni ) и на основе этой последовательности открыли и клонировали ортологи PGRP мыши и человека.[5] Сергей Киселев и его коллеги обнаружили и клонировали белок мыши аденокарцинома с той же последовательностью, что и PGRP мыши, которую они назвали Tag7.[7] Человеческий PGRP был одним из основателей семейства из четырех генов PGRP, обнаруженных у людей, которые были названы PGRP-S, PGRP-L, PGRP-Iα и PGRP-Iβ (для коротких, длинных и промежуточных транскриптов, по аналогии с насекомыми PGRP).[9] Их генные символы впоследствии были изменены на PGLYRP1 (белок распознавания пептидогликана 1), PGLYRP2 (белок распознавания пептидогликана 2 ), PGLYRP3 (белок распознавания пептидогликана 3 ), и PGLYRP4 (белок распознавания пептидогликана 4 ), соответственно, Комитетом по номенклатуре генов Организации генома человека, и эта номенклатура в настоящее время также используется для других млекопитающее PGRP. В 2005 году Рой Мариуцца и его коллеги кристаллизовали человеческий PGLYRP1 и решили его структуру.[10]
Распределение тканей и секреция
PGLYRP1 имеет самый высокий уровень экспрессии среди всех PGRP млекопитающих. PGLYRP1 высоко конститутивно экспрессируется в Костный мозг[5][9][11] и в третичных гранулах полиморфноядерные лейкоциты (нейтрофилы и эозинофилы ),[11][12][13][14][15][16] и в меньшей степени в активированных макрофаги[15][16] и плода печень.[9] PGLYRP1 также экспрессируется в период лактации. молочная железа,[17] и на гораздо более низкий уровень в эпителий роговицы в глаз,[18] в воспаленный кожа,[19][20] селезенка,[5] вилочковая железа,[5] И в эпителиальные клетки в респираторный[15][16] и кишечный трактаты.[5][21] PGLYRP1 явно экспрессируется в кишечнике. Патчи Пейера в микроскладывание (M) клетки[22][23] а также является одним из маркеров дифференциации Т помощник 17 (Th17) клетки в T нормативный (Treg) клетки мышей.[24] PGLYRP1 мыши экспрессируется в развивающихся мозг и на это выражение влияет кишечная микробиом.[25] Экспрессия PGLYRP1 в головном мозге крысы индуцируется недосыпанием.[26] и в мозгу мыши ишемия.[27]
PGLYRP1 человека также обнаруживается в сыворотке после высвобождения из лейкоциты гранулы экзоцитоз.[28][29] PGLYRP1 присутствует в верблюжьем молоке в количестве 120 мкг / мл.[17] и в гранулах полиморфноядерных лейкоцитов - 2,9 мг / 109 клетки.[11]
Структура
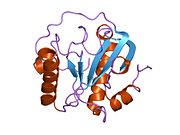
Как и большинство PGRP, PGLYRP1 имеет один карбокси-конец. пептидогликан-связывающий домен амидазы 2 типа (также известный как домен PGRP), который, однако, не имеет амидаза ферментативная активность.[30] Этот домен PGRP состоит из трех альфа-спиралей, пяти бета-цепей и спиралей и N-концевого сегмента (остатки 1–30, специфичный для PGRP сегмент), структура которого существенно варьирует среди PGRP.[10] PGLYRP1 имеет три пары консервативных цистеины, которые образуют три дисульфид связи в положениях 9 и 133, 25 и 70 и 46 и 52 в PGLYRP1 человека.[10] Дисульфид Cys46 – Cys52 широко консервативен в беспозвоночный и позвоночное животное PRGPs, дисульфид Cys9-Cys133 консервативен во всех PGRPs млекопитающих, а дисульфид Cys25-Cys70 является уникальным для PGLYRP1, PGLYRP3 и PGLYRP4 млекопитающих, но не обнаруживается в амидазно-активном PGLYRP2.[9][10] PGLYRP1 человека имеет пептидогликан-связывающую щель длиной 25 Å, стенки которой образованы двумя α-спиралями, а дно - β-слоем.[10]
PGLYRP1 человека секретируется и образует гомодимеры с дисульфидной связью.[29][31] Структура димера с дисульфидной связью неизвестна, поскольку кристаллическая структура только мономерного PGLYRP1 человека была решена, поскольку в кристаллизованном белке отсутствовали 8 N-концевых аминокислот, включая Cys8,[10] который, вероятно, участвует в образовании димера с дисульфидной связью. PGLYRP1 крысы также может образовывать димеры с дисульфидной связью, поскольку он содержит Cys в том же положении, что и Cys8 в PGLYRP1 человека,[26] тогда как мышь[5] и бычий[11] PGLYRP1 не содержат этого Cys и, вероятно, не образуют димеров с дисульфидной связью.
PGLYRP1 верблюда может образовывать два недисульфидно-связанных димера: первый с пептидогликан-связывающими сайтами двух участвующих молекул, полностью открытыми на противоположных концах димера, а второй с пептидогликан-связывающими сайтами, скрытыми на границе раздела, и открытыми противоположными сторонами. на концах димера.[32] Такое расположение уникально для верблюда PGLYRP1.[32]
PGLYRP1 - это гликозилированный и гликозилирование необходимо для его бактерицидной активности.[31][33]
Функции
Белок PGLYRP1 играет важную роль во врожденном иммунном ответе.
Связывание пептидогликанов
PGLYRP1 связывает пептидогликан, полимер β (1-4) -связанного N-ацетилглюкозамин (GlcNAc) и N-ацетилмурамовая кислота (MurNAc) сшит короткими пептиды, основной компонент бактериальный клеточная стенка.[5][9][12][14][34][35] PGLYRP1 человека связывает GlcNAc-MurNAc-трипептид с высокой аффинностью (Kd = 5.5 x 10−8 M)[14] и MurNAc-трипептид, MurNAc-тетрапептид и MurNAc-пентапептид с Kd = 0,9-3,3 × 10−7 M[35] с предпочтением мезо-диаминопимелиновая кислота (м-DAP) над L-лизин -содержащие фрагменты пептидогликана.[35] м-DAP присутствует в третьей позиции пептидогликанового пептида в Грамотрицательные бактерии и Грамположительный bacilli, тогда как L-лизин находится в этом положении в пептидогликановом пептиде в грамположительных кокках. Фрагменты пептидогликана меньшего размера не связываются или связываются с гораздо более низким сродством.[14][35]
PGLYRP1 верблюда связывает MurNAc-дипептид с низким сродством (Kd = 10−7 M)[36] а также связывает бактериальные липополисахарид с Kd = 1,6 x 10−9 М и липотейхоевая кислота с Kd = 2,4 x 10−8 M на сайтах связывания за пределами канонической пептидогликан-связывающей щели с лигандами и тетрамером PGLYRP1.[37] Такие тетрамеры уникальны для PGLYRP1 верблюда и не обнаруживаются в PGLYRP1 человека из-за стеариновых препятствий.[37]
Бактерицидная активность
PGLYRP1 человека обладает прямым бактерицидным действием как в отношении грамположительных (Bacillus subtilis, Bacillus licheniformis, Lactobacillus acidophilus, Золотистый стафилококк, Streptococcus pyogenes ) и грамотрицательные (кишечная палочка, Proteus vulgaris, Salmonella enterica, Shigella sonnei, Синегнойная палочка ) бактерии[12][14][31][33][38] а также активен против Хламидия трахоматис.[39] Мышь[12][13] и бычий[11][28] PGLYRP1 обладают антибактериальной активностью против Bacillus megaterium, Гемолитический стафилококк, S. aureus, Кишечная палочка, и S. enterica, а бычий PGLYRP1 также обладает противогрибковой активностью против Криптококк neoformans.[11]
У грамположительных бактерий человеческий PGLYRP1 связывается с участками разделения вновь образованных дочерних клеток, созданными бактериальными пептидогликанолитическими эндопептидазами, LytE и LytF в Б. subtilis, которые отделяют дочерние клетки после деления клеток.[38] Эти разделяющие клетки эндопептидазы, вероятно, экспонируют PGLYRP1-связывающие мурамиловые пептиды, как показано совместной локализацией PGLYRP1 и LytE и LytF в сайтах разделения клеток, а также отсутствием связывания PGLYRP1 с другими участками клеточной стенки с сильно сшитым пептидогликаном. .[38] Эта локализация необходима для уничтожения бактерий, потому что мутанты которые лишены LytE и LytF эндопептидаз и не разделяются после деления клеток, не связываются с PGLYRP1 и также нелегко уничтожаются PGLYRP1.[38] У грамотрицательных бактерий (Кишечная палочка) PGLYRP1 связывается с внешней мембраной.[38] Как у грамположительных, так и у грамотрицательных бактерий PGLYRP1 остается связанным с клеточной оболочкой и не проникает в цитоплазма.[38]
Механизм уничтожения PGLYRP1 основан на индукции летального стресса оболочки и продукции активные формы кислорода в бактериях и последующем отключении транскрипция и перевод.[38] PGLYRP1-индуцированное уничтожение бактерий не связано с проницаемостью клеточной мембраны, что типично для дефенсины и другие антимикробные пептиды, гидролиз клеточной стенки или осмотический шок.[31][33][38]
PGLYRP1 человека обладает синергическим бактерицидным действием с лизоцим[14] и антибактериальные пептиды.[33] Стрептококки производят белок (SP1), который ингибирует антибактериальную активность человеческого PGLYRP1.[40]
Защита от инфекций
PGLYRP1 играет ограниченную роль в защите хозяина от инфекций. PGLYRP1-дефицитные мыши более чувствительны к системным инфекциям, вызываемым непатогенными бактериями (Micrococcus luteus и Б. subtilis)[13] и чтобы P. aeruginosa-индуцированный кератит,[18] но не к системным инфекциям патогенными бактериями (S. aureus и Кишечная палочка).[13] Внутривенное введение PGLYRP1 защищает мышей от системного Listeria monocytogenes инфекционное заболевание.[41]
Поддержание микробиома
PGLYRP1 мыши играет роль в поддержании здорового микробиома, так как PGLYRP1-дефицитные мыши имеют значительные изменения в составе микробиомов кишечника и легких, что влияет на их чувствительность к колит и воспаление легких.[21][42][43]
Воздействие на воспаление
PGLYRP1 мыши играет роль в поддержании противовоспалительного и провоспалительного гомеостаза в кишечнике, коже, легких, суставах, глазах и мозге. PGLYRP1-дефицитные мыши более чувствительны, чем мыши дикого типа, к колиту, вызванному декстрансульфатом натрия (DSS), что указывает на то, что PGLYRP1 защищает мышей от колита, индуцированного DSS.[21][42] Однако в модели мыши артрит PGLYRP1-дефицитные мыши развивают более тяжелый артрит, чем мыши дикого типа.[44] Кроме того, мыши с дефицитом обоих PGLYRP1 и PGLYRP2 развить более тяжелый артрит, чем PGLYRP2-дефицитные мыши, устойчивые к артриту.[44] Эти результаты показывают, что PGLYRP2 способствует развитию артрита и что PGLYRP1 противодействует провоспалительному эффекту PGLYRP2.[44] PGLYRP1-дефицитные мыши также нарушили роговица заживление ран по сравнению с мышами дикого типа, что указывает на то, что PGLYRP1 способствует заживлению ран роговицы.[18]
PGLYRP1-дефицитные мыши более устойчивы, чем мыши дикого типа, к экспериментально индуцированному аллергический астма,[15][16] атопический дерматит,[20] контактный дерматит,[20] и псориаз -подобное кожное воспаление.[19] Эти результаты показывают, что мышиный PGLYRP1 способствует воспалению легких и кожи. Эти провоспалительные эффекты обусловлены увеличением количества и активности Т-хелперных 17 (Th17) клеток и уменьшением количества Т-регуляторных (Treg) клеток.[15][19][20] а в случае астмы также увеличилось количество Т-хелперных клеток 2 (Th2) и уменьшилось количество плазмацитоидные дендритные клетки.[15] Провоспалительный эффект PGLYRP1 при астме зависит от регулируемого PGLYRP1 кишечного микробиома, поскольку повышенная устойчивость к экспериментально индуцированной аллергической астме может передаваться дикому типу. без микробов мышей путем трансплантации микробиома из PGLYRP1-дефицитные мыши.[43]
Цитотоксичность
Сообщается, что мышь PGLYRP1 (Tag7) цитотоксический для опухолевых клеток и функционировать как Фактор некроза опухоли-α (TNF-α) -подобный цитокин.[7] Последующие эксперименты показали, что PGLYRP1 (Tag7) сам по себе не обладает цитотоксической активностью,[12][45] но PGLYRP1 (Tag7) образует комплекс с белком теплового шока 70 (Hsp70 ) и что только эти комплексы цитотоксичны для опухолевых клеток,[45] тогда как PGLYRP1 (Tag7) сам по себе действует как антагонист цитотоксичности комплексов PGLYRP1-Hsp70.[46]
Взаимодействие с белками и рецепторами хозяина
PGLYRP1 (Tag7) человека и мыши связывают белок теплового шока 70 (Hsp70 ) в растворе и комплексы PGLYRP1-Hsp70 также секретируются цитотоксическими лимфоцитами, и эти комплексы цитотоксичны для опухолевых клеток.[45][47] Этой цитотоксичности противодействуют метастазины (S100A4 )[48] и связывающий тепловой шок белок HspBP1.[49] Комплексы PGLYRP1-Hsp70 связываются с TNFR1 (рецептор фактора некроза опухоли-1, который является рецептором смерти) и вызывают цитотоксический эффект через апоптоз и некроптоз.[46] Эта цитотоксичность связана с повышением проницаемости лизосомы и митохондрии.[50] Напротив, свободный PGLYRP1 действует как антагонист TNFR1, связываясь с TNFR1 и ингибируя его активацию комплексами PGLYRP1-Hsp70.[46] Пептид PGLYRP1 человека (аминокислоты 163–175) также подавляет цитотоксические эффекты комплексов TNF-α и PGLYRP1-Hsp70.[51]
PGLYRP1 человека в комплексе с пептидогликаном или мультимеризованный связывается и стимулирует TREM-1 (запускающий рецептор, экспрессируемый на миелоидных клетках-1), рецептор, присутствующий на нейтрофилах, моноциты и макрофаги, которые индуцируют выработку провоспалительных цитокинов.[52]
Медицинское значение
Генетический PGLYRP1 варианты или измененная экспрессия PGLYRP1 часто связаны с различными заболеваниями. Пациенты с воспалительное заболевание кишечника (IBD), который включает Болезнь Крона и язвенный колит, имеют значительно более частые варианты миссенс в PGLYRP1 ген (а также в трех других PGLYRP гены), чем у здоровых людей.[53] Эти результаты предполагают, что PGLYRP1 защищает людей от этих воспалительных заболеваний и что мутации в PGLYRP1 ген являются одними из генетических факторов, предрасполагающих к этим заболеваниям. PGLYRP1 варианты также связаны с увеличением гемоглобин плода в серповидноклеточная анемия.[54]
Несколько заболеваний связаны с повышенной экспрессией PGLYRP1, в том числе: атеросклероз,[55][56] инфаркт миокарда,[57] сепсис,[58] воспаленные ткани при болезни Крона и язвенном колите,[59] легочный фиброз,[60] астма[61] хроническая болезнь почек,[62] ревматоидный артрит,[63] воспаление десен,[64][65][66][67][68] остеоартроз,[69] сердечно-сосудистые события и смерть в трансплантацияпочки пациенты,[70] алопеция,[71] сердечная недостаточность,[72] диабет I типа,[73] инфекционные осложнения в гемодиализ,[74] и тромбоз,[75] соответствует провоспалительным эффектам PGLYRP1. Более низкая экспрессия PGLYRP1 была обнаружена в эндометриоз.[76]
Смотрите также
- Белок распознавания пептидогликана
- Белок распознавания пептидогликана 2
- Белок распознавания пептидогликана 3
- Белок распознавания пептидогликана 4
- Пептидогликан
- Врожденная иммунная система
- Стенки бактериальных клеток
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000008438 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000030413 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d е ж грамм час я Канг Д., Лю Дж., Лундстрём А., Гелиус Е., Штайнер Х. (август 1998 г.). «Белок распознавания пептидогликана в врожденном иммунитете, сохраненный от насекомых к человеку». Труды Национальной академии наук Соединенных Штатов Америки. 95 (17): 10078–82. Bibcode:1998PNAS ... 9510078K. Дои:10.1073 / пнас.95.17.10078. ЧВК 21464. PMID 9707603.
- ^ «Ген Entrez: белок 1 распознавания пептидогликана PGLYRP1».
- ^ а б c d Киселев С.Л., Кустикова О.С., Коробко Е.В., Прохорчук Е.Б., Кабышев А.А., Луканидин Е.М., Георгиев Г.П. (июль 1998 г.). «Молекулярное клонирование и характеристика гена tag7 мыши, кодирующего новый цитокин». Журнал биологической химии. 273 (29): 18633–9. Дои:10.1074 / jbc.273.29.18633. PMID 9660837. S2CID 11417742.
- ^ «Белок распознавания пептидогликана Pglyrp1 1 [Mus musculus (домовая мышь)] - Ген - NCBI». www.ncbi.nlm.nih.gov. Получено 2020-11-03.
- ^ а б c d е Лю Ц., Сюй З., Гупта Д., Дзиарски Р. (сентябрь 2001 г.). «Белки распознавания пептидогликанов: новое семейство из четырех молекул распознавания паттернов врожденного иммунитета человека». Журнал биологической химии. 276 (37): 34686–94. Дои:10.1074 / jbc.M105566200. PMID 11461926. S2CID 44619852.
- ^ а б c d е ж Гуан Р., Ван К., Сундберг Э. Дж., Мариуцца Р. А. (апрель 2005 г.). «Кристаллическая структура человеческого белка распознавания пептидогликана S (PGRP-S) при разрешении 1,70 A». Журнал молекулярной биологии. 347 (4): 683–91. Дои:10.1016 / j.jmb.2005.01.070. PMID 15769462.
- ^ а б c d е ж Тайделл С.К., Йонт Н., Тран Д., Юань Дж., Селстед, штат Мэн (май 2002 г.). «Выделение, характеристика и противомикробные свойства бычьего олигосахарид-связывающего белка. Микробицидный гранулярный белок эозинофилов и нейтрофилов». Журнал биологической химии. 277 (22): 19658–64. Дои:10.1074 / jbc.M200659200. PMID 11880375. S2CID 904536.
- ^ а б c d е Лю Ч., Гелиус Э., Лю Г, Штайнер Х., Дзиарски Р. (август 2000 г.). «Белок распознавания пептидогликана млекопитающих связывает пептидогликан с высоким сродством, экспрессируется в нейтрофилах и подавляет рост бактерий». Журнал биологической химии. 275 (32): 24490–9. Дои:10.1074 / jbc.M001239200. PMID 10827080. S2CID 24226481.
- ^ а б c d Дзиарски Р., Платт К.А., Гелиус Э., Штайнер Х., Гупта Д. (июль 2003 г.). «Нарушение уничтожения нейтрофилов и повышенная восприимчивость к инфекции непатогенными грамположительными бактериями у мышей с дефицитом белка S (PGRP-S) распознавания пептидогликана». Кровь. 102 (2): 689–97. Дои:10.1182 / кровь-2002-12-3853. PMID 12649138.
- ^ а б c d е ж Чо Дж. Х., Фрейзер И. П., Фукасе К., Кусумото С., Фудзимото Ю., Шталь Г. Л., Эзековиц Р. А. (октябрь 2005 г.). «Белок распознавания человеческого пептидогликана S является эффектором опосредованного нейтрофилами врожденного иммунитета». Кровь. 106 (7): 2551–8. Дои:10.1182 / кровь-2005-02-0530. ЧВК 1895263. PMID 15956276.
- ^ а б c d е ж Пак С.Ю., Цзин X, Гупта Д., Дзиарски Р. (апрель 2013 г.). «Белок распознавания пептидогликана 1 усиливает экспериментальную астму, стимулируя Th2 и Th17 и ограничивая ответы регуляторных Т-клеток и плазмоцитоидных дендритных клеток». Журнал иммунологии. 190 (7): 3480–92. Дои:10.4049 / jimmunol.1202675. ЧВК 3608703. PMID 23420883.
- ^ а б c d Яо Х, Гао М., Дай С., Мейер К.С., Чен Дж., Киран К.Дж. и др. (Декабрь 2013). «Белок распознавания пептидогликана 1 способствует воспалению дыхательных путей у мышей, вызванному клещами домашней пыли». Американский журнал респираторной клетки и молекулярной биологии. 49 (6): 902–11. Дои:10.1165 / rcmb.2013-0001OC. ЧВК 3931111. PMID 23808363.
- ^ а б Каппелер С.Р., Хойбергер С., Фарах З., Пухан З. (август 2004 г.). «Экспрессия белка распознавания пептидогликана, PGRP, в лактирующей молочной железе». Журнал молочной науки. 87 (8): 2660–8. Дои:10.3168 / jds.S0022-0302 (04) 73392-5. PMID 15328291.
- ^ а б c Гош А., Ли С., Дзиарски Р., Чакраварти С. (сентябрь 2009 г.). «Новый антимикробный белок распознавания пептидогликана в роговице». Исследовательская офтальмология и визуализация. 50 (9): 4185–91. Дои:10.1167 / iovs.08-3040. ЧВК 3052780. PMID 19387073.
- ^ а б c Парк С.Ю., Гупта Д., Хурвич Р., Ким С.Х., Дзиарски Р. (декабрь 2011 г.). «Белок распознавания пептидогликана Pglyrp2 защищает мышей от псориазоподобного кожного воспаления, стимулируя регуляторные Т-клетки и ограничивая ответы Th17». Журнал иммунологии. 187 (11): 5813–23. Дои:10.4049 / jimmunol.1101068. ЧВК 3221838. PMID 22048773.
- ^ а б c d Парк С.Ю., Гупта Д., Ким СН, Дзярски Р. (2011). «Дифференциальные эффекты белков распознавания пептидогликана на экспериментальный атопический и контактный дерматит, опосредованный клетками Treg и Th17». PLOS ONE. 6 (9): e24961. Bibcode:2011PLoSO ... 624961P. Дои:10.1371 / journal.pone.0024961. ЧВК 3174980. PMID 21949809.
- ^ а б c Saha S, Jing X, Park SY, Wang S, Li X, Gupta D, Dziarski R (август 2010 г.). «Белки распознавания пептидогликана защищают мышей от экспериментального колита, способствуя нормальной микрофлоре кишечника и предотвращая индукцию гамма-интерферона». Клеточный хозяин и микроб. 8 (2): 147–62. Дои:10.1016 / j.chom.2010.07.005. ЧВК 2998413. PMID 20709292.
- ^ Ло Д., Тайнан В., Дикерсон Дж., Менди Дж., Чанг Х.В., Шарф М. и др. (Июль 2003 г.). «Экспрессия белка распознавания пептидогликанов в эпителии, ассоциированном с фолликулами Пейера-пятна мыши, предполагает функциональную специализацию». Клеточная иммунология. 224 (1): 8–16. Дои:10.1016 / с0008-8749 (03) 00155-2. PMID 14572796.
- ^ Ван Дж., Густи В., Сарасвати А., Ло Д.Д. (ноябрь 2011 г.). «Конвергентное и дивергентное развитие среди линий М-клеток в эпителии слизистой оболочки мыши». Журнал иммунологии. 187 (10): 5277–85. Дои:10.4049 / jimmunol.1102077. ЧВК 3208058. PMID 21984701.
- ^ Даунс-Каннер С., Берки С., Делгоффе Г.М., Эдвардс Р.П., Куриэль Т., Одунси К. и др. (Март 2017 г.). "клетки рег". Nature Communications. 8: 14649. Дои:10.1038 / ncomms14649. ЧВК 5355894. PMID 28290453.
- ^ Арентсен Т., Цянь Ю., Гкоцис С., Фемения Т., Ван Т., Удекву К. и др. (Февраль 2017). «Бактериальная молекула Pglyrp2, чувствительная к пептидогликану, модулирует развитие и поведение мозга». Молекулярная психиатрия. 22 (2): 257–266. Дои:10.1038 / mp.2016.182. ЧВК 5285465. PMID 27843150.
- ^ а б Рехман А., Тайши П., Фанг Дж., Майде Дж. А., Крюгер Дж. М. (январь 2001 г.). «Клонирование крысиного белка распознавания пептидогликана (PGRP) и его индукция в головном мозге путем лишения сна». Цитокин. 13 (1): 8–17. Дои:10.1006 / cyto.2000.0800. PMID 11145837.
- ^ Ланг М.Ф., Шнайдер А., Крюгер С., Шмид Р., Дзиарски Р., Шванингер М. (январь 2008 г.). «Белок распознавания пептидогликана-S (PGRP-S) активируется с помощью NF-kappaB». Письма о неврологии. 430 (2): 138–41. Дои:10.1016 / j.neulet.2007.10.027. PMID 18035491. S2CID 54406942.
- ^ а б Тайделл С.К., Юань Дж., Тран П., Селстед М.Э. (январь 2006 г.). «Бычий белок распознавания пептидогликана-S: антимикробная активность, локализация, секреция и связывающие свойства». Журнал иммунологии. 176 (2): 1154–62. Дои:10.4049 / jimmunol.176.2.1154. PMID 16394004. S2CID 11173657.
- ^ а б Де Марци М.К., Тодоне М., Ганем МБ, Ван Кью, Мариуцца Р.А., Фернандес М.М., Мальчиоди Е.Л. (июль 2015 г.). «Комплексы белок-пептидогликан, распознающие пептидогликан, увеличивают активацию моноцитов / макрофагов и усиливают воспалительный ответ». Иммунология. 145 (3): 429–42. Дои:10.1111 / imm.12460. ЧВК 4479541. PMID 25752767.
- ^ Ван З.М., Ли Х, Коклин Р.Р., Ван М., Ван М., Фукасе К. и др. (Декабрь 2003 г.). «Белок распознавания пептидогликана человека-L представляет собой N-ацетилмурамоил-L-аланинамидазу». Журнал биологической химии. 278 (49): 49044–52. Дои:10.1074 / jbc.M307758200. PMID 14506276. S2CID 35373818.
- ^ а б c d Лу Х, Ван М., Ци Дж., Ван Х, Ли Х, Гупта Д., Дзиарски Р. (март 2006 г.). «Белки распознавания пептидогликанов представляют собой новый класс бактерицидных белков человека». Журнал биологической химии. 281 (9): 5895–907. Дои:10.1074 / jbc.M511631200. PMID 16354652. S2CID 21943426.
- ^ а б Шарма П., Сингх Н., Синха М., Шарма С., Пербандт М., Бетцель С. и др. (Май 2008 г.). «Кристаллическая структура белка распознавания пептидогликана при разрешении 1,8 A показывает двойную стратегию борьбы с инфекцией с помощью двух независимых функциональных гомодимеров». Журнал молекулярной биологии. 378 (4): 923–32. Дои:10.1016 / j.jmb.2008.03.018. PMID 18395744.
- ^ а б c d Ван М., Лю Л. Х., Ван С., Ли Х, Лу Х, Гупта Д., Дзиарски Р. (март 2007 г.). «Белки распознавания пептидогликанов человека требуют цинка для уничтожения как грамположительных, так и грамотрицательных бактерий и обладают синергическим действием с антибактериальными пептидами». Журнал иммунологии. 178 (5): 3116–25. Дои:10.4049 / jimmunol.178.5.3116. PMID 17312159. S2CID 22160694.
- ^ «Reactome | PGLYRP1 связывает бактериальный пептидогликан». reactome.org. Получено 2020-11-03.
- ^ а б c d Кумар С., Ройчоудхури А., Эмбер Б., Ван К., Гуан Р., Мариуцца Р.А., Бунс Г.Дж. (ноябрь 2005 г.). «Селективное распознавание синтетического лизина и фрагментов пептидогликана типа мезо-диаминопимелиновой кислоты белками распознавания пептидогликана человека I {альфа} и S». Журнал биологической химии. 280 (44): 37005–12. Дои:10.1074 / jbc.M506385200. PMID 16129677. S2CID 44913130.
- ^ Шарма П., Дубе Д., Синха М., Мишра Б., Дей С., Мал Дж. И др. (Сентябрь 2011 г.). «Многолигандная специфичность сайта связывания патоген-ассоциированного молекулярного паттерна в белке распознавания пептидогликана». Журнал биологической химии. 286 (36): 31723–30. Дои:10.1074 / jbc.M111.264374. ЧВК 3173064. PMID 21784863.
- ^ а б Шарма П., Дубе Д., Сингх А., Мишра Б., Сингх Н., Синха М. и др. (Май 2011 г.). «Структурная основа распознавания патоген-ассоциированных молекулярных паттернов и ингибирования провоспалительных цитокинов белком распознавания верблюжьего пептидогликана». Журнал биологической химии. 286 (18): 16208–17. Дои:10.1074 / jbc.M111.228163. ЧВК 3091228. PMID 21454594.
- ^ а б c d е ж грамм час Кашьяп Д.Р., Ван М., Лю Л.Х., Бунс Г.Дж., Гупта Д., Дзиарски Р. (июнь 2011 г.). «Белки распознавания пептидогликанов убивают бактерии, активируя двухкомпонентные системы, чувствительные к белкам». Природа Медицина. 17 (6): 676–83. Дои:10,1038 / нм. 2357. ЧВК 3176504. PMID 21602801.
- ^ Бобровский П., Манувера В., Полина Н., Подгорный О., Прусаков К., Говорун В., Лазарев В. (июль 2016 г.). «Рекомбинантные белки распознавания пептидогликанов человека обнаруживают антихламидийную активность». Инфекция и иммунитет. 84 (7): 2124–2130. Дои:10.1128 / IAI.01495-15. ЧВК 4936355. PMID 27160295.
- ^ Ван Дж., Фэн Й., Ван С., Сринивас С., Чен С., Ляо Х. и др. (Июль 2017 г.). «Патогенные штаммы Streptococcus используют новую стратегию ускользания для подавления бактериостатического эффекта, опосредованного белком распознавания пептидогликана млекопитающих». Клеточная микробиология. 19 (7): e12724. Дои:10,1111 / cmi,12724. PMID 28092693. S2CID 3534029.
- ^ Осанай А., Сашинами Х., Асано К., Ли С.Дж., Ху Д.Л., Накане А. (февраль 2011 г.). «Белок распознавания пептидогликана мыши PGLYRP-1 играет роль в врожденном иммунном ответе хозяина против инфекции Listeria monocytogenes». Инфекция и иммунитет. 79 (2): 858–66. Дои:10.1128 / IAI.00466-10. ЧВК 3028829. PMID 21134971.
- ^ а б Дзиарски Р., Парк С.Ю., Кашьяп Д.Р., Дауд С.Е., Гупта Д. (2016). «Pglyrp-регулируемая кишечная микрофлора Prevotella falsenii, Parabacteroides distasonis и Bacteroides eggerthii Enhance и Alistipes finegoldii ослабляет колит у мышей». PLOS ONE. 11 (1): e0146162. Bibcode:2016PLoSO..1146162D. Дои:10.1371 / journal.pone.0146162. ЧВК 4699708. PMID 26727498.
- ^ а б Банскар С., Детцнер А.А., Хуарес-Родригес, доктор медицины, Ходзо И., Гупта Д., Дзиарски Р. (декабрь 2019 г.). «Регулируемый Pglyrp1 микробиом усиливает экспериментальную аллергическую астму». Журнал иммунологии. 203 (12): 3113–3125. Дои:10.4049 / jimmunol.1900711. PMID 31704882. S2CID 207942798.
- ^ а б c Saha S, Qi J, Wang S, Wang M, Li X, Kim YG и др. (Февраль 2009 г.). «PGLYRP-2 и Nod2 оба необходимы для пептидогликанового артрита и местного воспаления». Клеточный хозяин и микроб. 5 (2): 137–50. Дои:10.1016 / j.chom.2008.12.010. ЧВК 2671207. PMID 19218085.
- ^ а б c Сащенко Л.П., Духанина Е.А., Яшин Д.В., Шаталов Ю.В., Романова Е.А., Коробко Е.В. и др. (Январь 2004 г.). «Белок распознавания пептидогликана tag7 образует цитотоксический комплекс с белком теплового шока 70 в растворе и в лимфоцитах». Журнал биологической химии. 279 (3): 2117–24. Дои:10.1074 / jbc.M307513200. PMID 14585845. S2CID 23485070.
- ^ а б c Яшин Д.В., Иванова О.К., Сошникова Н.В., Шелудченков А.А., Романова Е.А., Духанина Е.А. и др. (Август 2015 г.). «Tag7 (PGLYRP1) в комплексе с Hsp70 индуцирует альтернативные цитотоксические процессы в опухолевых клетках через рецептор TNFR1». Журнал биологической химии. 290 (35): 21724–31. Дои:10.1074 / jbc.M115.639732. ЧВК 4571894. PMID 26183779.
- ^ Сащенко Л.П., Духанина Е.А., Шаталов Ю.В., Яшин Д.В., Лукьянова Т.И., Кабанова О.Д. и др. (Сентябрь 2007 г.). «Цитотоксические Т-лимфоциты, несущие белок распознавания образов Tag7, могут обнаруживать уклончивые, HLA-отрицательные, но Hsp70-экспонирующие опухолевые клетки, тем самым обеспечивая FasL / Fas-опосредованное контактное уничтожение». Кровь. 110 (6): 1997–2004. Дои:10.1182 / кровь-2006-12-064444. PMID 17551095.
- ^ Духанина Е.А., Кабанова О.Д., Лукьянова Т.И., Шаталов Ю.В., Яшин Д.В., Романова Е.А. и др. (Август 2009 г.). «Противоположные роли метастазина (S100A4) в двух потенциально опухолевых механизмах с участием человеческого лимфоцитарного белка Tag7 и Hsp70». Труды Национальной академии наук Соединенных Штатов Америки. 106 (33): 13963–7. Bibcode:2009PNAS..10613963D. Дои:10.1073 / pnas.0900116106. ЧВК 2729003. PMID 19666596.
- ^ Яшин Д.В., Духанина Е.А., Кабанова О.Д., Романова Е.А., Лукьянова Т.И., Тоневицкий А.Г. и др. (Март 2011 г.). «Белок, связывающий теплового шока (HspBP1), защищает клетки от цитотоксического действия комплекса Tag7-Hsp70». Журнал биологической химии. 286 (12): 10258–64. Дои:10.1074 / jbc.M110.163436. ЧВК 3060480. PMID 21247889.
- ^ Яшин Д.В., Романова Е.А., Иванова О.К., Сащенко Л.П. (апрель 2016 г.). «Цитотоксический комплекс Tag7-Hsp70 индуцирует некроптоз опухолевых клеток через проницаемость лизосом и митохондрий». Биохимия. 123: 32–6. Дои:10.1016 / j.biochi.2016.01.007. PMID 26796882.
- ^ Романова Е.А., Шарапова Т.Н., Телегин Г.Б., Минаков А.Н., Чернов А.С., Иванова О.К. и др. (Февраль 2020 г.). «12-мерный пептид Tag7 (PGLYRP1) образует цитотоксический комплекс с Hsp70 и ингибирует гибель клеток, индуцированную TNF-альфа». Клетки. 9 (2): 488. Дои:10.3390 / ячейки9020488. ЧВК 7072780. PMID 32093269.
- ^ Прочтите CB, Kuijper JL, Hjorth SA, Heipel MD, Tang X, Fleetwood AJ, et al. (Февраль 2015 г.). «Передний край: идентификация нейтрофилов PGLYRP1 в качестве лиганда для TREM-1». Журнал иммунологии. 194 (4): 1417–21. Дои:10.4049 / jimmunol.1402303. ЧВК 4319313. PMID 25595774.
- ^ Зульфикар Ф., Хозо I, Рангараджан С., Мариуцца Р.А., Дзиарски Р., Гупта Д. (2013). "Генетическая ассоциация вариантов белков распознавания пептидогликанов с воспалительным заболеванием кишечника". PLOS ONE. 8 (6): e67393. Bibcode:2013PLoSO ... 867393Z. Дои:10.1371 / journal.pone.0067393. ЧВК 3686734. PMID 23840689.
- ^ Nkya S, Mwita L, Mgaya J, Kumburu H, van Zwetselaar M, Menzel S, et al. (Июнь 2020 г.). «Выявление генетических вариантов и путей, связанных с экстремальным уровнем гемоглобина плода при серповидно-клеточной анемии в Танзании». BMC Medical Genetics. 21 (1): 125. Дои:10.1186 / s12881-020-01059-1. ЧВК 7275552. PMID 32503527.
- ^ Рохатги А., Айерс С.Р., Кхера А., Макгуайр Д.К., Дас С.Р., Матулявичюс С.Р. и др. (Апрель 2009 г.). «Связь между белком распознавания пептидогликана-1 и коронарным и периферическим атеросклерозом: наблюдения из Далласского исследования сердца». Атеросклероз. 203 (2): 569–75. Дои:10.1016 / j.atherosclerosis.2008.07.015. PMID 18774573.
- ^ Brownell NK, Khera A, de Lemos JA, Ayers CR, Rohatgi A (май 2016 г.). «Связь между протеином-1 распознавания пептидогликана и инцидентными атеросклеротическими сердечно-сосудистыми заболеваниями: исследование сердца в Далласе». Журнал Американского колледжа кардиологии. 67 (19): 2310–2312. Дои:10.1016 / j.jacc.2016.02.063. PMID 27173041.
- ^ Пак Х. Дж., Но Дж. Х., Ын Дж. У., Ко Ю. С., Со С. М., Парк В. С. и др. (Май 2015 г.). «Оценка и диагностическая значимость новых биомаркеров сыворотки для раннего решения инфаркта миокарда с подъемом сегмента ST». Oncotarget. 6 (15): 12970–83. Дои:10.18632 / oncotarget.4001. ЧВК 4536992. PMID 26025919.
- ^ Чжан Дж, Ченг И, Дуань М, Ци Н, Лю Дж (май 2017 г.). «Выявление дифференциально экспрессируемых генов при регуляции факторов транскрипции при сепсисе». 3 Биотехнологии. 7 (1): 46. Дои:10.1007 / с13205-017-0713-х. ЧВК 5428098. PMID 28444588.
- ^ Бриньольфссон С.Ф., Магнуссон М.К., Конг П.Л., Йенсен Т., Куиджпер Дж.Л., Хоканссон К. и др. (Август 2016 г.). «Антитело против триггерного рецептора, экспрессируемого на миелоидных клетках 1 (TREM-1), подавляет секрецию провоспалительных цитокинов клетками Lamina Propria от пациентов с ВЗК». Воспалительные заболевания кишечника. 22 (8): 1803–11. Дои:10.1097 / MIB.0000000000000822. PMID 27243593. S2CID 3637291.
- ^ Molyneaux PL, Willis-Owen SA, Cox MJ, James P, Cowman S, Loebinger M и др. (Июнь 2017 г.). «Взаимодействие между хозяином и микробами при идиопатическом фиброзе легких». Американский журнал респираторной медицины и реанимации. 195 (12): 1640–1650. Дои:10.1164 / rccm.201607-1408OC. ЧВК 5476909. PMID 28085486.
- ^ Kasaian MT, Lee J, Brennan A, Danto SI, Black KE, Fitz L, Dixon AE (июль 2018 г.). «Протеомный анализ аналитов сыворотки и мокроты позволяет различать контролируемых и плохо контролируемых астматиков». Клиническая и экспериментальная аллергия. 48 (7): 814–824. Дои:10.1111 / cea.13151. PMID 29665127. S2CID 4938216.
- ^ Нюлунд К.М., Руоконен Х., Сорса Т., Хейккинен А.М., Меурман Дж. Х., Ортиз Ф. и др. (Январь 2018). «Ассоциация рецептора запуска слюны, экспрессируемого на миелоидных клетках / его лиганд, ось белка распознавания пептидогликана 1, с воспалением полости рта при заболевании почек». Журнал пародонтологии. 89 (1): 117–129. Дои:10.1902 / jop.2017.170218. PMID 28846062. S2CID 21830535.
- ^ Ло Цюй, Ли Х, Чжан Л., Яо Ф, Дэн З., Цин Ц. и др. (Январь 2019). «Сыворотка PGLYRP ‑ 1 - это очень дискриминационный биомаркер для диагностики ревматоидного артрита». Отчеты по молекулярной медицине. 19 (1): 589–594. Дои:10.3892 / ммр.2018.9632. PMID 30431075.
- ^ Silbereisen A, Hallak AK, Nascimento GG, Sorsa T., Belibasakis GN, Lopez R, Bostanci N (октябрь 2019 г.). «Регулирование PGLYRP1 и TREM-1 во время прогрессирования и разрешения воспаления десен». Клинические и трансляционные исследования JDR. 4 (4): 352–359. Дои:10.1177/2380084419844937. PMID 31013451. S2CID 129941967.
- ^ Райвисто Т., Хейккинен А.М., Силберайзен А., Кованен Л., Руоконен Х., Тервахартиала Т. и др. (Октябрь 2020 г.). «Регулирование белка 1 распознавания пептидогликанов в слюне у подростков». Клинические и трансляционные исследования JDR. 5 (4): 332–341. Дои:10.1177/2380084419894287. PMID 31860804.
- ^ Yucel ZP, Silbereisen A, Emingil G, Tokgoz Y, Kose T., Sorsa T. и др. (Октябрь 2020 г.). «Биомаркеры слюны в контексте воспаления десен у детей с муковисцидозом». Журнал пародонтологии. 91 (10): 1339–1347. Дои:10.1002 / JPER.19-0415. PMID 32100289.
- ^ Карсияка Хендек М., Киса У, Ольгун Э. (январь 2020 г.). «Влияние курения на уровень белка-1 распознавания пептидогликана десневой жидкости десны после начальной пародонтальной терапии хронического пародонтита». Оральные заболевания. 26 (1): 166–172. Дои:10.1111 / odi.13207. PMID 31587460.
- ^ Тейшейра М.К., Лира-Джуниор Р., Лоуренсо Э.Д., Теллес Д.М., Бострем Е.А., Фигередо С.М., Бостанджи Н. «Модуляция оси TREM-1 / PGLYRP1 / MMP-8 при периимплантных заболеваниях». Клинические оральные исследования. 24 (5): 1837–1844. Дои:10.1007 / s00784-019-03047-z. PMID 31444693. S2CID 201283050.
- ^ Ян З, Ни Дж, Куанг Л., Гао Й, Тао С. (сентябрь 2020 г.). «Идентификация генов и путей, связанных с субхондральной костью при остеоартрите, с помощью биоинформатического анализа». Лекарство. 99 (37): e22142. Дои:10.1097 / MD.0000000000022142. ЧВК 7489699. PMID 32925767.
- ^ Ортиз Ф., Нюлунд К.М., Руоконен Х., Меурман Дж. Х., Фурухольм Дж., Бостанси Н., Сорса Т. (август 2020 г.). «Слюнные биомаркеры воспаления полости рта связаны с сердечно-сосудистыми событиями и смертью пациентов с трансплантацией почки». Трансплантация. Дои:10.1016 / j.transproceed.2020.07.007. PMID 32768288.
- ^ Glickman JW, Dubin C, Renert-Yuval Y, Dahabreh D, Kimmel GW, Auyeung K и др. (Май 2020 г.). «Поперечное исследование биомаркеров крови пациентов с очаговой алопецией от умеренной до тяжелой выявляет дисрегуляцию системных иммунных и сердечно-сосудистых биомаркеров». Журнал Американской академии дерматологии. Дои:10.1016 / j.jaad.2020.04.138. PMID 32376430.
- ^ Klimczak-Tomaniak D, Bouwens E, Schuurman AS, Akkerhuis KM, Constantinescu A, Brugts J, et al. (Июнь 2020 г.). «Временные паттерны маркеров, связанных с макрофагами и нейтрофилами, связаны с клиническим исходом у пациентов с сердечной недостаточностью». ESC Сердечная недостаточность. 7 (3): 1190–1200. Дои:10.1002 / ehf2.12678. ЧВК 7261550. PMID 32196993.
- ^ Ян С., Цао Ц, Се З, Чжоу З (март 2020 г.). «Анализ потенциальных узловых генов, участвующих в патогенезе китайских пациентов с диабетом 1 типа». Анналы трансляционной медицины. 8 (6): 295. Дои:10.21037 / атм.2020.02.171. ЧВК 7186604. PMID 32355739.
- ^ Арениус I, Руоконен Х., Ортис Ф., Фурухольм Дж., Валимаа Х., Бостанси Н. и др. (Июль 2020 г.). «Взаимосвязь между заболеваниями полости рта и инфекционными осложнениями у пациентов, находящихся на диализе». Оральные заболевания. 26 (5): 1045–1052. Дои:10.1111 / odi.13296. PMID 32026534.
- ^ Го Ц., Ли З (декабрь 2019 г.). «Биоинформатический анализ ключевых генов и путей, связанных с тромбозом при эссенциальной тромбоцитемии». Монитор медицинских наук. 25: 9262–9271. Дои:10.12659 / MSM.918719. ЧВК 6911306. PMID 31801935.
- ^ Гранде Дж., Винченцони Ф., Миларди Д., Помпа Дж., Риккарди Д., Фрушелла Е. и др. (2017). «Протеом цервикальной слизи при эндометриозе». Клиническая протеомика. 14: 7. Дои:10.1186 / s12014-017-9142-4. ЧВК 5290661. PMID 28174513.
дальнейшее чтение
- Дзиарски Р., Ройет Дж., Гупта Д. (2016). «Белки распознавания пептидогликанов и лизоцим». В Ratcliffe MJ (ред.). Энциклопедия иммунобиологии. 2. Elsevier Ltd., стр. 389–403. Дои:10.1016 / B978-0-12-374279-7.02022-1. ISBN 978-0123742797.
- Ройет Дж., Гупта Д., Дзиарски Р. (ноябрь 2011 г.). «Белки распознавания пептидогликанов: модуляторы микробиома и воспаления». Обзоры природы. Иммунология. 11 (12): 837–51. Дои:10.1038 / nri3089. PMID 22076558. S2CID 5266193.
- Ройет Дж., Дзиарски Р. (апрель 2007 г.). «Белки распознавания пептидогликанов: плейотропные сенсоры и эффекторы антимикробной защиты». Обзоры природы. Микробиология. 5 (4): 264–77. Дои:10.1038 / nrmicro1620. PMID 17363965. S2CID 39569790.
- Дзярский Р., Гупта Д. (2006). «Белки распознавания пептидогликана (PGRP)». Геномная биология. 7 (8): 232. Дои:10.1186 / gb-2006-7-8-232. ЧВК 1779587. PMID 16930467.
- Bastos PA, Wheeler R, Boneca IG (сентябрь 2020 г.). «Поглощение, распознавание и ответы на пептидогликан в организме млекопитающего-хозяина». Обзор микробиологии FEMS. Дои:10.1093 / femsre / fuaa044. PMID 32897324.
- Вольф AJ, Андерхилл DM (апрель 2018 г.). «Распознавание пептидогликанов врожденной иммунной системой». Обзоры природы. Иммунология. 18 (4): 243–254. Дои:10.1038 / № 2017.136. PMID 29292393. S2CID 3894187.
- Ламан Дж. Д., 'т Харт Б. А., Power C, Дзиарски Р. (июль 2020 г.). «Бактериальный пептидогликан как фактор хронического воспаления головного мозга». Тенденции в молекулярной медицине. 26 (7): 670–682. Дои:10.1016 / j.molmed.2019.11.006. PMID 32589935.
- Гонсалес-Сантана А., Диас Хейц Р. (август 2020 г.). «Бактериальные пептидогликаны из микробиоты в нервном развитии и поведении». Тенденции в молекулярной медицине. 26 (8): 729–743. Дои:10.1016 / j.molmed.2020.05.003. PMID 32507655.