Гипонитрит натрия - Sodium hyponitrite
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol ) |
|
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| Na2N2О2 | |
| Молярная масса | 105,99 г / моль |
| Внешность | бесцветные кристаллы |
| Плотность | 2,466 г / см3 |
| Температура плавления | 100 ° С (212 ° F, 373 К) |
| Точка кипения | 335 ° С (635 ° F, 608 К) разлагается |
| растворимый | |
| Растворимость | не растворим в этиловый спирт |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
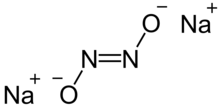
Гипонитрит натрия твердый ионное соединение с формулой Na
2N
2О
2 или же (Na+
)2[ВКЛ = НЕТ]2−.[1]
Есть СНГ и транс формы гипонитрит ион N
2О2−
2. В транс форма более распространена, но СНГ форма также может быть получена, и она более реактивна, чем транс форма.[1][2]
Транс изомер
В транс изомер бесцветен, растворим в воде и не растворим в этиловый спирт и эфир.[3][4]
Подготовка
Гипонитрит натрия (транс) обычно готовится снижение из нитрат натрия с амальгама натрия.[5][6][7]
- 2 NaNO2 + 4 Na (Hg) + 2 Н2O → Na2N2О2 + 4 NaOH + 4 Hg
Гипонитрит натрия (транс) был подготовлен в 1927 г. А. В. Скотт реагируя алкил нитриты, гидроксиламмоний хлорид, и этоксид натрия[4][8]
- RONO + NH2ОН + 2 EtONa → Na2N2О2 + ROH + 2 EtOH
Более ранний метод, опубликованный Д. Менденхолл в 1974 г. прореагировал газообразный оксид азота (НЕТ) с натрий металл в 1,2-диметоксиэтан, толуол, и бензофенон. Затем соль экстрагировали водой.[9] Позже метод был изменен для использования пиридин[нужна цитата ].
Включены другие методы окисление концентрированного раствора гидроксиламин с нитритом натрия в щелочной среде[нужна цитата ]; или же электролиз нитрита натрия.[10]
Увлажняет
Разнообразие гидраты Na
2N
2О
2(ЧАС
2О)Икс из транс изомера сообщалось, с Икс в том числе 2, 3,5, 4, 5, 6, 7, 8 и 9;[11][3][12] но есть спор.[13]
Гидратная вода, кажется, просто захвачена в кристаллической решетке, а не координирована с ионами.[13] Безводное вещество может быть получено сушкой гидратов над пятиокись фосфора а затем нагревают их до 120 ° C.[13]
Реакции
Гипонитрит натрия (транс) в растворе разлагается на углекислый газ CO
2 из воздуха в форму карбонат натрия.[14]
Жидкость N2О4 окисляет гипонитрит натрия (транс) дать натрий пероксогипонитрит Na2+
2[ON = НЕТ]2−).[15][1]
СНГ изомер
В СНГ изомер гипонитрита натрия представляет собой белое кристаллическое твердое вещество, не растворимое в апротический растворители, и (в отличие от транс изомер) разлагается водой и другими протический растворители.[2]
Подготовка
В СНГ изомер может быть получен путем пропускания оксид азота (НЕТ) через раствор натрий металл в жидкости аммиак при -50 ° С.[1]
В СНГ изомер был также получен в 1996 г. К. Фельдманн и М. Янсен путем нагрева оксид натрия Na
2О с 77 кПа из оксид азота N
2О (веселящий газ) в закрытой пробирке при 360 ° C в течение 2 часов. Два реагента объединили, чтобы получить СНГ гипонитрит количественно в виде белых микрокристаллов.[8][2]
Свойства и реакции
Безводный СНГ соль устойчива до 325 ° C, когда она непропорциональна азот и ортонитрит натрия:[2]
- 3 Na
2N
2О
2 → 2 Na
3О(НЕТ
2) + 2 N
2
Обычно он более реактивен, чем транс изомер.[1]
Смотрите также
Рекомендации
- ^ а б c d е Эгон Виберг, Арнольд Фредерик Холлеман (2001) Неорганическая химия, Эльзевьер ISBN 0-12-352651-5
- ^ а б c d Клаус Фельдманн, Мартин Янсен (1996) "СНГ-Гипонитрит натрия - новый метод получения и анализ кристаллической структуры ». Angewandte Chemie International Edition на английском языке, том 35, выпуск 15, страницы 1728–1730. Дои:10.1002 / anie.199617281
- ^ а б Трамбаклал Моханлал Оза, Раджникант Харипрасад Такер (1955), «Термическое разложение гипонитрита серебра». Журнал Американского химического общества, том 77, выпуск 19, страницы 4976–4980. Дои:10.1021 / ja01624a007
- ^ а б А. В. Скотт (1927), «Гипонитрит натрия». Варенье. Chem. Soc., том = 49, выпуск 4, страниц = 986–987. Дои:10.1021 / ja01403a502
- ^ Addison, C.C .; Гамлен Г. А .; Томпсон, Р. (1952). «70. Ультрафиолетовые спектры поглощения гипонитрита натрия и α-оксигипонитрита натрия: анализ смесей с нитритом и нитратом натрия». J. Chem. Soc.: 338. Дои:10.1039 / jr9520000338.
- ^ Нойманн, Р. К., младший Бусси, Р. Дж. (1970). «Исследования высокого давления. V. Активационные объемы для объединения и диффузии геминатных трет-бутоксильных радикалов». Варенье. Chem. Soc. 92 (8): 2440. Дои:10.1021 / ja00711a039.CS1 maint: несколько имен: список авторов (связь)
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б Кэтрин Э. Хаукрофт; Алан Г. Шарп (2008). «Глава 15: Группа 15 элементов». Неорганическая химия (3-е изд.). Пирсон. п. 468. ISBN 978-0-13-175553-6.
- ^ Г. Дэвид Менденхолл (1974), «Удобный синтез гипонитрита серебра». Журнал Американского химического общества, том 96, выпуск 15, страница 5000. Дои:10.1021 / ja00822a054
- ^ Polydoropoulos, C. N. Chem. Ind. (Лондон) 1963, 1686 и ссылки в них.
- ^ Джеймс Риддик Партингтон и Чандулал Чхоталал Шах (1931), «Исследования гипонитритов. Часть I. Гипонитрит натрия: получение и свойства». Журнал химического общества (возобновленный), статья CCLXXXII, страницы 2071-2080. Дои:10.1039 / JR9310002071
- ^ C.N. Полидоропулос, С. Voliotis (1967), «Гексагидрат гипонитрита натрия». Журнал неорганической и ядерной химии, том 29, выпуск 12, страницы 2899–2901. Дои:10.1016/0022-1902(67)80121-0
- ^ а б c Гэри Л. Стаки, Джек Л. Ламберт, Р. Дин Драгсдорф (1969), «Гидраты гипонитрита натрия». Журнал неорганической и ядерной химии, том 31, выпуск 1, страницы 29–32 Дои:10.1016/0022-1902(69)80050-3
- ^ Шарлотта Н. Коннер, Кэролайн Э. Дональд, Мартин Н. Хьюз, Кристина Сами (1989), "Молярная поглощающая способность гипонитрита натрия". Многогранник, том 8, выпуск 21, страницы 2621-2622. Дои:10.1016 / S0277-5387 (00) 81166-3
- ^ М. Н. Хьюз и Г. Г. Никлин (1969), "Действие тетроксида диазота на гипонитрит натрия". Журнал химического общества D: Химические коммуникации, том 1969, выпуск 2, стр. 80a. Дои:10.1039 / C2969000080A
