Глатирамера ацетат - Glatiramer acetate
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Копаксон,[1] Глатопа,[2] Брабио |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a603016 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Подкожная инъекция |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider |
|
| UNII | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.248.824 |
| Химические и физические данные | |
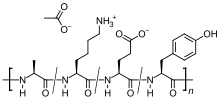
| Формула | C25ЧАС45N5О13 |
| Молярная масса | 623.657 г · моль−1 |
| | |
Глатирамера ацетат (также известный как Сополимер 1, Полицейский-1), продается под торговой маркой Копаксон среди прочего, это иммуномодулятор лекарства, используемые для лечения рассеянный склероз.[1][2] Глатирамера ацетат одобрен в США для уменьшения частоты рецидивов, но не для уменьшения прогрессирования инвалидности. Наблюдательные исследования, но не рандомизированные контролируемые испытания, предполагают, что это может уменьшить прогрессирование инвалидности. В то время как убедительный диагностика рассеянного склероза требует наличия в анамнезе двух или более эпизодов симптомов и признаков, глатирамера ацетат одобрен для лечения первого эпизода в ожидании диагноза. Он также используется для лечения ремиттирующего рассеянного склероза. Он находится в ведении подкожная инъекция.[1][2]
Это смесь пептидов случайного размера, состоящая из четырех аминокислоты нашел в основной белок миелина, а именно глютаминовая кислота, лизин, аланин, и тирозин. Основной белок миелина - это антиген в миелиновые оболочки нейронов, которые стимулируют аутоиммунный реакция у людей с РС, поэтому пептид может работать как приманка для атакующих иммунных клеток.
История
Глатирамера ацетат был первоначально обнаружен в Институт Вайцмана. Чтобы продемонстрировать безопасность и эффективность, последовали три основных клинических испытания: первое испытание было проведено в едином центре, двойное слепое, плацебо-контролируемое испытание и включили 50 пациентов.[5]Второе испытание было двухлетним многоцентровым рандомизированным двойным слепым плацебо-контролируемым испытанием, в котором участвовал 251 пациент.[6] Третье испытание было двойным слепым. МРТ исследование с участием 239 пациентов.[7]
Медицинское использование
Глатирамера ацетат указал для лечения рецидивирующих форм рассеянного склероза (РС), включая клинически изолированный синдром, рецидивирующе-ремиттирующее заболевание и активное вторично-прогрессирующее заболевание у взрослых.[1] Глатопа[2]
2010 г. Кокрейн обзор пришел к выводу, что глатирамера ацетат имел частичную эффективность в отношении «клинических исходов, связанных с рецидивом», но не влиял на прогрессирование заболевания.[8] В результате он одобрен FDA для уменьшения частоты рецидивов, но не для уменьшения прогрессирования инвалидности.[1][2]
В ходе 15-летнего наблюдения за первоначальным исследованием сравнивали пациентов, продолжавших принимать глатирамер, с пациентами, выбывшими из исследования. Пациенты, принимавшие глатирамер, имели более низкую частоту рецидивов, снижение прогрессирования инвалидности и переход к вторично прогрессирующему РС по сравнению с пациентами, которые не принимали глатирамер. Однако эти две группы не обязательно были сопоставимы, поскольку это больше не было рандомизированным исследованием. Долговременных проблем безопасности не было.[9]
Побочные эффекты

Побочные эффекты могут включать опухоль в месте инъекции (реакция в месте инъекции) примерно у 30% пользователей и боли, лихорадка, озноб (симптомы гриппа) примерно у 10% пользователей.[10] Симптомы побочного действия обычно легкие. О реакции, включающей покраснение кожи, одышку, беспокойство и учащенное сердцебиение, сообщалось вскоре после инъекции почти у 5% пациентов (обычно после случайной инъекции непосредственно в вену). Эти побочные эффекты проходят в течение тридцати минут. Со временем может появиться видимая вмятина в месте повторной инъекции из-за местного разрушения жировой ткани, известного как липоатрофия, что может развиться.
Сообщалось о более серьезных побочных эффектах глатирамера ацетата, согласно предписаниям FDA, они включают серьезные побочные эффекты для сердечно-сосудистой, пищеварительной (включая печень), кроветворной, лимфатической, скелетно-мышечной, нервной, дыхательной и мочеполовой систем, а также особые чувства (в частности, глаза). Сообщалось также о нарушениях обмена веществ и питания; однако связь между глатирамера ацетатом и этими побочными эффектами не установлена.[1][2]
Это также может вызвать Лимфоцитарный инфильтрат Джесснера.[11]
Механизм действия
Глатирамера ацетат представляет собой статистический полимер (средняя молекулярная масса 6,4кД ) в составе четырех аминокислоты нашел в основной белок миелина. Механизм действия глатирамера ацетата полностью не выяснен. Считается, что он действует путем модификации иммунных процессов, которые, как считается, ответственны за патогенез РС. Введение глатирамера ацетата сдвигает популяцию Т-клеток с провоспалительного действия. Th1 Т-клетки к нормативным Th2 Т-клетки подавляют воспалительную реакцию.[12] Учитывая его сходство с основным белком миелина, глатирамера ацетат может действовать как приманка, отклоняя аутоиммунный ответ против миелина. Эта гипотеза подтверждается результатами исследований, проведенных с целью изучения патогенеза экспериментальный аутоиммунный энцефаломиелит (EAE), состояние, вызываемое у нескольких видов животных путем иммунизации против материала, полученного из центральной нервной системы, содержащего миелин, и часто используется в качестве экспериментальной модели рассеянного склероза на животных. Исследования на животных и в системах in vitro показывают, что при его введении специфический глатирамера ацетат регуляторные Т-клетки (Tregs) индуцируются и активируются на периферии, подавляя воспалительную реакцию на основной белок миелина.[1][2]
Целостность гематоэнцефалический барьер однако на него не оказывает заметного влияния глатирамера ацетат, по крайней мере, на ранних стадиях лечения. В клинических испытаниях было показано, что глатирамера ацетат снижает количество и тяжесть обострений рассеянного склероза.[13]
Общество и культура
Маркетинг
Глатирамера ацетат был одобрен для продажи во многих странах мира, включая Соединенные Штаты, Израиль, Канада и 24 Евросоюз страны.[14][15] Утверждение в США было получено в 1997 году.[16] Глатирамера ацетат был одобрен для продажи в ВЕЛИКОБРИТАНИЯ. в августе 2000 г. и запущен в декабре.[17] Это первое одобрение на крупном европейском рынке привело к одобрению в Евросоюз под процедура взаимного признания. Иран продолжает отечественное производство глатирамера ацетата.[18][19]
Патентный статус
Новартис дочерняя компания Sandoz продает Glatopa с 2015 года, генерическую версию оригинальной рецептуры Teva 20 мг, которая требует ежедневных инъекций.[20]
Teva разработала препарат длительного действия на 40 мг, продаваемый с 2015 года, что позволило сократить количество инъекций до трех в неделю.[21] В октябре 2017 года FDA одобрило генерическую версию, которая производится в Индии компанией Натко Фарма, и импортировано и продано голландской фирмой Mylan.[22][23] В феврале 2018 года Sandoz получил одобрение FDA на свою генерическую версию.[24] Параллельно с процессами разработки и утверждения генерические конкуренты оспаривали новые патенты Teva, любой из которых, если он будет поддержан, помешает сбыту дженериков длительного действия.[25]
В то время как патент по химическому препарату истек в 2015 году,[26] Teva получила новые патенты в США, касающиеся фармацевтических препаратов длительного действия.[27] Судебные тяжбы со стороны отраслевых конкурентов в 2016-2017 годах привели к признанию новых патентов недействительными.[28][29] В октябре 2018 г. Апелляционный суд США для Федеральный округ поддержал признание патента недействительным для очевидность.[30][31] Случай отражает большие споры по поводу вечнозеленый дженериков.
Рекомендации
- ^ а б c d е ж грамм час «Копаксон-глатирамера ацетат для инъекций, раствор». DailyMed. 23 июля 2020 г.. Получено 11 ноября 2020.
- ^ а б c d е ж грамм час «Глатопаглатирамера ацетат для инъекций, раствор». DailyMed. 31 июля 2020 г.. Получено 11 ноября 2020.
- ^ «Раствор для инъекций Brabio 20 мг / мл, предварительно заполненный шприц - Сводка характеристик продукта (SmPC)». (emc). Получено 11 ноября 2020.
- ^ «Раствор для инъекций копаксона 20 мг / мл в предварительно заполненном шприце - Сводка характеристик продукта (SmPC)». (emc). 29 сентября 2020 г.. Получено 11 ноября 2020.
- ^ Борнштейн М.Б., Миллер А., Слэгл С., Вайцман М., Кристал Х., Дрекслер Э., Кейлсон М., Мерриам А., Вассертхайль-Смоллер С., Спада В. (август 1987 г.). «Пилотное испытание полицейского 1 при обострении ремиттирующего рассеянного склероза». Медицинский журнал Новой Англии. 317 (7): 408–14. Дои:10.1056 / NEJM198708133170703. PMID 3302705.
- ^ Джонсон К.П., Брукс Б.Р., Коэн Д.А., Форд С.К., Гольдштейн Дж., Лисак Р.П., Майерс Л.В., Панич С.С., Роуз Д.В., Шиффер Р.Б. (июль 1995 г.). «Сополимер 1 снижает частоту рецидивов и улучшает инвалидность при рецидивирующе-ремиттирующем рассеянном склерозе: результаты фазы III многоцентрового двойного слепого плацебо-контролируемого исследования. Группа изучения рассеянного склероза сополимера 1». Неврология. 45 (7): 1268–76. Дои:10.1212 / WNL.45.7.1268. PMID 7617181. S2CID 28895177.
- ^ Коми Дж., Филиппи М., Волински Дж. С. (март 2001 г.). «Европейское / канадское многоцентровое двойное слепое рандомизированное плацебо-контролируемое исследование эффектов глатирамера ацетата на магнитно-резонансную томографию - измеряли активность и бремя заболевания у пациентов с рецидивирующим рассеянным склерозом. Европейская / канадская группа по изучению глатирамера ацетата». Анналы неврологии. 49 (3): 290–7. Дои:10.1002 / ana.64. PMID 11261502. S2CID 35614752.
- ^ Ла Мантия Л., Мунари Л. М., Ловати Р. (май 2010 г.). «Глатирамера ацетат при рассеянном склерозе». Кокрановская база данных систематических обзоров. 5 (5): CD004678. Дои:10.1002 / 14651858.CD004678.pub2. PMID 20464733.
- ^ Форд С., Гудман А.Д., Джонсон К., Качак Н., Линдси Дж. В., Лисак Р. и др. (Март 2010 г.). «Непрерывная долгосрочная иммуномодулирующая терапия при рецидивирующем рассеянном склерозе: результаты 15-летнего анализа проспективного открытого исследования глатирамера ацетата в США». Рассеянный склероз. 16 (3): 342–50. Дои:10.1177/1352458509358088. ЧВК 2850588. PMID 20106943.
- ^ «Копаксон». MediGuard.
- ^ Крафчик Б.Р. (2011). «Паттерны реакции». В Schachner LA, Hansen RC (ред.). Детская дерматология. Elsevier Health Sciences. п. 1022. ISBN 978-0-7234-3665-2.
- ^ Арнон Р., Села М. (1999). «Химия препарата Копаксон» (PDF). Chem. Израиль. 1: 12–17. Архивировано из оригинал (PDF) на 07.09.2003.
- ^ «Копаксон». Все о рассеянном склерозе.
- ^ Маккидж К. (май 2015 г.). «Глатирамера ацетат 40 мг / мл при рецидивирующе-ремиттирующем рассеянном склерозе: обзор». Препараты ЦНС. 29 (5): 425–32. Дои:10.1007 / s40263-015-0245-z. PMID 25906331. S2CID 30186027.
- ^ Коми Дж., Амато М.П., Бертолотто А., Чентонзе Д., Де Стефано Н., Фарина С. и др. (2016). «Наследие глатирамера ацетата и его использование при рассеянном склерозе». Рассеянный склероз и демиелинизирующие заболевания. 1 (1). Дои:10.1186 / s40893-016-0010-2.
- ^ «Копаксон». CenterWatch.
- ^ «Копаксон Teva одобрен в Великобритании». Фармацевтическое письмо.
- ^ «Глатирамер ацетат». Исследовательская и инженерная компания Тофиг Дару.
- ^ Исаев С., Джафаров Т. (1 мая 2012 г.). «Иран будет производить лекарство от рассеянного склероза». Информационное агентство Trend.
- ^ «Sandoz объявляет о запуске Glatopa в США». Новартис. 2015 г.
- ^ Сильва П. (9 октября 2015 г.). «Новый режим приема копаксона Тева 3 раза в неделю». Новости о рассеянном склерозе сегодня.
- ^ Эрман М., Гровер Д. (3 октября 2017 г.). «Mylan подскакивает, Teva упала после того, как FDA одобрило копию Copaxone». Рейтер. Получено 4 октября 2017.
- ^ «Маркетинговый партнер NATCO Mylan получает окончательное одобрение генерического глатирамера ацетата для версий 20 и 40 мг / мл». NATCO Pharma (Индия). 3 октября 2017 г.. Получено 4 октября 2017.>
- ^ «Sandoz объявляет об одобрении FDA США и выпуске Glatopa 40 мг / мл». Novartis International AG. 13 февраля 2018 г.. Получено 10 мая, 2018.
- ^ «Объем продаж копаксона Teva продолжает расти, несмотря на патентные риски». BioPharmaDive.
- ^ Гельфанд К. «Копаксон». FiercePharma.
- ^ Decker S (1 сентября 2016 г.). «Teva теряет решение о сроке действия патента на копаксон 302». Рынки Bloomberg.
- ^ Декер С., Фланаган С., Бенмелех Ю. (30 января 2017 г.). «Teva проиграла решение о признании недействительными патентов на препарат копаксон». Рынки Bloomberg.
- ^ «Тева теряет патентное решение». Портфель. The Philadelphia Inquirer. Bloomberg News. 2 сентября 2017. с. A12. Получено 23 июня, 2018 - через Newspapers.com (Publisher Extra).
- ^ «Апелляционный суд США оставил в силе постановление об отмене патентов Teva Copaxone». Рейтер. 12 октября 2018 г.. Получено 12 октября, 2018.
- ^ "In Re: Copaxone Consolidated Cases" (PDF). Апелляционный суд Федерального округа США. 12 октября 2018 г.. Получено 12 октября, 2018.
дальнейшее чтение
- «Глатирамера ацетат». Портал информации о наркотиках. Национальная медицинская библиотека США.
