Plerixafor - Википедия - Plerixafor
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Mozobil |
| Другие имена | JM 3100, AMD3100 |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a609018 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Подкожная инъекция |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Связывание с белками | До 58% |
| Метаболизм | Никто |
| Устранение период полураспада | 3–5 часов |
| Экскреция | Почка |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
| Формула | C28ЧАС54N8 |
| Молярная масса | 502.796 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Plerixafor (ГОСТИНИЦА и USAN, торговое наименование Mozobil) является иммуностимулятор используется для мобилизации гемопоэтические стволовые клетки у онкологических больных в кровоток. Затем стволовые клетки извлекаются из крови и пересажен обратно пациенту. Препарат был разработан компанией AnorMED, которую впоследствии купила Genzyme.
Медицинское использование
Мобилизация стволовых клеток периферической крови, которая важна как источник гемопоэтические стволовые клетки за трансплантация, обычно выполняется с использованием колониестимулирующий фактор гранулоцитов (G-CSF), но неэффективен примерно у 15-20% пациентов. Комбинация G-CSF с Plerixafor увеличивает процент людей, которые реагируют на терапию и производят стволовые клетки в количестве, достаточном для трансплантации.[1] Препарат разрешен для пациентов с лимфома и множественная миелома.[2]
Противопоказания
Беременность и период лактации
Исследования на беременных животных показали тератогенный последствия. Поэтому плериксафор противопоказан беременным женщинам, за исключением критических случаев. Фертильным женщинам необходимо употреблять контрацепция. Неизвестно, выделяется ли препарат в грудное молоко. Во время терапии следует прекратить кормление грудью.[2]
Побочные эффекты
Тошнота, понос и местные реакции наблюдались более чем у 10% пациентов. Другие проблемы с пищеварением и общие симптомы, такие как головокружение, головная боль и мышечная боль, также относительно распространены; они были обнаружены более чем у 1% пациентов. Аллергия возникает менее чем в 1% случаев. Большинство побочных эффектов в клинических испытаниях были легкими и преходящими.[2][3]
В Европейское агентство по лекарствам перечислил ряд проблем безопасности, которые необходимо оценить на постмаркетинговой основе, в первую очередь теоретические возможности селезенка разрыв и мобилизация опухолевых клеток. Первая проблема возникла потому, что спленомегалия наблюдался в исследованиях на животных, и в редких случаях Г-КСФ может вызвать разрыв селезенки. Мобилизация опухолевых клеток произошла у пациентов с лейкемией, получавших плериксафор.[4]
Взаимодействия
Исследования взаимодействия не проводились. Тот факт, что плериксафор не взаимодействует с системой цитохрома, указывает на низкий потенциал взаимодействия с другими лекарственными средствами.[2]
Фармакология
Механизм действия
В форме цинкового комплекса плериксафор действует как антагонист (или, возможно, точнее частичный агонист ) альфа хемокиновый рецептор CXCR4 и аллостерический агонист CXCR7.[5]CXCR4 альфа-хемокин рецептор и один из его лиганды, SDF-1, важны в гемопоэтические стволовые клетки возвращение к Костный мозг И в гемопоэтические стволовые клетки покой. В in vivo эффект plerixafor в отношении убиквитин, альтернативный эндогенный лиганд CXCR4, неизвестен. Было обнаружено, что Plerixafor является сильным индуктором мобилизации гемопоэтические стволовые клетки из костного мозга в кровоток как стволовые клетки периферической крови.[6] Кроме того, плериксафор ингибирует CD20 экспрессия на В-клетках путем вмешательства в ось CXCR4 / SDF1, которая регулирует его экспрессию.[нужна цитата ]
Фармакокинетика
Следующий подкожная инъекция, plerixafor быстро всасывается, и пиковые концентрации достигаются через 30-60 минут. До 58% связывается с белками плазмы, остальное в основном находится в внесосудистые отсеки. Препарата нет метаболизируется в значительных количествах; нет взаимодействия с цитохром P450 ферменты или Р-гликопротеины был найден. Период полураспада в плазме составляет от 3 до 5 часов. Plerixafor выводится через почки, при этом 70% препарата выводится в течение 24 часов.[2]
Химия
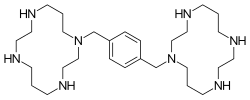
Plerixafor - это макроциклическое соединение и бициклам производное, причем кольца циклама связаны у аминовых атомов азота 1,4-ксилил распорка.[1] Это сильный основание; все восемь атомов азота принимают протоны охотно. Два макроциклических кольца образуют хелатные комплексы с ионами двухвалентных металлов, особенно цинк, медь и никель, а также кобальт и родий. Биологически активной формой плериксафора является его цинковый комплекс.[7]
Синтез
Три из четырех атомов азота макроцикла циклам ... (1,4,8,11-тетраазациклотетрадекан) защищены с помощью тозил группы. Продукт обрабатывают 1,4-бис (бромметил) бензолом и карбонат калия в ацетонитрил. После отщепления тозильных групп бромистоводородная кислота, получается плерикса для октагидробромида.[8].
История
Молекула была впервые синтезирована в 1987 году для проведения фундаментальных исследований редокс химия диметаллических координационных соединений.[9] Тогда это было по счастливой случайности обнаружил другим химиком, что такая молекула может иметь потенциальное применение при лечении ВИЧ из-за ее роли в блокировании CXCR4, хемокинового рецептора, который действует как корецептор для определенных штаммов ВИЧ (наряду с основными клеточными вирусами). рецептор, CD4).[10] Разработка этого показания была прекращена из-за отсутствия пероральной доступности и сердечный беспорядки. Дальнейшие исследования привели к новому показанию для онкологических больных.[10]
Общество и культура
Plerixafor имеет орфанный препарат статус в Соединенных Штатах и Европейском Союзе для мобилизации гемопоэтические стволовые клетки. Он был одобрен США. Управление по контролю за продуктами и лекарствами (FDA) по этому показанию 15 декабря 2008 г.[11] В Евросоюзе препарат был одобрен после положительного Комитет по лекарственным средствам для человека оценочный отчет от 29 мая 2009 г.[4] Препарат был одобрен для использования в Канаде Министерство здравоохранения Канады 8 декабря 2011 г.[12]
Исследование
Противораковые свойства
В нескольких исследованиях было замечено, что Plerixafor снижает метастазирование у мышей.[13] Также было показано, что он уменьшает рецидивы глиобластома в модели мыши после лучевой терапии. В этой модели раковые клетки, которые пережили облучение, критически зависели от клеток, полученных из костного мозга, для васкулогенеза, и рекрутирование последних опосредовано взаимодействиями SDF-1 CXCR4, которые блокируются плериксафором.[14]
Использование в исследованиях стволовых клеток
Исследователи Имперского колледжа продемонстрировали, что plerixafor в сочетании с фактор роста эндотелия сосудов (VEGF) может мобилизовать мезенхимальные стволовые клетки и эндотелиальные клетки-предшественники в периферическую кровь мышей.[15]
В двойном слепом рандомизированном плацебо-контролируемом исследовании мобилизация стволовых клеток с помощью плериксафора не улучшила заживление ишемических диабетических ран.[16].
Неврологический
Блокада CXCR4 передача сигналов с помощью plerixafor также неожиданно оказалась эффективной в противодействии гипералгезия, вызванная опиоидами произведено хроническим лечением с морфий, хотя пока проводились только исследования на животных.[17]
Рекомендации
- ^ а б «Плериксафор». Лекарства в исследованиях и разработках. 8 (2): 113–119. 2007. Дои:10.2165/00126839-200708020-00006. PMID 17324009.
- ^ а б c d е Haberfeld, H, ed. (2009). Кодекс Австрии (на немецком языке) (изд. 2009/2010). Вена: Österreichischer Apothekerverlag. ISBN 978-3-85200-196-8.
- ^ Вагстафф, А. Дж. (2009). «Plerixafor: у пациентов с неходжкинской лимфомой или множественной миеломой». Наркотики. 69 (3): 319–26. Дои:10.2165/00003495-200969030-00007. PMID 19275275.
- ^ а б «Отчет об оценке CHMP для Mozobil» (PDF). Европейское агентство по лекарствам.
- ^ Калацкая, И .; Berchiche, Y.A .; Гравий, С .; Limberg, B.J .; Rosenbaum, J. S .; Хевекер, Н. (2009). «AMD3100 представляет собой лиганд CXCR7 со свойствами аллостерического агониста». Молекулярная фармакология. 75 (5): 1240–7. Дои:10,1124 / моль. 108,053389. PMID 19255243. S2CID 28540154.
- ^ Cashen, A. F .; Nervi, B .; Диперсио, Дж. (2007). «AMD3100: антагонист CXCR4 и агент быстрой мобилизации стволовых клеток». Будущая онкология. 3 (1): 19–27. Дои:10.2217/14796694.3.1.19. PMID 17280498.
- ^ Esté, J. A .; Cabrera, C .; De Clercq, E .; Struyf, S .; Van Damme, J .; Bridger, G .; Skerlj, R.T .; Abrams, M. J .; Henson, G .; Gutierrez, A .; Clotet, B .; Schols, D. (1999). «Активность различных производных бициклама против вируса иммунодефицита человека зависит от их взаимодействия с хемокиновым рецептором CXCR4». Молекулярная фармакология. 55 (1): 67–73. Дои:10,1124 / моль. 55.1.67. PMID 9882699.
- ^ Bridger, G .; и другие. (1993). "Связанные циклические полиамины с активностью против ВИЧ. WO / 1993/012096".[постоянная мертвая ссылка ]
- ^ Ciampolini, M .; Fabbrizzi, L .; Perotti, A .; Poggi, A .; Seghi, B .; Занобини, Ф. (1987). «Комплексы диникеля и дикоппера с N, N-связанными бис (цикламовыми) лигандами. Идеальная система для исследования электростатических эффектов на окислительно-восстановительное поведение пар ионов металлов». Неорганическая химия. 26 (21): 3527–3533. Дои:10.1021 / ic00268a022.
- ^ а б Davies, S.L .; Serradell, N .; Bolós, J .; Байес, М. (2007). «Плериксафор гидрохлорид». Наркотики будущего. 32 (2): 123. Дои:10.1358 / DOF.2007.032.02.1071897.
- ^ «Mozobil одобрен для лечения неходжкинской лимфомы и множественной миеломы» (Пресс-релиз). Ежемесячная справка по назначению. 18 декабря 2008 г. Архивировано с оригинал 6 января 2009 г.. Получено 3 января, 2009.
- ^ Уведомление о соответствии
- ^ Smith, M. C. P .; Luker, K. E .; Garbow, J. R .; Prior, J. L .; Jackson, E .; Piwnica-Worms, D .; Люкер, Г. Д. (2004). «CXCR4 регулирует рост как первичного, так и метастатического рака груди». Исследования рака. 64 (23): 8604–8612. Дои:10.1158 / 0008-5472.CAN-04-1844. PMID 15574767.
- ^ Kioi, M .; Vogel, H .; Schultz, G .; Hoffman, R.M .; Harsh, G.R .; Браун, Дж. М. (2010). «Ингибирование васкулогенеза, но не ангиогенеза, предотвращает рецидив глиобластомы у мышей после облучения». Журнал клинических исследований. 120 (3): 694–705. Дои:10.1172 / JCI40283. ЧВК 2827954. PMID 20179352.
- ^ Pitchford, S .; Furze, R .; Jones, C .; Wengner, A .; Ранкин, С. (2009). «Дифференциальная мобилизация подмножеств клеток-предшественников из костного мозга». Стволовая клетка клетки. 4 (1): 62–72. Дои:10.1016 / j.stem.2008.10.017. HDL:10044/1/23497. PMID 19128793.
- ^ Бонора, Бенедетта Мария; Каппеллари, Роберта; Маццукато, Марта; Ригато, Мауро; Грассо, Марко; Менеголо, Мирко; Бруттокао, Андреа; Авогаро, Анджело; Фадини, Джан Паоло (2020). «Мобилизация стволовых клеток с помощью plerixa для и заживления диабетических ишемических ран: фаза IIA, рандомизированное, двойное слепое, плацебо-контролируемое исследование». Трансляционная медицина стволовых клеток. 9 (9): 965–973. Дои:10.1002 / sctm.20-0020. S2CID 219285881.
- ^ Уилсон Н.М., Юнг Х., Рипш М.С., Миллер Р.Дж., Уайт Ф.А. (март 2011 г.). «Передача сигналов CXCR4 опосредует индуцированную морфином тактильную гипералгезию». Мозг, поведение и иммунитет. 25 (3): 565–73. Дои:10.1016 / j.bbi.2010.12.014. ЧВК 3039030. PMID 21193025.
внешняя ссылка
- «Плериксафор». Портал информации о наркотиках. Национальная медицинская библиотека США.
- MeSH JM + 3100
