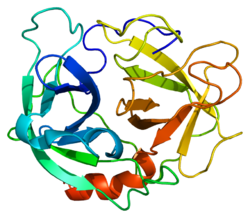
Нейтрофильная эластаза - Neutrophil elastase
Нейтрофильная эластаза (EC 3.4.21.37, лейкоцитарная эластаза, ELANE, ELA2, эластаза 2, нейтрофил, elaszym, сериновая эластаза, подтип эластаза лейкоцитов человека (HLE)) представляет собой серин протеиназа в той же семье, что и химотрипсин и имеет широкую субстратную специфичность. Секретируемый нейтрофилами и макрофагами во время воспаления, он уничтожает бактерии и ткани хозяина.[5] Он также локализуется на внеклеточные ловушки нейтрофилов (NET), благодаря высокому сродству к ДНК, необычному свойству для сериновых протеаз.[6]
Как и другие сериновые протеиназы, он содержит систему реле заряда, состоящую из каталитическая триада из гистидин, аспартат, и серин остатки, которые распределены по всей первичной последовательности полипептида, но собраны вместе в трехмерной конформации свернутого белка. Ген, кодирующий эластазу нейтрофилов, ELA2, состоит из пяти экзоны. Эластаза нейтрофилов тесно связана с другими цитотоксическими иммунными сериновыми протеазами, такими как гранзимы и катепсин G. Это более отдаленно связано с пищеварительной системой. CELA1.[6]
Нейтрофильная форма эластазы (EC 3.4.21.37 ) составляет 218 аминокислоты длинный, с двумя аспарагин -связанный углевод цепи (см. гликозилирование ). Он присутствует в азурофил гранулы в нейтрофил цитоплазма. По-видимому, существует две формы эластазы нейтрофилов, названные IIa и IIb.
Ген
У человека эластаза нейтрофилов кодируется ELANE ген, который находится на хромосоме 19.[7]
Функция
Эластазы образуют подсемейство сериновых протеаз, которые гидролизуют многие белки в дополнение к эластину. У людей есть шесть генов эластазы, которые кодируют структурно похожие белки эластазы 1, 2, 2A, 2B, 3A и 3B. Эластаза нейтрофилов гидролизует белки в специализированных лизосомах нейтрофилов, называемых азурофильные гранулы, а также белки внеклеточного матрикса после высвобождения белка из активированных нейтрофилов. Эластаза нейтрофилов может играть роль в дегенеративных и воспалительных заболеваниях за счет протеолиза коллагена-IV и эластина внеклеточного матрикса. Этот белок разрушает белок А внешней мембраны (OmpA) E. coli, а также факторы вирулентности таких бактерий, как Shigella, Salmonella и Yersinia.[8] Мутации в этом гене связаны с циклическая нейтропения (CyN) и тяжелая врожденная нейтропения (SCN). Этот ген сгруппирован с другими членами семейства генов сериновых протеаз, генами азуроцидина 1 и протеиназы 3, на хромосоме 19pter. Все 3 гена экспрессируются скоординированно, и их белковые продукты упаковываются вместе в азурофильные гранулы во время дифференцировки нейтрофилов.[9]
Клиническое значение
Нейтрофильная эластаза - важный фермент протеазы, который при аберрантной экспрессии может вызывать эмфизема или эмфизематозные изменения. Это включает в себя нарушение структуры легких и увеличение воздушного пространства. Мутации ELANE генная причина циклический и суровый врожденный нейтропения, что является неспособностью нейтрофилов созреть.[10] В 2019 году исследование подтвердило, что ELANE делеция не вызывает нейтропении.[11]
Ингибиторы
Чтобы минимизировать повреждение тканей, существует несколько ингибиторов эластазы нейтрофилов. Одна группа ингибиторов - это Серпины (Ингибиторы сериновых протеаз).[12] Было показано, что эластаза нейтрофилов взаимодействовать с Альфа 2-антиплазмин, который принадлежит к семейству белков Serpin.[13][14]
Смотрите также
Рекомендации
- ^ а б c ENSG00000197561 GRCh38: Общий выпуск 89: ENSG00000277571, ENSG00000197561 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000020125 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Белаауадж А., Ким К.С., Шапиро С.Д. (август 2000 г.). «Деградация белка А внешней мембраны при уничтожении Escherichia coli эластазой нейтрофилов». Наука. 289 (5482): 1185–8. Дои:10.1126 / science.289.5482.1185. PMID 10947984.
- ^ а б Thomas MP, Whangbo J, McCrossan G, Deutsch AJ, Martinod K, Walch M, Lieberman J (июнь 2014 г.). «Связывание протеазы лейкоцитов с нуклеиновыми кислотами способствует ядерной локализации и расщеплению белков, связывающих нуклеиновые кислоты». J. Immunol. 192 (11): 5390–7. Дои:10.4049 / jimmunol.1303296. ЧВК 4041364. PMID 24771851.
- ^ Takahashi H, Nukiwa T, Yoshimura K, Quick CD, States DJ, Holmes MD, Whang-Peng J, Knutsen T., Crystal RG (октябрь 1988 г.). «Структура гена эластазы нейтрофилов человека». J. Biol. Chem. 263 (29): 14739–47. PMID 2902087.
- ^ Weinrauch Y, Drujan D, Shapiro SD, Weiss J, Zychlinsky A (май 2002 г.). «Нейтрофильная эластаза нацелена на факторы вирулентности энтеробактерий». Природа. 417 (6884): 91–4. Дои:10.1038 / 417091a. PMID 12018205. S2CID 4341470.
- ^ «Энтрез Ген: ELA2 эластаза 2, нейтрофил».
- ^ Дейл, округ Колумбия, Линк, округ Колумбия (январь 2009 г.). «Множество причин тяжелой врожденной нейтропении». N. Engl. J. Med. 360 (1): 3–5. Дои:10.1056 / NEJMp0806821. ЧВК 4162527. PMID 19118300.
- ^ Хорвиц М.С., Лаурино М.Ю., Кил С.Б. (август 2019 г.). "Мутация делеции целого гена ELANE". Кровавые достижения. 3 (16): 2470–2473. Дои:10.1182 / bloodadvances.2019000498. ЧВК 6712528. PMID 31427279.
- ^ Коркмаз Б., Хорвиц М.С., Дженн Д.Е., Готье Ф. (декабрь 2010 г.). «Нейтрофильная эластаза, протеиназа 3 и катепсин G в качестве терапевтических мишеней при заболеваниях человека». Pharmacol. Rev. 4 (62): 726–59. Дои:10.1124 / пр.110.002733. ЧВК 2993259. PMID 21079042.
- ^ Брауэр MS, Harpel PC (август 1982 г.). «Протеолитическое расщепление и инактивация ингибитора альфа-2-плазмина и инактиватора С1 полиморфно-ядерной лейкоцитарной эластазой человека». J. Biol. Chem. 257 (16): 9849–54. PMID 6980881.
- ^ Шие Б.Х., Трэвис Дж. (Май 1987 г.). «Реактивный сайт человеческого альфа-2-антиплазмина». J. Biol. Chem. 262 (13): 6055–9. PMID 2437112.
дальнейшее чтение
- Дейл Д.К., Лайлс В.К., Гарвич Д., Априкян А.Г. (2001). «Клинические последствия мутаций эластазы нейтрофилов при врожденной и циклической нейтропении». J. Pediatr. Гематол. Онкол. 23 (4): 208–10. Дои:10.1097/00043426-200105000-00005. PMID 11846296.
- Хорвиц М., Бенсон К.Ф., Дуан З., Лицо Р.Э., Векслер Дж., Уильямс К., Албани Д., Ли Ф.К. (2003). «Роль нейтрофильной эластазы в синдромах недостаточности костного мозга: молекулярно-генетическое возрождение гипотезы халона». Curr. Мнение. Гематол. 10 (1): 49–54. Дои:10.1097/00062752-200301000-00008. PMID 12483111. S2CID 22277675.
- Анклифф П.Дж., Гейл Р.Э., Линч, округ Колумбия (2003). «Мутации нейтрофильной эластазы при врожденной нейтропении». Гематология. 8 (3): 165–71. Дои:10.1080/1024533031000107497. PMID 12745650. S2CID 19283939.
- Хорвиц М., Бенсон К.Ф., Дуан З., Ли Ф.К., Человек RE (2004). «Наследственная нейтропения: собаки объясняют мутации эластазы нейтрофилов человека». Тенденции Мол Мед. 10 (4): 163–70. Дои:10.1016 / молмед.2004.02.002. PMID 15059607.
внешняя ссылка
- GeneReviews / NCBI / NIH / UW запись о нейтропении, связанной с ELANE
- Нейтрофил + эластаза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P08246 (Нейтрофильная эластаза) в PDBe-KB.