Paracoccidioides brasiliensis - Paracoccidioides brasiliensis
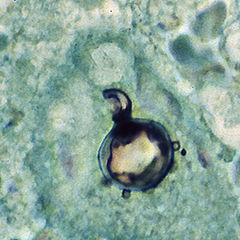
| Paracoccidioides brasiliensis | |
|---|---|
 | |
| Научная классификация | |
| Королевство: | |
| Разделение: | |
| Учебный класс: | |
| Заказ: | |
| Семья: | |
| Род: | |
| Разновидность: | P. brasiliensis |
| Биномиальное имя | |
| Paracoccidioides brasiliensis (Великолепно. ) Ф.П. Алмейда (1930) | |
| Синонимы | |
Zymonema brasiliensis Великолепно. (1912) | |
Paracoccidioides brasiliensis это диморфный гриб и один из двух видов, вызывающих паракокцидиоидомикоз (другое существо Paracoccidioides lutzii ).[1][2][3][4] Грибок был связан с семьей Ajellomycetaceae (разделение Аскомикота ) хотя сексуальное состояние или телеоморф пока не найден.[5]
История
Paracoccidioides brasiliensis был впервые обнаружен Адольфо Лутц в 1908 году в Бразилии.[6] Хотя Лутц не предложил названия болезни, вызываемой этим грибком, он отметил структуры, которые он назвал «псевдококцидными», вместе с мицелием в культурах, выращенных при 25 ° C.[6] В 1912 году Альфонс Сплендор[7] предложил название Зимонема бразильская и описаны особенности гриба в культуре.[6] Наконец, в 1930 году Флориано де Алмейда создал род Paracoccidioides для размещения вида, отмечая его отличие от Coccidioides immitis.[6]
Физиология
Paracoccidioides brasiliensis нефотосинтетический эукариот с жесткой клеточной стенкой и органеллами, очень похожими на таковые у высших эукариот.[3][8] Быть диморфный гриб, он имеет способность выращивать овальную дрожжеподобную форму при 37 ° C и удлиненную мицелиальную форму, полученную при комнатной температуре.[9] Фазы мицелия и дрожжей различаются по своей морфологии, биохимии и ультраструктуре.[8] Дрожжевая форма содержит большое количество α- (1,3) -связанного глюкана.[10][11] Содержание хитина в мицелиальной форме больше, чем в дрожжевой, но содержание липидов в обеих фазах сопоставимо.[10]Дрожжи размножаются бесполым путем. подающий надежды, где дочерние клетки асинхронно переносятся в нескольких случайных положениях по поверхности клетки. Почки начинаются слоями клеточной стенки, оптическая плотность которых увеличивается в точке, которая в конечном итоге дает начало дочерней клетке.[3] После того, как зачаток расширился, между растущей клеткой и материнской клеткой развивается плоскость дробления. После расхождения шрам от бутона исчезает.[8] В ткани почкование происходит внутри гранулематозный центр поражения, что визуализируется окрашиванием гематоксилином и эозином (H&E) гистологических срезов.[10] Клетки, не имеющие бутонов, имеют диаметр 5–15 мкм, тогда как клетки с множеством сферических зачатков имеют диаметр от 10 до 20 мкм.[10] При электронной микроскопии было обнаружено, что клетки с множественными зачатками имеют периферически расположенные ядра и цитоплазму, окружающую большую центральную вакуоль.[12] В тканевой форме P. brasiliensis, дрожжевые клетки больше, с более тонкими стенками и более узким основанием почек, чем у родственных диморфных грибов, Бластомикоз дерматит.[10] Дрожжеподобная форма P. brasiliensis содержит несколько ядер, пористую двухслойную ядерную мембрану и толстую клеточную стенку, богатую волокнами, тогда как мицелиальная фаза имеет более тонкие клеточные стенки с тонким электронно-плотным внешним слоем.[8]
Диморфизм
Мицелиальная форма P. brasiliensis можно преобразовать в дрожжевую форму in vitro ростом на агар для инфузий мозга и сердца или агар с глюкозой и цистеином в крови при инкубации в течение 10–20 дней при 37 ° C.[10] В этих условиях клетки гиф либо погибают, либо преобразуются в переходные формы диаметром 6–30 мкм, которые в конечном итоге отделяются или остаются на клетках гиф, давая почки.[10] Развиваются новые бутоны мезосомы и стали многоядерными.[10] Напротив, дрожжеподобные культуры можно преобразовать в мицелиальную форму, снизив температуру инкубации с 37 до 25 ° C.[13] Первоначально потребности в питательных веществах дрожжевой и мицелиальной фаз P. brasiliensis считались идентичными;[14] однако более поздние исследования показали, что дрожжевая форма ауксотрофный, требующие для роста экзогенные серосодержащие аминокислоты, включая цистеин и метионин.[15]
Экология
Хотя среда обитания P. brasiliensis остается неизвестным, это обычно связано с почвами, на которых выращивают кофе.[5][16][17] Это также было связано с девятиполосный броненосец, Dasypus novemcinctus.[18] Заболевание, вызванное P. brasiliensis в основном географически ограничен странами Латинской Америки, такими как Бразилия, Колумбия, и Венесуэла, с наибольшим количеством случаев в Бразилии.[10] Эндемичные районы характеризуются жарким влажным летом, сухой умеренной зимой, среднегодовыми температурами от 17 до 23 ° C и годовым количеством осадков от 500 до 800 мм.[19] Однако точные экологические закономерности гриба остаются неуловимыми, и P. brasiliensis редко встречается в природе за пределами человеческого хозяина.[3] Об одном таком редком примере экологической изоляции сообщила в 1971 году Мария Б. де Альборнос и ее коллеги, которые изолировали P. brasiliensis из образцов сельской почвы, собранных в Paracotos в состоянии Миранда, Венесуэла.[20] В in vitro Исследования показали, что грибок растет при заражении почвой и стерильными экскрементами лошади или коровы.[21] Также было показано, что мицелиальная фаза выживает дольше, чем дрожжевая фаза в кислой почве.[22] Несмотря на то, что сексуальное состояние не было задокументировано, молекулярные исследования предполагают существование рекомбинирующих популяций P. brasiliensisпотенциально посредством неизвестного сексуального состояния.[23]
Эпидемиология
P. brasiliensis вызывает болезнь, известную как паракокцидиоидомикоз характеризуется медленными прогрессирующими гранулематозными изменениями слизистой оболочки головы, особенно носа и носовых пазух или кожи. В редких случаях заболевание поражает лимфатическую систему, центральную нервную систему, желудочно-кишечный тракт или скелетную систему.[10] Из-за высокой доли случаев поражения слизистой оболочки полости рта первоначально считалось, что эти ткани являются основным путем проникновения грибка.[3] Тем не менее, убедительные доказательства указывают на то, что дыхательные пути являются главной точкой входа.[10] и P. brasiliensis поражения легких встречаются почти в трети прогрессирующих случаев.[24] Заболевание не заразно.[10]Паракокцидиоидомикоз чаще встречается у взрослых мужчин, чем у женщин.[10][25] Гормон эстроген считается, что ингибирует преобразование мицелия в дрожжевую форму, что подтверждается in vitro экспериментальные данные, и этот фактор может объяснить относительную устойчивость женщин к инфекции.[26]
Обнаружение и наблюдение
Номер серологические тесты были использованы для диагностики паракокцидиоидомикоза.[10] Двойная диффузия в геле агара и тест фиксации комплемента, являются одними из наиболее часто используемых тестов в серодиагностике.[10] Экстракты культур дрожжей или мицелия используются для производства эффективных, быстрых и воспроизводимых антигенов.[10][27] В исследовании сообщается об обнаружении антигена 43 кДа в объединенных сыворотках пораженных людей, что может послужить основой для разработки диагностического теста.[28] Тесты на наличие сывороточных антител к P. brasiliensis одновременно обнаруживают как активные, так и исторические инфекции и не могут отличить активную инфекцию. Оценка популяций в эндемичных зонах показала примерно равные уровни сероконверсии между мужчинами и женщинами, что предполагает равные уровни воздействия, несмотря на сильное преобладание мужчин, показанное клиническим заболеванием.[10]
Клинические проявления
P. brasiliensis вызывает изъязвление слизистой оболочки рта и носа с распространением через лимфатическая система. Гипотеза о попадании грибка в организм проходит через пародонтальная мембрана.[29][30] Предполагается, что путь заражения вдыхание после чего инфекционный отросток дает начало характерным многополярным почкующимся дрожжевым формам в легких, напоминающим "штурвал "видно на гистологических срезах.[9][31] Риску заражения подвержены как иммунологически нормальные, так и ослабленные люди.[9]Наиболее часто инфицированными тканями являются легкие, лимфатические узлы и слизистая оболочка рта.[10] Патологические признаки паракокцидиоидомикоза аналогичны тем, которые наблюдаются при кокцидиоидомикоз и бластомикоз.[32] Однако в первом случае поражения сначала появляются в лимфоидной ткани, а затем распространяются на слизистые оболочки,[32] вызывая локализованный диффузный некроз тканей лимфатических узлов.[32] Обычно обширное поражение лимфоидной ткани и ограниченное распространение желудочно-кишечного тракта, костей и простаты отличают клиническую картину паракокцидиоидомикоза от таковой при бластомикозе.[10][32]
Рекомендации
- ^ Мартинес, Роберто; Моретти, Мария Луиза; Камарго, Зойло Пирес де; Хури, Зарифа; Дурлахер, Руи Рафаэль; Хан, Розане; Кавальканте, Рикардо де Соуза; Перейра, Рикардо Мендес; Сильва-Вергара, Марио Леон (сентябрь 2017 г.). «Бразильское руководство по клиническому лечению паракокцидиоидомикоза». Revista da Sociedade Brasileira de Medicina Tropical. 50 (5): 715–740. Дои:10.1590/0037-8682-0230-2017. ISSN 0037-8682. PMID 28746570.
- ^ Райан, KJ (2004). Шеррис Медицинская микробиология (4-е изд.). Макгроу Хилл. п. 683. ISBN 0-8385-8529-9.
- ^ а б c d е Панамериканская организация здравоохранения. Научная публикация № 254 (1971). Паракокцидиоидомикоз (1-е изд.). Вашингтонская Панамериканская организация здравоохранения. п. 325.
- ^ Браммер Э., Кастанеда Э., Рестрепо А (1993). «Паракокцидиоидомикоз: новости». Clin. Microbiol. Rev. 6 (2): 89–117. Дои:10,1128 / см. 6.2.89. ЧВК 358272. PMID 8472249.
- ^ а б Багагли Э., Теодоро Р.С., Боско С.М. и др. (2008). "Paracoccidioides brasiliensis: филогенетические и экологические аспекты ». Микопатология. 165 (4–5): 197–207. Дои:10.1007 / s11046-007-9050-7. PMID 18777629.
- ^ а б c d Lacaz, CS; Франко (1994). «Историческая эволюция знаний о паракокцидиоидомикозе и его этиологическом агенте, Paracoccidioides brasiliensis». Бока-Ратон: CRC Press: 1–11. Цитировать журнал требует
| журнал =(помощь) - ^ http://www.whonamedit.com/doctor.cfm/1534.html
- ^ а б c d Карбонелл, Луис М. (1963). «Ультраструктура Paracoccidiodes brasiliensis». Mycopathologia et Mycologia Applicata. 19 (3): 184–204. Дои:10.1007 / bf02051247. ISSN 0027-5530. PMID 14045074.
- ^ а б c Рейсс, Э (2011). Фундаментальная медицинская микология. Нью-Джерси: Уайли-Блэквелл: Хобокен. п. 624. ISBN 9780470177914.
- ^ а б c d е ж грамм час я j k л м п о п q р s Kwon-Chung, K.J; Беннетт, Джон Э (1992). Медицинская микология. Филадельфия: Филадельфия: Леа и Фебигер. ISBN 0812114639.
- ^ Канетсуна, Ф; и другие. (1969). «Состав клеточной стенки дрожжевых и мицелиальных форм Paracoccidioides brasiliensis". J. Bacteriol. 97 (3): 1036–1041. ЧВК 249811. PMID 5776517.
- ^ Фуртадо, J.S; Фреймуллер Э. (1967). «Структура и воспроизведение Paracoccidioides brasiliensis в тканях человека ». Sabouraudia. 5 (3): 226–229. Дои:10.1080/00362176785190431. PMID 6036228.
- ^ Рамирес-Мартинес, Дж. Р. (1971). "Paracoccidioides brasiliensis: Превращение дрожжеподобных форм в мицелий в погруженной культуре ». J. Bacteriol. 105 (2): 523–526. ЧВК 248414. PMID 5541529.
- ^ Джиларди, Г.Л (1965). «Питание систематических и подкожных патогенных грибов». Бактериол. Rev. 29 (3): 406–424. ЧВК 441289. PMID 5318450.
- ^ Париж, S; Дюран-Гонсалес С. (1985). "Исследования питания на Paracoccidioides brasiliensis: роль органической серы в диморфизме ». Sabouraudia. 23 (2): 85–92. Дои:10.1080/00362178585380151. PMID 4012515.
- ^ Фланниган, Брайан (2001). Микроорганизмы в домашних условиях и в рабочей среде: разнообразие, влияние на здоровье, исследования и контроль. Нью-Йорк: Тейлор и Фрэнсис. п. 479. ISBN 9780203302934.
- ^ Terçarioli GR, Bagagli E, Reis GC и др. (2007). «Экологическое исследование Paracoccidioides brasiliensis в почве: способность к росту, образование конидий и молекулярное обнаружение ». BMC Microbiol. 7: 92–99. Дои:10.1186/1471-2180-7-92. ЧВК 2180180. PMID 17953742.
- ^ Багаглы, Эдуардо; Боско, Сандра М.Г .; Теодоро, Ракель Кордейро; Франко, Марчелло (сентябрь 2006 г.). «Филогенетические и эволюционные аспекты Paracoccidioides brasiliensis свидетельствуют о длительном сосуществовании с животными-хозяевами, что объясняет некоторые биологические особенности патогена». Инфекция, генетика и эволюция. 6 (5): 344–351. Дои:10.1016 / j.meegid.2005.12.002.
- ^ Борелли, Д. (1969). "Reservareas de algunos Agenttes de micosis". Med. Кутан. Ибер. Лат. Являюсь. 3: 367–370.
- ^ Альборноз, М; Альборноз (1971). "Estudio de la sensibilidad especifica en members de un area endemica a la paracoccidiodomycosis en Venezuela". Микопатология. 45 (2): 65–75. Дои:10.1007 / bf02059246. PMID 5129432.
- ^ Борелли, Д. (1961). "Hipotesis sobre ecologia de Paracoccidioides". Derm. Venez. 3: 130–132.
- ^ Рестрепо, М; и другие. (1969). "Влияние концентрации ионов водорода и температуры на рост Paracoccidioides brasiliensis в почвенной вытяжке ». Sabouraudia. 7 (3): 207–215. Дои:10.1080/00362177085190371. PMID 5385156.
- ^ Matute, D. R .; Эль Аль (24 августа 2005 г.). «Загадочное видообразование и рекомбинация у гриба Paracoccidioides brasiliensis, выявленные генеалогией». Молекулярная биология и эволюция. 23 (1): 65–73. Дои:10.1093 / molbev / msj008. PMID 16151188.
- ^ Лондеро, A.T; Рамос К.Д. (1972). «Паракокцидиоидомикоз: клиническое и микологическое исследование сорока одного случая, наблюдавшегося в Санта-Мария, РС, Бразилия». Являюсь. J. Med. 52 (6): 771–775. Дои:10.1016/0002-9343(72)90083-6. PMID 5030174.
- ^ Рестрепо, М; Рестрепо А (1970). «Паракокцидиомикоз (южноамериканский бластомикоз): исследование 39 случаев, наблюдаемых в Медельине, Колумбия». Являюсь. J. Trop. Med. Hyg. 19 (1): 68–76. Дои:10.4269 / ajtmh.1970.19.68. PMID 4984585.
- ^ Рестрепо, М; и другие. (1984). «Эстрогены ингибируют трансформацию мицелия в дрожжи гриба. Paracoccidioides brasiliensis: значение для устойчивости женщин к паракокцидиоидомикозу ». Заразить. Иммунная. 46 (2): 346–353. ЧВК 261537. PMID 6500694.
- ^ Блумер, С.О .; Джалберт М (1984). «Быстрый и надежный метод производства специфических Paracoccidioides brasiliensis антиген иммунодиффузионного теста ". J. Clin. Микробиол. 19 (3): 404–407. ЧВК 271074. PMID 6425358.
- ^ Мендес-Джаннини, M.J.S; и другие. (1989). «Обнаружение гликопротеина с молекулярной массой 43 000 в сыворотке крови пациентов с паракокцидиоидомикозом». J. Clin. Микробиол. 27 (12): 2842–2845. ЧВК 267138. PMID 2592544.
- ^ Смит Дж. М. (1969). «Микозы пищеварительного тракта». Кишечник. 10 (12): 1035–1040. Дои:10.1136 / гут.10.12.1035. ЧВК 1553013. PMID 4904223.
- ^ Гарсия А.М., Эрнандес О., Аристисабаль Б.Х. и др. (2010). "Анализ экспрессии генов Paracoccidioides brasiliensis переход от конидиума к дрожжевой клетке ». Med. Mycol. 48 (1): 147–154. Дои:10.3109/13693780903055673. PMID 19568977.
- ^ Рестрепо А, МакИвен Дж.Г., Кастаньеда Э. (2001). «Среда обитания Paracoccidioides brasiliensis: как далеко от разгадки загадки?». Med. Mycol. 39 (3): 233–41. Дои:10.1080/714031028. PMID 11446526.
- ^ а б c d Риппон, Джон (1982). Медицинская микология: патогенные грибы и патогенные актиномицеты (2-е изд.). Филадельфия: Сондерс. ISBN 0721675867.
внешняя ссылка
- Paracoccidioides в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- http://botit.botany.wisc.edu/toms_fungi/jan2005.html
