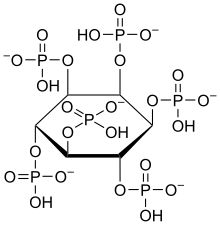
Фитаза - Phytase
А фитаза (мио-инозитол гексакисфосфат фосфогидролаза) представляет собой любой тип фосфатаза фермент, катализирующий гидролиз фитиновая кислота (мио-инозитол гексакисфосфат) - неперевариваемая органическая форма фосфор который содержится во многих тканях растений, особенно в зерна и масличные семена - и выделяет пригодную для использования форму неорганического фосфора.[1] В то время как фитазы обнаруживаются у животных, растений, грибов и бактерий, фитазы чаще всего обнаруживаются и характеризуются с помощью грибов.[2]
История
Первая фитаза растений была обнаружена в 1907 году из риса. отруби[3][4] а в 1908 г. от животного (Телец печень и кровь).[4][5] В 1962 году началась первая попытка коммерциализации фитаз для корма для животных цели улучшения питания, когда Международные минералы и химикаты (IMC) изучили более 2000 микроорганизмов, чтобы найти наиболее подходящие для производства фитазы. Этот проект был запущен частично из-за опасений по поводу того, что добываемые источники неорганического фосфора в конечном итоге закончатся (см. пик фосфора ), которые IMC в то время поставляла для кормовой промышленности. Аспергиллы (фикум) Нигер грибковый напряжение NRRL 3135 (ATCC 66876) был определен как многообещающий кандидат.[6] поскольку он был способен производить большое количество внеклеточных фитаз.[7] Однако работоспособности организма было недостаточно для коммерциализации, поэтому в 1968 году проект закончился провалом.[6]
Тем не менее, выявление A. niger привел в 1984 г. к новой попытке с A. niger мутанты сделано с относительно недавно изобретенным рекомбинантная ДНК технологии. Этот USDA финансируемый проект был инициирован доктором Руди Водзински, который ранее участвовал в проекте IMC.[6] Этот проект 1984 года привел в 1991 году к первой частично клонированный фитаза ген phyA (из A. niger NRRL 31235)[6][8] а затем в 1993 году к клонированию полного гена, и это чрезмерное выражение в А. нигер.[6][9]
В 1991 г. BASF начали продавать первую коммерческую фитазу, произведенную в А. нигер под товарный знак Natuphos который использовался для увеличения содержания питательных веществ в корма для животных.[6]
В 1999 году кишечная палочка бактериальные фитазы были определены как более эффективные, чем A. niger грибковые фитазы.[6][10][11] Впоследствии это привело к использованию в кормах этого нового поколения бактериальных фитаз, которые превосходили грибковые фитазы во многих аспектах.[6]
Классы
В литературе охарактеризованы четыре различных класса фитаз: гистидиновые кислые фосфатазы (HAPS), бета-винтовые фитазы (BPP), пурпурные кислые фосфатазы (PAP),[2] и совсем недавно протеинтирозинфосфатаза -подобные фитазы (PTP-подобные фитазы).[12]
Фосфатазы гистидиновой кислоты (HAP)
Большинство известных фитаз относятся к классу ферментов, называемых гистидинокислыми фосфатазами (HAP). HAP были выделены из мицелиальных грибов, бактерий, дрожжей и растений.[1] Все члены этого класса фитаз имеют общий мотив последовательности активного сайта (Arg-His-Gly-X-Arg-X-Pro) и имеют двухступенчатый механизм, который гидролизует фитиновую кислоту (а также некоторые другие фосфоэфиры).[2] Фитаза из гриба Aspergillus niger представляет собой HAP и хорошо известен своей высокой специфической активностью и коммерческой ролью в качестве кормовой добавки для животных для увеличения биодоступности фосфата из фитиновой кислоты в рационах на основе зерна для домашней птицы и свиней.[13] ГП также сверхэкспрессируется в нескольких трансгенных растениях в качестве потенциального альтернативного метода производства фитазы для производства кормов для животных.[14] и совсем недавно ген фитазы HAP из Кишечная палочка был успешно экспрессирован у трансгенной свиньи.[15]
β-пропеллерные фитазы
β-пропеллерные фитазы составляют недавно открытый класс фитаз. Эти первые образцы этого класса ферментов были первоначально клонированы из Бациллы разновидность,[2] но с тех пор было идентифицировано множество микроорганизмов, продуцирующих β-пропеллерные фитазы. Трехмерная структура фитазы β-пропеллера подобна пропеллеру с шестью лопастями. Текущие исследования показывают, что β-пропеллерные фитазы являются основными ферментами, разлагающими фитат, в воде и почве и могут играть важную роль в круговороте фитата и фосфора.[16]
Фиолетовые кислые фосфатазы
Недавно из семядолей прорастающих соевых бобов была выделена фитаза, имеющая мотив активного центра пурпурной кислой фосфатазы (PAP). Этот класс металлоферментов хорошо изучен, и поиск в геномных базах данных обнаруживает PAP-подобные последовательности у растений, млекопитающих, грибов и бактерий. Однако было обнаружено, что только PAP из соевых бобов обладает какой-либо значительной фитазной активностью. Для PAP определены трехмерная структура, мотив последовательности активного сайта и предполагаемый механизм катализа.[нужна цитата ]
Фитазы, подобные протеинтирозинфосфатазе
Лишь немногие из известных фитаз относятся к надсемейство ферментов, называемых протеинтирозинфосфатазы (PTP). PTP-подобные фитазы, относительно недавно открытый класс фитаз, были выделены из бактерий, которые обычно населяют кишечник жвачных животных.[17] Все охарактеризованные PTP-подобные фитазы имеют общий мотив последовательности активного сайта (His-Cys- (X) 5-Arg), двухступенчатый кислотно-основной механизм дефосфорилирования и активность по отношению к остаткам фосфрилированного тирозина, характеристики, которые являются общими для всех. Ферменты суперсемейства ПТП.[18][19] Как и для многих ферментов суперсемейства PTP, точные биологические субстраты и роль бактериальных PTP-подобных фитаз еще не определены. Охарактеризованные PTP-подобные фитазы из бактерий рубца имеют общую последовательность и структурную гомологию с PTP-подобной фосфоинозитидной / -инозитолфосфатазой PTEN млекопитающих,[12] и значительная гомология последовательности с доменом PTP секретируемый типом III белок вирулентности из Pseudomonas syringae (HopPtoD2).[20]
Биохимические характеристики
Специфичность субстрата
Большинство фитаз проявляют широкую субстратную специфичность, имея способность гидролизовать многие фосфорилированные соединения, которые структурно не похожи на фитиновую кислоту, такие как ADP, АТФ, фенилфосфат, фруктозо-1,6-бисфосфат, глюкозо-6-фосфат, глицерофосфат и 3-фосфоглицерат. Лишь несколько фитаз были описаны как высокоспецифичные для фитиновой кислоты, например фитазы из Бациллы sp., Аспергиллы sp., Кишечная палочка[21] и те фитазы, которые принадлежат к классу PTP-подобных фитаз[18]
Пути дефосфорилирования фитиновой кислоты
Фитиновая кислота имеет шесть фосфатных групп, которые могут высвобождаться фитазами с разной скоростью и в разном порядке. Фитазы поэтапно гидролизуют фосфаты из фитиновой кислоты, давая продукты, которые снова становятся субстратами для дальнейшего гидролиза. Большинство фитаз способны отщеплять пять из шести фосфатных групп от фитиновой кислоты. Фитазы были сгруппированы на основе первого фосфатного положения фитиновой кислоты, которая подвергается гидролизу. Комитет по номенклатуре ферментов Международного союза биохимиков признает три типа фитаз в зависимости от положения первого гидролизованного фосфата, а именно: 3-фитаза (EC 3.1.3.8 ), 4-фитаза (EC 3.1.3.26 ), и 5-фитаза (EC 3.1.3.72 ). На сегодняшний день большинство известных фитаз - это 3-фитазы или 4-фитазы,[21] только ГАП, очищенный от пыльцы лилии[22] и PTP-подобная фитаза из Selenomonas ruminantium subsp. lactilytica[20] были определены как 5-фитазы.
Биологическое значение
Фитиновая кислота и его метаболиты играют несколько важных ролей в семенах и зернах, в первую очередь, фитиновая кислота действует как хранилище фосфора, как хранилище энергии, как источник катионов и как источник мио-инозита (предшественника клеточной стенки). Фитиновая кислота является основной формой хранения фосфора в семенах растений и основным источником фосфора в зерновых рационах, используемых при интенсивном животноводстве. Органический фосфат, содержащийся в фитиновой кислоте, в основном недоступен для животных, которые его потребляют, но неорганический фосфат, выделяемый фитазами, может легко абсорбироваться. Жвачные животные животные могут использовать фитиновую кислоту в качестве источника фосфора, потому что бактерии, населяющие их кишечник, являются хорошо изученными продуцентами многих типов фитаз. Однако животные с однокамерным желудком не являются носителями бактерий, продуцирующих фитазу, таким образом, эти животные не могут использовать фитиновую кислоту в качестве основного источника фосфора, и она выводится с калом.[23] Однако человек - особенно вегетарианцы и веганы из-за повышенной адаптации микробиома кишечника - в кишечнике могут быть микробы, которые могут производить фитазу, расщепляющую фитиновую кислоту.[24]
Фитиновая кислота и ее метаболиты играют еще несколько важных ролей в Эукариотический физиологические процессы. Таким образом, фитазы, которые гидролизуют фитиновую кислоту и ее метаболиты, также играют важную роль. Фитиновая кислота и ее метаболиты участвуют в репарации ДНК, клатрин -покрытый рециклинг пузырьков, контроль нейротрансмиссии и пролиферации клеток.[25][26][27] Точная роль фитаз в регуляции фитиновой кислоты и ее метаболитов и, как следствие, роль в физиологических процессах, описанных выше, все еще в значительной степени неизвестны и являются предметом многочисленных исследований.
Сообщалось, что фитаза вызывает гиперчувствительный пневмонит у человека, подвергшегося воздействию при добавлении фермента в корм для крупного рогатого скота.[28][29]
Сельскохозяйственное и промышленное использование
Фитаза вырабатывается бактериями, обнаруженными в кишечнике жвачный животных (крупный рогатый скот, овцы), что позволяет им использовать фитиновая кислота содержится в зернах как источник фосфора.[30] Нежвачные животные (однокамерный животные), такие как люди, собаки, свиньи, птицы и т. д., не производят фитазу. Исследования в области питания животных выдвинули идею дополнения кормов фитазой, чтобы сделать доступными для животных питательные вещества, связанные с фитатом, такие как кальций, фосфор, минералы, углеводы, аминокислоты и белки.[31] В Канаде генетически модифицированная свинья под названием Enviropig, который способен производить фитазу в основном через слюнные железы, был разработан и одобрен для ограниченного производства.[32][33]
Фитаза используется в качестве добавки к корму для животных - часто у домашней птицы и свиней - для улучшения питательная ценность растительного материала путем высвобождения неорганического фосфата из фитиновой кислоты (мио-инозитол гексакисфосфат). Фитазу можно очистить от трансгенный микробы и недавно был получен в трансгенных канола, люцерна и рис растения.[34]
Смотрите также
Рекомендации
- ^ а б Маллэйни Э.Дж., Дейли С.Б., Улла А.Х. (2000). Достижения в исследованиях фитазы. Adv Appl Microbiol. Успехи прикладной микробиологии. 47. С. 157–199. Дои:10.1016 / S0065-2164 (00) 47004-8. ISBN 9780120026470. PMID 12876797.
- ^ а б c d Маллани Э.Дж., Уллах А.Х. (2003). «Термин фитаза включает несколько различных классов ферментов». Biochem Biophys Res Commun. 312 (1): 179–184. Дои:10.1016 / j.bbrc.2003.09.176. PMID 14630039.
- ^ Suzuki, U .; Yoshimura, K .; Такаиши, М. (1907). "Убер-энзим" Фитаза "das anhydro-oxy-methylen diphosphorsaure" spalter " [О ферменте «фитаза», расщепляющем ангидро-оксиметилендифосфорную кислоту] (PDF). Бюллетень сельскохозяйственного колледжа Императорского университета Токио. 7: 502–512.
- ^ а б Кумар, В .; Sinha, A.K .; Маккар, Х. П. С .; Беккер, К. (15.06.2010). «Диетические роли фитата и фитазы в питании человека: обзор». Пищевая химия. 120 (4): 945–959. Дои:10.1016 / j.foodchem.2009.11.052. ISSN 0308-8146.
- ^ McCollum, E.V .; Харт, Э. (1908). «О возникновении фермента, расщепляющего фитин, в тканях животных» (PDF). Журнал биологической химии. 4: 497–500.
- ^ а б c d е ж грамм час Lei, X. G .; Weaver, J.D .; Mullaney, E .; Ullah, A.H.J .; Азаин, М. Дж. (Январь 2013 г.). «Фитаза, новая жизнь для« старого »фермента». Ежегодный обзор биологических наук о животных. 1: 283–309. Дои:10.1146 / annurev-animal-031412-103717. ISSN 2165-8110. PMID 25387021.
- ^ Konietzny, U .; Грейнер, Р. (2002). «Молекулярные и каталитические свойства фитат-разлагающих ферментов (фитаз)». Международный журнал пищевой науки и технологий. 37 (7): 791–812. Дои:10.1046 / j.1365-2621.2002.00617.x. ISSN 0950-5423.
- ^ Mullaney, E.J .; Гибсон, Д. М .; Уллах, А. Х. Дж. (1 августа 1991 г.). «Положительная идентификация клона лямбда gt11, содержащего область гена грибной фитазы, с помощью иммунологического зонда и проверки последовательности». Прикладная микробиология и биотехнология. 35 (5): 611–614. Дои:10.1007 / BF00169625. ISSN 0175-7598. PMID 1369340.
- ^ van Hartingsveldt, W .; van Zeijl, C.M .; Harteveld, G.M .; Gouka, R.J .; Suykerbuyk, M.E .; Luiten, R.G .; ван Паридон, П. А .; Selten, G.C .; Винстра, А. Э. (15 мая 1993 г.). «Клонирование, характеристика и сверхэкспрессия гена, кодирующего фитазу (phyA) Aspergillus niger». Ген. 127 (1): 87–94. Дои:10.1016 / 0378-1119 (93) 90620-И. ISSN 0378-1119. PMID 8387447.
- ^ Rodriguez, E .; Han, Y .; Лей, X.G. (1999-04-02). «Клонирование, секвенирование и экспрессия гена кислой фосфатазы / фитазы Escherichia coli (appA2), выделенного из толстой кишки свиньи». Сообщения о биохимических и биофизических исследованиях. 257 (1): 117–123. Дои:10.1006 / bbrc.1999.0361. ISSN 0006-291X. PMID 10092520.
- ^ Rodriguez, E .; Porres, J.M .; Han, Y .; Лей, X. Г. (май 1999 г.). «Различная чувствительность рекомбинантной фитазы Aspergillus niger (r-PhyA) и кислой фосфатазы Escherichia colipH 2,5 (r-AppA) к трипсину и пепсинину Vitro». Архивы биохимии и биофизики. 365 (2): 262–267. Дои:10.1006 / abbi.1999.1184. ISSN 0003-9861. PMID 10328821.
- ^ а б Пуль А.А., Грунингер Р.Дж., Грейнер Р., Янзен Т.В., Мосиманн С.К., Селинджер Л.Б. (2007). «Кинетический и структурный анализ бактериальной протеинтирозинфосфатазоподобной мио-инозитолполифосфатазы». Белковая наука. 16 (7): 1368–1378. Дои:10.1110 / пс. 062738307. ЧВК 2206706. PMID 17567745.
- ^ Ким Т., Маллани Э.Дж., Поррес Дж.М., Ронекер К.Р., Кроу С., Райс С., Ко Т., Улла А.Х., Дейли С.Б., Уэлч Р., Лей XG (2006). «Сдвиг профиля pH фитазы Aspergillus niger PhyA в соответствии с pH желудка повышает ее эффективность в качестве добавки к корму для животных». Appl Environ Microbiol. 72 (6): 4397–4403. Дои:10.1128 / AEM.02612-05. ЧВК 1489644. PMID 16751556.
- ^ Чен Р., Сюэ Г, Чен П, Яо Б., Ян В., Ма Кью, Фань И, Чжао З., Тарчинский М.С., Ши Дж. (2006). «Трансгенные растения кукурузы, экспрессирующие ген грибной фитазы». Трансгенный Res. 17 (4): 633–643. Дои:10.1007 / s11248-007-9138-3. PMID 17932782.
- ^ Голован С.П., Мейдингер Р.Г., Аджакайе А., Коттрилл М., Видеркер М.З., Барни Д.Д., Планте С., Поллард Дж. В., Фан М.З., Хейс М.А., Лаурсен Дж., Хьорт Дж. П., Хакер Р. Р., Филлипс Дж. П., Форсберг К. В. (2006). «Свиньи, экспрессирующие фитазу слюны, производят навоз с низким содержанием фосфора». Nat Biotechnol. 19 (8): 741–745. Дои:10.1038/90788. PMID 11479566.
- ^ Лим Б.Л., Йунг П., Ченг С., Хилл Дж. Э. (2007). «Распространение и разнообразие фитатоминерализующих бактерий». ISME J. 1 (4): 321–330. Дои:10.1038 / ismej.2007.40. PMID 18043643.
- ^ Накашима Б.А., Макаллистер Т.А., Шарма Р., Селинджер Л. Б. (2007). «Разнообразие фитаз в рубце». Microb Ecol. 53 (1): 82–88. Дои:10.1007 / s00248-006-9147-4. PMID 17186149.
- ^ а б Пуль А.А., Грейнер Р., Селинджер Л. Б. (2009). «Стереоспецифичность гидролиза мио-инозитола гексакисфосфата с помощью протеинтирозинфосфатазоподобной инозитолполифосфатазы из Megasphaera elsdenii». Appl Microbiol Biotechnol. 82 (1): 95–103. Дои:10.1007 / s00253-008-1734-5. PMID 18853154.
- ^ Чжан З.Ы. (2003). Механистические исследования протеинтирозинфосфатаз. Прог. Nucleic Acid Res. Мол. Биол. Прогресс в исследованиях нуклеиновых кислот и молекулярной биологии. 73. С. 171–220. Дои:10.1016 / S0079-6603 (03) 01006-7. ISBN 9780125400732. PMID 12882518.
- ^ а б Пуль А., Грейнер Р., Селинджер Л. Б. (2008). «Подобная протеинтирозинфосфатазе инозитолполифосфатаза из Selenomonas ruminantium subsp. Lactilytica обладает специфичностью к 5-фосфату мио-инозитолгексакисфосфата». Международный журнал биохимии и клеточной биологии. 40 (10): 2053–2064. Дои:10.1016 / j.biocel.2008.02.003. PMID 18358762.
- ^ а б Konietzny U, Greiner R (2002). «Молекулярные и каталитические свойства фитат-разлагающих ферментов (фитаз)». Int J Food Sci Technol. 37 (7): 791–812. Дои:10.1046 / j.1365-2621.2002.00617.x.
- ^ Барриентос Л., Скотт Дж. Дж., Мурти П. П. (1994). «Специфика гидролиза фитиновой кислоты щелочной фитазой из пыльцы лилии».. Физиология растений. 106 (4): 1489–1495. Дои:10.1104 / pp.106.4.1489. ЧВК 159689. PMID 7846160.
- ^ Редди Н.Р., Сате СК, Салунхе Д.К. (1982). Фитаты в бобовых и злаках. Adv Food Res. Достижения в исследованиях пищевых продуктов. 28. С. 1–92. Дои:10.1016 / с0065-2628 (08) 60110-х. ISBN 9780120164288. PMID 6299067.
- ^ Markiewicz, L.h .; Honke, J .; Haros, M .; Witecka, D .; Wróblewska, B. (01.07.2013). «Диета определяет способность кишечной микробиоты человека расщеплять фитат - исследования in vitro» (PDF). Журнал прикладной микробиологии. 115 (1): 247–259. Дои:10.1111 / jam.12204. HDL:10261/128848. ISSN 1365-2672. PMID 23551617.
- ^ Конвей SJ, Миллер GJ (2007). «Биологические инозитолфосфаты, фосфатидилинозитолфосфаты и производные». Nat Prod Rep. 24 (4): 687–707. Дои:10.1039 / b407701f. PMID 17653355.
- ^ Brailoiu E, Miyamoto MD, Dun NJ (2003). «Производные инозита модулируют спонтанное высвобождение медиатора в нервно-мышечном соединении лягушки». Нейрофармакология. 45 (5): 691–701. Дои:10.1016 / S0028-3908 (03) 00228-4. PMID 12941382.
- ^ Банс М.В., Бергендаль К., Андерсон Р.А. (2006). «Ядерный ПИ (4,5) П (2): новое место для старого сигнала». Biochim Biophys Acta. 1761 (5–6): 560–569. Дои:10.1016 / j.bbalip.2006.03.002. PMID 16750654.
- ^ Жирар М, Кормье Й (2010). «Гиперчувствительный пневомонит». Текущее мнение в области аллергии и клинической иммунологии. 10 (2): 99–103. Дои:10.1097 / ACI.0b013e3283373bb8. PMID 20093932.
- ^ van Heemst RC, Sander I., Rooyackers J, et al. (2009). «Гиперчувствительный пневмонит, вызванный профессиональным воздействием фитазы». Eur Respir J. 33 (6): 1507–09. Дои:10.1183/09031936.00035408. PMID 19483053.
- ^ Frias, J .; Добладо, Р .; Antezana, J. R .; Видаль-Вальверде, К. Н. (2003). «Разложение инозитолфосфата под действием фермента фитазы в семенах бобовых». Пищевая химия. 81 (2): 233. Дои:10.1016 / S0308-8146 (02) 00417-X. HDL:10261/131058.
- ^ Mesina, Von G.R .; Лагос, Л. Ванесса; Sulabo, Rommel C .; Прогулка, Кэрри Л .; Штейн, Ханс Х. (01.02.2019). «Влияние микробной фитазы на синтез муцина, гидролиз желудочного белка и разложение фитата в желудочно-кишечном тракте растущих свиней». Журнал зоотехники. 97 (2): 756–767. Дои:10.1093 / jas / sky439. ISSN 1525-3163. ЧВК 6358309. PMID 30452657.
- ^ "Генетически измененный" Enviropig "для уменьшения мертвых зон?". National Geographic News. 2010-03-30. Получено 2020-04-24.
- ^ Головань, Сергей П .; Мейдингер, Рой Дж .; Аджакайе, Айоделе; Коттрилл, Майкл; Wiederkehr, Miles Z .; Барни, Дэвид Дж .; Плант, Клэр; Поллард, Джон В .; Fan, Ming Z .; Хейс, М. Энтони; Лаурсен, Джеспер; Хьорт, Дж. Питер; Хакер, Роджер Р .; Филлипс, Джон П .; Форсберг, Сесил В. (2001). «Свиньи, экспрессирующие фитазу слюны, производят навоз с низким содержанием фосфора». Природа Биотехнологии. 19 (8): 741–745. Дои:10.1038/90788. PMID 11479566.
- ^ «Трансгенные растения, экспрессирующие ген фитазы микробного происхождения, и их предполагаемое применение в качестве корма». ResearchGate. Получено 2020-04-24.