Пектинэстераза - Pectinesterase
| пектинэстераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.1.1.11 | ||||||||
| Количество CAS | 9025-98-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Пектинэстераза (PE) (EC 3.1.1.11 ) является повсеместным, связанным с клеточной стенкой фермент это представляет несколько изоформы которые способствуют модификации клеточной стенки растений и ее последующему разрушению. Он содержится во всех высших растениях, а также в некоторых бактерии и грибы. Пектинэстераза действует в первую очередь за счет изменения локализованных pH клеточной стенки, что приводит к нарушениям целостности клеточной стенки.
Пектинэстераза катализирует деэтерификация из пектин в грудной и метанол. Пектин - один из основных компонентов клеточной стенки растений. У растений пектинэстераза играет важную роль в метаболизме клеточной стенки во время созревания плодов. У растений бактериальные патогены, такие как Эрвиния каротовора и в грибковых патогенах, таких как Aspergillus niger, пектинэстераза участвует в мацерации и мягком гниении тканей растений. Пектинэстеразы растений регулируются ингибиторами пектинэстеразы, которые неэффективны против микробных ферментов.[2]
Функция
Недавние исследования[нужна цитата ] показали, что манипуляции с пектинэстеразой выражение может влиять на многие физиологические процессы. У растений пектинэстераза играет роль в модуляции механической стабильности клеточной стенки во время созревание плодов, расширение клеточной стенки при прорастании пыльцы и пыльцевая трубка рост, опадение, удлинение стебля, клубень урожайность и развитие корней. Также было показано, что пектинэстераза играет роль в реакции растений на возбудитель атака. Связанная с клеточной стенкой пектинэстераза Nicotiana tabacum участвует в распознавании рецепторов клетки-хозяина для вирус табачной мозаики белок движения, и было показано, что это взаимодействие необходимо для транслокации вируса от клетки к клетке.
Действие пектинэстеразы на компоненты клеточной стенки растений может вызывать два диаметрально противоположных эффекта. Первый - это вклад в укрепление клеточной стенки путем производства блоков неэтерифицированных карбоксил группы, которые могут взаимодействовать с ионы кальция образуя пектатный гель. Во-вторых, высвобождение протонов может стимулировать активность клеточной стенки. гидролазы способствуя разрыхлению клеточной стенки.
Этерификация пектина
Пектины составляют примерно 35% от сухой массы двудомный клеточные стенки. Полимеризуются в СНГ. Гольджи, метилэстерифицированный в медиальной части Гольджи и замещенный боковыми цепями в транс-цистернах Гольджи. Биохимия пектина может быть довольно сложной, но, проще говоря, основная цепь пектина состоит из 3 типов полимеров: гомогалактуронана (HGA); рамногалактуронан I (RGI); рамногалактуронан II (RGII).
Гомогалактуронан сильно этерифицируется метилом при экспорте в клеточные стенки и впоследствии деэтерифицируется под действием пектинэстеразы и других пектиновых ферментов. Пектинэстераза катализирует деэтерификацию метилэтерифицированных звеньев D-галактозидуроновой кислоты в пектиновых соединениях, давая субстраты для деполимеризующих ферментов, особенно кислых пектинов и метанол.
Большинство очищенных пектинэстераз растений имеют нейтральные или щелочные изоэлектрические точки и связаны с клеточной стенкой через электростатический взаимодействия. Однако пектинэстеразы могут иметь кислые изоэлектрические точки, обнаруженные в растворимых фракциях тканей растений. До недавнего времени обычно считалось, что растительные пектинэстеразы удаляют метиловые эфиры прогрессивным блочным способом, приводя к длинным непрерывным участкам неэтерифицированных остатков GalA в гомогалактуронановых доменах пектин. Альтернативно считалось, что грибковые пектинэстеразы обладают случайной активностью, приводящей к деэтерификации отдельных остатков GalA на взаимодействия фермент / субстрат. Было показано, что некоторые пектинэстеразы растений изоформы могут проявлять оба механизма, и что такие механизмы вызваны изменениями в pH. Оптимальный pH для высших растений обычно находится между pH 7 и pH 8, хотя pH пектинэстеразы от грибы и бактерии обычно намного ниже этого.
Молекулярная биология и биохимия
Белки PE синтезируются как пре-белки 540-580 аминокислоты обладающий сигнальной последовательностью и большим амино-концевым удлинением около 22 кДа. Это концевое удлинение в конечном итоге удаляют с получением зрелого белка 34-37 кДа. Большинство ПЭ не имеют консенсусные последовательности за N-гликозилирование в зрелом белке, хотя по крайней мере один сайт присутствует в аминоконцевой области удлинения.
Пространственная и временная регуляция активности пектинэстеразы во время развития растений основана на большом семействе изоформ. В последнее время систематическое определение последовательности Arabidopsis thaliana геном привел к идентификации 66 открытые рамки для чтения которые аннотированы как пектинэстеразы, большинство из которых кодируются как большие пре-пропротеины. Сигнал пептид пре-область необходима для нацеливания фермента на эндоплазматический ретикулум и состоит примерно из 25 аминокислотных остатков. Эти N-концевой регионы содержат несколько гликозилирование сайты, и считается, что эти сайты также играют роль в таргетинге.
Считается, что пектинэстераза секретируется в апоплазму с высокометилированным пектином, хотя в какой-то момент на этом секреторном пути N-концевой пропептид отщепляется. В настоящее время роль про-региона неизвестна, хотя было высказано предположение, что он может действовать как внутримолекулярный шаперон, обеспечивая правильную укладку или дезактивирующую активность до завершения вставки PE в клеточную стенку.
В последнее время особое внимание было уделено молекулярным исследованиям пектинэстеразы, ведущим к характеристике нескольких родственных изоформ у различных видов высших растений. Было показано, что некоторые из этих пектинэстераз экспрессируются повсеместно, тогда как другие специфически экспрессируются во время созревания плодов, прорастания пыльцевого зерна или удлинения стебля. Такие данные позволяют предположить, что пектинэстеры кодируются семейством генов, которые по-разному регулируются в зависимости от типа клетки в ответ на специфические сигналы развития или окружающей среды.
Изоформы растений
Несколько изоформ пектинэстеразы, различающихся молекулярный вес, изоэлектрическая точка и биохимическая активность были выявлены в двудольные растения. Изоформы пектинэстеразы кодируются семейством генов, некоторые из которых конститутивно экспрессируются во всем растении, тогда как другие по-разному экспрессируются в определенных тканях и на разных стадиях развития. Изоформы пектинэстеразы различаются по различным биохимическим параметрам, таким как относительная молекулярная масса, изоэлектрическая точка, оптимальный pH, сродство к субстрату, потребность в ионах и местоположение.
Структура
| Пектинэстераза, каталитическая | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||||
| Символ | Пектинэстераза_ кошка | ||||||||||
| Pfam | PF01095 | ||||||||||
| ИнтерПро | IPR000070 | ||||||||||
| PROSITE | PDOC00413 | ||||||||||
| |||||||||||
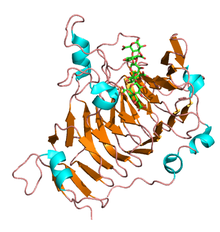
N-концевые пропептиды пектинэстеразы различаются по размеру и последовательности и демонстрируют низкий уровень аминокислотной идентичности. В качестве альтернативы C-терминал каталитическая область является высококонсервативной и представляет собой зрелый фермент. Первая трехмерная структура, решенная для пектинэстеразы растений, была для изоформы из морковь (Daucus carota) корень и состоит из правой параллельной β-спирали, как видно на всех углевод эстераза семья СЕ-8, а трансмембранный домен и пектин-связывающая щель.[3] Подобным образом несколько структур пектинэстеразы были выяснены у грибов и Кишечная палочка и разделяют большинство структурных мотивов растений.
Прокариотические и эукариотические пектинэстеразы имеют несколько областей сходства последовательностей. Кристаллическая структура пектинэстеразы Erwinia chrysanthemi выявила структуру бета-спирали, аналогичную структуре пектинолитических ферментов, хотя она отличается от большинства структур эстераз.[4] Предполагаемые каталитические остатки находятся в том же месте, что и активный центр и субстрат-связывающая щель пектатлиазы.
Рекомендации
- ^ Фри, М .; Ihrig, J .; Brocklehurst, K .; Шевчик, В. Э .; Пикерсгилл, Р. У. (2007). «Молекулярные основы активности пектинметилэстеразы фитопатогена». Журнал EMBO. 26 (17): 3879–3887. Дои:10.1038 / sj.emboj.7601816. ЧВК 2000356. PMID 17717531.
- ^ Джоване А., Церноглоу Д., Камарделла Л., Ди Маттео А., Райола А., Бонивенто Д., Де Лоренцо Дж., Червоне Ф., Беллинкампи Д. (2005). «Структурная основа взаимодействия между пектинметилэстеразой и специфическим белком-ингибитором». Растительная клетка. 17 (3): 849–858. Дои:10.1105 / tpc.104.028886. ЧВК 1069703. PMID 15722470.
- ^ PDB: 1GQ8; Йоханссон К., Эль-Ахмад М., Фриманн Р., Йорнвалл Х., Маркович О., Эклунд Х. (март 2002 г.). «Кристаллическая структура пектинметилэстеразы растений». FEBS Lett. 514 (2–3): 243–9. Дои:10.1016 / S0014-5793 (02) 02372-4. PMID 11943159.
- ^ PDB: 1QJV; Пикерсгилл Р. У., Смит Д., Дженкинс Дж., Майанс О, Уорбойз К. (2001). «Трехмерная структура пектинметилэстеразы Erwinia chrysanthemi выявляет новый активный сайт эстеразы». J. Mol. Биол. 305 (4): 951–960. Дои:10.1006 / jmbi.2000.4324. PMID 11162105.
внешняя ссылка
- пектинэстераза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
