Пируват декарбоксилаза - Pyruvate decarboxylase
| Пируват декарбоксилаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
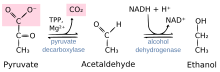 Реакция, катализируемая пируватдекарбоксилазой: пируват + тиаминпирофосфат (TPP) → гидроксиэтил-TPP + CO2 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.1.1.1 | ||||||||
| Количество CAS | 9001-04-1 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Пируват декарбоксилаза это гомотетрамерный фермент (EC 4.1.1.1 ) который катализирует декарбоксилирование пировиноградная кислота к ацетальдегид и углекислый газ в цитоплазме прокариот, а также в цитоплазме и митохондриях[нужна цитата ] эукариот. Его также называют 2-оксокислотной карбоксилазой, альфа-кетокислотной карбоксилазой и пировиноградной декарбоксилазой.[1] В анаэробных условиях этот фермент является частью процесса ферментации дрожжей, особенно дрожжей Сахаромицеты, производить этиловый спирт путем брожения. Он также присутствует в некоторых видах рыб (в том числе золотая рыбка и карп ), где он позволяет рыбе выполнять брожение этанола (наряду с брожением молочной кислоты) при недостатке кислорода.[2] Пируват декарбоксилаза запускает этот процесс, превращая пируват в ацетальдегид и диоксид углерода.[3] Пируватдекарбоксилаза зависит от кофакторы пирофосфат тиамина (TPP) и магний. Этот фермент не следует принимать за несвязанный фермент. пируватдегидрогеназа, оксидоредуктаза (EC 1.2.4.1 ), который катализирует окислительное декарбоксилирование пирувата до ацетил-КоА.
Структура
Пируватдекарбоксилаза представляет собой димер димеров с двумя активными центрами, общими для мономеров каждого димера. Фермент содержит бета-альфа-бета структуру, дающую параллельные бета-листы. Он содержит 563 субъединицы остатка в каждом димере; фермент имеет сильное притяжение к интермономерам, но димеры слабо взаимодействуют с образованием рыхлого тетрамера.[4]
- Кристаллографические структуры пируватдекарбоксилазы

Мультяшная диаграмма мономера пируват-декарбоксилазы с присоединенным TPP.
Мультфильм диаграмма тетрамера пируват декарбоксилазы.

Активный центр пируватдекарбоксилазы с выбранными аминокислотами: Glu-51, Glu-477, Asp-444 и Asp-28. Также отображаются кофакторы TPP и Mg.2+.
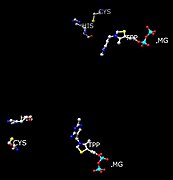
Положение остатков His и Cys по отношению к активному центру (TPP и Mg), участвующим в конформации, изменяется при взаимодействии с пируватным субстратом.
Остатки активного сайта
Этот фермент является гомотетрамером и поэтому имеет четыре активных центра. Активные центры находятся внутри полости в ядре фермента, где может возникать водородная связь и где пируват реагирует с TPP. Каждый активный сайт состоит из 20 аминокислот, включая кислую Glu-477 (способствует стабильности кольца TPP) и Glu-51 (способствует связыванию кофактора). Эти глутаматы также способствуют формированию ТПП-илида, действуя как донаторы протонов аминопиримидинового кольца ТПП. Микросреда вокруг этого Glu 477 очень неполярная, что способствует более высокому, чем обычно, pKа (нормальные pKa Glu и Asp составляют около 4,6 в малых белках).[5]
Липофильные остатки Ile-476, Ile-480 и Pro-26 вносят вклад в неполярность области вокруг Glu-477. Единственным другим отрицательно заряженным остатком, кроме кофермента TPP, является Asp-28, который также способствует увеличению pKа Glu-477. Таким образом, окружающая среда фермента должна обеспечивать протонирование гамма-карбоксильной группы Glu-477 до pH около 6.[5]
Аминопиримидиновое кольцо на TPP действует как основание, будучи однажды в иминной форме, для отрыва протона C2 от TPP с образованием нуклеофила. илида.[4] Это должно происходить, потому что фермент не имеет основных боковых цепей, которые депротонировали бы TPP C2. Мутация в активном сайте с участием этих Glu может привести к неэффективности или неактивности фермента. Эта неактивность была доказана в экспериментах, в которых отсутствовали N1 'и / или 4'-аминогруппы. При ЯМР-анализе было определено, что, когда TPP связывается с ферментом вместе с аналогом субстатического пирувамида, скорость образования илида выше, чем нормальная скорость фермента. Кроме того, скорость мутации Glu 51 в Gln значительно снижает эту скорость.[4]
Также включены Asp-444 и Asp-28, которые стабилизируют активный сайт. Они действуют как стабилизаторы Mg2+ ион, который присутствует в каждом активном центре. Чтобы гарантировать, что связывается только пируват, два Cys-221 (более 20 Ангстремов от каждого сайта) и His-92 запускают конформационное изменение который ингибирует или активирует фермент в зависимости от субстрата, который с ним взаимодействует. Если субстрат, связанный в активном центре, представляет собой пируват, то фермент активируется за счет конформационного изменения этого регулирующий сайт.[6] Конформационное изменение включает 1,2-нуклеофильное присоединение. Эта реакция, образование тиокеталя, переводит фермент из неактивного в активное состояние.
Подавление сайта осуществляется XC6ЧАС4CH = CHCOCOOH класс ингибиторов / аналогов субстратов, а также продукт декарбоксилирования из таких соединений, как коричный альдегид. Другие потенциальные нуклеофильные сайты для ингибитора включают Cys-152, Asp-28, His-114, His-115 и Gln-477.[6]
Нормальная каталитическая скорость пируватдекарбоксилазы составляет kКот = 10 с−1. Однако скорость фермента с мутацией Glu-51 в Gln составляет 1,7 с.−1.[4]
Протезная группа ТПП
Кофактор TPP, C12 ЧАС18 N4 О7 п2 S, необходим для механизма этой реакции; он действует как простетическая группа фермента. Атом углерода между атомами серы и азота на тиазольном кольце действует как карбанион, который связывается с пируватом. ТФП имеет кислую Н+ на его C2, который действует как функциональная часть тиазолиевого кольца; кольцо действует как «сток электронов», позволяя карбанионным электронам стабилизироваться за счет резонанса.[3] Затем TPP может действовать как нуклеофил с потерей этого водорода C2, образуя илидную форму TPP. Этот илид может затем атаковать пируват, который удерживается ферментом пируватдекарбоксилазой. Во время декарбоксилирования пирувата TPP стабилизирует карбанионные промежуточные соединения как электрофил за счет нековалентных связей.[4] В частности, пиридильный азот N1 'и 4'-аминогруппа TPP важны для каталитической функции комплекса фермент-TDP.[5]
Механизм
Фермент расщепляет пируват на двуокись углерода и 2-углеродный фрагмент, который присоединен к его кофактору TPP. Этот 2-углеродный фрагмент присоединен к пятичленному кольцу TPP в его илидной форме. Это необратимый этап, на котором образуется ацетальдегид для второй стадии спиртовой ферментации (анаэробной ферментации), на которой ацетальдегид восстанавливается NADH с помощью алкогольдегидрогеназы до этанола.[7]

Дрожжи
В дрожжи, пируватдекарбоксилаза действует независимо во время анаэробный ферментация и высвобождает 2-углеродный фрагмент в виде ацетальдегида плюс диоксид углерода. Пируватдекарбоксилаза создает средства CO2 устранение, которое клетка рассеивает. Фермент также предназначен для создания этанола, который используется в качестве антибиотика для уничтожения конкурирующих организмов.[4] Фермент необходим для декарбоксилирования альфа-кетокислот, поскольку в переходном состоянии на карбонильном атоме углерода происходит накопление отрицательного заряда; следовательно, фермент обеспечивает подходящую среду для встречи ТФП и альфа-кетокислоты (пирувата).[4]
Рекомендации
- ^ "Обзор ENZYME в NiceZyme: EC 4.1.1.1". Сервер ExPASy Proteomics.
- ^ Арен ван Ваард; Г. Ван ден Тилларт; Мария Верхаген (1993). «Образование этанола и регулирование pH у рыб». Пережить гипоксию. С. 157-170. HDL:11370 / 3196a88e-a978-4293-8f6f-cd6876d8c428. ISBN 0-8493-4226-0.
- ^ а б Тадг П. Бегли; Макмерри, Джон (2005). Органическая химия биологических путей. Робертс и Ко. Издатели. п. 179. ISBN 0-9747077-1-6.
- ^ а б c d е ж грамм PDB: 1pyd; Дайда Ф., Фьюри В., Сваминатан С., Сакс М., Фарренкопф Б., Джордан Ф. (июнь 1993 г.). «Каталитические центры в тиаминдифосфат-зависимом ферменте пируватдекарбоксилазе при разрешении 2,4-А». Биохимия. 32 (24): 6165–70. Дои:10.1021 / bi00075a008. PMID 8512926.
- ^ а б c Лобелл М, Краут Д.Х. (1996). «Пируват декарбоксилаза: исследование молекулярного моделирования декарбоксилирования пирувата и образования ацилоина». Варенье. Chem. Soc. 118 (8): 1867–1873. Дои:10.1021 / ja951830t.
- ^ а б Бабурина И., Дикдан Г., Го Ф, Тус Г. И., Корень Б, Иордания Ф (февраль 1998 г.). «Реактивность на сайте активации субстрата дрожжевой пируватдекарбоксилазы: ингибирование путем искажения доменных взаимодействий». Биохимия. 37 (5): 1245–55. Дои:10.1021 / bi9709912. PMID 9477950.
- ^ Х., Гарретт, Реджинальд (2013). Биохимия. Гришем, Чарльз М. (5-е изд.). Бельмонт, Калифорния: Брукс / Коул, Cengage Learning. ISBN 9781133106296. OCLC 777722371.
внешняя ссылка
- Пируват + декарбоксилаза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)




